CLONING AND TISSUE EXPRESSION OF FOUR WNT GENES IN YELLOW CATFISH PELTEOBAGRUS FULVIDRACO AND THEIR RESPONSE TO COPPER EXPOSURE
-
摘要: 为探究Wnt家族成员在黄颡鱼卵巢发育中的作用, 研究首先采用RT-PCR和RACE技术获取了黄颡鱼Wnt5a、Wnt5b、Wnt7a和Wnt9b基因的全长cDNA序列, 即1984、2905、2158和1622 bp, 其中ORF长度分别为1124、1124、1049和1073 bp, 编码375、375、350和358个氨基酸。氨基酸序列比对和系统树分析显示, 这些基因十分保守, 黄颡鱼WNT与墨西哥丽脂鲤和斑马鱼比较接近。组织表达分析表明, 这些基因的mRNA在脑、脾脏、肾脏、鳃、心脏、肌肉、脂肪、肝脏及卵巢等组织中都有表达, 但表达水平不尽相同。Wnt家族基因对铜的响应研究表明: 在暴露28d时, Wnt7a mRNA水平随着铜浓度先上升后下降, 但是Wnt5a、Wnt5b和Wnt9b基因表达各个处理组无显著性差异; 在56d, Wnt5b在60 μg Cu/L组最低, 其他2个组差异不显著, Wnt9b mRNA水平随着铜浓度先上升后下降, 但是Wnt5a和Wnt7a基因表达各个处理组无显著性差异, 表明Wnt家族这些基因的功能发生了分化, 部分成员介导了铜影响黄颡鱼卵巢发育的调控。研究首次揭示了黄颡鱼Wnt家族部分成员的基因结构和功能, 为深入探讨他们在卵巢发育中的作用奠定了基础。Abstract: Four full length Wnt cDNA sequences, designated Wnt5a, Wnt5b, Wnt7a and Wnt9b, were amplified by RT-PCR and RACE approaches from yellow catfish Pelteobagrus fulvidraco. The validated cDNAs of Wnt5a, Wnt5b, Wnt7a and Wnt9b were 1984, 2905, 2158 and 1622 bp in length, encoding peptides of 375, 375, 350 and 358 amino acid residues, respectively. The amino acid alignment and phylogenetic analysis revealed that Wnt sequences were relatively conserved among different vertebrates. All Wnt mRNAs were expressed in tested tissues (brain, spleen, kidney, gill, heart, muscle, mesenteric fat, liver and ovary) but with variable levels. Cu exposure for 28 days highly induced Wnt7a mRNA levels only at 30 μg Cu/L group. Cu exposure had no impact on mRNA levels of Wnt5a, Wnt5b and Wnt9b at day 28. On 56-day Cu exposure, mRNA levels of Wnt5b were not lowest at 60 μg Cu/L group and Wnt9b were the highest at 30 μg Cu/L group. Wnt5a and Wnt7a showed no significant differences among three groups. The present study indicated that functional differentiation exists in members of Wnt family, and some members may mediate the effect of Cu exposure on ovary development of yellow catfish.
-
Keywords:
- Pelteobagrus fulvidraco /
- Wnt /
- Molecular characterization /
- Tissue distribution /
- Copper exposure
-
在纤毛虫原生动物中, 寡毛类(Oligotrichs)为一营浮游生活的类群。广义寡毛类纤毛虫包括无壳寡毛类和具壳丁丁虫类[1, 2]。作为海洋微食物网的重要组成部分, 该类纤毛虫在海洋初-次级能量流动和碳循环过程中起着重要的枢纽作用[1-3]。
国际间对该类纤毛虫的研究已开展了一个多世纪, 迄今为止报道了约200余种无壳寡毛类[2]。但由于该类群纤毛虫通常个体较小、运动快速、表膜脆弱易破、大量种类活体上十分相似以及前人研究、历史文献中的累计性错误, 长期以来, 对本类群的分类学研究一直是(纤毛虫各目级阶元)种类鉴定中最为困难的。在迄今已经报道的命名种中, 约半数类群或种类资料仍然仅限于基于传统研究方法的描述(来自活体或固定后样本的观察), 因此在该类群中: 大部分重要分类性状均处于缺失状态, 许多种类的分类地位未明、未定或是错误的。即便是在其余的经过“现代方法”研究过的类群中, 许多种类也因种种原因而存在着程度不同的混乱和错误[2]。
有鉴于此, 作者于2003—2010年间对我国沿海多类生境(开放海区、潮间带、水产养殖水体等)中的无壳寡毛类纤毛虫开展了现代标准的(活体形态学、统计资料建立、纤毛图式揭示等)专项分类学研究, 本文对其中10种较罕见种类进行了形态学描述, 讨论了种群间的形态差异, 对新认定的特征信息进行了补充, 并对若干种的分类学进行了修订。
1. 材料与方法
十种寡毛类纤毛虫于2003—2010年采自青岛、大亚湾及湛江近岸水体。分离、培养、活体观察、染色制片等研究方法主要参照宋微波等[4]。名词术语和分类系统分别参照Agatha and Riedel-Lorjé[5]和Gao等[6]。
2. 结果与讨论
2.1 侧扁急游虫Strombidium apolatum Wilbert & Song, 2005 (图版Ⅰ-1—3, 图版Ⅱ-1—5)
![]() 图版Ⅰ 十种寡毛类纤毛虫的活体形态(1、4、7、10、13、16、19、22、23、29)和纤毛模式(2—3、5—6、8—9、11—12、14—15、17—18、20—21、24—28、30)1—3. 侧扁急游虫; 4—6. 具头急游虫; 7—9. 广东急游虫; 10—12. 拟卡氏急游虫, 箭头示背部趋触膜; 13—15. 拟楔尾急游虫, 自宋微波等[4]; 16—18. 铃木急游虫, 自宋微波等[4]; 19—21. 束腰旋游虫; 22—26. 杨科夫平游虫, 箭头示口原基, 22自宋微波等[4]; 27—28. 卡尔平游虫, 自宋微波等[4]; 29—30. 最小拟盗虫. 比例尺: 20 μm. GK. 环带动基列; VK. 腹面动基列; BM. 口区小膜; Exk. 额外动基列图版Ⅰ. Schematic drawings of ten oligotrich ciliates from life (1, 4, 7, 10, 13, 16, 19, 22, 23, 29) and after protagol impregnation (2—3, 5—6, 8—9, 11—12, 14—15, 17—18, 20—21, 24—28, 30)1—3. Strombidium apolatum; 4—6. Strombidium capitatum; 7—9. Strombidium guangdongense; 10—12. Strombidium paracalkinsi, arrow marks thigmotactic membranelles on dorsal side; 13—15. Strombidium parastylifer, from Song, et al.[4]; 16—18. Strombidium suzukii, from Song, et al.[4]; 19—21. Spirostrombidium cinctum; 22—26. Parallelostrombidium jankowski, arrow marks oral primordium, 22 from Song, et al.[4] ; 27—28. Parallelostrombidium kahli, from Song, et al.[4]; 29—30. Strombidinopsis minima. GK. girdle kinety; VK. ventral kinety; BM. buccal membranelles; Exk. Extra kirety
图版Ⅰ 十种寡毛类纤毛虫的活体形态(1、4、7、10、13、16、19、22、23、29)和纤毛模式(2—3、5—6、8—9、11—12、14—15、17—18、20—21、24—28、30)1—3. 侧扁急游虫; 4—6. 具头急游虫; 7—9. 广东急游虫; 10—12. 拟卡氏急游虫, 箭头示背部趋触膜; 13—15. 拟楔尾急游虫, 自宋微波等[4]; 16—18. 铃木急游虫, 自宋微波等[4]; 19—21. 束腰旋游虫; 22—26. 杨科夫平游虫, 箭头示口原基, 22自宋微波等[4]; 27—28. 卡尔平游虫, 自宋微波等[4]; 29—30. 最小拟盗虫. 比例尺: 20 μm. GK. 环带动基列; VK. 腹面动基列; BM. 口区小膜; Exk. 额外动基列图版Ⅰ. Schematic drawings of ten oligotrich ciliates from life (1, 4, 7, 10, 13, 16, 19, 22, 23, 29) and after protagol impregnation (2—3, 5—6, 8—9, 11—12, 14—15, 17—18, 20—21, 24—28, 30)1—3. Strombidium apolatum; 4—6. Strombidium capitatum; 7—9. Strombidium guangdongense; 10—12. Strombidium paracalkinsi, arrow marks thigmotactic membranelles on dorsal side; 13—15. Strombidium parastylifer, from Song, et al.[4]; 16—18. Strombidium suzukii, from Song, et al.[4]; 19—21. Spirostrombidium cinctum; 22—26. Parallelostrombidium jankowski, arrow marks oral primordium, 22 from Song, et al.[4] ; 27—28. Parallelostrombidium kahli, from Song, et al.[4]; 29—30. Strombidinopsis minima. GK. girdle kinety; VK. ventral kinety; BM. buccal membranelles; Exk. Extra kirety![]() 图版Ⅱ 侧扁急游虫、具头急游虫、广东急游虫、拟卡氏急游虫、拟楔尾急游虫的活体照片(1—4、6—9、11—13、17—19、21—22)和蛋白银染色制片照片(5、10、14—16、20、23—24)1—5. 侧扁急游虫, 2中箭头示沿腹面动基列分布的射出体, 5中箭头示环带动基列和腹面动基列之间的间隙; 6—10. 具头急游虫, 箭头示透明的前端凸起; 11—16. 广东急游虫, 箭头示射出体; 17—20. 拟卡氏急游虫, 18中箭头示射出体, 19—20中箭头示背部趋触膜; 21—24. 拟楔尾急游虫, 22中箭头示棘刺状尾, 23中箭头示腹面动基列前端, 21自宋微波等[4]. 比例尺: 20 μm. VK. 腹面动基列图版Ⅱ. Photomicrographs of Strombidium apolatum, Strombidium capitatum, Strombidium guangdongense, Strombidium paracalkinsi and Strombidium suzukii from life (1—4, 6—9, 11—13, 17—19, 21—22) and after protagol impregnation (5, 10, 14—16, 20, 23—24)1—5. Strombidium apolatum, arrow in 2 marks the extrusomes along the ventral kinety, arrow in 5 marks the gap between girdle and ventral kineties; 6—10. Strombidium capitatum, arrow notes the hyaline apical protrusion; 11—16. Strombidium guangdongense, arrow marks the extrusomes; 17—20. Strombidium paracalkinsi, arrow in 18 marks the extrusomes, arrows in 19 and 20 mark the thigmotactic membranelles on dorsal side; 21—25. Strombidium parastylifer, arrow in 22 marks the tail, arrow in 23 marks the anterior end of ventral kinety, 21 from Song, et al.[4] VK. ventral kinety
图版Ⅱ 侧扁急游虫、具头急游虫、广东急游虫、拟卡氏急游虫、拟楔尾急游虫的活体照片(1—4、6—9、11—13、17—19、21—22)和蛋白银染色制片照片(5、10、14—16、20、23—24)1—5. 侧扁急游虫, 2中箭头示沿腹面动基列分布的射出体, 5中箭头示环带动基列和腹面动基列之间的间隙; 6—10. 具头急游虫, 箭头示透明的前端凸起; 11—16. 广东急游虫, 箭头示射出体; 17—20. 拟卡氏急游虫, 18中箭头示射出体, 19—20中箭头示背部趋触膜; 21—24. 拟楔尾急游虫, 22中箭头示棘刺状尾, 23中箭头示腹面动基列前端, 21自宋微波等[4]. 比例尺: 20 μm. VK. 腹面动基列图版Ⅱ. Photomicrographs of Strombidium apolatum, Strombidium capitatum, Strombidium guangdongense, Strombidium paracalkinsi and Strombidium suzukii from life (1—4, 6—9, 11—13, 17—19, 21—22) and after protagol impregnation (5, 10, 14—16, 20, 23—24)1—5. Strombidium apolatum, arrow in 2 marks the extrusomes along the ventral kinety, arrow in 5 marks the gap between girdle and ventral kineties; 6—10. Strombidium capitatum, arrow notes the hyaline apical protrusion; 11—16. Strombidium guangdongense, arrow marks the extrusomes; 17—20. Strombidium paracalkinsi, arrow in 18 marks the extrusomes, arrows in 19 and 20 mark the thigmotactic membranelles on dorsal side; 21—25. Strombidium parastylifer, arrow in 22 marks the tail, arrow in 23 marks the anterior end of ventral kinety, 21 from Song, et al.[4] VK. ventral kinety本种于2008年3月18日采集自大亚湾近岸潮间带, 水温22.7℃, 盐度26.0‰, pH 7.9。
形态学描述 虫体活体大小(35—50) μm× (20—35) μm, 银染后通常(36—59) μm× (22—31) μm。体型长锥形, 前端右侧口缘隆起形成球形前端凸起, 后端钝圆且背腹扁平(图版Ⅰ-1, 图版Ⅱ-1)。体表环带动基列后方具壳板, 由不规则多边形网格组成(图版Ⅱ-4)。体内存在大量共生色素体, 卵圆形, 直径约5—8 μm (图版Ⅱ-2、3)。射出体长杆状, 长约15—20 μm, 沿环带动基列和腹面动基列呈单列紧密排列, 表膜附着点位于环带动基列上方及腹面动基列左侧表膜沟内(图版Ⅱ-2、3)。椭圆形大核位于体中央。
口沟较浅。领取小膜13—16片, 口区小膜4—6片, 两部分小膜区紧密相连。最下面几片口区小膜基部明显变短(图版Ⅰ-2)。环带动基列由44—64个双动基体组成, 位于体前段1/3处。环带动基列未形成闭合环, 与体右侧开口且右端于体边缘向体后方弯曲。腹面动基列具27—42个双动基体, 前端开始于体右侧环带动基列右端下方, 沿体右边缘向下延伸, 绕体末端至左侧亚尾端(图版Ⅰ-2、3, 图版Ⅱ-5)。腹面动基列与环带动基列的间隙较短, 位于体右缘中部。
比较与讨论 本种最先由Wilbert和Song[7]发现于南极海域, 其形态特征及纤毛图式被报道描述; 随后Xu等[8]对该种的青岛种群进行了重描述并补充了部分活体特征信息。该种最显著的特征是环带动基列于腹面右侧开口, 且环带动基列右端于体边缘向体后方弯曲。本文种群是该种首次在亚热带海域被发现, 环带动基列排列方式与种的特征完全一致; 此外其他形态特征(如口区小膜、腹面动基列)与前人报道的种群均相符, 因此鉴定为该种。本种群发现的沿腹面动基列排布的射出体排列带, 在原始报道的南极种群中同样被观察到, 但在青岛种群中并无描述, 可能由于细节观察的忽略; 本文在此对该种腹面射出体特征及图片进行了补充。此外与南极种群相比, 本种群及青岛种群的体纤毛略短, 且体内均存在共生色素体(vs. 南极种群未发现), 这些差异可认定为种群间差异, 可能由环境差异所致。
Lei等[9]曾描述了该种的另外一个青岛种群, 但将该种群鉴定为Strobilidium syowaensis Hada, 1970, 并根据其纤毛图式将其归入Spirostrombidium属。该种群与侧扁急游虫相比, 无论在活体形态学还是蛋白银染色后的纤毛图式及统计数据, 均能较好的相符。因此, 这里将Lei等[9]鉴定的Spirostrombidium syowaensis (Hada, 1970) Lei, et al., 1999归为侧扁急游虫的同物异名。
2.2 具头急游虫Strombidium capitatum (Lee-gaard, 1995) Kahl, 1932 (图版Ⅰ-4—6, 图版Ⅱ-6—10)
本种于2007年3月31日采集自大亚湾近岸潮间带, 水温23.1℃, 盐度28.6‰, pH 8.2。
形态学描述 虫体活体大小(50—65) μm× (35—50) μm, 银染后通常(38—53) μm× (41—52) μm。体型球形, 具明显的透明的前端凸起, 约10 μm高, 位于口区右侧(图版Ⅰ-4, 图版Ⅱ-6—9)。体内包含大量小型绿藻等食物残渣, 使细胞低倍镜下呈黑色。射出体针状, 15 μm长, 单行排列, 体表附着点位于环带动基列上方的体表沟内(图版Ⅰ-4)。大核腊肠状, 右半段水平位于口区下方, 左半段弯向体后方。
口区极大且深, 向下延伸至体长3/5处(图版Ⅰ-5, 图版Ⅱ-7、8、10)。领区小膜13—17片, 口区小膜15—19片。两部分小膜区由一段空隙明显分开, 口区小膜中部的小膜基部明显较两端长(图版Ⅱ-10)。环带动基列于赤道区下方水平分布, 由107—163个密集排列的双动基体组成, 在腹面中部形成一段开口。腹面动基列位于环带动基列开口区下方, 包含5—10个双动基体(图版Ⅰ-5、6)。
比较与讨论 具头急游虫曾被报道于世界上的很多地方, 例如大西洋北部[10]、大西洋南部[11]、青岛近岸[12]。Montagnes等[11]首次揭示了该种的纤毛图式, Xu等[12]基于青岛种群对该种的活体特征进行了补充, 本工作系首次在我国南海发现该种。该种的主要特征为显著阔大的口区及透明的口缘。本种群在体型、口区形态、体动基列排列方式等性状均与前人报道的种群相符; 但本种群发现的环带动基列开口, 在青岛种群中同样被观察到, 但在大西洋种群中并不存在, 此差异可被认为种群间差异。
Agatha和Riedel-Lorjé[13]报道了一寡毛类新种Strombidium triquetrum, 无论在活体特征(体形, 虫体前端明显、透明的前端突起, 大小, 阔大且深的口区)还是蛋白银染色后的特征(领区小膜数目, 腹面小膜数目, 大核的形状、分布方式)都与S. capitatum非常相符, 最大的区别为前者没有发现腹动基列。由于S. capitatum的腹动基列很短(仅有几个至十几个毛基粒), 在很多个体中腹动基列这一结构难于观察, 这一现象在S. capitatum的大西洋种群中也有存在, 因此, S. triquetrum很有可能是S. capitatum的同物异名。由于缺少直接证据, 此处尚不做定论, 待日后获取S. triquetrum的标本或基因信息后再做讨论。
2.3 广东急游虫Strombidium guangdongense Liu, et al., 2016 (图版Ⅰ-7—9, 图版Ⅱ-11—16)
本种于2004年4月采集自青岛近岸潮间带, 水温20.8℃, 盐度21.3‰, pH 7.7。
形态学描述 虫体活体大小 (20—30) μm× (15—25) μm, 银染后(20—28) μm× (12—20) μm。个体间存在体型差异, 大多为卵圆形或心形, 体前端具不明显前端凸起, 后端钝圆(图版Ⅰ-7, 图版Ⅱ-11、12)。射出体斜向插入虫体中后部, 呈漏斗状(图版Ⅰ-7, 图版Ⅱ-13)。虫体内充满大量褐色细小球形颗粒, 可能为藻类食物残渣。大核纺锤形于体中央。
口沟较小, 占体长1/5。领区小膜具12—15片, 口区小膜3—5片, 两者紧密相连(图版Ⅰ-8)。环带动基列于虫体中部水平分布, 由约18—23个双动基体稀疏排列组成; 腹面动基列位于虫体右侧, 由4—6对毛基粒稀疏排列((图版Ⅰ-8—9, 图版Ⅱ-14—16)。
比较与讨论 该种最近由Liu等[14]报道于南海北部近岸, 提供了详细的形态及纤毛图式信息。该种区别与其他种的主要特征为极小的个体及稀疏排列的体动基列毛基体。与原始种群相比, 本种群虫体体型略胖(长宽比约1—1.5 vs. 原始种群为1.5—2), 且并未发现虫体后端的棘刺状尾(vs. 原始种群具棘刺状尾), 这些差异证实了原始种群描述中发现的: 该种个体间体型变化明显的特征[14]。此外, 两种群体内均发现大量褐色球形食物颗粒, 表明该种食物来源比较专一。
2.4 拟卡氏急游虫Strombidium paracalkinsi (Lei, et al., 1999) Agatha, 2004 (图版Ⅰ-10—12, 图版Ⅱ-17—20)
本种于2008年12月22日采集自深圳近岸潮间带, 水温20.1℃, 盐度27.8‰, pH 8.1。
形态学描述 虫体活体大小(30—50) μm× (25—45) μm, 银染后通常(37—59) μm× (33—59) μm。体型呈球形, 左侧肩部向下倾斜, 右侧领区隆起形成前端凸起(图版Ⅰ-10, 图版Ⅱ-17)。射出体杆状, 于体后半部均匀排列, 表膜附着点在体赤道区形成隆起(图版Ⅰ-10, 图版Ⅱ-18)。卵球形大核与体后部中央。细胞喜在基质上爬行, 同时将趋触膜附着在基质上。
口沟较窄但深, 延伸至体长2/5处。领区小膜14—17片, 口区小膜6—9片, 两部分小膜区紧密相连。三片趋触膜位于体背部, 于第8—10片领区小膜下方, 每片小膜由两列毛基体组成, 通过稀疏排列的无纤毛毛基体与领区小膜相连。趋触纤毛明显较领区小膜长, 基部从左向右依次变短(图版Ⅰ-11, 图版Ⅱ-18—20)。环带动基列由41—58个双动基体组成, 位于赤道区, 具腹面开口。腹面动基列与腹面后部中央, 包含9—13个双动基体(图版Ⅰ-11、12)。
比较与讨论 拟卡氏急游虫由Lei等[8]首次报道于青岛沿海, 随后Song等[15]对该种进行了重描述, Lee等[16]对该种的韩国种群又进行了描述。该种的最重要特征为体背部具三片趋触膜。本种群是该种首次在亚热带海域报道, 形态特征数据均与前人报道的种群相符。基于本种群的观察, 趋触膜的细节特征及图片在此补充。此外在该种群的观察中发现趋触膜与领区小膜是分开的, 两者之间由稀疏排列的无纤毛毛基体相连, 且每片趋触小膜均由两列毛基体组成(其他口区小膜大多由三列毛基体组成)。在寡毛类中Spirostrombidium和Parallelostrombidium这2个属的大多数种也具有趋触膜, 但该趋触膜生长在领区小膜与口区小膜之间, 与其他口区小膜一致, 每片趋触小膜均由三列毛基体组成, 且全部生长纤毛[4]。部分发生学信息表明这两种趋触膜类型虽然都是由领区小膜分化出来, 具有同源性, 但在进化过程中可能存在分歧, 最终导致结构上的差异, 但无论哪种趋触膜类型, 都为纤毛虫附着在基质上生活提供了适应性。详细的细胞发生学研究或许可以为探究趋触膜的进化提供证据。
2.5 拟楔尾急游虫Strombidium parastylifer Song, et al., 2009 (图版Ⅰ-13—15, 图版Ⅱ-21—24)
本种于2003年6月18日采集自青岛近岸潮间带。
形态学描述 虫体活体大小约(25—40) μm× (25—35) μm, 银染后约(20—35) μm× (20—30) μm; 体型倒锥形。虫体前端平截且宽, 具前端突起(图版Ⅰ-13, 图版Ⅱ-21), 后端变窄末端形成尖削的棘, 长约5 μm, 棘尾不可伸缩, 但可弯曲(图版Ⅱ-22)。射出体针状, 沿环带动基列分布(图版Ⅰ-13, 图版Ⅱ-22)。胞质含有大量球形内质颗粒, 使虫体低倍镜下呈灰黑色; 大核球形, 位于虫体中靠左, 直径约10—14 μm。
口沟开阔, 占体长约1/3。领区小膜约为15—18片, 口区小膜约5—7片, 两者紧密连接; 领区小膜纤毛极长, 约30—35 μm, 几乎大于虫体长度(图版Ⅰ-14, 图版Ⅱ-24)。环带动基列水平分布, 由34—44个双动基体组成, 位于虫体赤道区靠下, 腹面中央具有小的开口, 约间隔1对毛基粒; 腹动基列位于虫体腹面中部, 前端距环带动基列开口处间隔1对毛基粒, 向下延伸至亚尾端, 由约5—9对毛基粒组成(图版Ⅰ-14、15, 图版Ⅱ-23)。体纤毛长约2 μm。
比较与讨论 该种由宋微波等[4]首次发表, 并包含简单描述。本文对该种形态信息细节进行了补充, 并提供了活体及银染图片。该种与相似种S. stylifer[17]的最大差异在于环带动基列开口(有vs.无)和口区小膜的数目(5—7 vs. 9—13), 此外该种体型为锥形(vs.卵圆形)。
2.6 铃木急游虫Strombidium suzukii Song, et al., 2009 (图版Ⅰ-16—18, 图版Ⅲ-1—5)
![]() 图版 Ⅲ 铃木急游虫、束腰旋游虫、杨科夫平游虫、卡尔平游虫、最小拟盗虫的活体照片(1—3、6—9、11—13、16、20—23)和蛋白银染色制片照片(4—5、10、14—15、17—19、24)1—5. 铃木急游虫, 箭头示前端凸起; 6—10. 束腰旋游虫, 7、8、10中箭头示趋触膜, 9中箭头示肩部射出体; 11—16. 杨科夫平游虫, 14中箭头示趋触膜, 15中箭头示环带动基列和腹面动基列腹面起点, 16中箭头示体后端射出体, 11自宋微波等[4]; 17—19. 卡尔平游虫, 箭头示趋触膜; 20—24. 最小拟盗虫, 箭头示体表黏着颗粒. 比例尺: 20 μm. GK. 环带动基列; VK. 腹面动基列图版 Ⅲ. Photomicrographs of Strombidium suzukii, Spirostrombidium cinctum Parallelostrombidium jankowski, Parallelostrombidium kahli, and Strombidinopsis minima
图版 Ⅲ 铃木急游虫、束腰旋游虫、杨科夫平游虫、卡尔平游虫、最小拟盗虫的活体照片(1—3、6—9、11—13、16、20—23)和蛋白银染色制片照片(4—5、10、14—15、17—19、24)1—5. 铃木急游虫, 箭头示前端凸起; 6—10. 束腰旋游虫, 7、8、10中箭头示趋触膜, 9中箭头示肩部射出体; 11—16. 杨科夫平游虫, 14中箭头示趋触膜, 15中箭头示环带动基列和腹面动基列腹面起点, 16中箭头示体后端射出体, 11自宋微波等[4]; 17—19. 卡尔平游虫, 箭头示趋触膜; 20—24. 最小拟盗虫, 箭头示体表黏着颗粒. 比例尺: 20 μm. GK. 环带动基列; VK. 腹面动基列图版 Ⅲ. Photomicrographs of Strombidium suzukii, Spirostrombidium cinctum Parallelostrombidium jankowski, Parallelostrombidium kahli, and Strombidinopsis minimafrom life (1—3, 6—9, 11—13, 16, 20—23) and after protagol impregnation (4—5, 10, 14—15, 17—19, 24) 1—5. Strombidium suzukii, arrow notes the apical protrusion; 6—10. Spirostrombidium cinctum, arrow in 7, 8, 10 marks the thigmotactic membranelles, arrow in 9 marks the extrusomes on shoulder of dorsal side; 11—16. Parallelostrombidium jankowski, arrow in 14 notes the thigmotactic membranelles, arrows in 15 mark the ventral ends of girdle and ventral kineties, arrow in 16 marks the extrusomes, 11 from Song, et al.[4]; 17—19. Parallelostrombidium kahli, arrow notes the thigmotactic membranelles; 20—24. Strombidinopsis minima, arrow notes the mineral envelope covering the body surface. GK. gridle kinety; VK. ventral kinety本种于2004年4月1日采集自青岛近岸潮间带。
形态学描述 虫体活体大小 (35—50) μm× (35—45) μm, 银染后(35—50) μm × (32—45) μm。体型球形, 口缘右侧隆起形成前端凸起(图版Ⅰ-16, 图版Ⅲ-1、2)。体内含大量微小金色藻类食物颗粒。射出体杆状, 于体中部形成漏斗状(图版Ⅰ-16)。射出体附着点于环带动基列上方形成体表突起(图版Ⅲ-3)。大核球形位于虫体中部。虫体通常在水中缓缓游动, 体绕体轴不停旋转, 受惊扰后, 可沿直线快速游走。
口沟较浅, 占体长1/5。领区小膜约15—16片, 口区小膜约6—7片, 两者相连(图版Ⅰ-17, 图版Ⅲ-4)。环带动基列水平分布, 位于虫体赤道区, 由约50—66双动基体形成闭合环状; 腹动基列位于虫体略右侧腹面, 前端距环带动基列间隔2个双动基体, 后端延伸至虫体末端, 由约15—17个双动基体组成(图版Ⅰ-17、18, 图版Ⅲ-4、5)。
比较与讨论 该种由宋微波等[4]首次发表并进行了简单描述。本文对该种形态信息细节进行了补充, 并提供了活体及银染图片。根据一般的形态学特征(大小, 体形等), 下列几种急游虫应该与铃木急游虫进行比较。
铃木急游虫与Strombidium basimorphum Martin & Montagnes, 1993最为相近, 二者的主要区别为: (1)前者环带动基列为双动基系, 而后者为单动基系; (2)前者环带动基列毛基粒数目较多约101—135个, 且位于虫体前1/3处, 而后者毛基粒50—66个, 位于虫体赤道区[18, 19]。
铃木急游虫与Strombidium taylori Martin & Montagnes, 1993可由下列几点相区别: (1)腹面小膜数目(6—7 vs. 12—15); (2)环带动基列为双动基系(vs. 单动基系); (3)前者腹动基列长, 几乎伸展至环带动基列, 由15—17对毛基粒组成, 后者腹动基列短小, 局限于虫体末端, 由约6—8对毛基粒组成; (4)大核形状(近球形vs. U形)[18]。
与Strombidium compressum (Leegaard, 1915) Kahl, 1932相比, 铃木急游虫个体较大[(35—50) μm× (35—45) μm vs. (17—28) μm× (13—24) μm], 具有较多的领区小膜(15—16 vs. 12—15), 环带动基列由双动基系组成(vs. 环带动基列由单动基系组成), 腹动基列长几乎伸展至环带动基列处(vs. 腹动基列短小, 局限于虫体尾部)[20]。
铃木急游虫可通过下列特征与Strombidium acutum Leegaard, 1915明显区分开: (1)前者仅具有6—7片腹面小膜(vs. 10—22片); (2)环带动基列为双动基系(vs. 单动基系); (3)腹动基列长, 几乎伸展至环带动基列处(无腹动基列)[20]。
与Strombidium emergens (Leegaard, 1915) Kahl, 1932相比, 铃木急游虫具有较少的腹面小膜(6—7 vs. 8—11), 较小的口区(口区约占体长的1/3—1/4 vs. 口区约占体长的1/2—1/3)[20]。
2.7 束腰旋游虫Spirostrombidium cinctum (Kahl, 1932) Petz, et al., 1995 (图版Ⅰ-19—21, 图版Ⅲ-6—10)
本种于2007年11月23日采集自大亚湾近岸潮间带, 水温27.0℃, 盐度31.6‰, pH 8.3。
形态学描述 虫体活体大小(55—70) μm× (35—45) μm, 银染后通常(41—74) μm× (29—52) μm。体型卵圆形, 前端肩部区较平截, 具明显宽阔的前端凸起(图版Ⅰ-19, 图版Ⅲ-6)。体内含大量灰色食物颗粒。射出体沿环带动基列和腹面动基列均匀排列, 此外一列射出体水平排列在背部肩区(图版Ⅰ-19, 图版Ⅲ-9)。球形大核位于虫体中央。
口沟较深, 倾斜向下延伸至体长2/5处(图版Ⅰ-19、20, 图版Ⅲ-7、8)。口区小膜分化为21—28片领区小膜, 3片趋触小膜及10—14片口区小膜。趋触小膜明显较长且向体后方延伸(图版Ⅰ-20, 图版Ⅲ-7、10)。环带动基列由59—94个双动基体组成, 前端开始于腹面中部左侧, 末端终止于腹面右侧亚尾端。腹面动基列包含16—38个双动基体, 位于腹面右侧, 向上延伸至接近环带动基列。另一列片段状的额外动基列位于体左侧肩部区, 由14—31片双动基体组成(图版Ⅰ-20、21)。
比较与讨论 该种最先由Kahl[21]发现; 基于青岛种群的研究, Xu和Song[22]对该种的纤毛图式进行了揭示。本种群是该种首次在亚热带海域报道, 形态特征数据均与青岛种群相符。但本种群发现的背部肩区射出体排列带, 在原始报道中并未描述。射出体的分布通常与体动基列分布相吻合, 因此该背部肩区射出体排列带与肩区分布的额外动基列的位置一致, 表明该射出体排列带可能为稳定存在, 推测原始报道未描述可能由于细节观察的忽略。基于对本种群活体形态的详细观察, 准确的射出体排列模式及图示在此处给出。
2.8 杨科夫平游虫Parallelostrombidium jankow-skii (Song, et al., 2009) Song, et al., 2018 (图版Ⅰ-22—26, 图版Ⅲ-11—16)
本种于2002年8月10日采集自青岛虾养殖池。
形态学描述 虫体活体大小(110—150) μm× (50—75) μm, 银染后(100—140) μm× (48—68) μm。体型长锥形, 领区右侧隆起形成前端凸起, 后端尖细(图版Ⅰ-22、23, 图版Ⅲ-11—13)。环带动基列后方体表覆盖透明壳层, 壳层向下延伸形成尖尾, 无伸缩性(图版Ⅰ-22、23, 图版Ⅲ-11)。射出体沿环带动基列分布并延伸到体末端, 附着点在体表形成凸起(图版Ⅲ-11、16)。多枚大核连接在一起, 呈鹿角状。
口沟倾斜延伸占体长1/4。领区小膜具24—28片, 口区小膜16—19片, 两者之间具2片趋触膜(图版Ⅲ-14)。趋触膜基部略长于其他小膜, 纤毛与领区小膜纤毛长度相当。环带动基列开始于腹面趋触膜下方, 螺旋绕体一周半, 末端终止于虫体背面尾端, 由约93—126个双动基体组成; 腹面动基列起始于环带动基列右端下方, 距环带动基列约2对毛基粒, 腹面动基列与环带动基列下方部分平行, 右侧倾斜延伸至虫体背面尾端, 由约30—39个双动基体组成(图版Ⅰ-24, 图版Ⅲ-15)。腹面动基列与环带动基列平行部分方向一致, 每个双动基体上着生纤毛的毛基体均在上方。
早期发生个体显示口原基位于环带动基列右端的左侧, 腹面动基列表膜下方(图版Ⅰ-25); 后期发生个体纤毛图式显示随着口原基的发展及旋转, 口原基从腹面动基列与环带动基列斜向部分之间发生至体表, 腹面及环带动基列毛基粒增殖变长, 同时腹面动基列分化成两段, 其中后半段成为后仔虫的腹面动基列, 并保持与环带动基列后段平行, 前半段成为前仔虫的腹面动基列, 而环带动基列水平部分保留给前仔虫, 后半段保留给后仔虫(图版Ⅰ-26); 推测后续发生将出现环带动基列在虫体背部断裂, 后半段随着后仔虫口区的螺旋延伸至后仔虫腹面, 形成完整的后仔虫腹面动基列, 而原环带动基列断裂后的前半段则向前仔虫左侧延伸螺旋, 最终与前仔虫腹面动基列平行, 形成完整的前仔虫腹面动基列。
比较与讨论 该种最初被命名为Omegastrombidium jankowskii, 由宋微波等[4]首次发表并对该种进行了简单描述。后经Song等[23]对该种另外一个种群的纤毛图式进行深入研究, 发现该种的体动基列排列模式在原始描述中被误读: 环带动基列腹面右侧弯曲处并不连续而是具一开口, 而对开口下方的纵向动基列片段进一步观察发现其方向为向上(双动基体中着生纤毛的毛基体在上), 但开口右侧的横向动基列方向为向左(双动基体中着生纤毛的毛基体在左), 表明两者在细胞发生过程中来自不同的动基列原基, 证实纵向体动基列为腹面动基列。这一结果进而揭示该种应隶属于平游虫属, Song等[23]因此将该种种名进行了修订, 命名为Parallelostrombidium jankowskii。本文对该种的原始种群进行了进一步观察, 发现原始描述中对体动基列排列方式确实存在如上误读, 证实了该种确实应隶属于平游虫属。基于正确的体动基列排列方式解读, 本文对原始种群的纤毛图式做了详细描述, 对该种群活体照片进行了补充, 此外对早期及后期发生个体纤毛模式进行了描述。
该种群与Song等[23]的种群相比, 虫体体表覆盖透明壳层在后者中并未发现, 可能为种群差异; 大核形态不同(鹿角状vs.多枚椭圆形大核分散在体内), 推测前者种群可能均处于细胞发生前期, 大核发生融合因而产生鹿角状; 此外本种群环带及腹面动基列后段螺旋至体背部(vs.位于体右侧), 可能因本种群蛋白银制片虫体体位略偏左。
2.9 卡尔平游虫Parallelostrombidium kahli (Song, et al., 2009) Song, et al., 2018 (图版Ⅰ-27、28, 图版Ⅲ-17—19)
本种于2005年10月28日采集自青岛近岸潮间带, 水温20.8℃, 盐度21.3‰, pH 7.7。
形态学描述 虫体银染后(60—80) μm × (40—50) μm。体型长锥形, 领区右侧隆起形成前端凸起, 后端变窄略尖。球形大核数十枚, 散布于体内(图版Ⅰ-27)。口沟较浅, 向右延伸占体长1/5。领区小膜约50—60片, 口区小膜10—15片, 两者之间具2片趋触膜(图版Ⅰ-27, 图版Ⅲ-17)。趋触膜基部明显长于其他小膜。环带动基列起始于背部左侧肩部, 水平延伸于口围带下绕体一周, 随后在背面中部向下螺旋绕体约1.5周, 末端终止于虫体腹面尾端, 由约139—164个双动基体组成; 腹面动基列起始于环带动基列前端下方, 距环带动基列约2对毛基粒, 腹面动基列与环带动基列下方部分平行, 右侧倾斜延伸至虫体背面尾端, 由约75—88个双动基体组成(图版Ⅰ-27、28, 图版Ⅲ-18、19)。腹面动基列与环带动基列平行部分方向一致, 每个双动基体上着生纤毛的毛基体均在上方。
比较与讨论 该种最初被命名为Omegastrombidium kahli, 由宋微波等[4]首次发表并对该种进行了简单描述。后经Song等[23]对该种另外一个种群的纤毛图式进行深入研究, 发现该种的体动基列排列模式在原始描述中存在与Parallelostrombidium jankowskii类似的误读: 环带动基列腹面右侧弯曲处下方的纵向动基列片段应为腹面动基列。Song等 [23]因此将该种种名进行了修订, 命名为Parallelostrombidium kahli。本文对该种的原始种群进行了进一步观察, 同样发现原始描述中对体动基列排列方式确实存在如上误读, 证实了该种确实应隶属于平游虫属。基于正确的体动基列排列方式解读, 本文对原始种群的纤毛图式做了详细描述。
该种群与Song等[23]的种群相比, 本种群纤毛图式末端终止于虫体背部末端(vs.位于虫体腹面末端), 可能因本种群蛋白银制片虫体体位略偏左。
2.10 最小拟盗虫Strombidinopsis minima (Gruber, 1884) Song & Bradbury, 1998 (图版Ⅰ-29、30, 图版Ⅲ-20—24)
本种于2010年3月29日采集自湛江近岸潮间带, 水温20.8℃, 盐度21.3‰, pH 7.7。
形态学描述 虫体活体大小 (40—55) μm× (30—45) μm, 银染后(38—61) μm× (41—60) μm。体型椭球形, 后端钝圆(图版Ⅰ-29、30, 图版Ⅲ-20、21)。全身表面黏着大量砂质颗粒使体表明显粗糙(图版Ⅰ-29, 图版Ⅲ-20、23)。两个卵圆形大核位于口区下方, 水平排布。虫体喜将口区小膜附着在基质上, 向基质中钻行, 同时身体螺旋旋转(图版Ⅲ-21)。
领区小膜具20—24片小膜, 小膜基部等长, 口沟处无小膜伸长。小膜纤毛内外等长, 运动时无规律摆动(图版Ⅰ-29)。口沟内部具一片较短的口区小膜, 该小膜未紧贴领区小膜(图版Ⅲ-22、24)。约20—23列体动基列纵向均匀排列, 末端终止于体后部1/5处。每列体动基列由约12—16个双动基体组成, 这些动基体于体动基列前段密集排列而于后段稀疏排列(图版Ⅰ-30)。
比较与讨论 最小拟盗虫广泛分布于世界各海域, 例如地中海[24]、大西洋西岸[25]、青岛近岸[26]。Agatha[24]整合多个种群的信息, 对该种进行了详细描述, 本工作系首次在我国南海发现该种, 本工作对该种的活体描述及照片进行了详细的补充。作为该种的重要分类学特征, 目前体表黏着颗粒发现于该种的所有种群中[24—26]。与中国青岛种群相比, 本种群每列体动基列中具有较少的双动基体(12—16 vs. 18—22), 属种群间差异。
-
图 1 黄颡鱼(Pf: Pelteobagrus fulvidraco)WNT5A和WNT5B氨基酸序列与斑马鱼(Dr: Danio rerio)、墨西哥丽脂鲤(Am: Astyanax mexicanus)和人类(Hs: Homo sapiens)比对分析
灰色阴影部分表示相同的氨基酸残基; 上划线表示预测的信号肽酶切位点; 星号表示24个保守的半胱氨酸残基; 井号表示在寡糖连接一致区域的4个保守的天冬酰胺残基; 上划线表示Wnt-1家族特征, 实心点表示酪氨酸硫酸化位点
Figure 1. Alignment of P. fulvidraco (Pf: Pelteobagrus fulvidraco) WNT5A and WNT5B amino acid sequences with other species (Dr: Danio rerio; Am: Astyanax mexicanus; Hs: Homo sapiens)
The identical residues are shaded with light grey. The region of potential signal peptidase cleavage sites (overline), 24 cysteines residues conserved among most Wnt5a and Wnt5b proteins (asterisks), 4 conserved asparagine residues in oligosaccharide linkage consensus sequences (sharp), the Wnt1 “family signature” (double overline) and the conserved tyrosine sulfation site (dot) are indicated
图 2 黄颡鱼(Pf: Pelteobagrus fulvidraco) WNT7A氨基酸序列与斑马鱼(Dr: Danio rerio)、青鳉(Ol: Oryzias latipes)和人类(Hs: Homo sapiens)和其他硬骨鱼类比对分析
灰色阴影部分表示相同的氨基酸残基; 星号表示24个保守的半胱氨酸残基
Figure 2. Alignment of P. fulvidraco (Pf: Pelteobagrus fulvidraco) WNT7A amino acid sequences with other species (Dr: Danio rerio; Ol: Oryzias latipes; Hs: Homo sapiens)
The identical residues are shaded with light grey. 24 cysteines residues conserved among most Wnt7a proteins (asterisks) are indicated
图 3 黄颡鱼(Pf: Pelteobagrus fulvidraco) WNT9B氨基酸序列与斑马鱼(Dr: Danio rerio)、墨西哥丽脂鲤(Am: Astyanax mexicanus)和人类(Hs: Homo sapiens)比对分析
灰色阴影部分表示相同的氨基酸残基; 上划线表示预测的信号肽酶切位点; 波浪号表示潜在的N糖基化位点; 星号表示Wnt9b氨基酸中保守的半胱氨酸残基
Figure 3. Alignment of P. fulvidraco (Pf: Pelteobagrus fulvidraco) WNT9B amino acid sequences with other species (Dr: Danio rerio; Am: Astyanax mexicanus; Hs: Homo sapiens)
The identical residues are shaded with light grey. The region of potential signal peptidase cleavage sites (overlined), the potential N-linked glycosylation site (tilde), 23 cysteines residues conserved among most Wnt9b proteins (asterisks) are indicated
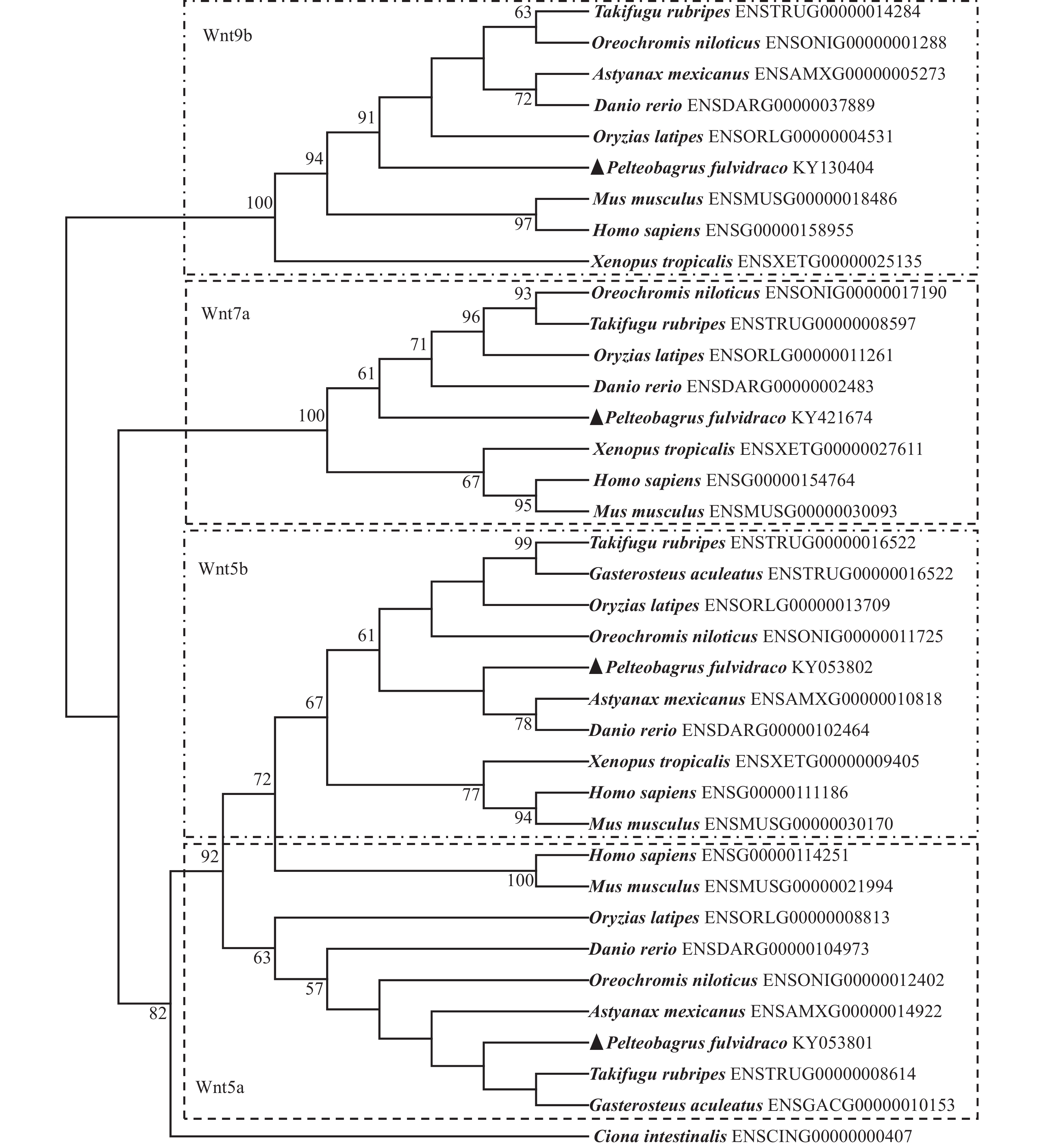
图 4 脊索动物Wnts系统进化树
图中▲所示为黄颡鱼。选择的分析方法为NJ, 每个节点的可信值进行1000次重复计算。物种名称后为GenBank和EMBL登录号
Figure 4. Phylogenetic tree based on the protein sequences of Wnts from P. fulvidraco (▲) and other chordate species using the neighbor-joining (NJ) method with 1000 bootstrap replicates
GenBank and EMBL accession numbers were shown next to each species
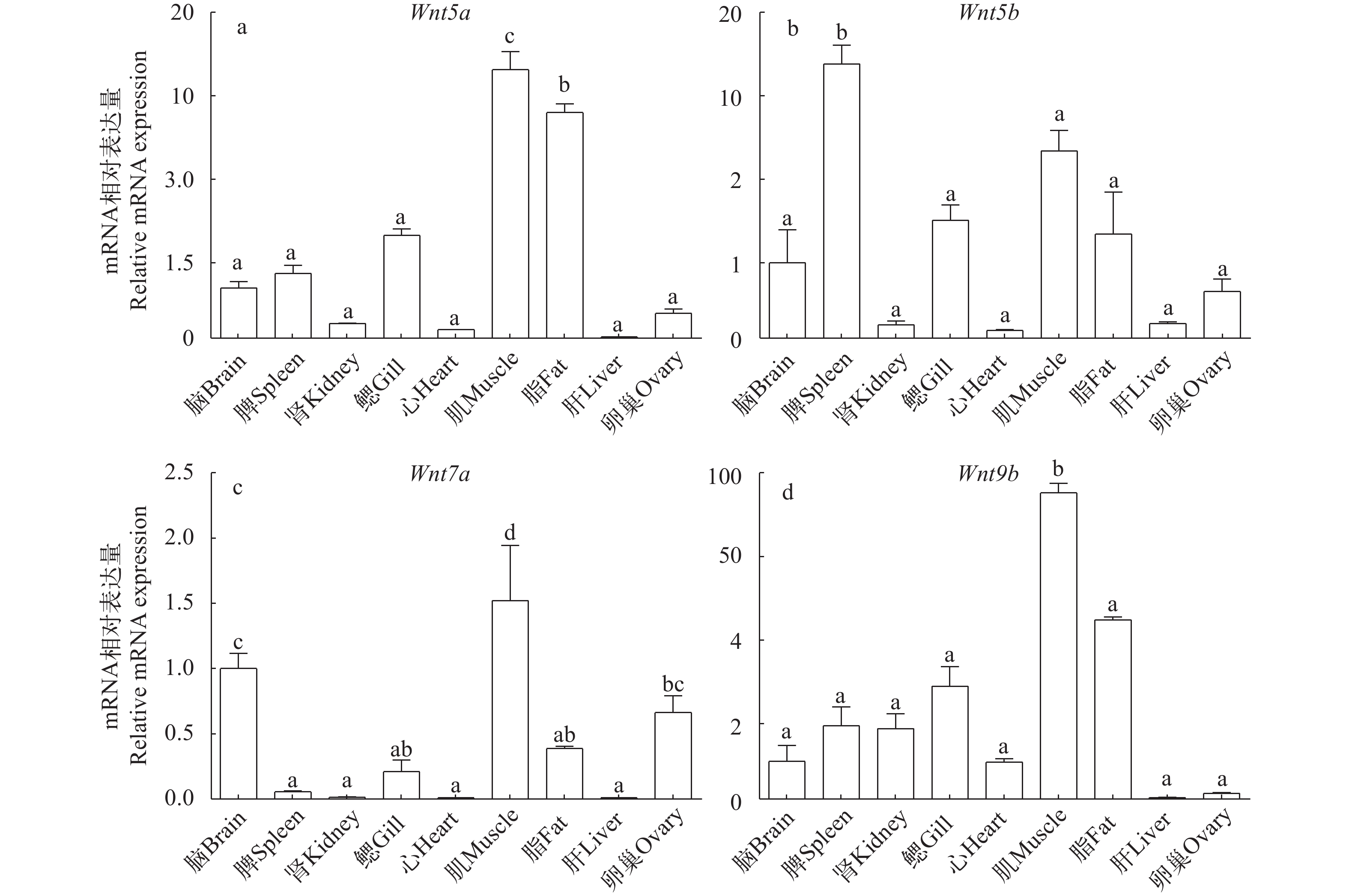
图 5 黄颡鱼Wnts组织特异性表达分析
相对mRNA水平通过qPCR定量, 数值 (平均值±标准误, n=3) 用内参基因 (β-actin和gadph) 标准化; 不同字母表示同一基因在不同组织中表达差异显著(P<0.05)
Figure 5. The mRNA level of Wnts in the brain, spleen, kindey, gill, heart, muscle, fat, liver and ovary
Data (mean±SEM, n=3 replicate tanks, and 3 fish were sampled for each tank) were normalized to housekeeping gene (β-actin and gadph). Bars that do not share a letter are significantly different among different tissues (P<0.05)
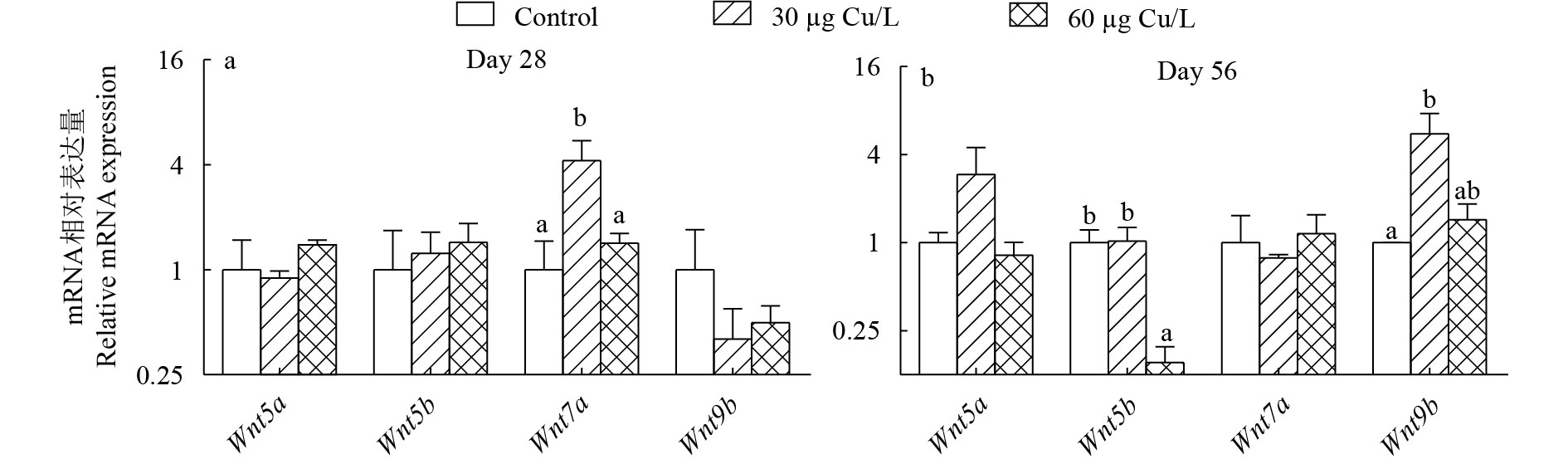
图 6 第28天和第56天铜暴露对黄颡鱼卵巢中Wnts基因(Wnt5a、Wnt5b、Wnt7a和Wnt9b)mRNA表达的影响
结果用平均值±标准误表示 (Mean±SEM, n=3), 用内参基因(β-actin和gapdh)标准化; 不同字母表示数据间有显著差异(P<0.05)
Figure 6. Effect of Cu exposure on the mRNA levels of genes (Wnt5a, Wnt5b, Wnt7a and Wnt9b) in the ovary of P. fulvidraco on days 28 and 56
Data (mean±SEM, n=3 replicate tanks, and 3 fish were sampled for each tank) were normalized to housekeeping gene (β-actin and gapdh). Different letters indicate significant differences among groups (P<0.05)
表 1 Wnt5a、Wnt5b、Wnt7a和Wnt9b基因克隆的引物序列
Table 1 Primers used for the cDNAs cloning of Wnt5a, Wnt5b, Wnt7a and Wnt9b genes
引物名Primers 序列Sequences (5′—3′) Primers for partial fragment Wnt5a-F TACGACAAGTDCTTGTCCGG Wnt5a-R CTTGCDCACAAACTGATCGA Wnt5b-F TACCTACABCCTTACTCCGT Wnt5b-R CTTGCAVACGAACTGGTCGA Wnt7a-F CTCATACCKCAAACCCATGG Wnt7a-R CTCKTCCACAGCACATCAAG Wnt9b-F CGTGANTCCAAAGTAAGC Wnt9b-R GCAGCAGGCAKGCGGTCC Primers for 3′ RACE PCR 3′Wnt5a-1 GAGCCGAGCCCAGACTAC 3′Wnt5a-2 ACGGGCTCGCTGGGCACG 3′Wnt5b-1 TAACGCTCCCACCACCGA 3′Wnt5b-2 GCACAGGCTCGCTGGGAA 3′Wnt7a-1 ACTTGATGTGCTGTGGACGAG 3′Wnt7a-2 CCTATGTTAGTAAGCATCCGTGA 3′Wnt9b-1 ACTTTATGAGAAGAACGA 3′Wnt9b-2 GTCATTTACCTGTCTATC 3′ RACE Outer TACCGTCGTTCCACTAGTGATTT 3′ RACE Inner CGCGGATCCTCCACTAGTGATTTCACTATAGG Primers for 5′ RACE PCR 5′Wnt5a-1 TTCATAGCCAGAGACCACCA 5′Wnt5a-2 TACTGCATGTGGTCCTGGTA 5′Wnt5b-1 AGCTGGCACAGCTTCCTCTG 5′Wnt5b-2 TCCACCGTGCTGCAGTTCCA 5′Wnt7a-1 ATGCTCCCTGCTTTAGTGT 5′Wnt7a-2 CCCTTACCTGGTGCTATTT 5′Wnt9b-1 CGTGAGTCCAAAGTAAGC 5′Wnt9b-2 ATTGCGAAACTGGTAGCG 5′ RACE Outer CATGGCTACATGCTGACAGCCTA 5′ RACE Inner CGCGGATCCACAGCCTACTGATGATCAGTCGATG Note: K-G/T; M-A/C; R-A/G; S-G/T; Y-C/T; B-G/T/C; D-G/A/T; H-A/T/C; V-G/A/C; N-A/T/G/C 表 2 荧光定量引物
Table 2 Primers used for real-time PCR
基因名
Gene正向引物
Forward primer (5′—3′)反向引物
Reverse primer (5′—3′)长度
Size (bp)登录号
Accession No.Wnt5a AAGACCTTCCACGAGACTGG ATCATGAGTCGTGCGCTTTC 104 KY053801 Wnt5b ATAGATCATGCACGCACCCT AACTCACCTACACGCCGGAA 144 KY053802 Wnt7a TTCACCTATGCCATCATTGCT CACCCCACTTCCAACCCTC 117 KY421674 Wnt9b GAAGTACAGCACCAGGTTCCTC TTCCAGCATGTCCGCACT 162 KY130404 β-actin GCACAGTAAAGGCGTTGTGA ACATCTGCTGGAAGGTGGAC 127 EU161065 Gadph CACTGCCACCCAGAAGACA AGGGACACGGAAAGCCAT 166 JQ068865 18S rRNA CTGCCGGTGGTCTTCTTCCA ATTCAGCGGGTCGTCTCGTC 185 GQ465236 B2m GCTGATCTGCCATGTGAGTG TGTCTGACACTGCAGCTGTA 185 KP938520 Ubce TCAAGAAGAGCCAGTGGAGG TAGGGGTAGTCGATGGGGAA 147 KP938524 Hprt ATGCTTCTGACCTGGAACGT TTGCGGTTCAGTGCTTTGAT 180 KP938523 Ef1a TGGAAGGTCGAGCGTAAGG GCAGAGGAAGGCGAAGAGG 112 KR061492 -
[1] Cabrera C V, Alonso M C, Johnston P et al. Phenocopies induced with antisense RNA identify the wingless gene[J]. Cell, 1987, 50(4): 659—663
[2] Huelsken J, Behrens J. The Wnt signalling pathway[J]. Journal of Cell Science, 2002, 115(21): 3977—3978
[3] Logan C Y, Nusse R. The Wnt signaling pathway in development and disease[J]. Annual Review of Cell and Developmental Biology, 2004, 20(1): 781—810
[4] MacDonald B T, Tamai K, He X. Wnt/β-catenin signaling: components, mechanisms, and diseases[J]. Developmental Cell, 2009, 17(1): 9—26
[5] 尹定子, 宋海云. Wnt信号通路: 调控机理和生物学意义. 中国细胞生物学学报, 2011, 33(2): 103—111 Yin D Z, Song H Y. Regulation of Wnt Signaling: Mechanisms and biological significance[J]. Chinese Journal of Cell Biology, 2011, 33(2): 103—111
尹定子, 宋海云. Wnt信号通路: 调控机理和生物学意义. 中国细胞生物学学报, 2011, 33(2): 103—111[6] Komiya Y, Habas R. Wnt signal transduction pathways[J]. Organogenesis, 2008, 4(2): 68—75
[7] Wu G C, Chang C F. Wnt4 is associated with the development of ovarian tissue in the protandrous black Porgy, Acanthopagrus schlegeli[J]. Biology of Reproduction, 2009, 81(6): 1073—1082
[8] Boerboom D, Paquet M, Hsieh M et al. Misregulated Wnt/β-catenin signaling leads to ovarian granulosa cell tumor development[J]. Cancer Research, 2005, 65(20): 9206—9215
[9] 华芳, 孙卫斌, 葛久禹. 斑马鱼Shh, Wnt5b和Catnb特异性基因片段的克隆. 口腔医学研究, 2009, 25(2): 129—131 Hua F, Sun W B, Gei J Y. Molecular cloning of Shh, Wnt5b and Catnb specific gene fragments from zebrafish embryos[J]. Journal of Oral Science Research, 2009, 25(2): 129—131
华芳, 孙卫斌, 葛久禹. 斑马鱼Shh, Wnt5b和Catnb特异性基因片段的克隆. 口腔医学研究, 2009, 25(2): 129—131[10] Liu A, Majumdar A, Schauerte H E, et al. Zebrafish wnt4b expression in the floor plate is altered in sonic hedgehog and gli-2 mutants[J]. Mechanisms of Development, 2000, 91(1): 409—413
[11] 李建中, 刘琼, 王德寿等. 日本青鳉2种WNT4基因的克隆及鉴定. 水生生物学报, 2012, 36(5): 983—986 Li J Z, Liu Q, Wang D S, et al. Molecular cloning and identification of two WNT4 genes from the medaka (Oryzias latipes)[J]. Acta Hydrobiologica Sinica, 2012, 36(5): 983—986
李建中, 刘琼, 王德寿等. 日本青鳉2种WNT4基因的克隆及鉴定. 水生生物学报, 2012, 36(5): 983—986[12] 曹梅, 王兴强, 崔春辉, 等. 鲶鱼Wnt基因家族序列分析. 淮海工学院学报(自然科学版), 2017, 26(1): 76—81 Cao M, Wang X, Cui C, et al. Sequence analysis of Wnt gene family from catfish[J]. Journal of Huaihai Insititute of Technology (Natural Science Edition), 2017, 26(1): 76—81
曹梅, 王兴强, 崔春辉, 等. 鲶鱼Wnt基因家族序列分析. 淮海工学院学报(自然科学版), 2017, 26(1): 76—81[13] Watanabe T, Kiron V, Satoh S. Trace minerals in fish nutrition[J]. Aquaculture, 1997, 151(1): 185—207
[14] Zhang L H, Luo Z, Song Y F et al. Effects and mechanisms of waterborne copper exposure influencing ovary development and related hormones secretion in yellow catfish Pelteobagrus fulvidraco[J]. Aquatic Toxicology, 2016, 178: 88—98
[15] Sanchez A M, Viganò P, Quattrone F, et al. The WNT/β-catenin signaling pathway and expression of survival promoting genes in luteinized granulosa cells: endometriosis as a paradigm for a dysregulated apoptosis pathway[J]. Fertility and Sterility, 2014, 101(6): 1688—1696
[16] Fan H Y, O’Connor A, Shitanaka M, et al. Beta-catenin (CTNNB1) promotes preovulatory follicular development but represses LH-mediate ovulation and luteinization[J]. Molecular Endocrinology, 2010, 24(8): 1529—1542
[17] Wu K, Zheng J L, Luo Z, et al. Carnitine palmitoyltransferases I gene in Synechogobius hasta: cloning, mRNA expression and transcriptional regulation by insulin in vitro[J]. Gene, 2016, 576(1): 429—440
[18] Wei C C, Luo Z, Song Y F, et al. Identification of autophagy related genes LC3 and ATG4 from yellow catfish Pelteobagrus fulvidraco and their transcriptional responses to waterborne and dietborne zinc exposure[J]. Chemosphere, 2017, 175: 228—238
[19] Tamura K, Peterson D, Peterson N et al. MEGA5: molecular evolutionary genetics analysis using maximum likelihood, evolutionary distance, and maximum parsimony methods[J]. Molecular Biology and Evolution, 2011, 28(10): 2731—2739
[20] Jones D T, Taylor W R, Thornton J M. The rapid generation of mutation data matrices from protein sequences[J]. Computer Applications in the Biosciences: CABIOS, 1992, 8(3): 275—282
[21] Livak K J, Schmittgen T D. Analysis of relative gene expression data using real-time quantitative PCR and the 2–ΔΔCT method[J]. Methods, 2001, 25(4): 402—408
[22] Clark C C, Cohen I, Eichstetter I et al. Molecular cloning of the human proto-oncogene Wnt-5A and mapping of the gene (WNT5A) to chromosome 3p14-p21[J]. Genomics, 1993, 18(2): 249—260
[23] Qian J, Jiang Z, Li M et al. Mouse Wnt9b transforming activity, tissue-specific expression, and evolution[J]. Genomics, 2003, 81(1): 34—46
[24] Fradkin L G, van Schie M, Wouda R R et al. The Drosophila Wnt5 protein mediates selective axon fasciculation in the embryonic central nervous system[J]. Developmental Biology, 2004, 272(2): 362—375
[25] 周春娅, 朱玲, 潘滢, 等. 海蜇(Rhopilema esculentum) Wnt5基因: cDNA克隆、基因组结构与表达. 海洋与湖沼, 2013, 44(4): 1115—1122 Zhou C Y, Zhu L, Pan Y, et al. Wnt5 gene from Rhopilema Esculentum: cDNA cloning, genomic organization and mRNA expression[J]. Oceanologia Et Limnologia Sinica, 2013, 44(4): 1115—1122
周春娅, 朱玲, 潘滢, 等. 海蜇(Rhopilema esculentum) Wnt5基因: cDNA克隆、基因组结构与表达. 海洋与湖沼, 2013, 44(4): 1115—1122[26] Mason J O, Kitajewski J, Varmus H E. Mutational analysis of mouse Wnt-1 identifies two temperature-sensitive alleles and attributes of Wnt-1 protein essential for transformation of a mammary cell line[J]. Molecular Biology of the Cell, 1992, 3(5): 521—533
[27] Lejeune S, Huguet E L, Hamby A, et al. WNT5A cloning, expression and upregulation in human primary breast cancers[J]. Clinical Cancer Research, 1995, 1(2): 215—222
[28] Bui T D, Lako M, Lejeune S et al. Isolation of a full-length WNT7A gene implicated in limb development and cell transformation, and mapping to chromosome 3p25[J]. Gene, 1997, 189(1): 25—29
[29] Topol L, Jiang X, Choi H et al. Wnt-5a inhibits the canonical WNT pathway by promoting GSK-3-independent beta-catenin degradation[J]. The Journal of Cell Biology, 2003, 162(5): 899—908
-
期刊类型引用(1)
1. 池洪树,江秋欢,潘滢,林能锋. 一株寄生于大黄鱼的盾纤毛虫分子鉴定与系统进化分析. 福建畜牧兽医. 2023(04): 1-6 .  百度学术
百度学术
其他类型引用(1)




 下载:
下载: