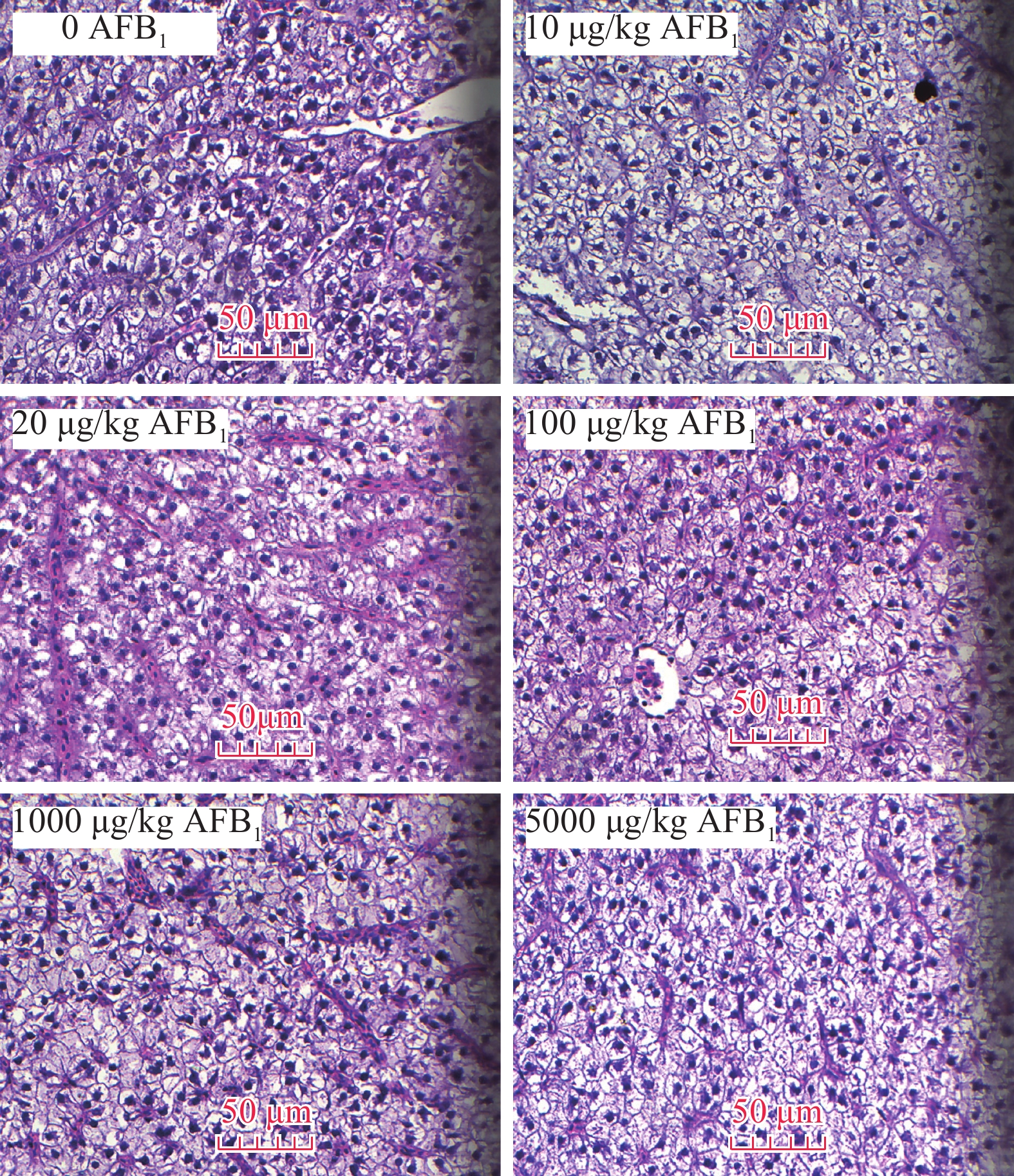
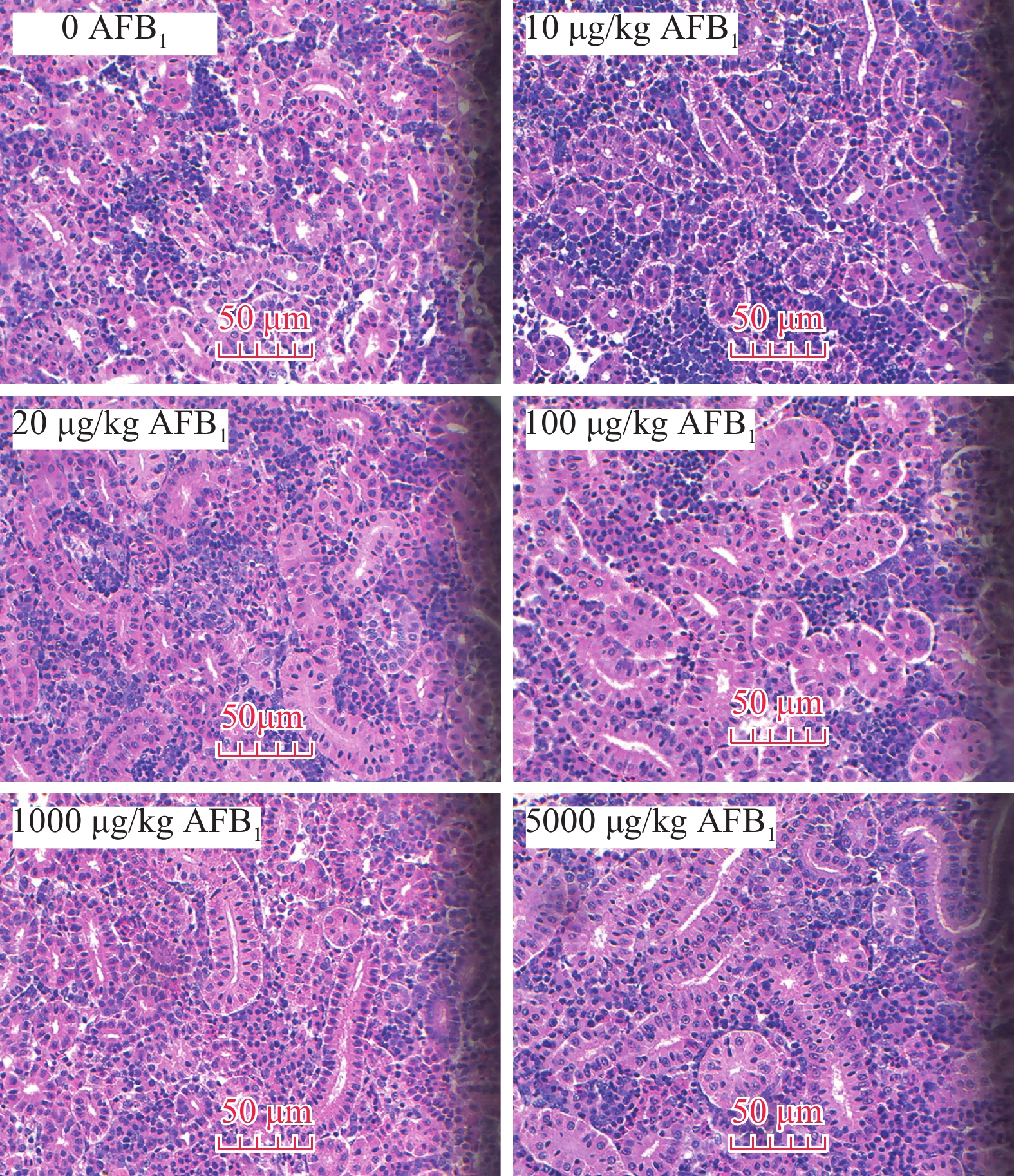
EFFECTS OF AFLATOXIN B1 ON GROWTH AND TISSUE ACCUMULATION OF JUVENILE GRASS CARP (CTENOPHARYNGODON IDELLUS)
-
摘要: 以含不同浓度黄曲霉毒素B1(AFB1)(0、10、20、100、1000和5000 μg/kg饲料)的6种等氮等能(32.96%蛋白质, 14.55 kJ/g能量)配合饲料饲喂平均初始体质量为(2.90±0.16) g草鱼(Ctenopharyngodon idellus)幼鱼84d, 探讨AFB1对草鱼幼鱼生长、肝胰脏和肾脏组织结构以及鱼体肌肉中的毒素积累的影响。实验分为6个实验组, 每组3个平行。结果表明, 在整个实验过程中各实验组幼鱼的行为均未表现出异常, 各组幼鱼的存活率、终末体重、摄食率、特定生长率、饲料效率、肝体比、脏体比均无显著差异。饲料AFB1水平对草鱼幼鱼血清谷丙转氨酶(ALT)、谷草转氨酶(AST)、碱性磷酸酶(AKP)、超氧化物岐化酶(SOD)和谷胱甘肽过氧化物酶(GSH-Px)活性均无显著影响。各毒素组和对照组肝胰脏、肾脏组织学观察中未发现病理变化。摄食AFB1≤1000 μg/kg的草鱼幼鱼肌肉中未检测出AFB1残留, 仅在5000 μg/kg实验组中检测出肌肉中含有(1.21±0.18) μg/kg的AFB1, 低于FDA食品安全限定标准。由此可见, 草鱼幼鱼至少可耐受AFB1含量达5000 μg/kg饲料(实测值: 4979.2 μg/kg饲料) 84d。Abstract: A 84-day feeding trial was conducted to evaluate the effects of dietary aflatoxin B1 (AFB1) on growth, physiological responses, histological changes, and accumulation in juvenile grass carp (Ctenopharyngodon idellus). Triplicate groups of grass carp [(2.90±0.16) g] were fed with six semipurified diets formulated with isonitrogenous (crude protein: 32.96%), isocaloric (gross energy: 14.55 kJ/g) containing 0, 10, 20, 100, 1000 and 5000 μg/kg AFB1. AFB1 did not significantly impact behavior, the survival rate, final body weight (FBW), feeding rate (FR), specific growth rate (SGR) or feed efficiency (FE). No significant differences were found in hepatosomatic index (HSI) and viscera index (VSI) among all groups. AFB1 had no significant effect in activities of serum alanine aminotransferase (ALT), aspartate aminotransferase (AST), alkaline phosphatase (ALP), superoxide dismutase (SOD) and glutathione peroxidase (GSH-Px). No significant histological lesions in hepatopancreas and kidney were identified between the control and increasing AFB1 treatments. No AFB1 residue was detected in muscles when fish fed with AFB1 up to 1000 μg/kg, however, tiny dose [(1.21±0.18) μg/kg] of AFB1 were detected in muscles in the group with 5000 μg/kg AFB1, which was below the safety limitation of FDA. The results indicated that juvenile grass carp is a little susceptible species to AFB1 exposure up to approximately 5000 μg/kg diet (determined level was 4979.2 μg/kg diet), at least for 84 days.
-
Keywords:
- Aflatoxin B1 /
- Ctenopharyngodon idellus /
- Growth /
- Liver /
- Kidney /
- Accumulation
-
年龄鉴定是研究鱼类生物学和生态学特性的重要组成部分, 也是分析和评价鱼类种群数量变动的基本依据之一[1]。鱼类年龄鉴定最普遍的方法是钙化组织分析法[2]。对于裂腹鱼类而言, 受特定生长环境的影响, 不同种类、不同阶段个体的鉴定材料年轮特征各不相同, 呈现出多样化的特点[3]。由于遗传差异和生存环境的差异, 鱼类的生长呈现出不同特点, 不同钙化组织上的年轮特征也表现各异。因此需要对不同的年龄材料进行对比, 最终选出最佳的年龄材料[4]。
双须叶须鱼(Ptychobarbus dipogon)隶属于裂腹鱼亚科(Schizothoracinae), 叶须鱼属(Ptychobarbus), 主要分布在西藏雅鲁藏布江中游干支流砂石底质的缓流处[5]。双须叶须鱼独特的种群特征、生活地理环境决定了其对环境变化和人为干扰极为敏感和脆弱[6]。近年来, 随着水利交通工程建设、渔业捕捞及工程材料索取加剧, 双须叶须鱼的种群数量和种群资源下降, 对双须叶须鱼种群资源构成了威胁。双须叶须鱼作为一个极为脆弱的种群资源, 为保护该物种的可持续性和稳定的种群而做出相应的管理是至关重要的[7]。杨鑫[6]主要研究雅鲁藏布江中游双须叶须鱼的耳石和脊椎骨两种年龄材料, Li等[7]主要研究雅鲁藏布江及其支流流域双须叶须鱼三对耳石年龄材料和微耳石的微结构特征及日增量。而本文研究主要是研究拉萨河流域双须叶须鱼8种年龄材料的年轮特征和年龄鉴定。
年龄鉴定结果可以阐明鱼类生长、性成熟年龄, 直接关系到鱼类种群分析与资源评估现状[8]。因此, 评估和比较每个物种所使用的年龄材料的研究是最基础和必要的内容[9]。本文对双须叶须鱼的微耳石、星耳石、脊椎骨、鳃盖骨、臀鳞、胸鳞、侧线鳞和背鳞等8种年龄材料的年轮特征进行了描述, 并对8种材料鉴定年龄的准确性和精确性进行了比较研究, 旨在为其生长特征、种群动态和资源变动提供可靠的年龄依据。
1. 材料与方法
1.1 样本采集
样本于2014年2月至12月在拉萨河上游采集双须叶须鱼193尾。全部测量全长、体长和体重, 长度精确到1 mm, 重量精确到0.1 g。取出左右微耳石、左右星耳石、鳃盖骨和6—8枚脊椎骨以及4种鳞片。样品用清水清洗, 晾干后放入封口袋冷冻保存。
1.2 年龄材料处理
微耳石 将微耳石远极面朝上, 用指甲油包埋, 固定在载玻片上, 静置, 让其凝固, 然后先用#1500的砂纸打磨, 再用#2000#的砂纸抛光, 打磨期间时刻加水, 并随时在显微镜下观察。直至微耳石核区年轮清晰为止, 最后放在显微镜下拍照保存。
星耳石 将星耳石内侧面朝上, 用指甲油包埋, 固定在载玻片上, 静置, 让其凝固。首先用#1500的砂纸打磨。再用#2000的砂纸抛光, 打磨期间时刻加水, 并在显微镜下拍照保存。
脊椎骨 将脊椎骨放入开水中浸泡1—2min, 用牙刷轻轻刷去附着的肌肉和结缔组织, 剪去多余的骨棘, 从中间将脊椎骨剪断, 静置让其干燥。调整好角度在显微镜下拍照保存。
鳃盖骨 将鳃盖骨放入开水中1min, 用牙刷剔除附着的肌肉的结缔组织, 让其自然干燥, 然后放在体视显微镜下用透射光观察, 并拍照保存。
鳞片 将鳞片放入清水中, 用牙刷轻轻刷去附着的黏膜, 取6片放在载玻片上, 然后盖上载玻片, 用胶带固定并用记号笔编号。最后放在显微镜下拍照保存。
1.3 年龄鉴定方法及年轮特征描述
根据殷名称[10]《鱼类生态学》的年轮鉴别特点及鉴定和分析鱼类年龄的方法, 在不清楚样本大小、性别的情况下对八种年龄材料进行年龄鉴定。每个年龄材料的年龄由同一观察者进行2次独立鉴定, 时间间隔不少于1周。
以体长大小为依据, 划分低龄、中龄和高龄3个年龄段[11], 并根据每一年龄段的同一样本, 描述8种年龄材料的年轮特征。
1.4 八种年龄材料的差异性
平均年龄的显著性分析 对8种年龄材料的平均年龄读数采用单因素方差分析(ANOVA)和多重比较进行统计检验和分析, 来解释8种年龄材料鉴定结果的差异性。
平均百分比误差(IAPE) 采用平均百分比误差(IAPE)来计算不同观察者年龄鉴定结果的精确性, 公式如下:
$ IAP{E_j} = \frac{1}{N}\sum\limits_{j = 1}^N {\left\{ {\frac{1}{R}\sum\limits_{{{i}} = 1}^R {\frac{{\left| {X_{ij} - X_j} \right|}}{X}} } \right\}} \times 100{{\%}} $


式中, N为进行年龄鉴定的鱼尾数; R为每尾鱼进行年龄鉴定的次数; Xij为第j尾鱼进行的第i次年龄鉴定结果; Xj为第j尾鱼的平均年龄。
为了更好地对不同年龄材料进行比较, 前后鉴定结果最终必须一致。若结果不一致, 则重新对该年龄材料进行年龄鉴定, 直到最终结果统一为止。若再次鉴定后, 结果差距较大, 则将其除去。在西藏其他裂腹鱼类[11, 12]的年龄材料鉴定中微耳石的清晰度是最好的, 并且双须叶须鱼微耳石的年轮比较清晰, 故以微耳石鉴定的年龄为准, 将星耳石、脊椎骨、鳃盖骨、臀鳞、胸鳞、侧线鳞和背鳞7种年龄材料分别和微耳石计算所得IAPE来进行比较。
清晰度评分 对8种年龄材料年轮的清晰度按照5个等级进行评分[11]: 1是非常好, 2是好, 3是一般, 4是很差, 5是难以辨认。
1.5 数据分析
统计分析采用SPSS 21和Excel 2003, 数据采用平均数±标准差表示, 当P<0.05时, 存在显著性差异。
2. 结果
总共采集到193尾双须叶须鱼, 体长为155—550 mm, 体重为46.5—1704.5 g。
2.1 年轮特征
微耳石 微耳石为不规则的椭圆形, 近极面前端膨大, 后端似铲型; 远极面微微隆起, 前端似由许多晶体组成, 从前端到后端逐渐变薄(图 1d1—d4)。中心核靠近前端, 在入射光下, 从微耳石核心向外边缘颜色逐渐变淡。在年轮排列区域, 年轮间距呈现有规律的缩短, 靠近中心核的年轮间距较大, 到10龄年轮间距明显变窄, 在20龄后年轮间距显著变窄(图 2f、图 3f、图 4g)。
![]() 图 1 双须叶须鱼背鳞(a)、侧线鳞(b)、胸鳞(c)、微耳石(d1、d2、d3、d4)、臀鳞(e)、鳃盖骨(f)、脊椎骨(g)、星耳石(h1、h2)的形态特征PZ为前区; UZ为上侧区; DZ为下侧区; BZ为后区; d1为远极面; d2为背面; d3为腹面; d4为近极面; h1为内侧面; h2为外侧面; 1为脊突; 2为翼叶; 3为主间沟; 4为基叶; 5为中央听沟; 6为叶突Figure 1. Morphological characteristics of back scale (a), lateral-line scale (b), chest scale (c), lapillus (d1, d2, d3, d4), hip scale (e), opercular bone (f), vertebrae (g), asteriscus (h1, h2) of Ptychobarbus dipogonPZ is the front zone; UZ is the upper zone; DZ is the lower zone; BZ is the rear zone; d1 is the far pole face; d2 is the back face; d3 is the ventral face; d4 is the near pole face; h1 is the inside face; h2 is the lateral side; 1 is the spinal protrusion; 2 is the wing leaf; 3 is the main groove; 4 is the basal leaf; 5 is the central auditory ditch; 6 is a leaf protrusion
图 1 双须叶须鱼背鳞(a)、侧线鳞(b)、胸鳞(c)、微耳石(d1、d2、d3、d4)、臀鳞(e)、鳃盖骨(f)、脊椎骨(g)、星耳石(h1、h2)的形态特征PZ为前区; UZ为上侧区; DZ为下侧区; BZ为后区; d1为远极面; d2为背面; d3为腹面; d4为近极面; h1为内侧面; h2为外侧面; 1为脊突; 2为翼叶; 3为主间沟; 4为基叶; 5为中央听沟; 6为叶突Figure 1. Morphological characteristics of back scale (a), lateral-line scale (b), chest scale (c), lapillus (d1, d2, d3, d4), hip scale (e), opercular bone (f), vertebrae (g), asteriscus (h1, h2) of Ptychobarbus dipogonPZ is the front zone; UZ is the upper zone; DZ is the lower zone; BZ is the rear zone; d1 is the far pole face; d2 is the back face; d3 is the ventral face; d4 is the near pole face; h1 is the inside face; h2 is the lateral side; 1 is the spinal protrusion; 2 is the wing leaf; 3 is the main groove; 4 is the basal leaf; 5 is the central auditory ditch; 6 is a leaf protrusion![]() 图 2 低龄双须叶须鱼(体长215 mm)背鳞(a)、侧线鳞(b)、胸鳞(c)、臀鳞(d)、星耳石(e)、微耳石(f)、鳃盖骨(g)、脊椎骨(h)的年轮特征(圆点示年轮)背鳞5龄(a); 侧线鳞4龄(b); 胸鳞5龄(c); 臀鳞5龄(d); 星耳石7龄(e); 微耳石7龄(f); 鳃盖骨7龄(g); 脊椎骨7龄(h)Figure 2. Annuli characteristics of back scale (a), lateral-line scale (b), chest scale (c), hip scale (d), asteriscus (e), lapillus (f), opercular bone (g), vertebrae (h) from the same Ptychobarbus dipogon with 215 mm SL(dots show annuli)back scale 5 years (a); lateral-line scale 4 years (b); chest scale 5 years (c); hip scale 5 years (d); asteriscus 7 years (e); lapillus 7 years (f); opercular bone 7 years (g); vertebrae 7 years (h)
图 2 低龄双须叶须鱼(体长215 mm)背鳞(a)、侧线鳞(b)、胸鳞(c)、臀鳞(d)、星耳石(e)、微耳石(f)、鳃盖骨(g)、脊椎骨(h)的年轮特征(圆点示年轮)背鳞5龄(a); 侧线鳞4龄(b); 胸鳞5龄(c); 臀鳞5龄(d); 星耳石7龄(e); 微耳石7龄(f); 鳃盖骨7龄(g); 脊椎骨7龄(h)Figure 2. Annuli characteristics of back scale (a), lateral-line scale (b), chest scale (c), hip scale (d), asteriscus (e), lapillus (f), opercular bone (g), vertebrae (h) from the same Ptychobarbus dipogon with 215 mm SL(dots show annuli)back scale 5 years (a); lateral-line scale 4 years (b); chest scale 5 years (c); hip scale 5 years (d); asteriscus 7 years (e); lapillus 7 years (f); opercular bone 7 years (g); vertebrae 7 years (h)![]() 图 3 中龄双须叶须鱼(体长400 mm)背鳞(a)、侧线鳞(b)、胸鳞(c)、臀鳞(d)、星耳石(e)、微耳石(f)、脊椎骨(g)、鳃盖骨(h)的年轮特征(圆点示年轮)背鳞9龄(a); 侧线鳞9龄(b); 胸鳞8龄(c); 臀鳞10龄(d); 星耳石17龄(e); 微耳石17龄(f); 脊椎骨15龄(g); 鳃盖骨15龄(h)Figure 3. Annuli characteristics of back scale (a), lateral-line scale (b), chest scale (c), hip scale (d), asteriscus (e), lapillus (f), vertebrae (g), opercular bone (h) from the same Ptychobarbus dipogon with 400 mm SL (dots show annuli)back scale 9 years (a); lateral-line scale 9 years (b); chest scale 8 years (c); hip scale 10 years (d); asteriscus 17 years (e); lapillus 17 years (f); vertebrae 15 years (g); opercular bone15 years (h)
图 3 中龄双须叶须鱼(体长400 mm)背鳞(a)、侧线鳞(b)、胸鳞(c)、臀鳞(d)、星耳石(e)、微耳石(f)、脊椎骨(g)、鳃盖骨(h)的年轮特征(圆点示年轮)背鳞9龄(a); 侧线鳞9龄(b); 胸鳞8龄(c); 臀鳞10龄(d); 星耳石17龄(e); 微耳石17龄(f); 脊椎骨15龄(g); 鳃盖骨15龄(h)Figure 3. Annuli characteristics of back scale (a), lateral-line scale (b), chest scale (c), hip scale (d), asteriscus (e), lapillus (f), vertebrae (g), opercular bone (h) from the same Ptychobarbus dipogon with 400 mm SL (dots show annuli)back scale 9 years (a); lateral-line scale 9 years (b); chest scale 8 years (c); hip scale 10 years (d); asteriscus 17 years (e); lapillus 17 years (f); vertebrae 15 years (g); opercular bone15 years (h)![]() 图 4 高龄双须叶须鱼(体长488 mm)背鳞(a)、侧线鳞(b)、胸鳞(c)、臀鳞(d)、鳃盖骨(e)、星耳石(f)、微耳石(g)、脊椎骨(h)的年轮特征(圆点示年轮)背鳞11龄(a); 侧线鳞12龄(b); 胸鳞12龄(c); 臀鳞16龄(d); 鳃盖骨23龄(e); 星耳石26龄(f); 微耳石34龄(g); 脊椎骨21龄(h)Figure 4. Annuli characteristics of back scale (a), lateral-line scale (b), chest scale (c), hip scale (d), opercular bone(e), asteriscus (f), lapillus (g), vertebrae (h) from the same Ptychobarbus dipogon with 488 mm SL (dots show annuli)back scale 11 years (a); lateral-line scale 12 years (b); chest scale 12 years (c); hip scale 16 years (d); opercular bone 23 years (e); asteriscus 26 years (f); lapillus 34 years (g); vertebrae 21 years (h)
图 4 高龄双须叶须鱼(体长488 mm)背鳞(a)、侧线鳞(b)、胸鳞(c)、臀鳞(d)、鳃盖骨(e)、星耳石(f)、微耳石(g)、脊椎骨(h)的年轮特征(圆点示年轮)背鳞11龄(a); 侧线鳞12龄(b); 胸鳞12龄(c); 臀鳞16龄(d); 鳃盖骨23龄(e); 星耳石26龄(f); 微耳石34龄(g); 脊椎骨21龄(h)Figure 4. Annuli characteristics of back scale (a), lateral-line scale (b), chest scale (c), hip scale (d), opercular bone(e), asteriscus (f), lapillus (g), vertebrae (h) from the same Ptychobarbus dipogon with 488 mm SL (dots show annuli)back scale 11 years (a); lateral-line scale 12 years (b); chest scale 12 years (c); hip scale 16 years (d); opercular bone 23 years (e); asteriscus 26 years (f); lapillus 34 years (g); vertebrae 21 years (h)星耳石 星耳石为星状, 轮纹不明显, 边缘为锯齿状, 内侧面中间长轴处为凹槽, 外侧面微微隆起, 具有辐射状脊(图 1h1、图 1h2)。到12龄间距明显变窄, 而到20龄后年轮间距显著变窄(图 2e、图 3e、图 4f)。
脊椎骨 脊椎骨为双凹型, 中心有一小孔, 前后凹面呈现出宽窄交替的同心圆轮纹, 在入射光下, 呈明暗交替分布。小孔的周围较为透明, 轮纹很少很细, 很难确认起始轮的位置。脊椎骨的边缘有较厚的结缔组织, 难以辨认末轮(图 1g)。脊椎骨的年轮宽度不会随着年龄的增加而显著变窄(图 2h、图 3g、图 4h)。
鳃盖骨 鳃盖骨为不规则的四边形, 基部内侧有许多小孔, 表面轮纹平行排列, 边缘为锯齿状。基部较厚, 且呈黄色, 难以辨认首轮位置(图 1f)。低龄鱼的鳃盖骨轮纹间隔大且稀疏, 不易分辨年轮; 高龄鱼轮纹排列紧密, 容易辨认。年轮间距呈现有规律的缩短, 到12龄年轮间距明显变窄(图 2g、图 3h、图 4e)。
臀鳞 臀鳞取自肛门至臀鳍的两侧, 大多数臀鳞形态特征特化, 下侧区向内弯曲, 呈“L”形。前区轮纹密集, 很难有效辨识年轮; 后区各年轮间隙较明显, 但夹杂副轮。有少部分鳞片上后区内的副轮与年轮十分相似, 较难区别, 需依靠侧区辅助观察(图 1e、图 2d、图 3d、图 4d)。
胸鳞、侧线鳞和背鳞 胸鳞取自侧线下方, 胸鳍基部(图 1c)。侧线鳞取自鱼体两侧的侧线部位, 中央有一条透明的管道(图 1b)。背鳞取自侧线上方, 背鳍附近(图 1a)。这3种环片疏密不明显, 但在入射光下可见到明亮的脊高出相邻环片, 脊的外缘即为年轮。前区、上侧区和下侧区均可作为年龄读取区。
2.2 八种年龄材料的比较
共采集193尾样本, 体长为155—550 mm, 体重为46.5—1704.5 g, 其中微耳石鉴定年龄在4—49龄, 星耳石鉴定年龄在4—35龄, 脊椎骨鉴定年龄范围在4—34龄, 鳃盖骨鉴定年龄范围在4—34龄, 臀鳞鉴定年龄范围在4—22龄, 胸鳞鉴定年龄范围在4—19龄, 侧线龄鉴定年龄范围在4—16龄, 背鳞鉴定年龄范围在4—17龄。不同年龄组的样本数和体长信息见表 1。
表 1 双须叶须鱼八种年龄材料所鉴定的各个年龄组的样本数和体长Table 1. Number of specimens and body length at different ages of Ptychobarbus dipogon年龄
Age (y)微耳石
Lapillus星耳石
Asteriscus脊椎骨
Vertebrae鳃盖骨
Opercular bones臀鳞
Hip scale胸鳞
Chest scale侧线鳞
Lateral-line scale背鳞
Back scaleN Mean±SD (mm) N Mean±SD (mm) N Mean±SD (mm) N Mean±SD (mm) N Mean±SD (mm) N Mean±SD (mm) N Mean±SD (mm) N Mean±SD (mm) 4 1 155.0 1 155.0 1 155.0 2 182.5±38.9 4 201.3±11.1 1 210 2 197.5±17.7 5 6 211.7±25.4 6 211.7±25.4 4 198.8±8.5 6 198.3±10.3 3 203.3±47.5 5 207.0±41.0 8 199.4±29.3 7 211.4±35.1 6 12 222.1±23.9 11 224.6±23.4 11 225.0±23.4 11 232.7±22.2 8 211.3±25.3 11 245.9±41.9 9 261.4±51.7 8 240.5±52.7 7 4 248.8±25.9 4 231.3±33.8 6 238.3±33.0 6 250.8±28.5 11 251.4±87.1 11 296.9±95.4 11 260.2±48.6 17 295.3±77.3 8 3 268.3±7.6 3 268.3±7.6 4 258.8±20.2 1 270.0 7 299.1±49.0 13 331.9±34.9 20 341.6±57.6 18 349.1±49.7 9 2 287.0±9.9 2 272.5±10.6 2 295.5±21.9 1 280.0 8 314.1±46.3 14 354.4±59.0 22 369.2±47.7 23 363.9±48.1 10 4 294.3±20.7 6 299.5±20.7 3 282.7±12.1 6 326.7±42.8 19 343.9±31.6 35 389.6±58.5 28 403.4±61.7 31 400.4±57.1 11 1 342.0 8 342.6±23.4 10 335.0±11.0 9 341.2±35.0 16 364.0±43.8 22 405.2±51.4 27 402.7±56.5 34 417.2±57.4 12 4 335.3±9.6 5 352.8±36.6 6 360.3±39.3 8 329.6±21.9 29 399.8±65.4 28 424.5±55.4 24 438.2±62.7 22 442.1±60.3 13 5 338.2±19.5 8 358.6±38.1 7 339.3±22.0 11 355.2±50.0 22 424.7±53.2 21 436.9±57.4 24 451.0±53.0 16 440.2±56.9 14 11 342.3±33.0 11 350.7±36.4 13 364.1±46.5 16 364.9±31.4 21 424.2±51.5 18 438.0±64.2 9 431.9±54.5 10 474.7±53.2 15 12 344.9±31.2 12 363.4±49.6 13 380.0±53.0 12 361.3±35.7 14 415.2±59.8 5 482.6±24.9 6 445.2±75.2 2 480.5±12.0 16 10 365.0±43.5 23 388.1±55.7 17 388.0±52.7 7 367.6±35.1 14 448.6±43.0 4 481.0±17.2 4 469.0±54.7 2 431.0±97.6 17 8 376.3±34.5 14 402.5±39.2 13 406.2±36.8 12 405.9±48.5 7 487.3±39.8 1 510.0 1 510.0 18 11 386.5±49.6 5 411.6±31.3 17 403.8±55.4 13 437.5±45.3 9 450.8±49.3 19 7 402.9±36.0 6 420.0±26.4 5 416.4±44.2 6 410.3±55.5 1 490.0 1 490.0 20 9 414.6±60.7 8 415.6±58.5 7 423.0±53.0 7 379.3±17.0 2 476.0±33.9 21 7 406.7±44.9 10 457.8±49.3 9 446.3±66.9 9 453.1±36.9 1 490.0 22 5 380.6±61.8 10 443.1±50.0 10 452.4±43.1 9 481.1±21.8 1 550.0 23 2 432.5±29.0 7 451.7±26.9 12 470.3±27.2 10 460.8±33.4 24 7 433.6±16.9 11 469.5±43.6 5 448.8±36.6 7 443.4±27.3 25 7 445.0±49.4 6 488.7±29.6 6 486.8±51.4 5 470.8±56.3 26 4 459.8±49.1 5 452.0±64.5 1 452.0 5 480.8±11.7 27 9 447.0±41.4 2 453.5±50.2 4 497.3±16.8 2 485.0±0.0 28 9 450.2±33.1 2 451.0±1.4 1 450.0 3 451.7±42.5 29 5 472.0±35.0 2 525.0±35.4 2 467.0±7.1 3 475.3±49.8 30 3 459.3±44.5 1 550.0 2 520.0 31 2 451.0±1.4 2 492.5±10.6 2 510.0±14.1 1 510.0 32 3 482.0±55.8 1 500.0 2 511.0±15.6 33 3 439.7±54.0 1 520.0 34 2 490.5±0.7 1 500.0 1 550.0 35 4 489.5±14.7 1 500.0 36 2 471.0±26.9 37 2 515.0±7.1 39 1 462.0 40 1 550.0 41 1 508.0 42 1 522.0 43 1 500.0 44 1 500.0 49 1 500.0 总计
Total193 193 193 193 193 193 193 193 2.3 八种年龄材料的平均年龄比较
双须叶须鱼不同年龄材料所鉴定的平均年龄见表 2。8种年龄材料所鉴定的平均年龄存在显著性差异(P<0.05)。用微耳石作为年龄材料所鉴定的平均年龄最高(20.05龄), 显著高于星耳石(16.84龄)、脊椎骨(16.56)、鳃盖骨(16.70龄)、臀鳞(11.34龄)、胸鳞(9.58龄)、侧线鳞(9.33龄)和背鳞(9.33龄)所鉴定的平均年龄(P<0.05)。23龄以下和23龄以上样本分开统计时, 4—23龄样本中, 微耳石鉴定的平均年龄与星耳石和脊椎骨鉴定的平均年龄较为接近, 分别为14.39龄、13.13龄、13.20龄, 显著高于鳃盖骨(12.96龄)、臀鳞(9.93龄)、胸鳞(8.49龄)、侧线鳞(8.30龄)和背鳞(8.13龄)所鉴定的平均年龄(P<0.05)。大于23龄时, 星耳石(23.52龄)、脊椎骨(22.61龄)和鳃盖骨(23.42龄)所鉴定的平均年龄较为接近, 星耳石、脊椎骨、鳃盖骨、臀鳞、胸鳞、侧线鳞和背鳞7种年龄鉴定材料都显著低于微耳石所鉴定的平均年龄30.23龄(P<0.05)。
表 2 不同年龄材料所鉴定的平均年龄的比较Table 2. The average age of different age materials年龄材料
Ages
structure平均年龄
Mean values of
age estimate年龄Total Age 4—14 Age 4—23 Age>23 微耳石
Lapillus20.05±9.32a 9.32±3.51a 14.39±5.26a 30.23±5.59a 星耳石
Asteriscus16.84±6.52b 9.11±3.25ab 13.13±4.44ab 23.52±3.71b 脊椎骨
Vertebrae16.56±6.18b 9.06±3.05ab 13.20±4.39ab 22.61±3.92b 鳃盖骨
Opercular
bones16.70±6.70b 8.98±3.28ab 12.96±4.62b 23.42±4.10b 臀鳞
Hip scale11.34±3.47c 7.74±2.49bc 9.93±3.04c 13.87±2.68c 胸鳞
Chest scale9.58±2.85d 6.62±2.26c 8.49±2.65d 11.54±2.03d 侧线鳞
Lateral-line
scale9.33±2.67d 6.49±1.85c 8.30±2.51d 11.17±1.81d 背鳞
Back scale9.33±2.68d 6.47±1.90c 8.13±2.41d 10.65±1.82d N 193 53 124 69 注: 表中同列数字上标不同字母表示有显著差异性(P<0.05)Note: Values with different superscripts in each column are significantly different from each other (P<0.05) 2.4 八种年龄材料的平均百分比误差比较
用微耳石鉴定年龄时, 多次读数的平均百分比误差(IAPE)最低(3.31%), 从小到大依次为: 星耳石(4.72%)、脊椎骨(4.79%)、臀鳞(5.11%)、鳃盖骨(5.17%)、胸鳞(5.19%)、侧线鳞(5.88%)、背鳞(5.86%)。其他7种年龄材料和微耳石比较的IAPE从小到大依次为星耳石(12.28%)、脊椎骨(15.67%)、鳃盖骨(17.81%)、臀鳞(41.63%)、侧线鳞(50.50%)、胸鳞(51.26%)、背鳞(51.74%)。从星耳石、脊椎骨、鳃盖骨、臀鳞、胸鳞、侧线鳞和背鳞分别与耳石作比较的IAPE值(图 5)可以看出, 星耳石、脊椎骨、鳃盖骨鉴定的年龄结果比四种鳞片准确。但仅从IAPE值来看, 并不能确定星耳石、脊椎骨和鳃盖骨做鉴定的年龄结果哪个更精确。但是统计分析表明(表 2), 星耳石和脊椎骨的年龄读数与微耳石的年龄读数在低于23龄时没有显著性差异(P>0.05), 而鳃盖骨所鉴定的年龄无论是在低龄还是高龄都显著低于耳石所鉴定的年龄(P<0.05)。随着年龄增加, IAPE值基本上呈现上升趋势, 差异也逐渐增大, 对于鉴定高龄鱼时所产生的差异越来越大。
2.5 八种年龄材料的清晰度评分比较
由于4种鳞片年龄读数在高于14龄组内都与微耳石有显著差异, 因此在清晰度评分中分为低于14龄组和高于14龄组。微耳石上的年龄较清晰, 在低于14龄和高于14龄组内被评为“非常好”和“好”的都较其他材料多, 故微耳石在进行年龄鉴定时准确性最好(表 3、表 4)。
表 3 双须叶须鱼不同年龄材料的清晰度评分(4—14龄)Table 3. Distribution of readability scores for different age materials of Ptychobarbus dipogon (4—14 years)年龄材料
Ages structure清晰度评分比例
Proportion of readability score1 2 3 4 5 微耳石
Lapillus9.43 66.04 18.87 5.66 星耳石
Asteriscus1.89 43.40 35.85 16.98 1.89 脊椎骨
Vertebrae3.77 43.40 45.28 3.77 3.77 鳃盖骨
Opercular bones1.89 64.15 30.19 1.89 1.89 臀鳞
Hip scale16.98 56.60 24.53 1.89 胸鳞
Chest scale9.43 50.94 30.19 9.43 侧线鳞
Lateral-line scale11.32 56.60 28.30 1.89 1.89 背鳞
Back scale11.32 60.38 24.53 3.77 表 4 双须叶须鱼不同年龄材料的清晰度评分(14龄以上)Table 4. Distribution of readability scores for different calcified struc-tures of Ptychobarbus dipogon (more than 14 years)年龄材料
Ages structure清晰度评分比例
Proportion of readability score1 2 3 4 5 微耳石
Lapillus4.29 57.86 29.29 6.43 2.14 星耳石
Asteriscus2.14 49.29 35.00 11.43 2.14 脊椎骨
Vertebrae4.29 50.00 34.29 8.57 2.86 鳃盖骨
Opercular bone2.86 51.43 36.43 6.43 2.86 2.6 年龄与体长关系
微耳石年龄鉴定的年龄读数(A)与相对应的体长(L)呈极显著的对数函数关系(P<0.01), 其相关关系式为: L=146.76 ln (A)–38.139, R2=0.8312。随着年龄的增加, 双须叶须鱼体长随之增长, 但其增长速率随之减缓(图 6)。
3. 讨论
3.1 年龄鉴定的准确性比较
鱼类年轮特征的研究是进行鱼类年龄鉴定的前提[1]。而年龄鉴定的准确性直接关系到鱼类生长参数估算的可靠程度[13], 这对于渔业的管理和资源的合理开发尤为重要; 低估年龄的结果将导致对鱼类生长估计过快和自然死亡率估计过高, 因而对产量做出过于乐观的估计, 往往会造成资源的过度开发[14]。
就同一种鱼而言, 不同的年龄材料轮纹的清晰度和数目不一定相同, 所以可能导致不同年龄段的最适材料也有所不同[15]。本文微耳石鉴定所得的最大年龄为49龄, 星耳石鉴定所得的最大年龄为35龄, 脊椎骨鉴定所得最大年龄为34龄, 鳃盖骨为34龄, 臀鳞为22龄, 胸鳞为19龄, 侧线鳞为16龄, 背鳞为17龄。在低于23龄时, 微耳石与星耳石和脊椎骨鉴定的平均年龄之间无显著性差异(P>0.05), 相差年龄在1龄以内, 显著高于鳃盖骨和四种鳞片(P<0.05)。反映出在鉴定低龄个体时, 微耳石、星耳石和脊椎骨作为年龄材料是可行的。分析原因为, 鳃盖骨仅在边缘可观察到明暗相间排列的环纹, 鳃盖骨基部变厚[16], 中心轮纹判别能力差, 不易确定年龄[13]; 鳞片随年龄增长易出现磨损或者停滞现象[17], 通常会低估高龄和生长速率慢的个体年龄[13], 只适用于对低龄、生长较快的鱼类进行年龄鉴定[18], 特别是裂腹鱼特有的臀鳞与其繁殖行为密切相关, 致使鳞片的磨损很难避免[19], 裂腹鱼类的鳞片在长期进化过程中为适应高原寒冷的水域环境而存在着不同程度的退化[12]。
然而高于23龄时, 7种年龄鉴定材料均显著低于微耳石鉴定的平均年龄(P<0.05)。星耳石高龄个体年轮特征不明显, 杂纹较多[20]; 脊椎骨首轮较难辨认[21], 轮纹较为密集, 增加高龄鱼年龄鉴定的误差[11], 生活的地理环境特殊、环境条件恶劣, 脊椎骨上年轮的形成和排列可能受到环境条件的影响[11, 12]。而耳石年轮标志明显, 可判读力高[22]。耳石生长是以与机体生长相对独立, 在慢生长和高龄个体中比其他骨质材料生长更快, 从而能更真实地记录周期性季节生长和年龄[23], 所以采用耳石估计生长缓慢和相对长寿命群体或种类的年龄更为准确[24]。此外, 与微耳石比较的平均百分比误差相比, 星耳石、脊椎骨、鳃盖骨与之相差不大, 4种鳞片与之差别较大。并且IAPE值随着年龄增加基本上呈现上升趋势反映出在高龄个体年龄鉴定水平上所产生的差异越来越大。
在国内许多学者对裂腹鱼不同年龄鉴定材料的比较研究中, 得出耳石读数较其他年龄材料准确。马宝珊[11]和周贤君[12]分别通过研究异齿裂腹鱼和拉萨裂腹鱼的3种年龄材料(耳石、脊椎骨和鳃盖骨)发现耳石是年龄鉴定的最合适材料, 霍斌[25]研究尖裸鲤年龄材料发现釆用耳石作为年龄鉴定材料其准确性和精确性要优于脊椎骨, 并且耳石还是伊犁裂腹鱼[26]、色林错裸鲤[14]、软刺裸裂尻鱼[27]、青海湖裸鲤[3]的最佳年龄材料。
总而言之, 双须叶须鱼8种年龄鉴定材料均为每年形成一个年轮, 本研究通过不同年龄鉴定材料的比较发现, 在进行年龄鉴定时微耳石所鉴定的最大年龄较其他年龄材料大, 而其他的几种年龄材料均有不同程度的年龄阶段性差异。在鉴定低龄个体时, 微耳石是双须叶须鱼年龄鉴定的最佳材料, 星耳石和脊椎骨次之, 鳃盖骨较差, 鳞片不宜作为年龄鉴定材料; 在鉴定高龄个体时, 微耳石是双须叶须鱼年龄鉴定的最佳材料。
3.2 双须叶须鱼年龄结构与年龄鉴定探讨
杨鑫[6]研究发现雅鲁藏布江中游的双须叶须鱼群体的年龄结构为3—24 龄, 反映出雅鲁藏布江双须叶须鱼群体年龄结构趋于简单。Li等[7]研究了雅鲁藏布江及其支流的双须叶须鱼, 其种群的年龄结构分别为2—44 龄, 与本文研究结果类似, 反映出双须叶须鱼在雅鲁藏布江中游流域年龄趋向低龄化, 而双须叶须鱼在拉萨河流域的年龄结构群体尚未受到严重干扰。究其原因, 采样点环境和人为干扰强度等差异是导致种群结构产生差异的主要因素[6]。而且在3—6月, 双须叶须鱼正处于繁殖期, 加之浮游生物在此季节繁殖生长, 易捕捞较大个体。
在不同水域中双须叶须鱼[6]2种年龄材料的比较显示, 脊椎骨与耳石鉴定的结果无显著性差异, 耳石鉴定10 龄以上的年龄大于脊椎骨鉴定的年龄。而本文研究仅是在鉴定低龄个体(小于23龄)时, 微耳石、星耳石和脊椎骨作为年龄材料是可行的。分析其原因, 可能是由于不同水域资源现状的差异和人为干扰的程度不同所致。交叉水域中双须叶须鱼3种耳石年龄材料的比较显示, 核心模棱两可的星耳石导致难以辨别年龄, 矢耳石易脆并经常破裂[7], 所以微耳石是双须叶须鱼的最佳年龄鉴定材料。
总而言之, 无论是不同水域或者交叉水域, 微耳石一直是双须叶须鱼最好的年龄鉴定材料, 这与杨鑫[6]、Li等[7]的研究结果一致。
-
表 1 实验基础饲料配方及化学组成(%干物质)
Table 1 Diet formulation and chemical composition of experiment diets (% in dry matter)
原料Ingredient 含量Content (%) 白鱼粉White fish meal 25.00 国产酪蛋白Domestic casein 16.50 鱼油Fish oil 3.00 玉米淀粉Corn starch 25.75 纤维素Cellulose 21.19 维生素预混物Vitamin premix1 0.45 胆碱Choline 0.11 矿物盐预混物Mineral premix2 5.00 海藻酸钠Sodium alginate 1.00 羧甲基纤维素Carboxymethyl cellulose 2.00 三氧化二钇Y2O3 0.50 饲料化学成分Chemical composition (% in dry matter) 粗蛋白Crude protein 32.96 粗脂肪Crude lipid 5.30 能量Energy (kJ/g) 14.55 注: 1. 维生素预混物Vitamin premix (mg/kg diet): 维生素B1 Thiamin, 20; 维生素B2 Riboflavin, 20; 烟酸Niacin, 100; 维生素B6 Pyridoxine, 20; 生物素Biotin, 0.1; 维生素B12 Cyanocobalamine, 0.020; 叶酸Folic acid, 5; 泛酸钙Calcium pantothenate, 50; 肌醇Inositol, 100; 维生素C Ascorbic acid, 100; 维生素A Retinol, 1.1; 维生素D Vitamin D, 20; 维生素E Vitamin E, 50; 维生素K Vitamin K, 10; 玉米淀粉Corn starch, 645.2; 2. 矿物盐预混物Mineral premix (mg/kg diet): NaCl, 500; MgSO4·7H2O, 8155.6; KH2PO4, 16000.0; Ca(HPO4)2·H2O, 7650.6; NaH2PO4·2H2O, 12500.0; FeSO4·7H2O, 2286.2; C6H10CaO6·5H2O, 1750.0; MnSO4·H2O, 61.4; ZnSO4·7H2O, 178.0; CuSO4·5H2O, 15.5; CoSO4·7H2O, 0.91; KI, 1.5; 玉米淀粉Corn starch, 753.7 表 2 饲料AFB1水平对草鱼幼鱼初始体重(IBW)、终末体重(FBW)、存活率、摄食率(FR)、特定生长率(SGR)和饲料效率(FE)的影响(平均值±标准误)
Table 2 Effects of dietary AFB1 on initial body weight (IBW), final body weight (FBW), survival rate, feeding rate (FR), specific growth rate (SGR), feed efficiency (FE) of juvenile grass carp (Mean±SE)
AFB1添加量
Supplemented AFB1
(μg/kg diet)初始体重
IBW (g)终末体重
FBW (g)存活率
Survival rate (%)摄食率
FR (%BW/d)特定生长率
SGR (%/d)饲料效率
FE (%)0 2.90±0.20 22.97±0.57 86.7±4.4 2.89±0.02 2.46±0.07 63.8±0.5 10 2.90±0.10 24.53±1.59 87.0±7.6 2.81±0.14 2.54±0.06 66.9±3.8 20 2.90±0.20 24.73±2.73 88.4±2.5 2.85±0.22 2.56±0.06 66.5±5.9 100 2.90±0.26 23.47±0.85 84.1±2.5 2.83±0.12 2.49±0.07 65.7±2.8 1000 2.90±0.20 24.03±1.46 84.1±6.6 2.87±0.08 2.52±0.06 65.1±1.7 5000 2.93±0.11 25.27±1.90 87.0±4.4 2.83±0.12 2.57±0.13 66.7±3.9 表 3 饲料AFB1水平对草鱼幼鱼血清谷丙转氨酶(ALT)、谷草转氨酶(AST)和碱性磷酸酶(ALP)、超氧化物歧化酶(SOD)、谷胱甘肽过氧化物酶(GSH-Px)活性的影响(平均值±标准误)
Table 3 Effects of dietary AFB1 on serum activities of glutamic-pyruvic transaminase (ALT), glutamic-oxalacetic transaminase (AST), alkaline phosphatase (ALP), superoxide dismutase (SOD), and glutathione peroxidase (GSH-Px) of juvenile grass carp (Mean± SE)
AFB1添加量
Supplemented AFB1 (μg/kg diet)ALT (U/L) AST (U/L) ALP (U/L) SOD (U/L) GSH-Px (U/L) 0 12.5±0.4 30.3±2.3 5.36±0.79 169.9±19.5 269.4±9.4 10 11.8±1.1 28.3±4.8 5.75±0.85 188.6±11.0 266.8±13.3 20 11.9±1.0 29.7±4.0 5.52±0.56 162.5±24.2 283.3±11.9 100 12.4±1.7 28.1±3.5 5.71±0.64 169.6±21.0 265.6±12.7 1000 13.1±0.6 28.3±2.7 5.69±1.25 171.9±10.4 274.9±9.6 5000 11.8±0.9 28.4±1.8 5.60±0.62 165.2±13.2 267.0±8.1 表 4 饲料中AFB1水平对草鱼幼鱼肝体比(HSI)、脏体比(VSI)的影响(平均值±标准误)
Table 4 Effects of dietary AFB1 on hepatosomatic index (HSI) and viscera index (VSI) of juvenile grass carp (Mean ± SE)
AFB1添加量
Supplemented AFB1 (μg/kg diet)肝体比
HSI脏体比
VSI0 1.80±0.04 8.27±0.47 10 1.77±0.10 7.57±0.75 20 1.76±0.07 7.73±0.99 100 1.76±0.08 7.63±0.40 1000 1.72±0.11 7.43±0.75 5000 1.73±0.19 7.25±0.33 表 5 饲料中AFB1水平对草鱼幼鱼肌肉AFB1积累(μg/kg湿重)的影响(平均值±标准误)
Table 5 Effects of dietary AFB1 on AFB1 accumulation (μg/kg wet weight) in muscle of juvenile grass carp (Mean± SE)
AFB1添加量
Supplemented AFB1
(μg/kg diet)肌肉AFB1积累量AFB1
accumulation in muscle
(μg/kg diet)0 未检出 10 未检出 20 未检出 100 未检出 1000 未检出 5000 1.21±0.18 -
[1] Huang Y, Han D, Zhu X M, et al. Response and recovery of gibel carp from subchronic oral administration of aflatoxin B1 [J]. Aquaculture, 2011, 319(1—2): 89—97 doi: 10.1016/j.aquaculture.2011.06.024
[2] 黄莹, 朱晓鸣, 韩冬, 等. 饲喂不同浓度黄曲霉毒素B1饲料对异育银鲫成鱼的生长和毒素积累的影响. 水生生物学报, 2012, 36(5): 817—825 Huang, Y, Z hu, X M, Han, D, et al. Growth and aflato-xin B1 accumulation of gibel carp adult fed with diets of different levels of aflatoxin B1 [J]. Acta Hydrobiologica Sinica, 2012, 36(5): 817—825
[3] Kowalska A, Walkiewicz K, Kozieł P, et al. Aflatoxins: characteristics and impact on human health [J]. Postpy Higieny I Medycyny Dowiadczalnej, 2017, 71(1): 315—327
[4] Deng S X, Tian L X, Liu F J, et al. Toxic effects and residue of aflatoxin B1 in tilapia (Oreochromis niloticus×O. aureus) [J]. Aquaculture, 2010, 307(3—4): 233—240 doi: 10.1016/j.aquaculture.2010.07.029
[5] Tuan N A, Grizzle J M, Lovell R T, et al. Growth and hepatic lesions of Nile tilapia (Oreochromis niloticus) fed diets containing aflatoxin B1 [J]. Aquaculture, 2002, 212(1—4): 311—319 doi: 10.1016/S0044-8486(02)00021-2
[6] Ngethe S, Horsberg T E, Mitema E, et al. Species differences in hepatic concentration of orally administered 3H AFB1 between rainbow trout (Oncorhynchus mykiss) and tilapia (Oreochromis niloticus) [J]. Aquaculture, 1993, 114(3—4): 355—358
[7] Ayyat M S, Ayyat A M N, Al-Sagheer A A, et al. Effect of some safe feed additives on growth performance, blood biochemistry and bioaccumulation of aflatoxin residues of Nile tilapia fed aflatoxin B1, contaminated diet [J]. Aquaculture, 2018, 495: 27—34 doi: 10.1016/j.aquaculture.2018.05.030
[8] Halver J E. Aflatoxicosis and trout hepatoma. In: Goldblatt L A (Eds.), Aflatoxin: Scientific Background, Control, and Implications [M]. New York: Academic Press. 1969, 265—306
[9] Schoenhard G L, Hendricks J D, Nixon J E, et al. Aflatoxicol-induced heatocellular carcinoma in rainbow trout (Salmo gairdneri) and the synergistic effects of cyclopropenoid fatty acids [J]. Cancer Research, 1981, 41(3): 1011—1014
[10] Yu Y Y, Niu J, Yin P, et al. Detoxification and immunoprotection of Zn (II)-curcumin in juvenile Pacific white shrimp (Litopenaeus vannamei) feed with aflatoxin B1 [J]. Fish and Shellfish Immunology, 2018, 80: 480—486 doi: 10.1016/j.fsi.2018.05.034
[11] 王静. 饲料中黄曲霉毒素B1对凡纳滨对虾生长、肝胰腺和血淋巴生化指标及肝胰腺显微结构的影响. 硕士毕业论文, 河北农业大学, 保定. 2014 Wang J. Toxic effects of aflatoxin B1 on growth perfor-mance, biochemical and hepatopancreas microstructure of Litopanaeus vannamei [D]. Thesis for Master of Science. Agriculture University of Hebei, Baoding. 2014
[12] Plakas S M, Loveland P M, Bailey G S, et al. Tissue deposition and excretion of 14C-labeled aflatoxin B1 after oral administration in channel catfish [J]. Food and Chemical Toxicology, 1991, 29(12): 805—808 doi: 10.1016/0278-6915(91)90106-H
[13] Sahoo P K, Mukherjee S C. Immunosuppressive effects of aflatoxin B1 in Indian major carp (Labeo rohita) [J]. Comparative Immunology Microbiology and Infectious Diseases, 2001, 24(3): 143—149 doi: 10.1016/S0147-9571(00)00017-5
[14] El-Banna R, Teleb H M, Hadi M M, et al. Performance and tissue residue of tilapia fed dietary aflatoxin [J]. Veterinary Medical Journal Giza, 1992, 40: 17—23
[15] Huang Y, Han D, Xiao X C, et al. Effect of dietary aflatoxin B1, on growth, fecundity and tissue accumulation in gibel carp during the stage of gonad development [J]. Aquaculture, 2014, 428—429(5): 236—242
[16] Hendricks J D. Carcinogenicity of aflatoxins in nonmammalian organisms. In: Eaton D L, Groopman J D (Eds.) Toxicology of Aflatoxins: Human Health, Veterinary, and Agricultural Significance. Academic Press, San Diego. 1994, 103—136
[17] AOAC (Association of Official Analytical Chemists) [M]. Animal Feed. In: Williams S (Eds.), Official Methods of Analysis, 14th edn AOAC, Inc., Arlington, VA, Washington, DC. 1984, 152—161
[18] Chávez-Sánchez M C, Martínez P C A., Osorio M I, et al Pathological effects of feeding young Oreochromis niloticus diets supplemented with different levels of aflatoxin B1 [J]. Aquaculture, 1994, 127(1): 49—60 doi: 10.1016/0044-8486(94)90191-0
[19] Jantrarotai W, Lovell, R T. Subchronic toxicity of dietary aflatoxin B1 to channel catfish [J]. Journal of Aquatic Ani-mal Health, 1990, 2(4): 248—254 doi: 10.1577/1548-8667(1990)002<0248:STODAB>2.3.CO;2
[20] Rui A G, Tu D C, Nguyen N T, et al. Aflatoxin B1(AFB1) reduces growth performance, physiological response, and disease resistance in Tra catfish (Pangasius hypophthalmus) [J]. Aquaculture International, 2018, 26(3): 921—936 doi: 10.1007/s10499-018-0259-x
[21] Ostrowski-Meissner H, LeaMaster B, Duerr E, et al. Sensitivity of the Pacific white shrimp, Penaeus vannamei, to aflatoxin B1 [J]. Aquaculture, 1995, 131(3—4): 155—164 doi: 10.1016/0044-8486(95)98125-U
[22] Boonyaratpalin M, Supamattaya K, Verakunpiriya V, et al. Effects of aflatoxin B1 on growth performance, blood components, immune function and histopathological changes in black tiger shrimp (Penaeus monodon Fabricius) [J]. Aquaculture Research, 2001, 32(Suppl.1): 388—398
[23] Raghavan P R, Zhu X M, Lei W, et al. Low levels of aflatoxin B1 could cause mortalities in juvenile hybrid sturgeon, Acipenser ruthenus ♀×A. baerii ♂ [J]. Aquaculture Nutrition, 2011, 17(2): 39—47 doi: 10.1111/anu.2011.17.issue-2
[24] Valsta L M, Hendricks J D, Bailey G S. The significance of glutathione conjugation for aflatoxin B1 metabolism in rainbow trout and coho salmon [J]. Food and Chemical Toxicology, 1988, 26(2): 129—135 doi: 10.1016/0278-6915(88)90109-3
[25] Zeng S L, Long W Q, Tian L X, et al. Effects of dietary aflatoxin B1 on growth performance, body composition, haematological parameters and histopathology of juve-nile Pacific white shrimp (Litopenaeus vannamei) [J]. Aquaculture Nutrition, 2016, 22(5): 1152—1159 doi: 10.1111/anu.2016.22.issue-5
[26] 史莹华, 许梓荣, 王成章. 黄曲霉毒素对猪生长性能及免疫和抗氧化指标的影响. 中国兽医学报, 2007, 27(5): 733—736 doi: 10.3969/j.issn.1005-4545.2007.05.033 Shi Y H, Xu Z R, Wang C Z. Effects of aflatoxin on growth performance and immunology and antioxidant indices in pigs [J]. Chinese Journal of Veterinary Science, 2007, 27(5): 733—736 doi: 10.3969/j.issn.1005-4545.2007.05.033
[27] Arana S, Alves V A F, Sabino M, et al. Immunohistochemical evidence for myofibroblast-like cells associa-ted with liver injury induced by Aflatoxin B1 in rainbow trout (Oncorhynchus mykiss) [J]. Journal of Comparative Pathology, 2014, 150(2—3): 258—265 doi: 10.1016/j.jcpa.2013.07.003
[28] Han D, Xie S, Zhu X M, et al. Growth and hepatopancreas in gibel carp fed diets containing low levels of aflatoxin B1 [J]. Aquaculture Nutrition, 2009, 16(4): 335—342 doi: 10.1111/j.1365-2095.2009.00669.x
[29] Shima S, Mahdi B, Behzad N H, et al. Histopathological study of common carp (Cyprinus carpio) fed aflatoxin-contaminated diets [J]. International Journal of Aquatic Biology, 2017, 5(2): 63—70
[30] Sahoo P K, Mukherjef S C, Jain A K, et al. Histopathological and electron microscopic studies of gills and opisthonephros of rohu, Labeo rohita to acute and subchronic aflatoxin B1 toxicity [J]. Asian Fisheries Science, 2003, 16(3-4): 257—268
[31] Wei W, Li R, He L, et al. Evaluation of toxicological impacts on Sprague-Dawley rat by successively low dose of aflatoxin B1 [J]. Journal of the Science of Food and Agriculture, 2014, 94(14): 3017—3022 doi: 10.1002/jsfa.2014.94.issue-14
[32] 邓世喜. 奥尼罗非鱼对黄曲霉毒素B1(AFB1)急性、慢性中毒的反应. 硕士毕业论文, 中山大学, 广州. 2010 Deng S X. The responses of acute and chronic toxicity of aflatoxin B1(AFB1) in the Tilapia (Oreochromis niloticus ♀ × O. aureus ♂) [D]. Thesis for Master of Science. Sun Yat-sen University, Guangzhou. 2010
[33] FDA. Action levels for poisonous or deleterious substances in human food and animal feed. United States Food and Drug Administration (USFDA). Available at: http://www.cfsan.fda.gov/~lrd/fdaact.html. Accessed 28 September 2007
[34] El-Sayed Y S, Khalil R H. Toxicity, biochemical effects and residue of aflatoxin B1 in marine water-reared sea bass (Dicentrarchus labrax L.) [J]. Food and Chemical Toxicology, 2009, 47(7): 1606—1609 doi: 10.1016/j.fct.2009.04.008
-
期刊类型引用(2)
1. 陈家琪,董丽,麻晓梅,田凯,白洁,赵彦伟. 基于eDNA技术的白洋淀微型生物群落监测. 农业环境科学学报. 2021(08): 1773-1786+1839 .  百度学术
百度学术
2. 姚新民,陈云,沈燕,李禹昕,龚美萍,金凤,邵未艾,刁永卿,师乐,胡洁兰. 2013—2019年上海市青浦区出厂水水质状况及趋势分析. 职业与健康. 2021(21): 2976-2978+2982 .  百度学术
百度学术
其他类型引用(3)




 下载:
下载: