BACTERIAL COMMUNITY STRUCTURE IN AQUAPONICS POND AND COMMON POND BASED ON HIGH-THROUGHPUT SEQUENCING TECHNOLOGY
-
摘要: 鱼菜共生(Aquaponics)作为一种可持续、循环型、零排放的新型的复合耕作体系, 因具有良好的生态环境效应和食品安全保障, 成为解决农业生态危机的有效途径。研究采用Illumina高通量测序平台对西北地区典型池塘鱼菜共生养殖模式下, 养殖水环境与根系细菌微生物16S rRNA基因(V3—V5区)进行高通量测序。比较群落结构和微生物多样性表明, 细菌总有效序列为56444条, 细菌物种平均注释OTU数目为945条。在鱼菜共生模式下的优势门类为变形菌门(Proteobacteria)、拟杆菌门(Bacteroidetes)、厚壁菌门(Firmicutes)、蓝菌门(Cyanobacteria)。根系微生物群落中占优势地位的分别为拟杆菌门(Bacteroidetes)和变形菌门(Proteobacteria)。OTU聚类分析结果显示6个样品共有OTU数目为165, 其中新疆水生野生动物救护中心鱼菜共生池塘水样(JH.KX)特有OTU数量最高(137), 其空心菜根系水样(JH.R)最低(30), 而乌鲁木齐市米东区长山子镇水源地养殖基地空心菜根系水样(MD.R)和新疆水生野生动物救护中心对照池塘水样(JH.C)数量相同(85)。通过对各OTU进行注释, 发现了根瘤菌、鱼类致病菌、耐寒细菌、降解有机物细菌、降低重金属及毒素危害的细菌。研究为鱼菜共生生态养殖模式下微生物群落结构及其生态调控机理提供了参考依据。Abstract: Aquaponics, a new type of sustainable, cyclic and zero-emission composite farming system, has become an effective method to solve the agricultural ecological crisis because of its good ecological environment effect and food safety guarantee. The 16S rRNA gene (V3-V5 region) of microorganisms in aquaculture environment and roots was sequenced by using Illumina high-throughput sequencing platform under the typical aquaculture pond mode in Northwest China. The comparison of microbial community structure and diversity showed that the total effective sequence of bacteria was 56444, and the average number of annotated OTU was 945. The dominant bacteria were phyla Proteobacteria, Bacteroidete, Firmicutes and Cyanobacteria. The dominant bacteria in MD.R and JH.R were phyla Bacteroidetes and Proteobacteria, respectively. There were 165 OTUs in the six samples with the highest OTU in JH.KX (137), the lowest one in JH.R (30), and the same OTU (85) in MD.R and JH.C. Rhizobia, fish pathogenic bacteria, cold-resistant bacteria and bacteria that decompose organism and reduce heavy metals and toxins were detected by annotating the OTUs. This study revealed the microbial community structure and its ecological regulation mechanism under the aquaponics model.
-
鱼菜共生(Aquaponics)最早可追溯到1500年前东南亚地区的稻田养鱼, 是一项涉及鱼类、微生物和植物三者共营共生的新型复合耕作技术, 通过系统内部可持续性的物质循环和能量流动, 将水产养殖(Aquaculture)和水耕栽培(Hydroponics)两种农耕技术有机结合, 达到鱼-菜-菌的和谐互利共生, 从而实现“养鱼不换水、种菜不施肥”的高效、清洁、健康的生态循环养殖模式[1]。近年来, 在食品安全问题备受关注的背景下, 鱼菜共生健康养殖模式由于其独特的生态、环保和安全优势, 目前已在国内外得到广泛推广和应用[2]。相较传统的线性池塘养殖模式而言, 在鱼菜共生系统中, 鱼类排泄物可作为植物营养, 而植物代谢作用既可改善水质、残根又可供鱼类食用, 微生物作为中间者能够有效调节鱼类和植物间的微生态平衡。新疆作为我国西北典型干旱缺水地区, 为了实现池塘养殖节水和资源循环利用, 近年来部分地区陆续开展了鱼菜共生体系的试验示范。目前关于鱼菜共生的研究多集中在养殖模式的设计和优化[3—6], 而对于环境微生物对水质调节机理方面的研究较少。
细菌作为养殖池塘生态系统的重要组成部分, 其群落结构与多样性组成在水质调节、疾病控制及维持生态系统稳定等方面发挥着重要作用, 很大程度影响着水产动物的健康与生存。基因组(Metagenome), 又称微生物环境基因组(Microbial Environmental genome)或元基因组, 由美国威斯康辛大学麦迪逊分校 Handelsman等[7]在前人研究的基础上于1998年首次提出, 指一定环境中整个微生物群落所有遗传物质的总和。宏基因组学(Metagenomics)是主要依靠生物信息学手段, 分析和比较微生物群落结构、功能及其进化关系的新型技术方法, 目前对宏基因组测序主要包括16S rRNA和全基因组测序两种方法[8], 其中16S rRNA作为揭示生物物种的特征核酸序列, 具有大小适中且突变率小的特点, 被认为是最适合细菌系统发育和分类鉴定的指标[9, 10]。近年来随着分子生物学的发展, 尤其是高通量测序技术的研发及应用, 为微生物分子生态学的研究策略注入了新的力量, 并逐渐成为研究微生物群落多样性的首选实验手段[11—13]。
本文以新疆水生野生动物救护中心和乌鲁木齐市米东区长山子镇水源地养殖基地鱼菜共生池塘为研究对象, 基于宏基因组学的方法, 采用Illumina HiSeq高通量测序技术, 从环境微生物角度探讨鱼菜共生系统中环境微生物和根系微生物群落组成差异及多样性水平, 以期为科学地解释鱼菜共生养殖模式水质调节机理, 以及池塘养殖水体生物调控技术的推广与应用提供参考资料。
1. 材料与方法
1.1 实验地点概况
实验地点位于新疆水生野生动物救护中心和乌鲁木齐市米东区长山子镇水源地养殖基地两处环境条件类似的标准化养殖池塘。池塘面积0.43 hm2, 平均水深1.80 m, 具有独立的进排水系统, 水源为地下深井水, 水质符合GB11607渔业水质标准, 2017年5月18日放养品种为80—100 g/尾的大规格罗非鱼鱼种, 放养量为15000尾/hm2。
1.2 浮床制作及蔬菜移植
池塘水面架设直径为75 mm的PVC排水管制作的浮床, 浮床规格为360 cm×120 cm。聚乙烯网片分上下两层包裹浮床, 其中上层为疏网, 网眼直径3 cm; 下层为密网, 网眼直径0.8 cm。网片用塑料扎带绷紧, 上下网片形成2—3 cm的间距。2017年6月中旬, 剪取长度为15 cm提前在菜地育成的空心菜茎秆, 使用扦插法将其按10 cm株距插入浮床网片中。空心菜茎杆露出下层网片约3—4 cm。将移植好空心菜的浮床用绳子串联, 分8行排布于池塘下风处, 每行12个, 共计96个。浮床面积共计415 m2, 覆盖率约为池塘养殖面积的10.4%。经过一定时间的生长, 待空心菜长至30 cm时开始采摘, 15d左右采摘1次。乌鲁木齐市米东区长山子镇水源地养殖基地鱼菜共生池塘在整个养殖期空心菜共收获5茬, 总产量6250 kg, 单产15.1 kg/m2, 而新疆水生野生动物救护中心鱼菜共生池塘空心菜生长状况较差, 未能形成采摘规模(图 1)。
1.3 样品采集及DNA提取
除两处鱼菜共生池塘外, 另各自选取1口未架设生物浮床的普通池塘作空白对照, 2017年9月10日分别采集水样进行实验, 采集信息详见表 1。每口池塘随机选取8个取样点, 采集距离水面约15 cm深处的10 mL等体积水样, 均匀混合后装入灭菌塑料螺口离心管。将随机剪取的空心菜根系悬浮于PBS缓冲液(0.15 mol/L NaCl, 0.1 mol/L Na2EDTA, pH 8.0)中, 充分摇匀后使用孔径0.22 μm (Millipore)无菌滤膜对水样进行过滤, 并将滤膜剪碎置于无菌冷冻管中。上述所有样品均置于–20℃保存。采用CTAB法[14]对水样基因组DNA进行提取, 紫外分光光度法检测DNA纯度和浓度, 并取适量的DNA样品于离心管中, 使用无菌水稀释至1 ng/μL备用。
表 1 样品信息Table 1. Sampling information养殖基地Aquafarm 鱼菜共生池塘水样Water samples of aquaponics pond 空心菜根系水样
Water samples of water spinach roots对照池塘水样Control group 新疆水生野生动物救护中心Xinjiang Uygur Autonomous Region Aquatic Wildlife Rescue Center JH.KX JH.R JH.C 乌鲁木齐市米东区长山子镇水源地养殖基地Aquaculture base of Changshanzi Town, Midong District, Urumqi MD.KX MD.R MD.C 1.4 PCR扩增及产物回收
以稀释后的基因组DNA为模板, 针对细菌16S rRNA的V3—V4双可变区域, 使用带Barcode的特异引物338F/806R进行扩增, 引物序列为338F(5′-ACTCCTACGGGAGGCAGCA-3′)和806R(5′-GGACTACHVGGGTWTCTAAT-3′)。使用New England Biolabs公司的Phusion® High-Fidelity PCR Master Mixwith GC Buffer和高保真聚合酶进行PCR。50 μL PCR反应体系为: 2×Phusion GC buffer 25 μL, 正反向引物各2.5 μL(10 μmol/L), 模板DNA 15 ng, 加去离子水至终体积至50 μL。PCR反应条件为: 95℃预变性3min; 95℃变性30s, 55℃退火30s, 72℃延伸45s, 30个循环; 最后72℃延伸10min。使用浓度为2%的琼脂糖凝胶对PCR产物进行电泳检测, 使用QIAgen公司的QIAquick Gel Extraction Kit试剂盒对目的条带进行回收, 并送至陕西博瑞德生物科技有限公司测定。
1.5 文库构建及高通量测序
使用 TruSeq® DNA PCR-Free Sample Preparation Kit建库试剂盒进行文库构建, 构建好的文库经过Qubit和Q-PCR定量, 合格后使用Illumina Hiseq2500 PE250测序平台进行高通量测序。
1.6 测序数据分析
在截去Barcode和引物序列后, 使用FLASH1.2.11软件[15]对每个样品的reads进行拼接, Qiime1.7.0软件[16]对拼接后的数据(Raw Tags)进行过滤处理得到高质量的Tags数据(CleanTags)。使用UCHIME 4.1 基于Gold database数据库比对后去除嵌合体序列[17]。Uparse7.0.1001软件[18]对最终有效数据(Effective Tags)进行聚类, 将相似性大于97%的序列定义为OTUs (Operational Taxonomic Units)。筛选OTUs 中出现频数最高的序列作为代表, 采用 Mothur方法与SILVA[19]的SSUrRNA数据库[20]进行物种注释分析(设定阈值为0.8—1.0)。
采用MUSCLE3.8.31软件[21]对OTUs进行序列比对, Qiime1.7.0软件计算Unifrac距离并构建UPGMA聚类树, 并同时计算Chao1指数、Shannon指数、Simpson指数和PD_whole_tree等多样性参数。基于R语言软件绘制样品稀释曲线, 并进行Alpha多样性指数的组间差异分析和无度量多维标定法(Non-Metric Multi-Dimensional Scaling, NMDS)统计。
2. 结果
2.1 样品测序质量及复杂度分析
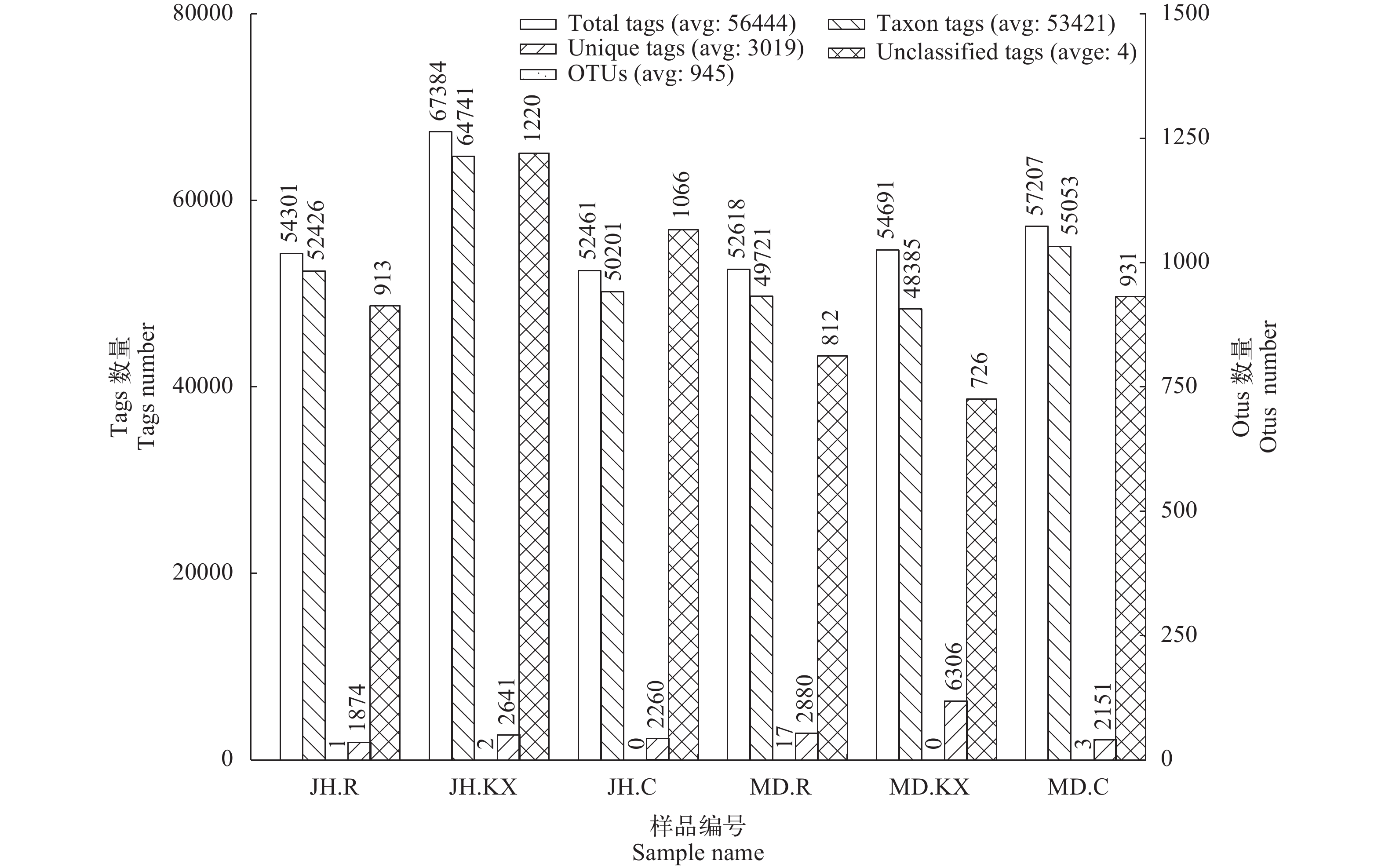
6个样品得到的原始序列为56444条, 用于构建OTU分类信息单元且获得注释信息的平均tags数(Taxon Tags)为53421条, 有效数据量达到94.64%。在相似度大于97%的水平上检测到OTU平均数为945 (图 2)。
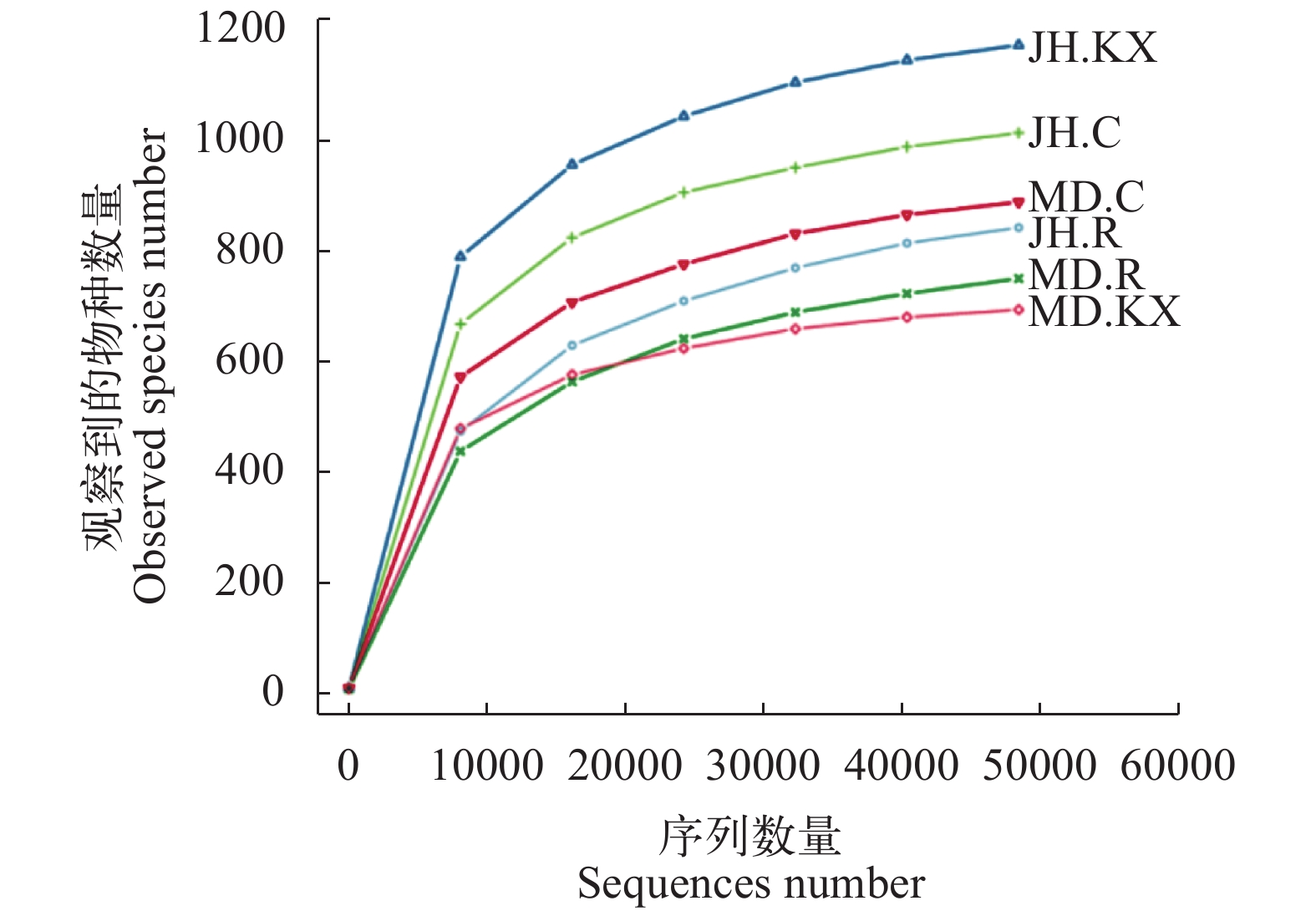
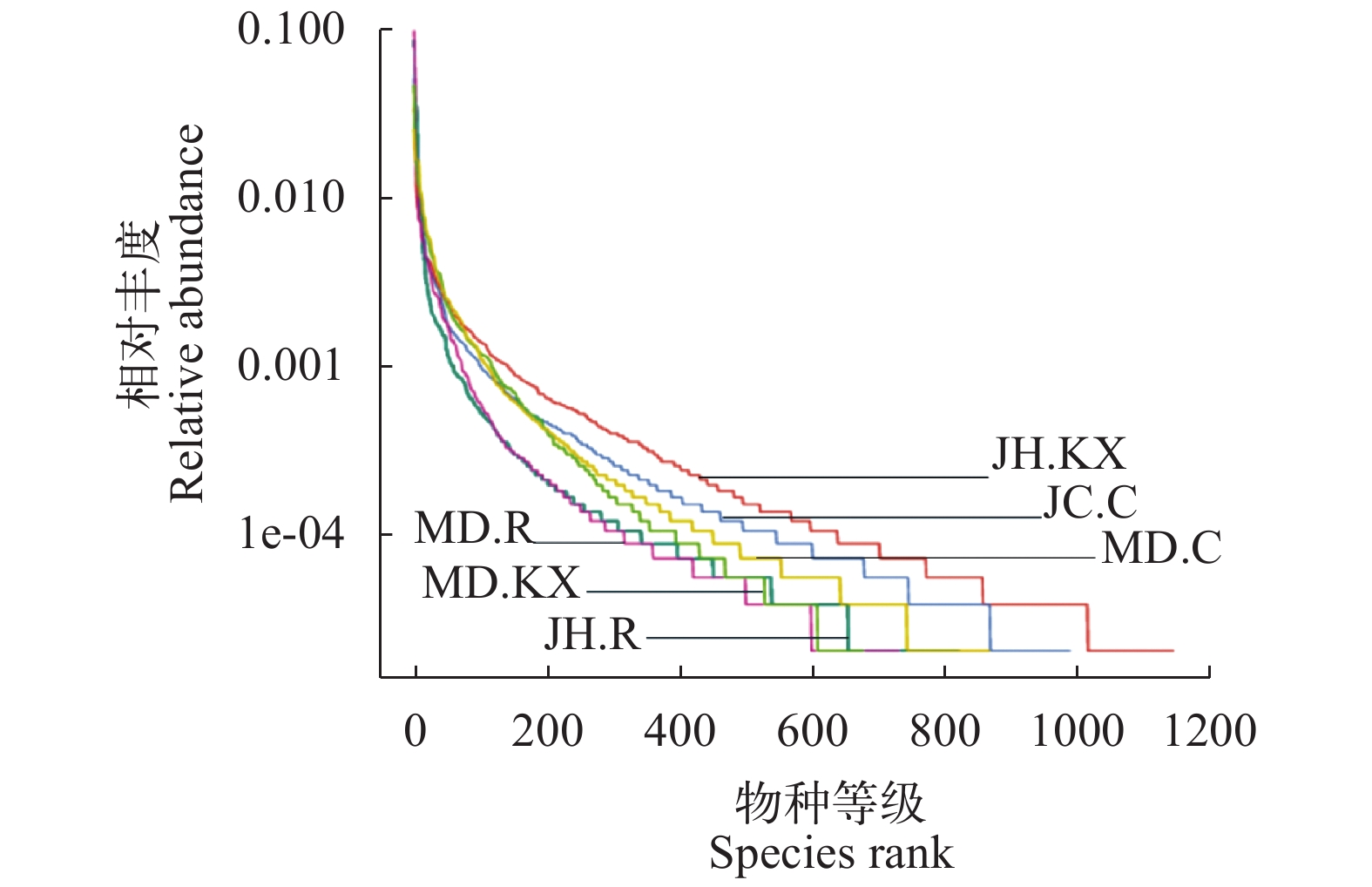
稀释曲线(Rarefaction Curve)是常见的用于描述组内样品多样性的曲线, 可直接反映测序数据量的合理性, 并间接反映样品中物种的丰富程度。对样品随机抽样, 以抽取的测序数据量与对应的物种数构建稀释曲线如图 3所示, 当随机抽取的测序数量大于30000条时, 曲线趋向平坦, 表明测序数据量渐进合理, 更多的数据量对发现新的OTU边际贡献率较小。而当测序数量相同时, 细菌群落OTU数量表现为JH.KX>JH.C>MD.C>JH.R>MD.R>MD.KX, 表明JH.KX微生物丰度明显高于其他样品。Rank Abundance曲线(图 4)直观的反映了样品中物种的丰富度和均匀度。在水平方向上曲线跨度较大, 表明物种的丰富度较高; 而在垂直方向上曲线平滑程度较小, 表明测定样品中物种的均匀程度相对较低。
2.2 细菌微生物群落组成
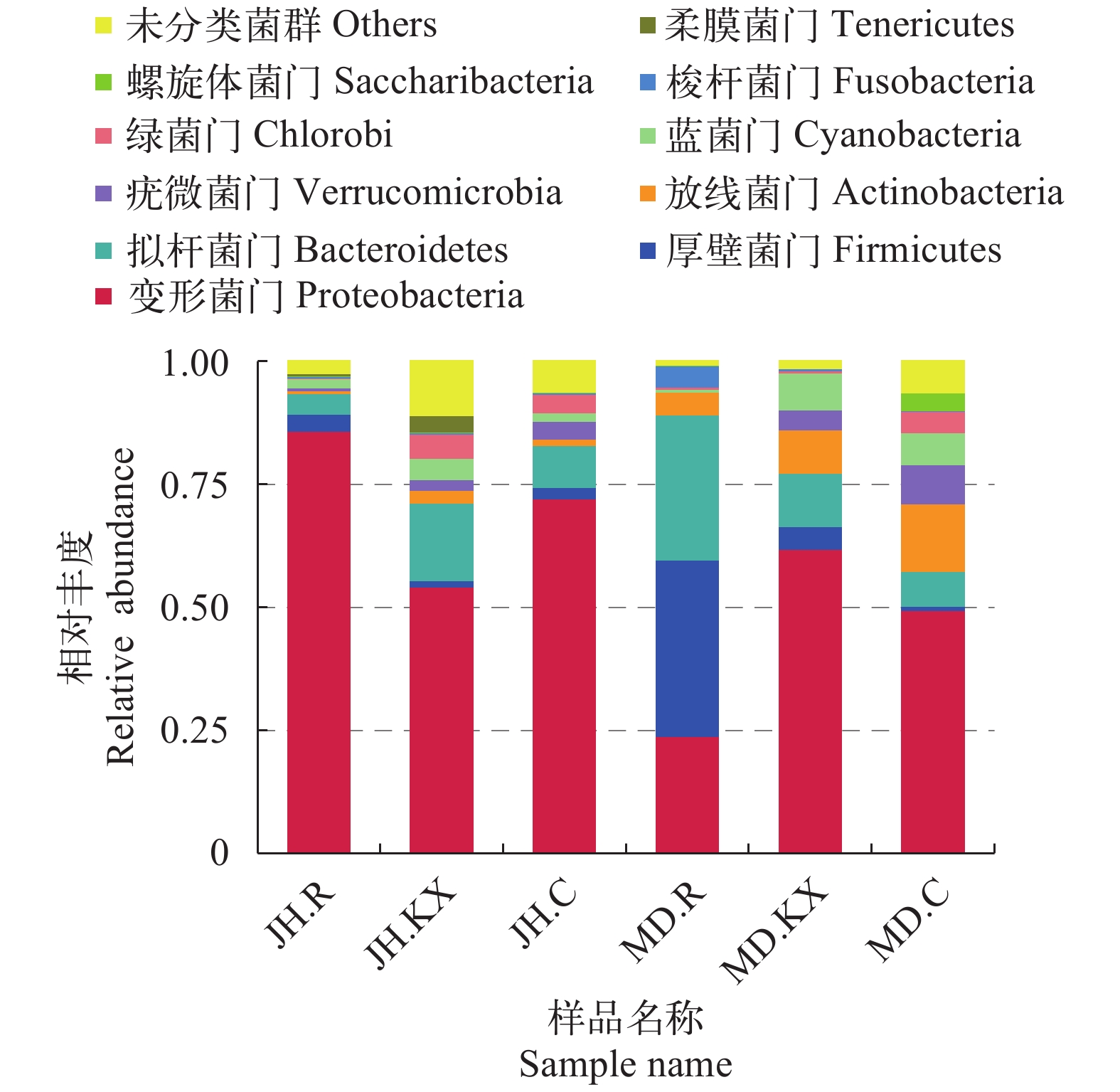
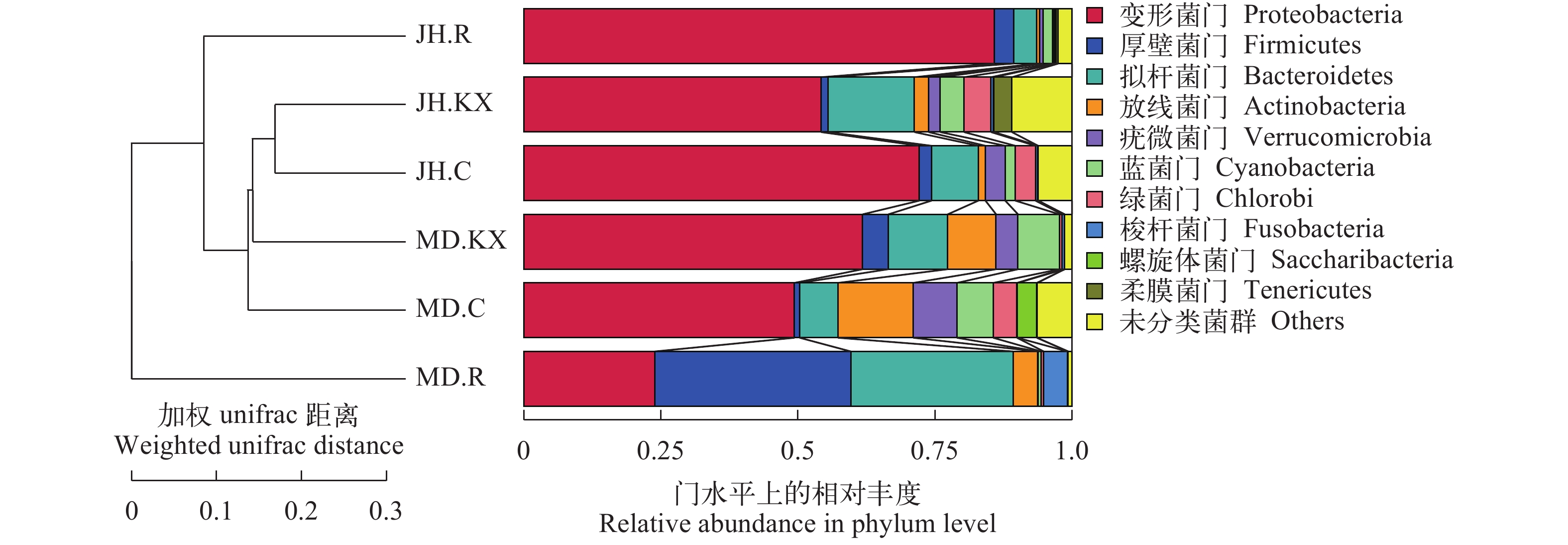
根据物种注释结果, 选取每个样品在各分类水平上最大丰度排名前10的物种, 绘制物种相对丰度柱状图, 以门(Phylum)的水平为例绘制物种相对丰度柱状图如图 5所示, 分别为柔膜菌门(Tenericutes)、螺旋体菌门(Saccharibacteria)、梭杆菌门(Fusobacteria)、绿菌门(Chlorobi)、蓝菌门(Cyanobacteria)、疣微菌门(Verrucomicrobia)、放线菌门(Actinobacteria)、拟杆菌门(Bacteroidetes)、厚壁菌门(Firmicutes)、变形菌门(Proteobacteria)和未分类菌群(Others)。从门分类水平上细菌相对丰度变化趋势来看, 除MD.R (23.86%)以外, 其余样品中检测到的优势菌群主要为变形菌门(Proteobacteria), 所占比例均在49%以上, 其中JH.R高达85.84%。柔膜菌门(Tenericutes)在JH.C、MD.R和MD.KX中均未检测到。实验组水环境微生物群落(JH.KX和MD.KX)中拟杆菌门(Bacteroidetes)、蓝菌门(Cyanobacteria)和梭杆菌门(Fusobacteria)相对丰度均高于各自对照组(JH.C和MD.C), 而疣微菌门(Verrucomicrobia)的相对丰度均明显低于其对照组; 在实验组空心菜根系微生物群落(JH.R和MD.R)中, JH.R微生物群落中变形菌门(Proteobacteria)相对丰度显著偏高, 而MD.R拟杆菌门(Bacteroidetes)和厚壁菌门(Firmicutes)占绝对优势, 比例分别为29.60%和35.79%。
从空心菜长势情况来看, 乌鲁木齐市米东区长山子镇水源地养殖基地鱼菜共生池塘空心菜长势较好, 无论其根系水样(MD.R)还是池塘水样(MD.KX)中, 厚壁菌门(Firmicutes)和放线菌门(Actinobacteria)细菌占比均高于新疆水生野生动物救护中心鱼菜共生池塘。在两处无空心菜生长的池塘中, 拟杆菌门(Bacteroidetes)细菌占比均低于种植空心菜池塘、疣微菌门(Verrucomicrobia)细菌占比均高于种植空心菜池塘。
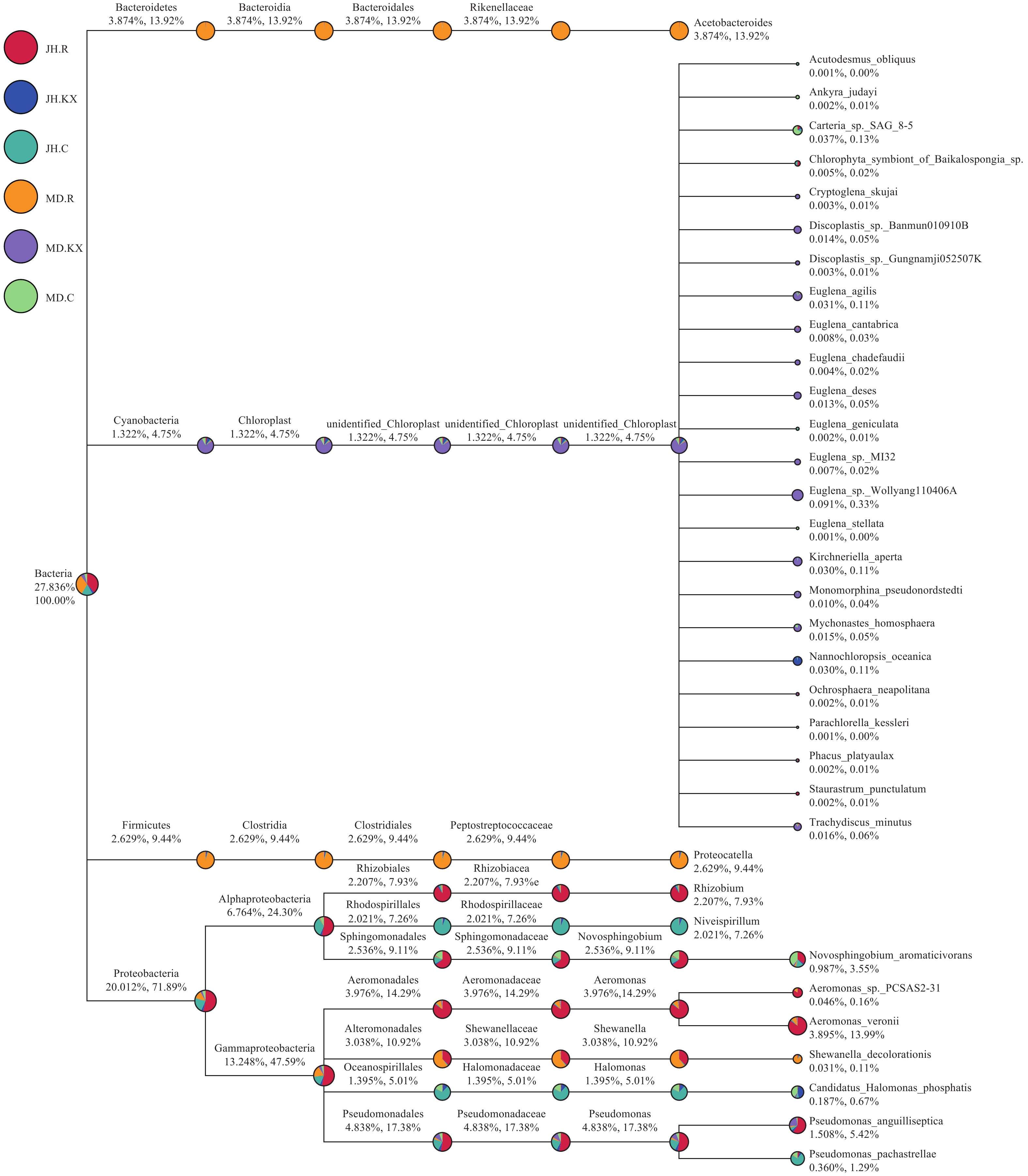
对每个分组的物种分类结果, 筛选特别关注的物种(默认选择最大相对丰度前10的属)进行物种分类树统计(图 6)[22]。图中扇形面积的大小代表分组在该分类上相对丰度的比例, 下方数字表示所有分组在该分类上的平均相对丰度百分率, 前者表示占所有物种的百分率, 后者表示占所选取物种的百分率。从目的水平上来看, MD.R样品中占优势地位的为拟杆菌门(Bacteroidetes)、拟杆菌纲(Bacteroidia)的拟杆菌目(Bacteroidales)和厚壁菌门(Firmicutes)、梭菌纲(Clostridia)的梭菌目(Clostridiales); JH.R样本中大量检测到变形菌门(Proteobacteria)、变形菌纲(Alphaproteobacteria)的根瘤菌目(Rhizobiales)和鞘脂单胞菌目(Sphingomonadales)以及γ-变形菌纲(Gammaproteobacteria)的气单胞菌目(Aeromonadales)和假单胞菌目(Pseudomonadales)的类群, MD.KX的优势菌群来自于蓝菌门(Cyanobacteria/Chloroplast); 红螺菌目(Rhodospirillales)和海洋螺菌目(Oceanospirillales)细菌在JH.C中占优势。
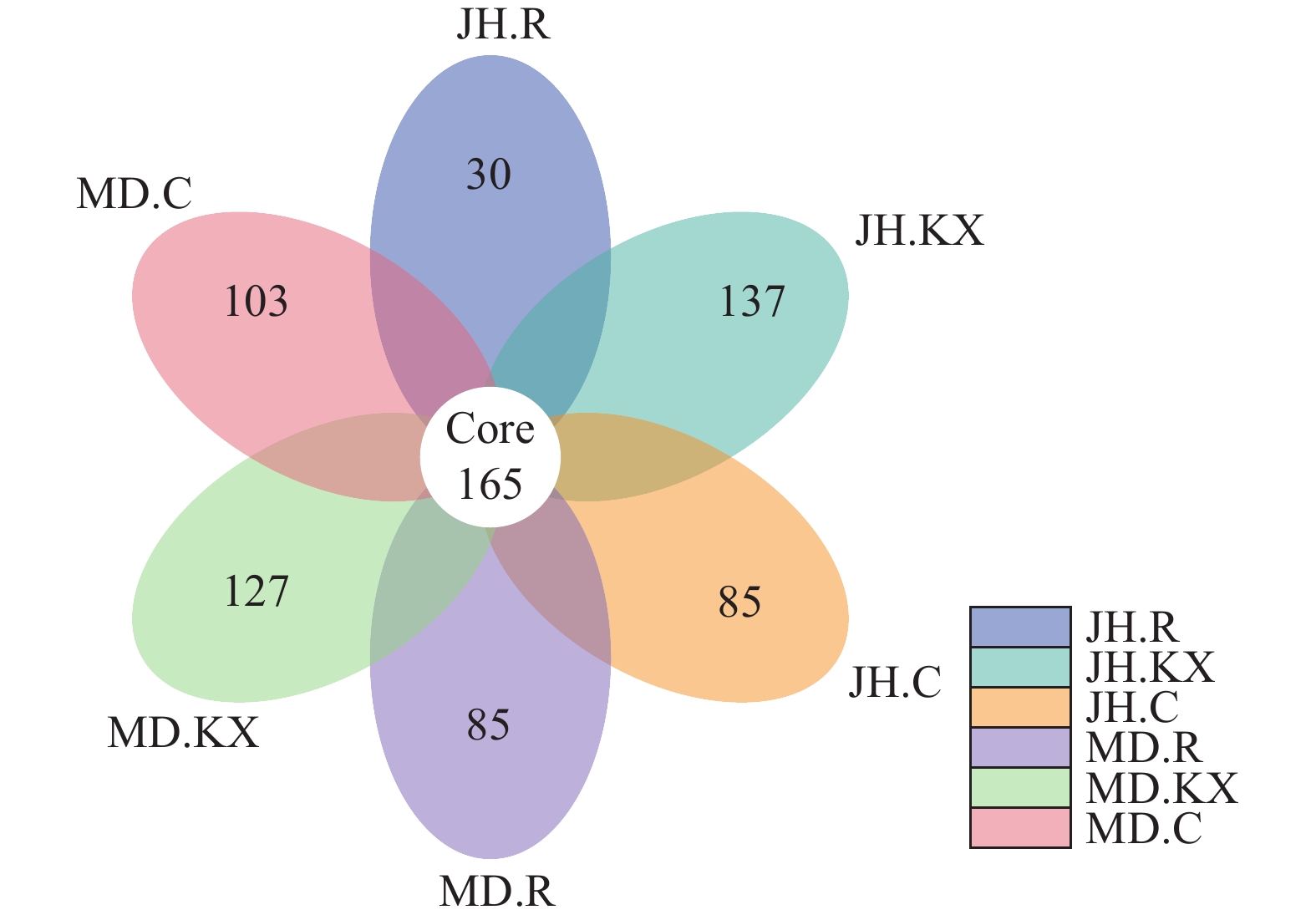
根据OTU聚类分析结果和研究需求, 当样品数大于5时, 对所有样品进行均一化处理, 分析不同样品之间共有和特有的OTU并绘制花瓣图(图 7)。从图中可以直观的看出不同样品OTU数目组成相似性及重叠情况, 6个样品共有的OTU数目为165, 不同样品中特有OTU表现为JH.KX最高(137), JH.R最低(30), 而MD.R和JH.C数量相同, 均为85。
2.3 样品复杂度分析
Alpha多样性分析 Alpha多样性主要关注局域生境或样品内(Within-community)的微生物群落多样性[23], 通过单样本的多样性分析可以反映样品内的微生物群的丰富度和多样性, 进而评估各样品中微生物群落的物种丰富度和多样性的差异。序列相似度大于97%的情况下可聚类成一个OTU, 通常被认为是源自同一个种(Species boundary)。利用Mothur软件对不同样品在97%相似度阈值下的多样性进行分析, 为排除因样本测序数量不同而造成的误差, 以序列最少的样品序列数为基准, 分别进行10次抽样重复, 所得的Alpha多样性指数取平均值如表 2所示。分析表明, 所有取样点的多样性测序结果Coverage均高于99%, 表明测序结果覆盖度好且具有较高可信度, 能够代表样本的真实情况。Shannon指数和Simpson指数是反映物种丰富度和均匀度的2个重要参数, 其值越大表明个体分配越均匀、群落多样性越高, 从表 2可以看出, 6个水样菌落的Shannon多样性指数和Simpson多样性指数排序分别为JH.KX>MD.C>JH.C>MD.KX>MD.R>JH.R和JH.KX>MD.C>MD.KX>JH.C>JH.R>MD.R, 结果表明空心菜根系水样(MD.R和JH.R)中细菌微生物群落多样性相对较低。Chao1指数和ACE指数是生态学中用于估算样本物种丰度的常用指数, 本研究中二者的变化趋势大体一致, 均表现为JH.KX值最大、MD.KX最低, 表明前者中含有的OTU数目最多, 即细菌种类数量最多、群落的丰度也最高, 而后者丰度最低。
表 2 微生物群落多样性指数Table 2. Diversity indices of different microbial communities样品名称Sample name 菌群多样性
Community diversity菌群丰度
Community richness测序深度
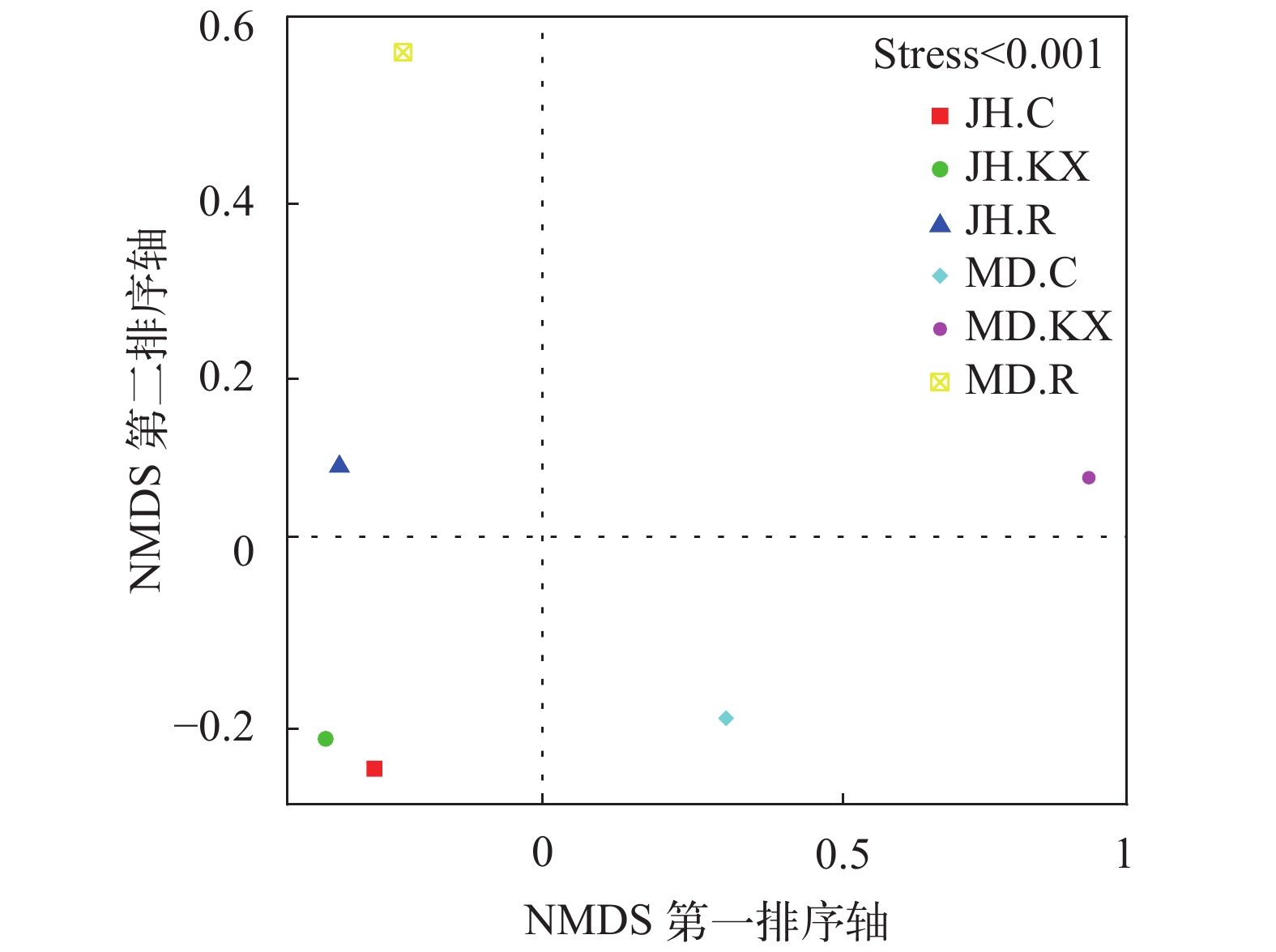
Sequencing depthShannon指数Shannon diversity index Simpson指数Simpson diversity index Chao1指数Chao1 diversity index ACE指数ACE diversity index 覆盖度Goods coverage (%) JH.R 5.368 0.925 941.897 937.193 0.997 JH.KX 7.894 0.987 1197.070 1214.754 0.997 JH.C 6.999 0.973 1047.548 1052.832 0.997 MD.R 5.382 0.910 823.364 818.967 0.997 MD.KX 6.844 0.977 707.188 712.967 0.999 MD.C 7.120 0.984 941.765 941.645 0.997 无度量多维标定法分析 无度量多维标定法(Non-Metric Multi-Dimensional Scaling, NMDS)统计是一种将多维空间样本简化到低维空间进行数据分析的方法, 能够很好地反映生态学数据的非线性结构[24, 25]。NMDS统计结果以点的形式反映在多维空间上, 各样点间的距离体现了彼此差异程度, 距离越近代表相似度越高。基于OTU水平的NMDS排序结果见图 8, 从图中可以看出在排序的胁强系数(Stress, S)小于0.001的情况下, JH.KX与JH.C差异最小, JH.R和MD.R位于第一象限, MD. KX和MD.C分别位于第二和第四象限。
2.4 聚类分析
为了进一步得到不同样品间群落结构差异, 对OTU进行多序列比对并基于Weighted Unifrac距离矩阵构建非加权组平均聚类树(Unweighted Pair-group Method with Arithmetic Mean, UPGMA), 并将聚类结果(左侧)与各样品在门水平上的物种相对丰度分布(右侧)整合展示, 结果如图 9所示, JH.KX与JH.C相似度最高, 与NMDS分析结果类似。MD.R与其他样品间距离最远, 相似度最低。
3. 讨论
3.1 细菌群落结构分析
从各组细菌物种分类树可以看出, JH样本中占绝对优势的细菌主要来自变形菌门(Proteobacteria), 其中来自于空心菜根系样本JH.R的根瘤菌目(Rhizobiales)、鞘脂单胞菌目(Sphingomonadales)、假单胞菌目(Pseudomonadales)、气单胞菌目(Aeromonadales)和交替单胞菌目(Alteromonadales)占优势。促生菌是一类具有固氮、溶磷、解钾、解硫、硝化、反硝化等作用, 参与无机盐循环或能产生植物激素直接或间接促进植物生长的菌[26]。氮循环是鱼菜共生系统的核心过程, 长期以来科研界普遍认为微生物对植物生长的促进作用主要体现在固氮作用和磷转化[27]。其中与固氮作用密切相关的根瘤菌是一类与豆科植物根系共生, 形成根瘤并固定空气中的氮气供植物营养的革兰氏阴性细菌, 在农业生产和固氮生态体系中起着极其重要的作用[28]。按照Jordan在1984年出版的《伯杰氏系统细菌学手册》中分类标准, 将根瘤菌目划分为四个科, 分别为: 慢生根瘤菌科(Bradyrhizobiaceae)、生丝微菌科(Hyphomicrobiaceae)、叶杆菌科(Phyllobacteriaceae)和根瘤菌科(Rhizobiaceae)[29]。有研究发现, 根瘤菌可侵入非豆科植物根内, 对促进植物生长有益, 尤其是对某些水生植物, 如水稻的生长和增产大有帮助[30]。王旭明[31]通过研究证实, 空心菜对污水中氮、磷的去除率分别可达87.36%和76.4%, 石焱等[32]通过大规模养殖试验表明人工浮床水培水雍菜对池塘养殖废水中氨氮、总氮和总磷有良好的去除效果。在本实验中空心菜根系样本中检测到根瘤菌的存在, 推测其改变了根系对无机营养盐和矿物质吸收的生理活动, 从而促进空心菜的生长。此外, 鞘脂单胞菌目(Sphingomonadales)中包含的新鞘氨醇杆菌属(Novosphingobium)可以降解芳香族化合物, 如苯酚、苯胺、硝基苯和菲[33], 这些细菌有利于改善水质、降低有机物污染, 促进水生植物生长, 降低水中鱼类受这些化合物的污染, 从而改善水产品质。然而, JH.R中假单胞菌目(Pseudomonadales)所包含的鱼类致病菌Pseudomonas anguilliseptica数量明显高于MD.R, 可能干扰了鱼类的正常代谢[34], 其负面影响高于益生菌的作用, 影响了空心菜的生长, 这可能是新疆水生野生动物救护中心鱼菜共生池塘空心菜生长较差一个重要原因。另外, 从池塘水质理化数据来看, pH (9.26)高于米东区长山子镇水源地养殖基地鱼菜共生池塘(8.05), 这对于喜中偏酸性环境的空心菜而言, 不利于其生长。而氨氮、钙、镁含量(0.525、25.2和7.462 mg/L)明显低于后者(0.834、125.94和46.056 mg/L), 这些营养物质的缺乏也使得空心菜长势较差。
3.2 水质条件和细菌多样性的关系
米东区长山子镇水源地养殖基地池塘样本中独有且占优势的类群为拟杆菌门(Bacteroidetes)、厚壁菌门(Firmicutes)和蓝菌门(Cyanobacteria), 其中前两者在根系中占优势。拟杆菌门(Bacteroidetes)涵盖了三大类革兰氏阴性菌, 即非孢子形成菌、厌(需)氧菌和杆状细菌, 它们广泛分布在土壤、沉积物和海水环境中, 以及动物的内脏和皮肤中。厚壁菌门(Firmicutes)下的Proteocatella属, 包含一些厌氧耐寒的细菌[35], 这些细菌在冬季温度较低时仍能够改变池塘水质。蓝菌门(Cyanobacteria)的蓝藻类是产生水华的主要原因, 也是水体富营养化的征兆[36, 37], 推测这可能是米东区长山子镇水源地养殖基地池塘中空心菜生长较好的原因之一, 此外, 空心菜的生长有利于净化水质, 消除富营养化, 利于水中鱼类的生存。JH.R和MD.R二者共有的细菌类群为气单胞菌目 (Aeromonadales)和交替单胞菌目(Alteromonadales), 气单胞菌目下的气单孢菌属(Aeromonas)普遍存在于淡水和半咸水中[38]。交替单胞菌目下的希瓦氏菌属(Shewanella), 大部分发现于温度较低的水体中[39], 这与西北地区水体温度较低的状况相一致。希瓦氏菌属(Shewanella)常用于环境的生物修复, 能够降低水中有毒物质和重金属的毒性, 从而提高生物浮床系统对污染物的去除效率。
3.3 细菌组成对水培蔬菜生长的影响
门水平上的物种丰度图显示MD.R样本中来自于变形菌门(Proteobacteria)、蓝菌门(Cyanobacteria)和厚壁菌门(Firmicutes)的细菌占优势, 且分布均匀, 占比相差不大。与其他组比较, 前者明显偏低, 而后两者明显偏高。有研究证实, 种植基质中微生物组成多样性越高、群落结构越复杂, 越能促进植物的生长, 单一细菌与真菌菌群对植物生长甚至产生抑制作用[40]。从本实验的结论以及现场抽样检测来看, 来自于米东区长山子镇水源地养殖基地鱼菜共生池塘的空心菜长势较好, 与其根系细菌分布均匀度呈正相关。这表明植株根际附近微生物生理活动更为活跃, 各种代谢功能也更为频繁。
从花瓣图中特有OTU可以看出, 种植空心菜的水样中的OTU数量最多, 明显高于未种植空心菜水样。水培蔬菜不仅增加水体的溶解氧含量, 根系还为微生物的生长和繁殖提供了场所, 其分泌物能促进某些固氮细菌、嗜磷细菌的生长, 降低水体中含氮化合物的浓度、改善养殖环境中的微生态平衡[41], 与此同时, 植物根际微生物数量的增加, 在其周围构建起一个物理屏障保护了植物根系, 从而减少病原菌和虫害的入侵。本研究结果证实了水培植物的种植有利于池塘水体中细菌微生物生长, 而这些共生细菌的存在反过来也极大地促进了蔬菜的生长。
对比两处试验点空心菜根系上特有OTU, 发现米东区长山子镇水源地养殖基地鱼菜共生池塘空心菜根系(MD.R)中特有OTU明显高于新疆水生野生动物救护中心(JH.R), 而这些特有OTU可能与该池塘空心菜生长较好有关。刘志敏等[42]通过研究发现, 根际细菌在提高蔬菜对环境胁迫的抗逆性上有着十分重要的作用, 能有效促进植物的生长。因此, 从某种意义上来讲, 蔬菜根际和种植环境中细菌微生物之间存在相互促进、相互调节的作用机制。
NMDS排序图显示JH.C与JH.KX处于同一象限, 且相聚最近, 表明两者微生物群落结构相似, 而MD.C与MD.KX位于不同象限, 显示两者微生物群落结构相差较大, 这可能是因为米东区长山子镇水源地养殖基地(MD)池塘空心菜生长较旺盛, 对水质改善较大, 改变水体细菌结构组成多样性的程度较高。此外, JH.R和MD.R也处于同一象限, 表明二者存在生长于空心菜根系上的共有细菌。在UPGMA聚类图中, 鱼菜共生池塘水中的细菌与对照水体较为相似, 而与根系上的细菌差别较大也证明了此点。这可能是由于受到根系的影响, 使得植物根际的微区域环境与其周围的环境主体在物理、化学和生物方面存在很大差别。
-
表 1 样品信息
Table 1 Sampling information
养殖基地Aquafarm 鱼菜共生池塘水样Water samples of aquaponics pond 空心菜根系水样
Water samples of water spinach roots对照池塘水样Control group 新疆水生野生动物救护中心Xinjiang Uygur Autonomous Region Aquatic Wildlife Rescue Center JH.KX JH.R JH.C 乌鲁木齐市米东区长山子镇水源地养殖基地Aquaculture base of Changshanzi Town, Midong District, Urumqi MD.KX MD.R MD.C 表 2 微生物群落多样性指数
Table 2 Diversity indices of different microbial communities
样品名称Sample name 菌群多样性
Community diversity菌群丰度
Community richness测序深度
Sequencing depthShannon指数Shannon diversity index Simpson指数Simpson diversity index Chao1指数Chao1 diversity index ACE指数ACE diversity index 覆盖度Goods coverage (%) JH.R 5.368 0.925 941.897 937.193 0.997 JH.KX 7.894 0.987 1197.070 1214.754 0.997 JH.C 6.999 0.973 1047.548 1052.832 0.997 MD.R 5.382 0.910 823.364 818.967 0.997 MD.KX 6.844 0.977 707.188 712.967 0.999 MD.C 7.120 0.984 941.765 941.645 0.997 -
[1] 饶伟, 李道亮, 位耀光, 等. 循环水养殖新模式-鱼菜共生系统. 中国水产, 2017, (5): 76—79 Rao W, Li D L, Wei Y G, et al. Aquaponics, a new mode of recirculating aquaculture [J]. China Fisheries, 2017, (5): 76—79
[2] Love D C, Fry J P, Genello L, et al. An international survey of aquaponics practitioners [J]. PLoS One, 2014, 9(7): e102662 doi: 10.1371/journal.pone.0102662
[3] 丁永良, 张明华, 张建华, 等. 鱼菜共生系统的研究. 中国水产科学, 1997, 4(5): 70—75 doi: 10.3321/j.issn:1005-8737.1997.05.013 Ding Y L, Zhang M H, Zhang J H, et al. Researches on fish and vegetable co-existing system [J]. Journal of Fishe-ry Sciences of China, 1997, 4(5): 70—75 doi: 10.3321/j.issn:1005-8737.1997.05.013
[4] 胡靖东, 车斌, 吴石桥, 等. 面向餐饮店生态化定位的鱼菜共生系统优化. 南方农业, 2017, 11(35): 39—42 Hu J D, Che B, Wu S Q, et al. System optimization of fish and vegetable co-existing oriented to ecological positioning restaurants [J]. South China Agriculture, 2017, 11(35): 39—42
[5] 张明华, 丁永良, 杨菁, 等. 鱼菜共生技术及系统工程研究. 渔业信息与战略, 2004, 19(4): 7—12 doi: 10.3969/j.issn.1004-8340.2004.04.002 Zhang M H, Ding Y L, Yang J, et al. A study on fish and vegetable co-existing technique and systems engineering [J]. Modern Fisheries Information, 2004, 19(4): 7—12 doi: 10.3969/j.issn.1004-8340.2004.04.002
[6] 张海生, 董海林. 中小型水库鱼菜共生立体生态养殖试验. 河北渔业, 2015, (6): 36—37 Zhang H S, Dong H L. Dimensional ecological aquaculture experiment on fish and vegetable co-existing in small and medium reservoirs [J]. Hebei Fisheries, 2015, (6): 36—37
[7] Handelsman J, Rondon M R, Brady S F, et al. Molecular biological access to the chemistry of unknown soil microbes: a new frontier for natural products [J]. Chemistry and Biology, 1998, 5(10): 245—249 doi: 10.1016/S1074-5521(98)90108-9
[8] Streit W S, Daniel R. Metagenomics: Methods and Protocols (Second edition) [M]. New York: Human Press. 2010, 13-21
[9] Langille M G I, Zaneveld J, Caporaso J G, et al. Predic-tive functional profiling of microbial communities using 16S rRNA marker gene sequences [J]. Nature Biotechnology, 2013, 31(9): 814—821 doi: 10.1038/nbt.2676
[10] Tran Q, Pham D T, Phan V. Using 16S rRNA gene as marker to detect unknown bacteria in microbial communities [J]. BMC Bioinformatics, 2017, 18(Suppl. 14): 499—505
[11] Rapin A, Pattaroni C, Marsland B J, et al. Microbiota analysis using an Illumina MiSeq platform to sequence 16S rRNA genes [J]. Current Protocols in Mouse Biology, 2017, 7: 100—129 doi: 10.1002/9780470942390.2017.7.issue-2
[12] Caporaso J G, Lauber C L, Walters W A, et al. Ultra-high-throughput microbial community analysis on the Illumina HiSeq and MiSeq platforms [J]. The ISME Journal, 2012, 6(8): 1621—1624 doi: 10.1038/ismej.2012.8
[13] 张正, 李彬, 王印庚, 等. 基于高通量测序的池塘养殖半滑舌鳎消化道菌群的结构特征分析. 水生生物学报, 2015, 39(1): 38—45 doi: 10.7541/2015.5 Zhang Z, Li B, Wang Y G, et al. The microflora structure in digestive tract of half-smooth tongue sole (Cynoglossus semilaevis Güther) cultured in outdoor pond basing on high-through sequencing technique [J]. Acta Hydrobiologica Sinica, 2015, 39(1): 38—45 doi: 10.7541/2015.5
[14] Murray M G, Thompson W F. Rapid isolation of high molecular weight plant DNA [J]. Nucleotide Acids Research, 1980, 8(19): 4321—4325 doi: 10.1093/nar/8.19.4321
[15] Magoč T, Salzberg S L. FLASH: fast length adjustment of short reads to improve genome assemblies [J]. Bioinformatics, 2011, 27(21): 2957—2963 doi: 10.1093/bioinformatics/btr507
[16] Caporaso J G, Kuczynski J, Stombaugh J, et al. QIIME allows analysis of high-throughput community sequencing data [J]. Nature Methods, 2010, 7(5): 335—336 doi: 10.1038/nmeth.f.303
[17] Edgar R C, Haas B J, Clemente J C, et al. UCHIME improves sensitivity and speed of chimera detection [J]. Bioinformatics, 2011, 27(16): 2194—2200 doi: 10.1093/bioinformatics/btr381
[18] Edgar R C. UPARSE: highly accurate OTU sequences from microbial applicant reads [J]. Nature Methods, 2013, 10(10): 996—998 doi: 10.1038/nmeth.2604
[19] Wang Q, Garrity G M, Tiedje J M, et al. Naive Bayesian classifier for rapid assignment of rRNA sequences into the new bacterial taxonomy [J]. Applied and Environmental Microbiology, 2007, 73(16): 5261—5267 doi: 10.1128/AEM.00062-07
[20] Quast C, Pruesse E, Yilmaz P, et al. The SILVA ribosomal RNA gene database project: improved data processing and web-based tools [J]. Nucleotide Acids Research, 2013, 14: 590—596
[21] Edgar R C. MUSCLE: multiple sequence alignment with high accuracy and high throughput [J]. Nucleic Acids Research, 2004, 32(5): 1792—1792 doi: 10.1093/nar/gkh340
[22] DeSantis T Z, Hugenholtz P, Keller K, et al. NAST: a multiple sequence alignment server for comparative analysis of 16S rRNA genes [J]. Nucleic Acids Research, 2006, 34(suppl. 2): 394—399
[23] Li B, Zhang X, Guo F, et al. Characterization of tetracycline resistant bacterial community in saline activated sludge using batch stress incubation with high-throughput sequencing analysis [J]. Water Research, 2013, 47(13): 4207—4216 doi: 10.1016/j.watres.2013.04.021
[24] Kruskal J B. Nonmetric multidimensional scaling: A numerical method [J]. Psychometrika, 1964, 29(2): 115—129 doi: 10.1007/BF02289694
[25] Kenkel N C, Orloci L. Applying metric and nonmetric multidimensional scaling to ecological studies: some new results [J]. Ecology, 1986, 67(4): 919—928 doi: 10.2307/1939814
[26] 肖蓉, 曹秋芬, 聂园军, 等. 基于高通量测序患炭疽病草莓根际与健康草莓根际细菌群落的比较研究. 中国农学通报, 2017, 33(11): 14—20 doi: 10.11924/j.issn.1000-6850.casb16050118 Xiao R, Cao Q F, Nie Y J, et al. A comparative study on Rhizosphere soil bacterial communities of healthy strawberry and infected strawberry with anthracnose by high-throughput sequencing [J]. Chinese Agricultural Science Bulletin, 2017, 33(11): 14—20 doi: 10.11924/j.issn.1000-6850.casb16050118
[27] Alexander M. Introduction to Soil Microbiology (Second Edition) [M]. New York: John Wiley & Sons. 1977, 35—46
[28] 陈文新, 汪恩涛. 中国根瘤菌. 北京: 科学出版社. 2011, 21—22 Chen W X, Wang E T. Rhizobia in China [M]. Beijing: Science Press. 2011, 21—22
[29] Holt J G, Krieg N R, Snealth P H A, et al. Bergey’s Manual of Determinative Bacteriology [M]. Philadelphia: Lippincott Williams & Wilkins. 1984, 157—158
[30] 李婷, 何来, 梁泉峰. 非豆科植物的根瘤菌促生机制的研究进展. 中国农业科技导报, 2013, 15(2): 97—102 Li T, He L, Liang Q F. Progress in the study of Rhizo-bium associated with non-leguminous plants [J]. Journal of Agricultural Science and Technology, 2013, 15(2): 97—102
[31] 王旭明. 水雍菜在污水净化系统中的作用. 农业环境与发展, 1997, 14(1): 33—48 Wang X M. The role of Ipomoea aquatica in sewage purification system [J]. Agricultural Environment and Deve-lopment, 1997, 14(1): 33—48
[32] 石焱, 马徐发, 吴志新, 等. 水雍菜浮床养殖模式下黄颡鱼肠道菌群结构分析. 华中农业大学学报, 2016, 35(2): 69—76 Shi Y, Ma X F, Wu Z X, et al. Intestinal microbial communities of yellow catfish (Pseudobagrus fulvidraco) in pond with Ipomoea aquatic forsk planted on artificial floating beds [J]. Journal of Huazhong Agricultural University, 2016, 35(2): 69—76
[33] Liu Z P, Wang B J, Liu Y H, et al. Novosphingobium taihuense sp nov., a novel aromatic-compound-degrading bacterium isolated from Lake Tai, China [J]. Internatio-nal Journal of Systematic and Evolutionary Microbiology, 2005, 55(3): 1229—1232 doi: 10.1099/ijs.0.63468-0
[34] Surhone L M, Tennoe M T, Henssonow S F, et al. Pseudomonas Anguilliseptica [M]. Montana: Betascript Publishing. 2011, 30-32
[35] Pikuta E V, Hoover R B, Marsic D, et al. Proteocatella sphenisci gen. nov. sp. nov. a psychrotolerant, spore-forming anaerobe isolated from penguin guano [J]. International Journal of Systematic and Evolutionary Microbio-logy, 2009, 59(9): 2302—2307 doi: 10.1099/ijs.0.002816-0
[36] 胡鸿钧. 水华蓝藻生物学. 北京: 科学出版社. 2011, 3—4 Hu H J. The Biology of Water-blooms Blue-green Algae [M]. Beijing: Science Press. 2011, 3—4
[37] 余博识, 吴忠兴, 朱梦灵, 等. 水果湖湾蓝藻水华的形成及其对东湖影响的评价. 水生生物学报, 2008, 32(2): 286—289 doi: 10.3321/j.issn:1000-3207.2008.02.024 Yu B S, Wu Z X, Zhu M L, et al. The formation of cyanobacteial bloom in the Shuiguohu Bay and its effect on Donghu Lake, Wuhan [J]. Acta Hydrobiologica Sinica, 2008, 32(2): 286—289 doi: 10.3321/j.issn:1000-3207.2008.02.024
[38] Graf J. Aeromonas [M]. Poole: Caister Academic Press. 2015, 37-38
[39] Wang X Y, Quinn P J. Endotoxins: Structure, Function and Recognition [M]. Berlin: Springer. 2010, 125-126
[40] 刘杰. 连作及轮作土壤微生物菌群对黄瓜生长的影响. 东北农业大学. 2015 Liu J. Growth response of cucumber to soil microbial communities from conventional monocropping and rotation system [D]. Northeast Agricultural University. 2015
[41] 罗竞, 柯卫东, 刘玉平, 等. 水生蔬菜在水体修复中的应用概况. 长江蔬菜, 2013, 18: 37—41 doi: 10.3865/j.issn.1001-3547.2013.24.013 Luo J, Ke W D, Liu Y P, et al. Application of aquatic vegetables in water restoration [J]. Journal of Changjiang Vegetables, 2013, 18: 37—41 doi: 10.3865/j.issn.1001-3547.2013.24.013
[42] 刘志敏, Nowak J, Asiedu S K, 等. 利用共生细菌提高蔬菜抗逆性的研究. 中国科学技术协会第二届青年学术年会园艺学论文集. 1995 Liu Z M, Nowak J, Asiedu S K, et al. Study on improving stress resistance of vegetables by symbiotic bacteria [C]. The 2nd Annual Youth Academic Confe-rence of China Association for Science and Technology, Horticulture Collection. 1995
-
期刊类型引用(18)
1. 李天沛,汪小旵,施印炎,丁为民. 鱼菜共生技术及其系统装备的研究现状与展望. 南京农业大学学报. 2025(01): 85-96 .  百度学术
百度学术
2. 刘美琦,叶旭婷,杨璐,陈姣宇,顾钱洪,李胜男. 荷-鱼共养与常规池塘养殖模式下环境微生物群落比较研究. 南方水产科学. 2025(01): 140-152 .  百度学术
百度学术
3. 任思齐,应赵晗,吴昕睿,李明,贺文芳,田磊,徐勇斌,程霄玲,郑善坚. 不同蔬菜种植对虾菜共生系统中微生物群落结构的影响. 安徽农业科学. 2024(10): 103-108 .  百度学术
百度学术
4. 钟可儿,王静宇,黄江峰,章海鑫,周智勇,徐先栋. 江西养殖水体细菌群落结构及其与环境因子的关系. 大连海洋大学学报. 2024(04): 675-683 .  百度学术
百度学术
5. 范立民,王庆,陈曦,裘丽萍,孟顺龙,宋超,苏永腾,胡庚东,陈家长. 浮床空心菜对罗非鱼养殖池塘水体微生态环境影响方式分析. 中国农学通报. 2023(02): 142-151 .  百度学术
百度学术
6. 张琴,陈灿,黄璜,张印. 水生蔬菜综合种养对水田生境的影响分析. 农业与技术. 2023(08): 1-5 .  百度学术
百度学术
7. 容庭,李贞明,余苗,崔艺燕,李袁飞,田志梅,马现永,陈卫东. 浅谈种养结合模式在水产养殖业中的应用. 广东畜牧兽医科技. 2023(03): 57-62 .  百度学术
百度学术
8. 温晴宇,李文红,徐鹏,杨卓,胡宏. 强降雨对鱼菜共生池塘水质和浮游植物及细菌群落结构的影响. 西南农业学报. 2022(03): 632-639 .  百度学术
百度学术
9. 陈倩茹,夏雪,王川,李前正,张洪培,陈迪松,吴振斌,周巧红. 沙颍河下游城市黑臭内河沉积物微生物群落季节变化特征. 水生生物学报. 2021(01): 182-189 .  本站查看
本站查看
10. 李小龙,位耀光,吴英昊,赵谦,张岚,贾楠,麻志宏,常晓莲,李志强,杨雅静,滕飞. 智能化鱼菜共生系统及其在都市农业中的应用综述. 安徽农业科学. 2021(14): 8-12 .  百度学术
百度学术
11. 聂志娟,邵乃磷,张志伟,胡佳雯,徐跑,徐钢春. 两种养殖模式下黑鲷肠道及养殖水体菌群结构特征的研究. 中国农学通报. 2021(27): 155-164 .  百度学术
百度学术
12. 王大贺,陈旺,蔡鹏飞,刘少贞,王伟伟,刘青. 罗氏沼虾及蔬菜在日光温室内不同养殖系统中生产性能的比较研究. 水产学杂志. 2021(05): 77-85 .  百度学术
百度学术
13. 谢梦琪,张诗雨,许荔立,蒋飞,袁军法,吴志新,陈孝煊. 不同性别和生长阶段对克氏原螯虾肠道菌群多样性的影响. 水生生物学报. 2021(06): 1243-1254 .  本站查看
本站查看
14. 黄薇,周华书,刘兰英,罗土炎,宋永康. 鲟鳇鱼网箱养殖环境微生物菌群结构及潜在病原菌分析. 水生生物学报. 2021(06): 1255-1263 .  本站查看
本站查看
15. 欧明烛,马菁华,杨朔,刘芳,任启飞. 鱼菜共生的关键技术及发展前景. 绿色科技. 2020(01): 183-184 .  百度学术
百度学术
16. 聂凌云,杨昌珍,皮杰. 鱼菜共生系统对水质净化的研究进展. 水产养殖. 2020(07): 24-28 .  百度学术
百度学术
17. 王一亭,李波,王厚红,吴法龙,张磊. 基于Miseq测序技术分析黄颡鱼不同养殖模式下池塘微生物群落结构多样性. 水生生物学报. 2020(04): 781-789 .  本站查看
本站查看
18. 王瑞宁,王淼,黄秋标,衣萌萌,李忠徽,李庆勇,朱德兴,卢迈新. 基于高通量测序的晒塘前后鳗鲡养殖池塘微生物群落结构差异分析. 农业生物技术学报. 2020(07): 1250-1259 .  百度学术
百度学术
其他类型引用(9)




 下载:
下载: