STUDY ON PHYSIOLOGICAL REACTION OF CERATOPHYLLUM DEMERSUM TO SALINITY AND ALKALINITY STRESS
-
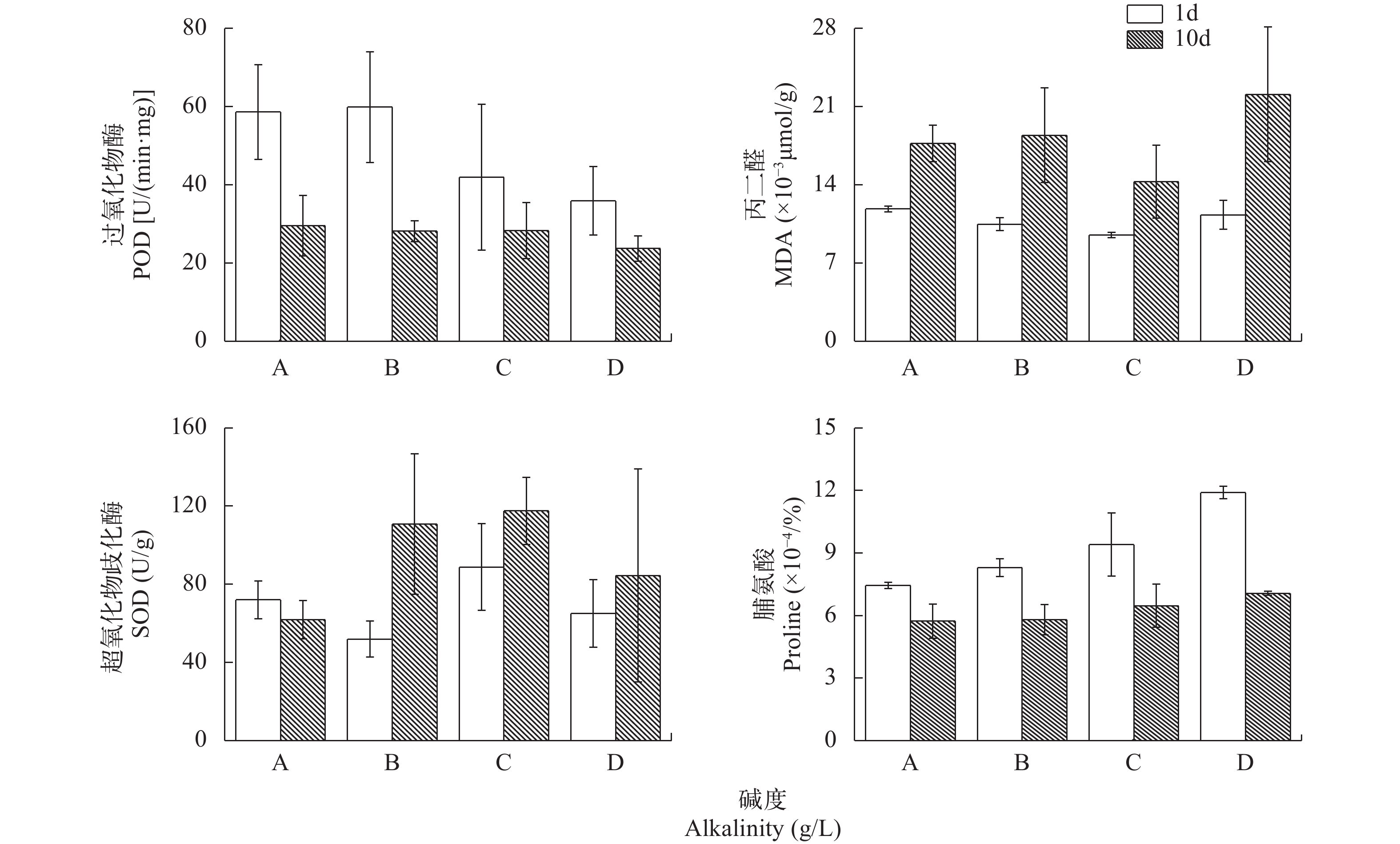
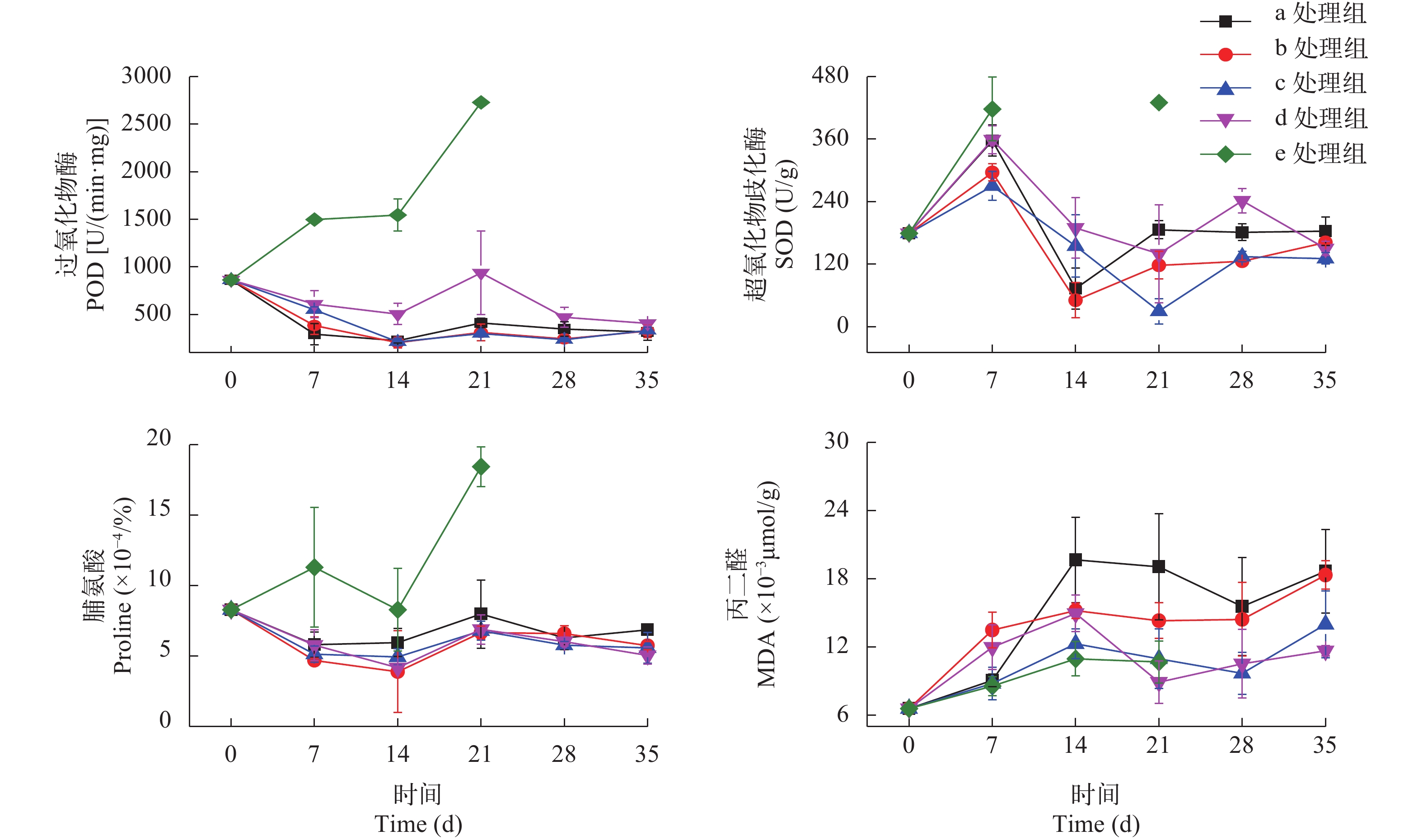
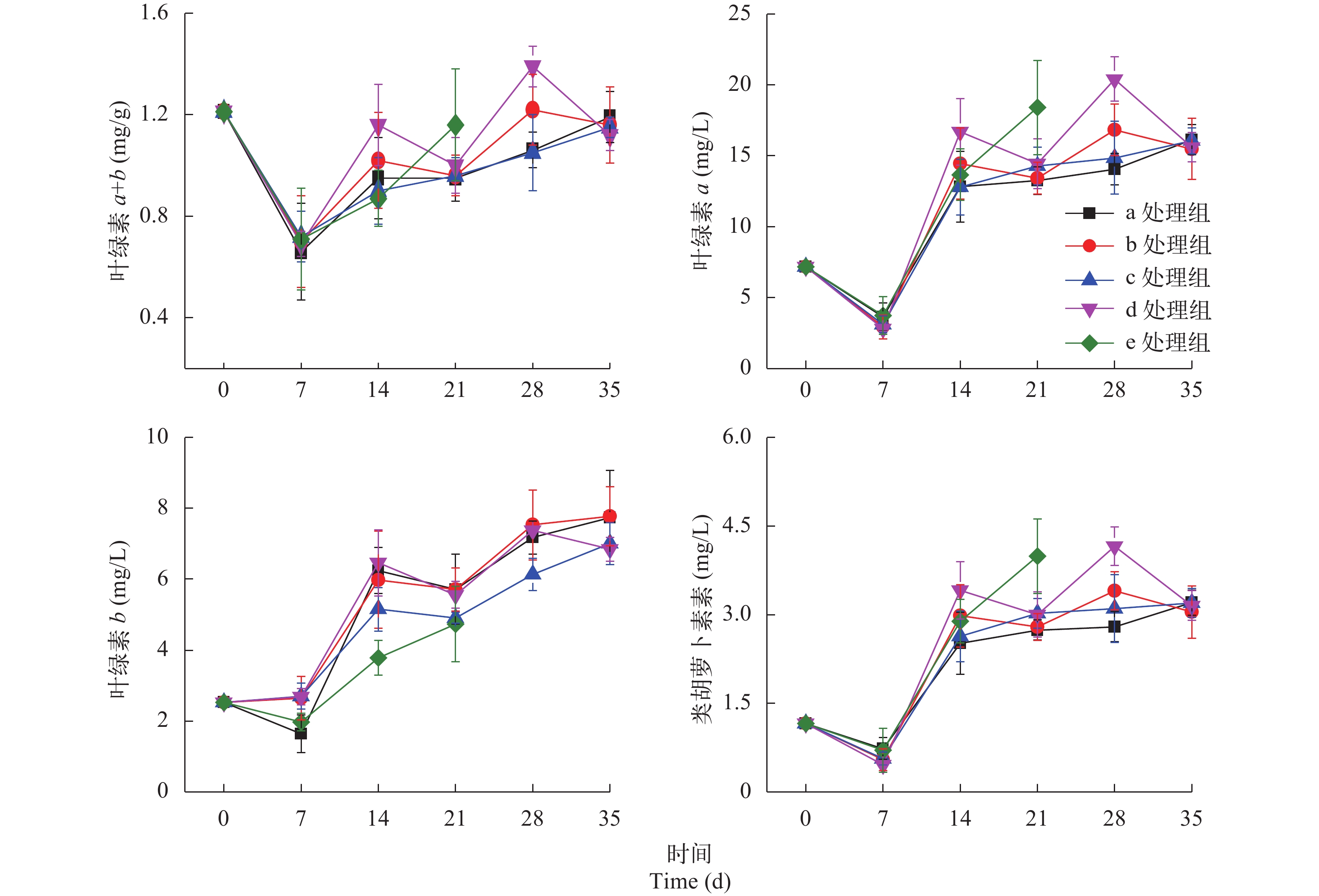
摘要: 白鹤湖作为莫莫格湿地保护区内的代表性湖泊, 正面临着盐碱化和富营养化的风险, 现存沉水植物种类稀少, 为了减缓白鹤湖盐碱化趋势, 为当地沉水植被恢复及物种多样化存续提供研究依据, 以在白鹤湖生物量相对大的金鱼藻(Ceratophyllum demersum)为对象, 研究了其在不同碱度(0、7、10、17 mmol/L)和混合盐碱(盐度0.3、0.6、1、2、4 g/L, 相应碱度1.9、3.8、6.3、12.6、25.2 mmol/L)条件下的生理指标变化。结果表明, 盐度在1.5 g/L以下时, 碱度变化没有对金鱼藻造成影响, 在实验设置的碱度梯度范围内, 金鱼藻均能正常生长, 尽管金鱼藻过氧化物酶(POD)、脯氨酸等均显示出梯度变化, 但依旧能够耐受17 mmol/L以下的碱度条件。随着混合盐碱浓度的升高, 金鱼藻长势呈现由盛至衰败的趋势, 在盐度0.6 g/L、碱度3.8 mmol/L的条件下, 金鱼藻长势最好, 表现出低促高抑的效应。随着盐度升高至2 g/L、碱度12.6 mmol/L, 金鱼藻能耐受胁迫并存活一部分, 尽管此时碱度<17 mmol/L, 也有部分金鱼藻死亡, POD含量急剧升高且植株间差异较大; 当盐度升高到4 g/L、碱度达到25.2 mmol/L时, 金鱼藻21天后全部死亡。在对水培液水质的检测中发现, 混合盐碱的浓度越高, 水中氮磷的去除率越低, 两者呈负相关关系。研究结果为盐碱化湖泊的沉水植被恢复提供了一定的参考。Abstract: As a representative lake in Momoge Wetland Reserve, White Crane Lake is facing the risk of salinization and eutrophication.In order to slow down the salinization trend and provide research basis for the restoration of submerged vegetation and survival of species diversity of White Crane Lake, this study investigated physiological indexes of Ceratophyllum demersum in different alkalinity (0, 7, 10 and 17 mmol/L) and mixed saline-alkaline (salinity of 0.3, 0.6, 1, 2 and 4 g/L, corresponding alkalinity of 1.9, 3.8, 6.3, 12.6 and 25.2 mmol/L). The results showed that when the salinity was below 1.5 g/L, alkalinity had no effect on C. demersum. Within the range of the alkalinity gradient set in the experiment, C. demersum grown normally. Although C. demersum peroxidase (POD) and proline showed gradient change, C. demersum was still able to tolerate the alkalinity conditions below 17 mmol/L. With the increase of mixed saline-alkaline concentration, the growth of C. demersum showed a trend from flourish to decline. Under the condition of salinity of 0.6 g/L and alkalinity of 3.8 mmol/L, C. demersum had the best growth with the high-promoting and low-inhibiting ability. With the increase of salinity to 2 g/L and alkalinity to 12.6 mmol/L, C. demersum were under stress and survived partially, and the POD content increased sharply and the difference between plants was large. When salinity increased to 4 g/L and alkalinity reached 25.2 mmol/L, all C. demersum died after 21 days explained by the high concentration of mixed saline-alkaline and the low removal rate of nitrogen and phosphorus that are negatively correlated. This study provides reference for the restoration of submerged vegetation in salinized lakes.
-
Keywords:
- Salt /
- Alkali /
- Stress /
- Ceratophyllum demersum /
- Momoge Wetland
-
在纤毛虫原生动物中, 寡毛类(Oligotrichs)为一营浮游生活的类群。广义寡毛类纤毛虫包括无壳寡毛类和具壳丁丁虫类[1, 2]。作为海洋微食物网的重要组成部分, 该类纤毛虫在海洋初-次级能量流动和碳循环过程中起着重要的枢纽作用[1-3]。
国际间对该类纤毛虫的研究已开展了一个多世纪, 迄今为止报道了约200余种无壳寡毛类[2]。但由于该类群纤毛虫通常个体较小、运动快速、表膜脆弱易破、大量种类活体上十分相似以及前人研究、历史文献中的累计性错误, 长期以来, 对本类群的分类学研究一直是(纤毛虫各目级阶元)种类鉴定中最为困难的。在迄今已经报道的命名种中, 约半数类群或种类资料仍然仅限于基于传统研究方法的描述(来自活体或固定后样本的观察), 因此在该类群中: 大部分重要分类性状均处于缺失状态, 许多种类的分类地位未明、未定或是错误的。即便是在其余的经过“现代方法”研究过的类群中, 许多种类也因种种原因而存在着程度不同的混乱和错误[2]。
有鉴于此, 作者于2003—2010年间对我国沿海多类生境(开放海区、潮间带、水产养殖水体等)中的无壳寡毛类纤毛虫开展了现代标准的(活体形态学、统计资料建立、纤毛图式揭示等)专项分类学研究, 本文对其中10种较罕见种类进行了形态学描述, 讨论了种群间的形态差异, 对新认定的特征信息进行了补充, 并对若干种的分类学进行了修订。
1. 材料与方法
十种寡毛类纤毛虫于2003—2010年采自青岛、大亚湾及湛江近岸水体。分离、培养、活体观察、染色制片等研究方法主要参照宋微波等[4]。名词术语和分类系统分别参照Agatha and Riedel-Lorjé[5]和Gao等[6]。
2. 结果与讨论
2.1 侧扁急游虫Strombidium apolatum Wilbert & Song, 2005 (图版Ⅰ-1—3, 图版Ⅱ-1—5)
![]() 图版Ⅰ 十种寡毛类纤毛虫的活体形态(1、4、7、10、13、16、19、22、23、29)和纤毛模式(2—3、5—6、8—9、11—12、14—15、17—18、20—21、24—28、30)1—3. 侧扁急游虫; 4—6. 具头急游虫; 7—9. 广东急游虫; 10—12. 拟卡氏急游虫, 箭头示背部趋触膜; 13—15. 拟楔尾急游虫, 自宋微波等[4]; 16—18. 铃木急游虫, 自宋微波等[4]; 19—21. 束腰旋游虫; 22—26. 杨科夫平游虫, 箭头示口原基, 22自宋微波等[4]; 27—28. 卡尔平游虫, 自宋微波等[4]; 29—30. 最小拟盗虫. 比例尺: 20 μm. GK. 环带动基列; VK. 腹面动基列; BM. 口区小膜; Exk. 额外动基列图版Ⅰ. Schematic drawings of ten oligotrich ciliates from life (1, 4, 7, 10, 13, 16, 19, 22, 23, 29) and after protagol impregnation (2—3, 5—6, 8—9, 11—12, 14—15, 17—18, 20—21, 24—28, 30)1—3. Strombidium apolatum; 4—6. Strombidium capitatum; 7—9. Strombidium guangdongense; 10—12. Strombidium paracalkinsi, arrow marks thigmotactic membranelles on dorsal side; 13—15. Strombidium parastylifer, from Song, et al.[4]; 16—18. Strombidium suzukii, from Song, et al.[4]; 19—21. Spirostrombidium cinctum; 22—26. Parallelostrombidium jankowski, arrow marks oral primordium, 22 from Song, et al.[4] ; 27—28. Parallelostrombidium kahli, from Song, et al.[4]; 29—30. Strombidinopsis minima. GK. girdle kinety; VK. ventral kinety; BM. buccal membranelles; Exk. Extra kirety
图版Ⅰ 十种寡毛类纤毛虫的活体形态(1、4、7、10、13、16、19、22、23、29)和纤毛模式(2—3、5—6、8—9、11—12、14—15、17—18、20—21、24—28、30)1—3. 侧扁急游虫; 4—6. 具头急游虫; 7—9. 广东急游虫; 10—12. 拟卡氏急游虫, 箭头示背部趋触膜; 13—15. 拟楔尾急游虫, 自宋微波等[4]; 16—18. 铃木急游虫, 自宋微波等[4]; 19—21. 束腰旋游虫; 22—26. 杨科夫平游虫, 箭头示口原基, 22自宋微波等[4]; 27—28. 卡尔平游虫, 自宋微波等[4]; 29—30. 最小拟盗虫. 比例尺: 20 μm. GK. 环带动基列; VK. 腹面动基列; BM. 口区小膜; Exk. 额外动基列图版Ⅰ. Schematic drawings of ten oligotrich ciliates from life (1, 4, 7, 10, 13, 16, 19, 22, 23, 29) and after protagol impregnation (2—3, 5—6, 8—9, 11—12, 14—15, 17—18, 20—21, 24—28, 30)1—3. Strombidium apolatum; 4—6. Strombidium capitatum; 7—9. Strombidium guangdongense; 10—12. Strombidium paracalkinsi, arrow marks thigmotactic membranelles on dorsal side; 13—15. Strombidium parastylifer, from Song, et al.[4]; 16—18. Strombidium suzukii, from Song, et al.[4]; 19—21. Spirostrombidium cinctum; 22—26. Parallelostrombidium jankowski, arrow marks oral primordium, 22 from Song, et al.[4] ; 27—28. Parallelostrombidium kahli, from Song, et al.[4]; 29—30. Strombidinopsis minima. GK. girdle kinety; VK. ventral kinety; BM. buccal membranelles; Exk. Extra kirety![]() 图版Ⅱ 侧扁急游虫、具头急游虫、广东急游虫、拟卡氏急游虫、拟楔尾急游虫的活体照片(1—4、6—9、11—13、17—19、21—22)和蛋白银染色制片照片(5、10、14—16、20、23—24)1—5. 侧扁急游虫, 2中箭头示沿腹面动基列分布的射出体, 5中箭头示环带动基列和腹面动基列之间的间隙; 6—10. 具头急游虫, 箭头示透明的前端凸起; 11—16. 广东急游虫, 箭头示射出体; 17—20. 拟卡氏急游虫, 18中箭头示射出体, 19—20中箭头示背部趋触膜; 21—24. 拟楔尾急游虫, 22中箭头示棘刺状尾, 23中箭头示腹面动基列前端, 21自宋微波等[4]. 比例尺: 20 μm. VK. 腹面动基列图版Ⅱ. Photomicrographs of Strombidium apolatum, Strombidium capitatum, Strombidium guangdongense, Strombidium paracalkinsi and Strombidium suzukii from life (1—4, 6—9, 11—13, 17—19, 21—22) and after protagol impregnation (5, 10, 14—16, 20, 23—24)1—5. Strombidium apolatum, arrow in 2 marks the extrusomes along the ventral kinety, arrow in 5 marks the gap between girdle and ventral kineties; 6—10. Strombidium capitatum, arrow notes the hyaline apical protrusion; 11—16. Strombidium guangdongense, arrow marks the extrusomes; 17—20. Strombidium paracalkinsi, arrow in 18 marks the extrusomes, arrows in 19 and 20 mark the thigmotactic membranelles on dorsal side; 21—25. Strombidium parastylifer, arrow in 22 marks the tail, arrow in 23 marks the anterior end of ventral kinety, 21 from Song, et al.[4] VK. ventral kinety
图版Ⅱ 侧扁急游虫、具头急游虫、广东急游虫、拟卡氏急游虫、拟楔尾急游虫的活体照片(1—4、6—9、11—13、17—19、21—22)和蛋白银染色制片照片(5、10、14—16、20、23—24)1—5. 侧扁急游虫, 2中箭头示沿腹面动基列分布的射出体, 5中箭头示环带动基列和腹面动基列之间的间隙; 6—10. 具头急游虫, 箭头示透明的前端凸起; 11—16. 广东急游虫, 箭头示射出体; 17—20. 拟卡氏急游虫, 18中箭头示射出体, 19—20中箭头示背部趋触膜; 21—24. 拟楔尾急游虫, 22中箭头示棘刺状尾, 23中箭头示腹面动基列前端, 21自宋微波等[4]. 比例尺: 20 μm. VK. 腹面动基列图版Ⅱ. Photomicrographs of Strombidium apolatum, Strombidium capitatum, Strombidium guangdongense, Strombidium paracalkinsi and Strombidium suzukii from life (1—4, 6—9, 11—13, 17—19, 21—22) and after protagol impregnation (5, 10, 14—16, 20, 23—24)1—5. Strombidium apolatum, arrow in 2 marks the extrusomes along the ventral kinety, arrow in 5 marks the gap between girdle and ventral kineties; 6—10. Strombidium capitatum, arrow notes the hyaline apical protrusion; 11—16. Strombidium guangdongense, arrow marks the extrusomes; 17—20. Strombidium paracalkinsi, arrow in 18 marks the extrusomes, arrows in 19 and 20 mark the thigmotactic membranelles on dorsal side; 21—25. Strombidium parastylifer, arrow in 22 marks the tail, arrow in 23 marks the anterior end of ventral kinety, 21 from Song, et al.[4] VK. ventral kinety本种于2008年3月18日采集自大亚湾近岸潮间带, 水温22.7℃, 盐度26.0‰, pH 7.9。
形态学描述 虫体活体大小(35—50) μm× (20—35) μm, 银染后通常(36—59) μm× (22—31) μm。体型长锥形, 前端右侧口缘隆起形成球形前端凸起, 后端钝圆且背腹扁平(图版Ⅰ-1, 图版Ⅱ-1)。体表环带动基列后方具壳板, 由不规则多边形网格组成(图版Ⅱ-4)。体内存在大量共生色素体, 卵圆形, 直径约5—8 μm (图版Ⅱ-2、3)。射出体长杆状, 长约15—20 μm, 沿环带动基列和腹面动基列呈单列紧密排列, 表膜附着点位于环带动基列上方及腹面动基列左侧表膜沟内(图版Ⅱ-2、3)。椭圆形大核位于体中央。
口沟较浅。领取小膜13—16片, 口区小膜4—6片, 两部分小膜区紧密相连。最下面几片口区小膜基部明显变短(图版Ⅰ-2)。环带动基列由44—64个双动基体组成, 位于体前段1/3处。环带动基列未形成闭合环, 与体右侧开口且右端于体边缘向体后方弯曲。腹面动基列具27—42个双动基体, 前端开始于体右侧环带动基列右端下方, 沿体右边缘向下延伸, 绕体末端至左侧亚尾端(图版Ⅰ-2、3, 图版Ⅱ-5)。腹面动基列与环带动基列的间隙较短, 位于体右缘中部。
比较与讨论 本种最先由Wilbert和Song[7]发现于南极海域, 其形态特征及纤毛图式被报道描述; 随后Xu等[8]对该种的青岛种群进行了重描述并补充了部分活体特征信息。该种最显著的特征是环带动基列于腹面右侧开口, 且环带动基列右端于体边缘向体后方弯曲。本文种群是该种首次在亚热带海域被发现, 环带动基列排列方式与种的特征完全一致; 此外其他形态特征(如口区小膜、腹面动基列)与前人报道的种群均相符, 因此鉴定为该种。本种群发现的沿腹面动基列排布的射出体排列带, 在原始报道的南极种群中同样被观察到, 但在青岛种群中并无描述, 可能由于细节观察的忽略; 本文在此对该种腹面射出体特征及图片进行了补充。此外与南极种群相比, 本种群及青岛种群的体纤毛略短, 且体内均存在共生色素体(vs. 南极种群未发现), 这些差异可认定为种群间差异, 可能由环境差异所致。
Lei等[9]曾描述了该种的另外一个青岛种群, 但将该种群鉴定为Strobilidium syowaensis Hada, 1970, 并根据其纤毛图式将其归入Spirostrombidium属。该种群与侧扁急游虫相比, 无论在活体形态学还是蛋白银染色后的纤毛图式及统计数据, 均能较好的相符。因此, 这里将Lei等[9]鉴定的Spirostrombidium syowaensis (Hada, 1970) Lei, et al., 1999归为侧扁急游虫的同物异名。
2.2 具头急游虫Strombidium capitatum (Lee-gaard, 1995) Kahl, 1932 (图版Ⅰ-4—6, 图版Ⅱ-6—10)
本种于2007年3月31日采集自大亚湾近岸潮间带, 水温23.1℃, 盐度28.6‰, pH 8.2。
形态学描述 虫体活体大小(50—65) μm× (35—50) μm, 银染后通常(38—53) μm× (41—52) μm。体型球形, 具明显的透明的前端凸起, 约10 μm高, 位于口区右侧(图版Ⅰ-4, 图版Ⅱ-6—9)。体内包含大量小型绿藻等食物残渣, 使细胞低倍镜下呈黑色。射出体针状, 15 μm长, 单行排列, 体表附着点位于环带动基列上方的体表沟内(图版Ⅰ-4)。大核腊肠状, 右半段水平位于口区下方, 左半段弯向体后方。
口区极大且深, 向下延伸至体长3/5处(图版Ⅰ-5, 图版Ⅱ-7、8、10)。领区小膜13—17片, 口区小膜15—19片。两部分小膜区由一段空隙明显分开, 口区小膜中部的小膜基部明显较两端长(图版Ⅱ-10)。环带动基列于赤道区下方水平分布, 由107—163个密集排列的双动基体组成, 在腹面中部形成一段开口。腹面动基列位于环带动基列开口区下方, 包含5—10个双动基体(图版Ⅰ-5、6)。
比较与讨论 具头急游虫曾被报道于世界上的很多地方, 例如大西洋北部[10]、大西洋南部[11]、青岛近岸[12]。Montagnes等[11]首次揭示了该种的纤毛图式, Xu等[12]基于青岛种群对该种的活体特征进行了补充, 本工作系首次在我国南海发现该种。该种的主要特征为显著阔大的口区及透明的口缘。本种群在体型、口区形态、体动基列排列方式等性状均与前人报道的种群相符; 但本种群发现的环带动基列开口, 在青岛种群中同样被观察到, 但在大西洋种群中并不存在, 此差异可被认为种群间差异。
Agatha和Riedel-Lorjé[13]报道了一寡毛类新种Strombidium triquetrum, 无论在活体特征(体形, 虫体前端明显、透明的前端突起, 大小, 阔大且深的口区)还是蛋白银染色后的特征(领区小膜数目, 腹面小膜数目, 大核的形状、分布方式)都与S. capitatum非常相符, 最大的区别为前者没有发现腹动基列。由于S. capitatum的腹动基列很短(仅有几个至十几个毛基粒), 在很多个体中腹动基列这一结构难于观察, 这一现象在S. capitatum的大西洋种群中也有存在, 因此, S. triquetrum很有可能是S. capitatum的同物异名。由于缺少直接证据, 此处尚不做定论, 待日后获取S. triquetrum的标本或基因信息后再做讨论。
2.3 广东急游虫Strombidium guangdongense Liu, et al., 2016 (图版Ⅰ-7—9, 图版Ⅱ-11—16)
本种于2004年4月采集自青岛近岸潮间带, 水温20.8℃, 盐度21.3‰, pH 7.7。
形态学描述 虫体活体大小 (20—30) μm× (15—25) μm, 银染后(20—28) μm× (12—20) μm。个体间存在体型差异, 大多为卵圆形或心形, 体前端具不明显前端凸起, 后端钝圆(图版Ⅰ-7, 图版Ⅱ-11、12)。射出体斜向插入虫体中后部, 呈漏斗状(图版Ⅰ-7, 图版Ⅱ-13)。虫体内充满大量褐色细小球形颗粒, 可能为藻类食物残渣。大核纺锤形于体中央。
口沟较小, 占体长1/5。领区小膜具12—15片, 口区小膜3—5片, 两者紧密相连(图版Ⅰ-8)。环带动基列于虫体中部水平分布, 由约18—23个双动基体稀疏排列组成; 腹面动基列位于虫体右侧, 由4—6对毛基粒稀疏排列((图版Ⅰ-8—9, 图版Ⅱ-14—16)。
比较与讨论 该种最近由Liu等[14]报道于南海北部近岸, 提供了详细的形态及纤毛图式信息。该种区别与其他种的主要特征为极小的个体及稀疏排列的体动基列毛基体。与原始种群相比, 本种群虫体体型略胖(长宽比约1—1.5 vs. 原始种群为1.5—2), 且并未发现虫体后端的棘刺状尾(vs. 原始种群具棘刺状尾), 这些差异证实了原始种群描述中发现的: 该种个体间体型变化明显的特征[14]。此外, 两种群体内均发现大量褐色球形食物颗粒, 表明该种食物来源比较专一。
2.4 拟卡氏急游虫Strombidium paracalkinsi (Lei, et al., 1999) Agatha, 2004 (图版Ⅰ-10—12, 图版Ⅱ-17—20)
本种于2008年12月22日采集自深圳近岸潮间带, 水温20.1℃, 盐度27.8‰, pH 8.1。
形态学描述 虫体活体大小(30—50) μm× (25—45) μm, 银染后通常(37—59) μm× (33—59) μm。体型呈球形, 左侧肩部向下倾斜, 右侧领区隆起形成前端凸起(图版Ⅰ-10, 图版Ⅱ-17)。射出体杆状, 于体后半部均匀排列, 表膜附着点在体赤道区形成隆起(图版Ⅰ-10, 图版Ⅱ-18)。卵球形大核与体后部中央。细胞喜在基质上爬行, 同时将趋触膜附着在基质上。
口沟较窄但深, 延伸至体长2/5处。领区小膜14—17片, 口区小膜6—9片, 两部分小膜区紧密相连。三片趋触膜位于体背部, 于第8—10片领区小膜下方, 每片小膜由两列毛基体组成, 通过稀疏排列的无纤毛毛基体与领区小膜相连。趋触纤毛明显较领区小膜长, 基部从左向右依次变短(图版Ⅰ-11, 图版Ⅱ-18—20)。环带动基列由41—58个双动基体组成, 位于赤道区, 具腹面开口。腹面动基列与腹面后部中央, 包含9—13个双动基体(图版Ⅰ-11、12)。
比较与讨论 拟卡氏急游虫由Lei等[8]首次报道于青岛沿海, 随后Song等[15]对该种进行了重描述, Lee等[16]对该种的韩国种群又进行了描述。该种的最重要特征为体背部具三片趋触膜。本种群是该种首次在亚热带海域报道, 形态特征数据均与前人报道的种群相符。基于本种群的观察, 趋触膜的细节特征及图片在此补充。此外在该种群的观察中发现趋触膜与领区小膜是分开的, 两者之间由稀疏排列的无纤毛毛基体相连, 且每片趋触小膜均由两列毛基体组成(其他口区小膜大多由三列毛基体组成)。在寡毛类中Spirostrombidium和Parallelostrombidium这2个属的大多数种也具有趋触膜, 但该趋触膜生长在领区小膜与口区小膜之间, 与其他口区小膜一致, 每片趋触小膜均由三列毛基体组成, 且全部生长纤毛[4]。部分发生学信息表明这两种趋触膜类型虽然都是由领区小膜分化出来, 具有同源性, 但在进化过程中可能存在分歧, 最终导致结构上的差异, 但无论哪种趋触膜类型, 都为纤毛虫附着在基质上生活提供了适应性。详细的细胞发生学研究或许可以为探究趋触膜的进化提供证据。
2.5 拟楔尾急游虫Strombidium parastylifer Song, et al., 2009 (图版Ⅰ-13—15, 图版Ⅱ-21—24)
本种于2003年6月18日采集自青岛近岸潮间带。
形态学描述 虫体活体大小约(25—40) μm× (25—35) μm, 银染后约(20—35) μm× (20—30) μm; 体型倒锥形。虫体前端平截且宽, 具前端突起(图版Ⅰ-13, 图版Ⅱ-21), 后端变窄末端形成尖削的棘, 长约5 μm, 棘尾不可伸缩, 但可弯曲(图版Ⅱ-22)。射出体针状, 沿环带动基列分布(图版Ⅰ-13, 图版Ⅱ-22)。胞质含有大量球形内质颗粒, 使虫体低倍镜下呈灰黑色; 大核球形, 位于虫体中靠左, 直径约10—14 μm。
口沟开阔, 占体长约1/3。领区小膜约为15—18片, 口区小膜约5—7片, 两者紧密连接; 领区小膜纤毛极长, 约30—35 μm, 几乎大于虫体长度(图版Ⅰ-14, 图版Ⅱ-24)。环带动基列水平分布, 由34—44个双动基体组成, 位于虫体赤道区靠下, 腹面中央具有小的开口, 约间隔1对毛基粒; 腹动基列位于虫体腹面中部, 前端距环带动基列开口处间隔1对毛基粒, 向下延伸至亚尾端, 由约5—9对毛基粒组成(图版Ⅰ-14、15, 图版Ⅱ-23)。体纤毛长约2 μm。
比较与讨论 该种由宋微波等[4]首次发表, 并包含简单描述。本文对该种形态信息细节进行了补充, 并提供了活体及银染图片。该种与相似种S. stylifer[17]的最大差异在于环带动基列开口(有vs.无)和口区小膜的数目(5—7 vs. 9—13), 此外该种体型为锥形(vs.卵圆形)。
2.6 铃木急游虫Strombidium suzukii Song, et al., 2009 (图版Ⅰ-16—18, 图版Ⅲ-1—5)
![]() 图版 Ⅲ 铃木急游虫、束腰旋游虫、杨科夫平游虫、卡尔平游虫、最小拟盗虫的活体照片(1—3、6—9、11—13、16、20—23)和蛋白银染色制片照片(4—5、10、14—15、17—19、24)1—5. 铃木急游虫, 箭头示前端凸起; 6—10. 束腰旋游虫, 7、8、10中箭头示趋触膜, 9中箭头示肩部射出体; 11—16. 杨科夫平游虫, 14中箭头示趋触膜, 15中箭头示环带动基列和腹面动基列腹面起点, 16中箭头示体后端射出体, 11自宋微波等[4]; 17—19. 卡尔平游虫, 箭头示趋触膜; 20—24. 最小拟盗虫, 箭头示体表黏着颗粒. 比例尺: 20 μm. GK. 环带动基列; VK. 腹面动基列图版 Ⅲ. Photomicrographs of Strombidium suzukii, Spirostrombidium cinctum Parallelostrombidium jankowski, Parallelostrombidium kahli, and Strombidinopsis minima
图版 Ⅲ 铃木急游虫、束腰旋游虫、杨科夫平游虫、卡尔平游虫、最小拟盗虫的活体照片(1—3、6—9、11—13、16、20—23)和蛋白银染色制片照片(4—5、10、14—15、17—19、24)1—5. 铃木急游虫, 箭头示前端凸起; 6—10. 束腰旋游虫, 7、8、10中箭头示趋触膜, 9中箭头示肩部射出体; 11—16. 杨科夫平游虫, 14中箭头示趋触膜, 15中箭头示环带动基列和腹面动基列腹面起点, 16中箭头示体后端射出体, 11自宋微波等[4]; 17—19. 卡尔平游虫, 箭头示趋触膜; 20—24. 最小拟盗虫, 箭头示体表黏着颗粒. 比例尺: 20 μm. GK. 环带动基列; VK. 腹面动基列图版 Ⅲ. Photomicrographs of Strombidium suzukii, Spirostrombidium cinctum Parallelostrombidium jankowski, Parallelostrombidium kahli, and Strombidinopsis minimafrom life (1—3, 6—9, 11—13, 16, 20—23) and after protagol impregnation (4—5, 10, 14—15, 17—19, 24) 1—5. Strombidium suzukii, arrow notes the apical protrusion; 6—10. Spirostrombidium cinctum, arrow in 7, 8, 10 marks the thigmotactic membranelles, arrow in 9 marks the extrusomes on shoulder of dorsal side; 11—16. Parallelostrombidium jankowski, arrow in 14 notes the thigmotactic membranelles, arrows in 15 mark the ventral ends of girdle and ventral kineties, arrow in 16 marks the extrusomes, 11 from Song, et al.[4]; 17—19. Parallelostrombidium kahli, arrow notes the thigmotactic membranelles; 20—24. Strombidinopsis minima, arrow notes the mineral envelope covering the body surface. GK. gridle kinety; VK. ventral kinety本种于2004年4月1日采集自青岛近岸潮间带。
形态学描述 虫体活体大小 (35—50) μm× (35—45) μm, 银染后(35—50) μm × (32—45) μm。体型球形, 口缘右侧隆起形成前端凸起(图版Ⅰ-16, 图版Ⅲ-1、2)。体内含大量微小金色藻类食物颗粒。射出体杆状, 于体中部形成漏斗状(图版Ⅰ-16)。射出体附着点于环带动基列上方形成体表突起(图版Ⅲ-3)。大核球形位于虫体中部。虫体通常在水中缓缓游动, 体绕体轴不停旋转, 受惊扰后, 可沿直线快速游走。
口沟较浅, 占体长1/5。领区小膜约15—16片, 口区小膜约6—7片, 两者相连(图版Ⅰ-17, 图版Ⅲ-4)。环带动基列水平分布, 位于虫体赤道区, 由约50—66双动基体形成闭合环状; 腹动基列位于虫体略右侧腹面, 前端距环带动基列间隔2个双动基体, 后端延伸至虫体末端, 由约15—17个双动基体组成(图版Ⅰ-17、18, 图版Ⅲ-4、5)。
比较与讨论 该种由宋微波等[4]首次发表并进行了简单描述。本文对该种形态信息细节进行了补充, 并提供了活体及银染图片。根据一般的形态学特征(大小, 体形等), 下列几种急游虫应该与铃木急游虫进行比较。
铃木急游虫与Strombidium basimorphum Martin & Montagnes, 1993最为相近, 二者的主要区别为: (1)前者环带动基列为双动基系, 而后者为单动基系; (2)前者环带动基列毛基粒数目较多约101—135个, 且位于虫体前1/3处, 而后者毛基粒50—66个, 位于虫体赤道区[18, 19]。
铃木急游虫与Strombidium taylori Martin & Montagnes, 1993可由下列几点相区别: (1)腹面小膜数目(6—7 vs. 12—15); (2)环带动基列为双动基系(vs. 单动基系); (3)前者腹动基列长, 几乎伸展至环带动基列, 由15—17对毛基粒组成, 后者腹动基列短小, 局限于虫体末端, 由约6—8对毛基粒组成; (4)大核形状(近球形vs. U形)[18]。
与Strombidium compressum (Leegaard, 1915) Kahl, 1932相比, 铃木急游虫个体较大[(35—50) μm× (35—45) μm vs. (17—28) μm× (13—24) μm], 具有较多的领区小膜(15—16 vs. 12—15), 环带动基列由双动基系组成(vs. 环带动基列由单动基系组成), 腹动基列长几乎伸展至环带动基列处(vs. 腹动基列短小, 局限于虫体尾部)[20]。
铃木急游虫可通过下列特征与Strombidium acutum Leegaard, 1915明显区分开: (1)前者仅具有6—7片腹面小膜(vs. 10—22片); (2)环带动基列为双动基系(vs. 单动基系); (3)腹动基列长, 几乎伸展至环带动基列处(无腹动基列)[20]。
与Strombidium emergens (Leegaard, 1915) Kahl, 1932相比, 铃木急游虫具有较少的腹面小膜(6—7 vs. 8—11), 较小的口区(口区约占体长的1/3—1/4 vs. 口区约占体长的1/2—1/3)[20]。
2.7 束腰旋游虫Spirostrombidium cinctum (Kahl, 1932) Petz, et al., 1995 (图版Ⅰ-19—21, 图版Ⅲ-6—10)
本种于2007年11月23日采集自大亚湾近岸潮间带, 水温27.0℃, 盐度31.6‰, pH 8.3。
形态学描述 虫体活体大小(55—70) μm× (35—45) μm, 银染后通常(41—74) μm× (29—52) μm。体型卵圆形, 前端肩部区较平截, 具明显宽阔的前端凸起(图版Ⅰ-19, 图版Ⅲ-6)。体内含大量灰色食物颗粒。射出体沿环带动基列和腹面动基列均匀排列, 此外一列射出体水平排列在背部肩区(图版Ⅰ-19, 图版Ⅲ-9)。球形大核位于虫体中央。
口沟较深, 倾斜向下延伸至体长2/5处(图版Ⅰ-19、20, 图版Ⅲ-7、8)。口区小膜分化为21—28片领区小膜, 3片趋触小膜及10—14片口区小膜。趋触小膜明显较长且向体后方延伸(图版Ⅰ-20, 图版Ⅲ-7、10)。环带动基列由59—94个双动基体组成, 前端开始于腹面中部左侧, 末端终止于腹面右侧亚尾端。腹面动基列包含16—38个双动基体, 位于腹面右侧, 向上延伸至接近环带动基列。另一列片段状的额外动基列位于体左侧肩部区, 由14—31片双动基体组成(图版Ⅰ-20、21)。
比较与讨论 该种最先由Kahl[21]发现; 基于青岛种群的研究, Xu和Song[22]对该种的纤毛图式进行了揭示。本种群是该种首次在亚热带海域报道, 形态特征数据均与青岛种群相符。但本种群发现的背部肩区射出体排列带, 在原始报道中并未描述。射出体的分布通常与体动基列分布相吻合, 因此该背部肩区射出体排列带与肩区分布的额外动基列的位置一致, 表明该射出体排列带可能为稳定存在, 推测原始报道未描述可能由于细节观察的忽略。基于对本种群活体形态的详细观察, 准确的射出体排列模式及图示在此处给出。
2.8 杨科夫平游虫Parallelostrombidium jankow-skii (Song, et al., 2009) Song, et al., 2018 (图版Ⅰ-22—26, 图版Ⅲ-11—16)
本种于2002年8月10日采集自青岛虾养殖池。
形态学描述 虫体活体大小(110—150) μm× (50—75) μm, 银染后(100—140) μm× (48—68) μm。体型长锥形, 领区右侧隆起形成前端凸起, 后端尖细(图版Ⅰ-22、23, 图版Ⅲ-11—13)。环带动基列后方体表覆盖透明壳层, 壳层向下延伸形成尖尾, 无伸缩性(图版Ⅰ-22、23, 图版Ⅲ-11)。射出体沿环带动基列分布并延伸到体末端, 附着点在体表形成凸起(图版Ⅲ-11、16)。多枚大核连接在一起, 呈鹿角状。
口沟倾斜延伸占体长1/4。领区小膜具24—28片, 口区小膜16—19片, 两者之间具2片趋触膜(图版Ⅲ-14)。趋触膜基部略长于其他小膜, 纤毛与领区小膜纤毛长度相当。环带动基列开始于腹面趋触膜下方, 螺旋绕体一周半, 末端终止于虫体背面尾端, 由约93—126个双动基体组成; 腹面动基列起始于环带动基列右端下方, 距环带动基列约2对毛基粒, 腹面动基列与环带动基列下方部分平行, 右侧倾斜延伸至虫体背面尾端, 由约30—39个双动基体组成(图版Ⅰ-24, 图版Ⅲ-15)。腹面动基列与环带动基列平行部分方向一致, 每个双动基体上着生纤毛的毛基体均在上方。
早期发生个体显示口原基位于环带动基列右端的左侧, 腹面动基列表膜下方(图版Ⅰ-25); 后期发生个体纤毛图式显示随着口原基的发展及旋转, 口原基从腹面动基列与环带动基列斜向部分之间发生至体表, 腹面及环带动基列毛基粒增殖变长, 同时腹面动基列分化成两段, 其中后半段成为后仔虫的腹面动基列, 并保持与环带动基列后段平行, 前半段成为前仔虫的腹面动基列, 而环带动基列水平部分保留给前仔虫, 后半段保留给后仔虫(图版Ⅰ-26); 推测后续发生将出现环带动基列在虫体背部断裂, 后半段随着后仔虫口区的螺旋延伸至后仔虫腹面, 形成完整的后仔虫腹面动基列, 而原环带动基列断裂后的前半段则向前仔虫左侧延伸螺旋, 最终与前仔虫腹面动基列平行, 形成完整的前仔虫腹面动基列。
比较与讨论 该种最初被命名为Omegastrombidium jankowskii, 由宋微波等[4]首次发表并对该种进行了简单描述。后经Song等[23]对该种另外一个种群的纤毛图式进行深入研究, 发现该种的体动基列排列模式在原始描述中被误读: 环带动基列腹面右侧弯曲处并不连续而是具一开口, 而对开口下方的纵向动基列片段进一步观察发现其方向为向上(双动基体中着生纤毛的毛基体在上), 但开口右侧的横向动基列方向为向左(双动基体中着生纤毛的毛基体在左), 表明两者在细胞发生过程中来自不同的动基列原基, 证实纵向体动基列为腹面动基列。这一结果进而揭示该种应隶属于平游虫属, Song等[23]因此将该种种名进行了修订, 命名为Parallelostrombidium jankowskii。本文对该种的原始种群进行了进一步观察, 发现原始描述中对体动基列排列方式确实存在如上误读, 证实了该种确实应隶属于平游虫属。基于正确的体动基列排列方式解读, 本文对原始种群的纤毛图式做了详细描述, 对该种群活体照片进行了补充, 此外对早期及后期发生个体纤毛模式进行了描述。
该种群与Song等[23]的种群相比, 虫体体表覆盖透明壳层在后者中并未发现, 可能为种群差异; 大核形态不同(鹿角状vs.多枚椭圆形大核分散在体内), 推测前者种群可能均处于细胞发生前期, 大核发生融合因而产生鹿角状; 此外本种群环带及腹面动基列后段螺旋至体背部(vs.位于体右侧), 可能因本种群蛋白银制片虫体体位略偏左。
2.9 卡尔平游虫Parallelostrombidium kahli (Song, et al., 2009) Song, et al., 2018 (图版Ⅰ-27、28, 图版Ⅲ-17—19)
本种于2005年10月28日采集自青岛近岸潮间带, 水温20.8℃, 盐度21.3‰, pH 7.7。
形态学描述 虫体银染后(60—80) μm × (40—50) μm。体型长锥形, 领区右侧隆起形成前端凸起, 后端变窄略尖。球形大核数十枚, 散布于体内(图版Ⅰ-27)。口沟较浅, 向右延伸占体长1/5。领区小膜约50—60片, 口区小膜10—15片, 两者之间具2片趋触膜(图版Ⅰ-27, 图版Ⅲ-17)。趋触膜基部明显长于其他小膜。环带动基列起始于背部左侧肩部, 水平延伸于口围带下绕体一周, 随后在背面中部向下螺旋绕体约1.5周, 末端终止于虫体腹面尾端, 由约139—164个双动基体组成; 腹面动基列起始于环带动基列前端下方, 距环带动基列约2对毛基粒, 腹面动基列与环带动基列下方部分平行, 右侧倾斜延伸至虫体背面尾端, 由约75—88个双动基体组成(图版Ⅰ-27、28, 图版Ⅲ-18、19)。腹面动基列与环带动基列平行部分方向一致, 每个双动基体上着生纤毛的毛基体均在上方。
比较与讨论 该种最初被命名为Omegastrombidium kahli, 由宋微波等[4]首次发表并对该种进行了简单描述。后经Song等[23]对该种另外一个种群的纤毛图式进行深入研究, 发现该种的体动基列排列模式在原始描述中存在与Parallelostrombidium jankowskii类似的误读: 环带动基列腹面右侧弯曲处下方的纵向动基列片段应为腹面动基列。Song等 [23]因此将该种种名进行了修订, 命名为Parallelostrombidium kahli。本文对该种的原始种群进行了进一步观察, 同样发现原始描述中对体动基列排列方式确实存在如上误读, 证实了该种确实应隶属于平游虫属。基于正确的体动基列排列方式解读, 本文对原始种群的纤毛图式做了详细描述。
该种群与Song等[23]的种群相比, 本种群纤毛图式末端终止于虫体背部末端(vs.位于虫体腹面末端), 可能因本种群蛋白银制片虫体体位略偏左。
2.10 最小拟盗虫Strombidinopsis minima (Gruber, 1884) Song & Bradbury, 1998 (图版Ⅰ-29、30, 图版Ⅲ-20—24)
本种于2010年3月29日采集自湛江近岸潮间带, 水温20.8℃, 盐度21.3‰, pH 7.7。
形态学描述 虫体活体大小 (40—55) μm× (30—45) μm, 银染后(38—61) μm× (41—60) μm。体型椭球形, 后端钝圆(图版Ⅰ-29、30, 图版Ⅲ-20、21)。全身表面黏着大量砂质颗粒使体表明显粗糙(图版Ⅰ-29, 图版Ⅲ-20、23)。两个卵圆形大核位于口区下方, 水平排布。虫体喜将口区小膜附着在基质上, 向基质中钻行, 同时身体螺旋旋转(图版Ⅲ-21)。
领区小膜具20—24片小膜, 小膜基部等长, 口沟处无小膜伸长。小膜纤毛内外等长, 运动时无规律摆动(图版Ⅰ-29)。口沟内部具一片较短的口区小膜, 该小膜未紧贴领区小膜(图版Ⅲ-22、24)。约20—23列体动基列纵向均匀排列, 末端终止于体后部1/5处。每列体动基列由约12—16个双动基体组成, 这些动基体于体动基列前段密集排列而于后段稀疏排列(图版Ⅰ-30)。
比较与讨论 最小拟盗虫广泛分布于世界各海域, 例如地中海[24]、大西洋西岸[25]、青岛近岸[26]。Agatha[24]整合多个种群的信息, 对该种进行了详细描述, 本工作系首次在我国南海发现该种, 本工作对该种的活体描述及照片进行了详细的补充。作为该种的重要分类学特征, 目前体表黏着颗粒发现于该种的所有种群中[24—26]。与中国青岛种群相比, 本种群每列体动基列中具有较少的双动基体(12—16 vs. 18—22), 属种群间差异。
-
表 1 金鱼藻水培营养液配方
Table 1 Nutrient solution formula for hydroponic culture of C. demersum
化学式Chemical formula 浓度Concentration (mmol/L) 化学式Chemical formula 浓度Concentration (mmol/L) KNO3 0.2 FeSO4·7H2O 0.05 KH2PO4 0.004 KI 0.0005 CaCl2 0.5 H3BO3 0.01 NaCl 0.05 MnSO4·H2O 0.01 MgSO4·7H2O 0.5 ZnSO4·7H2O 0.003 EDTA·Na2 0.05 Na2MoO4·2H2O 0.0001 表 2 两阶段实验的碱、混合盐碱成分
Table 2 Composition of alkali and mixed salt and alkali in two-stage experiments
组别Group 盐度Salinity
(g/L)碱度Alkalinity
(mmol/L)NaCl
(g/L)NaHCO3
(g/L)Na2CO3
(g/L)pH A 0 0 0 0 0 7.53 B 0.632 7 0 0.42 0.212 9.04 C 0.884 10 0 0.672 0.212 9.13 D 1.472 17 0 1.26 0.212 9.23 a 0.3 1.9 0.15 0.135 0.015 8.22 b 0.6 3.8 0.3 0.27 0.03 8.64 c 1 6.3 0.5 0.45 0.05 8.75 d 2 12.6 1 0.9 0.1 8.85 e 4 25.2 2 1.8 0.2 8.95 表 3 不同盐碱胁迫下水质指标去除率
Table 3 The removal rate of water quality index under different salinities and alkali stress (%)
组别 Gruop TN TP COD a 57.57 81.26 –514.01 b 51.49 80.11 –136.77 c 56.50 77.92 –191.60 d 51.51 70.98 –75.22 e 38.62 –608.38 –76.62 表 4 各项指标与混合盐碱相关性分析
Table 4 Correlation analysis of each index and mixed salinity
相关性系数 TN去除率 TP去除率 COD去除率 POD SOD MDA Pro 叶绿素a+b R –0.927** –0.909** 0.627* 0.952** 0.604* –0.254 0.697** –0.117 注: *、 **分别表示显著性差异P<0.05、 P<0.01Note: *, ** Represent significant correlations at P<0.05, P<0.01, respectively -
[1] 崔桢. 基于白鹤生境需求的湿地生态水文调控研究 [D]. 硕士学位论文, 长春: 中国科学院东北地理与农业生态研究所. 2017: 2 Cui Z. Eco-hydrological regulations based on habitat requirement of Grus leucogeranus—a case study in Baihe Lake, Momoge National Nature Wetland Reserve, Northeast China [D]. Thesis for Master of Science. Changchun: Northeast Institute of geography and Agroecology Chinese Academy of Science, 2017: 2
[2] 姚书春, 薛滨, 吕宪国, 等. 松嫩平原湖泊水化学特征研究 [J]. 湿地科学, 2010, 8(2): 169-175. Yao S C, Xue B, Lü X G, et al. The hydrochemical characteristic of Lakes in Songnen Plain [J]. Wetland Science, 2010, 8(2): 169-175.
[3] 李惠芳. 莫莫格湿地扁秆藨草对水盐交互作用的生理生态响应特征 [D]. 长春: 中国科学院东北地理与农业生态研究所, 2013: 23-50 Li H F. Eco-physiological responding characteristics of Scirpus planiculmis on coupling of water table depths and salinity in Momoge Wetland [D]. Changchun: Northeast Institute of geography and Agroecology, Chinese Academy of Sciences, 2013: 23-50
[4] 肖强, 郑海雷, 陈瑶, 等. 盐度对互花米草生长及脯氨酸、可溶性糖和蛋白质含量的影响 [J]. 生态学杂志, 2005, 24(4): 373-376. doi: 10.3321/j.issn:1000-4890.2005.04.005 Xiao Q, Zheng H L, Chen Y, et al. Effects of salinity on the growth and proline, soluble sugar and protein contents of Spartina alterniflora [J]. Chinese Journal of Ecology, 2005, 24(4): 373-376. doi: 10.3321/j.issn:1000-4890.2005.04.005
[5] 邓春暖, 章光新, 李红艳, 等. 莫莫格湿地芦苇对水盐变化的生理生态响应 [J]. 生态学报, 2012, 32(13): 4146-4153. Deng C N, Zhang G X, Li H Y, et al. Eco-physiological responses of Phragmites australis to different water-salt conditions in Momoge Wetland [J]. Acta Ecologica Sinica, 2012, 32(13): 4146-4153.
[6] 刘正鲁, 朱月林, 胡春梅, 等. 氯化钠胁迫对嫁接茄子生长、抗氧化酶活性和活性氧代谢的影响 [J]. 应用生态学报, 2007, 18(3): 537-541. doi: 10.3321/j.issn:1001-9332.2007.03.013 Liu Z L, Zhu Y L, Hu C M, et al. Effects of NaCl stress on the growth, antioxidant enzyme activities and reactive oxygenme tabolism of grafted eggplant [J]. Chinese Journal of Applied Ecology, 2007, 18(3): 537-541. doi: 10.3321/j.issn:1001-9332.2007.03.013
[7] 邹晓君, 列志旸, 薛立. 盐胁迫对4种园林植物土壤养分及酶活性的影响 [J]. 东北林业大学学报, 2019, 47(3): 74-78. Zou X J, Lie Z C, Xue L. Effects of salt stress on soil nutrient and enzyme activity of four landscape plants [J]. Journal of Northeast Forestry University, 2019, 47(3): 74-78.
[8] Munns R. Comparative physiology of salt and water stress [J]. Plant Cell and Environment, 2002, 25(2): 239-250. doi: 10.1046/j.0016-8025.2001.00808.x
[9] Yang J Y, Zheng W, Tian Y, et al. Effects of various mixed salt-alkaline stresses on growth, photosynthesis, and photosynthetic pigment concentrations of Medicago ruthenica seedlings [J]. Photosynthetica, 2011, 49(2): 275-284. doi: 10.1007/s11099-011-0037-8
[10] Gong B, Wang X, Wei M, et al. Overexpression of S-adenosylmethionine synthetase 1 enhances tomato callus tolerance to alkali stress through polyamine and hydrogen peroxide cross-linked networks [J]. Plant Cell Tissue & Organ Culture, 2016, 124(2): 377-391.
[11] 熊剑, 黄建团, 聂雷, 等. 不同营养条件对金鱼藻净化作用及其生理生态的影响 [J]. 水生生物学报, 2013, 37(6): 1066-1072. Xiong J, Huang J T, Nie L, et al. The effects of nutrient concentration on purification ability and eco-physiology of Ceratophyllum demersum [J]. Acta Hydrobiologica Sinica, 2013, 37(6): 1066-1072.
[12] Donk E V. Switches between Clear and Turbid Water States in a Biomanipulated Lake (1986—1996): The Role of Herbivory on Macrophytes [M]. New York: Springer, 1998: 290-297
[13] 顾庆龙, 陈刚, 谢田. 金鱼藻营养器官的形态解剖学研究 [J]. 中国野生植物资源, 2005, 24(6): 41-44. doi: 10.3969/j.issn.1006-9690.2005.06.013 Gu Q L, Chen G, Xie T. Anatomical studies on the vegetative organs of Ceratophyllum demersum L [J]. Chinese Wild Plant Resources, 2005, 24(6): 41-44. doi: 10.3969/j.issn.1006-9690.2005.06.013
[14] 李合生. 植物生理生化实验原理和技术 [M]. 北京: 高等教育出版社, 2000: 134-137, 164-169 Li H S. Principles and Techniques of Plant Physiological Biochemical Experiment [M]. Beijing: Higher Education Press, 2000: 134-137, 164-169
[15] 王学奎, 黄见良. 植物生理生化实验原理和技术 [M]. 第3版. 北京: 高等教育出版社, 2015: 274-287 Wang X K, Huang J L. Principles and Techniques of Plant Physiological Biochemical Experiment [M]. Beijing: Higher Education Press, 2015: 274-287
[16] 国家环境保护总局水和废水监测分析方法编委会. 水和废水监测分析方法 [M]. 北京: 中国环境科学出版社, 2002: 210-257 Editorial Board of Water and Wastewater Monitoring and Analysis Methods of the State Environmental Protection Administration. Methods for Monitoring and Analyzing Water and Wastewater [M]. Beijing: China Environmental Science Press, 2002: 210-257
[17] 马剑敏, 靳同霞, 靳萍, 等. 伊乐藻和苦草对硝氮胁迫的响应 [J]. 河南师范大学学报(自然科学版), 2007, 35(3): 115-118. doi: 10.3969/j.issn.1000-2367.2007.03.034 Ma J M, Jin T X, Jin P, et al. Responses of Elodea nuttallii and Vallisneria natans to the stress of nitrate [J]. Journal of Henan Normal University (
Natural Science ) , 2007, 35(3): 115-118. doi: 10.3969/j.issn.1000-2367.2007.03.034 [18] 李源, 刘贵波, 高洪文, 等. 紫花苜蓿种质耐盐性综合评价及盐胁迫下的生理反应 [J]. 草业学报, 2010, 19(4): 79-86. doi: 10.11686/cyxb20100411 Li Y, Liu G B, Gao H W, et al. A comprehensive evaluation of salt-tolerance and the physiological response of Medicago sativa at the seedling stage [J]. Acta Pratacultutae Sinica, 2010, 19(4): 79-86. doi: 10.11686/cyxb20100411
[19] 赵勇. 盐胁迫下植物组织中甜菜碱和脯氨酸变化的研究 [D]. 北京: 中国农业科学院, 2004: 14-57 Zhao Y. Determination of Betainens and proline in plant tissues under salt-stress [D]. Beijing: Chinese Academy of Agricultural Sciences, 2004: 14-57
[20] 杨升, 张华新, 张丽. 植物耐盐生理生化指标及耐盐植物筛选综述 [J]. 西北林学院学报, 2010, 25(3): 59-65. Yang S, Zhang H X, Zhang L. Physiological and biochemical indices of salt tolerance and scanning of salt-tolerance plants: a review [J]. Journal of Northwest Forestry University, 2010, 25(3): 59-65.
[21] 夏阳, 孙明高, 李国雷, 等. 盐胁迫对四园林绿化树种叶片中叶绿素含量动态变化的影响 [J]. 山东农业大学学报(自然科学版), 2005, 36(1): 30-34. doi: 10.3969/j.issn.1000-2324.2005.01.006 Xia Y, Sun M G, Li G L, et al. The effects of salt stress on the contents of chlorophyll in seedling leaves of four garden tree species [J]. Journal of Shandong Agricultural University (
Natural Science ) , 2005, 36(1): 30-34. doi: 10.3969/j.issn.1000-2324.2005.01.006 [22] 程宪伟. 湿地植物繁殖和生长在盐碱胁迫下的响应特征 [D]. 长春: 中国科学院东北地理与农业生态研究所, 2018: 59-66 Cheng X W. Response characteristics of wetland plant species under saline-alkaline stress during their propagation and growth stages [D]. Changchun: Northeast Institute of Geography and Agroecology, Chinese Academy of Sciences, 2018: 59-66
[23] 王卫红, 季民. 9种沉水植物的耐盐性比较 [J]. 农业环境科学学报, 2007, 26(4): 1259-1263. doi: 10.3321/j.issn:1672-2043.2007.04.011 Wang W H, Ji M. Comparison on salt tolerance of nine submerged macrophytes [J]. Journal of Agro-Environment Science, 2007, 26(4): 1259-1263. doi: 10.3321/j.issn:1672-2043.2007.04.011
[24] 乔旭, 黄爱军, 褚贵新. 植物对盐分胁迫的响应及其耐盐机理研究进展 [J]. 新疆农业科学, 2011, 48(11): 2089-2094. doi: 10.6048/j.issn.1001-4330.2011.11.023 Qiao X, Huang A J, Chu G X. Research Progress in the effects of salt stress on plant and the mechanism of plant resistance [J]. Xinjiang Agricultural Sciences, 2011, 48(11): 2089-2094. doi: 10.6048/j.issn.1001-4330.2011.11.023
[25] 陈书琴, 孙慧群, 储昭升. 氨胁迫下沉水植物抗氧化酶系统研究进展 [J]. 环境科学与技术, 2016, 39(11): 42-46. Chen S Q, Sun H Q, Chu Z S. Advance in antioxidative enzyme system of submerged macrophytes under ammonia stress [J]. Environmental Science & Technology, 2016, 39(11): 42-46.
[26] 曹特, 倪乐意. 金鱼藻抗氧化酶对水体无机氮升高的响应 [J]. 水生生物学报, 2004, 28(3): 299-303. doi: 10.3321/j.issn:1000-3207.2004.03.013 Cao T, Ni L Y. Responses of antioxidases of Ceratophyllum demersum to the increase of inorganic nitrogen in water column [J]. Acta Hydrobiologica Sinica, 2004, 28(3): 299-303. doi: 10.3321/j.issn:1000-3207.2004.03.013
[27] 刘燕, 王圣瑞, 金相灿, 等. 水体营养水平对3种沉水植物生长及抗氧化酶活性的影响 [J]. 生态环境学报, 2009, 18(1): 57-63. doi: 10.3969/j.issn.1674-5906.2009.01.011 Liu Y, Wang S R, Jin X C, et al. Effects of different nutritional condition on the growth and antioxidant enzyme activity of three submerged macrophytes [J]. Ecology and Environmental Sciences, 2009, 18(1): 57-63. doi: 10.3969/j.issn.1674-5906.2009.01.011
[28] 慈敦伟, 张智猛, 丁红, 等. 花生苗期耐盐性评价及耐盐指标筛选 [J]. 生态学报, 2015, 35(3): 805-814. Ci D W, Zhang Z M, Ding H, et al. Evaluation and selection indices of salinity tolerance in peanut seedling [J]. Acta Ecologica Sinica, 2015, 35(3): 805-814.
[29] 刘倩, 高娅妮, 柳旭, 等. 植物对盐碱胁迫的响应机制研究进展 [J]. 生态学报, 2017, 37(16): 5565-5577. Liu Q, Gao Y N, Liu X, et al. Review on the mechanisms of the response to salinity-alkalinity stress in plants [J]. Acta Ecologica Sinica, 2017, 37(16): 5565-5577.
[30] 王丽燕, 赵可夫. 玉米幼苗对盐胁迫的生理响应 [J]. 作物学报, 2005, 31(2): 264-266. doi: 10.3321/j.issn:0496-3490.2005.02.025 Wang L Y, Zhao K F. Some physiological response of Zea mays under salt-stress [J]. Acta Agronomica Sinica, 2005, 31(2): 264-266. doi: 10.3321/j.issn:0496-3490.2005.02.025
[31] 赵风斌, 王丽卿, 季高华, 等. 盐胁迫对3种沉水植物生物学指标及叶片中丙二醛含量的影响 [J]. 环境污染与防治, 2012, 34(10): 40-44. doi: 10.3969/j.issn.1001-3865.2012.10.009 Zhao F B, Wang L Q, Ji G H, et al. Effects of NaCl stress on plant biology and MDA content of 3 submerged plants [J]. Environmental Pollution & Control, 2012, 34(10): 40-44. doi: 10.3969/j.issn.1001-3865.2012.10.009
[32] Liu J, Zhu J K. Proline accumulation and salt-stress-induced gene expression in a salt-hypersensitive mutant of Arabidopsis [J]. Plant Physiology, 1997, 114(2): 591-596. doi: 10.1104/pp.114.2.591
[33] 王旭明, 赵夏夏, 陈景阳, 等. 低盐胁迫对5个海水稻种质若干生理生化指标的影响 [J]. 热带农业科学, 2018, 38(8): 1-6. Wang X M, Zhao X X, Chen J Y, et al. Effect of low salt stress on several physiological and biochemical indicators of five accessions of sea rice [J]. Chinese Journal of Tropical Agriculture, 2018, 38(8): 1-6.
[34] 肖雯, 贾恢先, 蒲陆梅. 几种盐生植物抗盐生理指标的研究 [J]. 西北植物学报, 2000, 20(5): 818-825. doi: 10.3321/j.issn:1000-4025.2000.05.020 Xiao W, Jia H X, Pu L M. Studies on physiological index of some halophytes [J]. Acta Botanica Boreali-Occidentalia Sinica, 2000, 20(5): 818-825. doi: 10.3321/j.issn:1000-4025.2000.05.020
[35] 窦艳艳, 王保忠, 张浏, 等. 碳酸氢根缓解高营养负荷下苦草(Vallisneria natans)胁迫的作用 [J]. 生态环境, 2008, 17(4): 1581-1585. doi: 10.3969/j.issn.1674-5906.2008.04.050 Dou Y Y, Wang B Z, Zhang L, et al. Mitigtive effect of HCO
${\bar 3}$ -DIC on eutrophication stress on Vallisneria natans [J]. Ecology and Environment, 2008, 17(4): 1581-1585. doi: 10.3969/j.issn.1674-5906.2008.04.050[36] Kahara S N, Vermaat J E. The effect of alkalinity on photosynthesis-light curves and inorganic carbon extraction capacity of freshwater macrophytes [J]. Aquatic Botany, 2003, 75(3): 217-227. doi: 10.1016/S0304-3770(02)00179-1
[37] 张彦辉, 安彦杰, 朱迟, 等. 水体无机碳条件对常见沉水植物生长和生理的影响 [J]. 水生生物学报, 2009, 33(6): 1020-1030. Zhang Y H, An Y J, Zhu C, et al. Physiological effects of dissolved inorganic carbon on common submerged macrophytes [J]. Acta Hydrobiologica Sinica, 2009, 33(6): 1020-1030.
[38] 张永亮, 王学愿, 刘杨, 等. 盐胁迫下氮磷钾肥对虉草离子吸收与分布的影响 [J]. 草地学报, 2014, 22(6): 1318-1323. doi: 10.11733/j.issn.1007-0435.2014.06.026 Zhang Y L, Wang X Y, Liu Y, et al. Effects of different NPK fertilizer rates on the ion absorptoin and distribution of reed canarygrass (Phalaris arundinacea) under salt stress [J]. Acta Agrestia Sinica, 2014, 22(6): 1318-1323. doi: 10.11733/j.issn.1007-0435.2014.06.026
-
期刊类型引用(1)
1. 池洪树,江秋欢,潘滢,林能锋. 一株寄生于大黄鱼的盾纤毛虫分子鉴定与系统进化分析. 福建畜牧兽医. 2023(04): 1-6 .  百度学术
百度学术
其他类型引用(1)




 下载:
下载: