COMPARATIVE ANALYSIS OF SKELETAL DEVELOPMENT BETWEEN WILDTYPE ZEBRAFISH AND INTERMUSCULAR BONE-DEFICIENT MUTANTS
-
摘要: 利用斑马鱼(Danio rerio)野生型与肌间刺完全缺失突变型个体, 从骨骼染色和骨骼发育相关基因表达两方面, 初步评价了肌间刺缺失对斑马鱼骨骼发育的影响。通过骨骼染色对比观察了两种肌间刺表型个体受精后8dpf(days post fertilization, dpf)到56dpf的骨骼发育情况, 结果显示, 两种肌间刺表型除肌间刺外, 其他骨骼发育基本同步。此外, 通过qRT-PCR实验检测分析了6个骨骼发育相关基因(bmp2a、bmp4、smad1、smad4a、runx2a和sp7)在不同肌间刺表型5个胚胎发育时期(3hpf囊胚期、6hpf原肠胚期、12hpf体节期、24hpf咽囊期和72hpf孵化期)和5个胚后生长阶段(15、30、45、60和75dpf)的表达情况。结果显示:在胚胎发育时期, 野生型和突变型个体中bmp2a、bmp4、smad1、smad4a基因和突变型个体中sp7基因的表达均呈现先升后降的变化趋势, 且在体节期达到最高表达水平;野生型和突变型个体中runx2a基因和野生型个体中sp7基因则表现为逐渐上升的趋势。6个基因在囊胚期和原肠胚期表达量无显著差异, bmp2a的表达水平在体节期、咽囊期和孵化期无显著差异, 野生型个体bmp4、smad1、smad4a、runx2a基因在体节期、咽囊期和孵化期的表达水平明显高于突变型, 而sp7基因则表现为突变型明显高于野生型。胚后发育阶段 6个基因在5个生长阶段均呈现逐渐下降的趋势, 且在两种肌间刺表型间其表达仅在个别时期差异显著。综上所述, 肌间刺的缺失对斑马鱼骨骼发育表现型无显著影响, 只在胚胎发育时期影响骨骼相关基因表达水平的变化;结合骨骼染色结果, 推测肌间刺缺失对斑马鱼骨骼发育无显著影响。Abstract: This study verified the impact of Imb (intermuscular bone) deficiency on skeletal development in two ways: analyses of skeletal staining and the expression of skeletal development-related genes between wildtype and Imb mutant zebrafish. First, this study revealed the skeletal development of two Imb phenotypes from 8 dpf to 56 dpf. The results indicated that the development of most of the skeleton was synchronous except for the intermuscular bones. Furthermore, we detected the expression of 6 skeletal development-related genes (bmp2a, bmp4, smad1, smad4a, runx2a and sp7) in 5 embryonic stages (blastula, 3 hpf; gastrula, 6 hpf; segmentation, 12 hpf; pharyngula, 24 hpf; and the hatching period, 72 hpf) and 5 postembryonic stages (15 dpf, 30 dpf, 45 dpf, 60 dpf and 75 dpf). The results for the different embryonic stages showed that the expression of 4 genes (bmp2a, bmp4, smad1 and smad4a) in both wildtype and mutant individuals and the expression of sp7 in mutant individuals was increased in the blastula, gastrula and segmentation stages, then declined in the pharyngula and hatching period. However, the expression of runx2a in both wildtype and mutant individuals and the expression of sp7 in wildtype zebrafish continued to rise during embryonic development. In addition, there was no difference in the expression of the 6 genes between wildtype and mutant zebrafish in the blastula and gastrula stages, whereas a significant difference in the expression of the genes existed in the other 3 stages. The expression of bmp4, smad1, smad4a and runx2a in wildtype zebrafish was higher than that in mutant zebrafish, and the expression of sp7 in wildtype zebrafish was lower than that in mutant individuals, whereas there was no difference in bmp2a expression between wildtype and mutant individuals. Moreover, the results during postembryonic development indicated that the expression of the 6 genes declined significantly in 5 periods and that there was no difference between wildtype and mutant individuals. In summary, considering the results of the skeletal staining and gene expression analyses together, we speculate that the deletion of intermuscular bones does not impact the skeletal development of zebrafish.
-
Keywords:
- Intermuscular bones /
- Zebrafish /
- Wildtype /
- Imb mutant /
- Skeletal development /
- Skeletal staining
-
与其他脊椎动物相同, 斑马鱼(Danio rerio)的骨骼也是由软骨和硬骨两种组织组成的, 其中软骨是由软骨细胞组成, 硬骨则是由成骨细胞和破骨细胞构成。软骨细胞和成骨细胞均起源于间充质细胞, 破骨细胞起源于髓单核细胞系[1]。间充质细胞在接收到分子信号后, 迁移至特定的部位, 随后这些间充质细胞紧密浓缩形成成骨、软骨的原基。在骨骼发育过程中, 这些原基会分泌一些转录因子, 如TGF-β家族的多肽等, 用于起始和调控早期骨骼发育相关因子的表达[2-4]。其中, 骨形态发生蛋白(Bone morphogenetic proteins, BMPs)是TGF-β超家族的一类生长因子。bmp2a、bmp4是BMPs家族的成员, bmp2a可促进间充质细胞分化形成成骨骨细胞, 缺少bmp2a会抑制骨祖细胞向骨细胞的分化; bmp4是软骨内骨化的早期因子, 在原始间充质细胞、软骨细胞和骨膜形成层、骨髓腔等部位均有表达[5-7]。此外, SMADs蛋白家族(Mothers against decapentaplegic protein, SMADs)是TGF-β超家族的重要细胞因子。研究认为BMPs信号通路的调控主要是依赖SMAD基因家族来引发细胞应答[8-10]; 其中, smad1是BMPs的通路受体底物, 能被BMP-I型受体磷酸化而被激活, 磷酸化的R-SMADs与受体分离, 而与smad4结合形成复合物, 随后这一蛋白异二聚体进入核内, 与相关的转录基因结合并调控下游基因的表达[11-13], 如runx2a(runt-related transcription factor 2a)。runx2a是一种成骨特异性转录因子, 其表达是间充质细胞向成骨细胞分化的重要标志。研究认为, 成骨细胞分化初期, runx2a起始骨基质蛋白的生成, 从而使成骨细胞向骨细胞转化[14, 15]。sp7(也称osterix)是成骨细胞分化和骨骼形成的标记基因, runx2a能够促进sp7基因的表达[14]。
肌间刺是影响鲤科鱼类品质的重要因素之一, 是鲤科鱼类遗传育种的重要目标性状, 但因肌间刺位于体内, 科学家认为其起到支撑肌肉和力量传递的作用, 对肌间刺是否能进行选育, 以及肌间刺缺失后是影响否生长、脂肪酸、肌纤维等其他性状的形成仍存在疑问。为探讨这些问题, 本实验室采用基因敲除和遗传筛选技术, 获得了1个可稳定遗传的斑马鱼肌间刺完全缺失突变系, 本研究利用该突变系和野生型斑马鱼, 从胚胎发育5个发育时期(3、6、12、24和72hpf)和胚后5个生长阶段(15、30、45、60和75dpf), 对比分析了6个骨骼发育相关基因(bmp2a、bmp4、smad1、smad4a、runx2a和sp7)的表达差异; 并结合胚后发育两种肌间刺表型骨骼发育的情况, 初步评估了肌间刺缺失对斑马鱼除肌间刺外, 其他骨骼发育的影响。
1. 材料与方法
1.1 试验鱼准备
为了去除遗传背景不同带来的影响, 将基因敲除后获得的斑马鱼肌间刺完全缺失突变型个体与野生型AB系个体杂交, 构建F2代家系。F2代家系自交可分别获得25%的野生型、25%的突变型纯合个体和50%杂合个体。将野生型个体和纯合突变个体分别按雌﹕雄比例1﹕1构建实验家系, 分别获得14个突变型家系和13个野生型家系。养殖3个月后达到性成熟, 按家系配对繁殖并将受精卵置于28℃培养箱中孵化。破膜4d(即8dpf)后的仔鱼置于静水中养殖, 用草履虫饲喂至20dpf, 转入斑马鱼养殖系统中, 并用丰年虫投喂, 养殖水温(27±1)℃, 光周期14 L﹕10 D。
1.2 骨骼染色观察
选择3个野生型家系和3个突变型家系, 用于骨骼染色试验。自8dpf开始, 至56dpf截止, 每隔6d采样一次, 各家系随机选择5尾试验鱼用多聚甲醛固定。其中, 8—26dpf仔稚鱼用4%多聚甲醛固定, 32—56dpf幼鱼用2%多聚甲醛固定, 避光保存2d。
采用阿尔新蓝—茜素红双染色法进行骨骼染色。操作步骤如下: (1)8—26dpf 仔稚鱼: a)脱水: 去除固定液, 用50%乙醇脱水, 轻微摇匀10min; b)染色: 将浸泡过的样本用阿尔新蓝-茜素红混合液 (10 μL 0.5%的茜素红溶液加入到1 mL 0.4%的阿尔新蓝工作液混合) 染色过夜; c)漂白: 去除染液, 用蒸馏水洗去浮色, 加入漂白液(3%双氧水, 2%氢氧化钾溶液等体积混合配制), 室温放置20min; d)透明: 去除漂白液, 用硬毛笔轻轻剥离鱼体表面鳞片, 用透明剂Ⅰ(40%甘油与0.5%氢氧化钾溶液等体积混匀配制)处理至鱼体透明, 用透明剂Ⅱ(甘油与0.5%氢氧化钾溶液等体积混匀配制)透明至透明剂不再变色; e)保存: 透明后的样本于50%甘油和0.1%氢氧化钾混合液中4℃长期保存。(2)32—56dpf 幼鱼: a)脱水: 与仔稚鱼相同; b)阿尔新蓝染色: 去除50%乙醇, 用0.4%阿尔新蓝染色1d; c)复水: 用50%和30%乙醇分别复水10min, 用去离子水清洗2h; d)消化: 用50 mg/mL的胰蛋白酶溶液消化过夜, 至日光灯下可见脊椎骨为宜; e)漂白: 同仔稚鱼; f)透明与保存: 同仔稚鱼。
用Olympus SZX2-TR30显微成像系统观察斑马鱼在不同生长阶段骨骼发育情况。
1.3 基因表达检测
胚胎发育阶段: 按照斑马鱼胚胎发育分期[16], 并结合镜检结果, 在受精后3(囊胚期)、6(原肠胚期)、12(体节期)、24(咽囊期)和72hpf(孵化期)5个发育时期采集胚胎样本。随机选择3个突变型家系与3个野生型家系, 每个家系随机选取发育正常的受精卵50粒, 用于总RNA的提取。胚后生长阶段: 随机选择3个野生型家系和3个突变型家系分5个生长阶段(15、30、45、60和75dpf)进行骨骼样品采集, 各家系子代随机选择3尾试验鱼, 冰冻处死后于冰上去除内脏、皮肤和肌肉等组织, 每个家系做1个混样, 用于总RNA提取。采用Trizol法提取(Invitrogen, USA)总RNA, 采用High Capacity cDNA Reverse Transcription kits(Roache, USA)合成cDNA。
采用qRT-PCR方法检测6个基因(bmp2a、bmp4、smad1、smad4a、runx2a和sp7)的表达水平, 扩增引物采用Primer3 plus设计(表 1)。采用10 µL反应体系进行qRT-PCR实验, 包括: 5 µL 2×Luna Universal qPCR Master Mix(NEB, USA), 0.25 µL 10 µmol/L的正向、反向引物, 1 µL 50 ng/µL cDNA, 3.5 µL nuclease-free水。扩增条件为: 95℃预变性60s; 之后, 95℃变性15s, 60℃延伸30s, 循环40次。以gapdh为内参基因。
表 1 骨骼发育相关基因引物设计Table 1. Skeletal development related gene primers for qRT-PCRNCBI登录号NCBI accession number 基因Gene 序列Primer sequences (5′-3′) NM_131359.1 bmp2a GCCAGCAGAGCCAACACTAT GCACTTGCGTTGTTTAGCGA NM_131342.2 bmp4 CTGCCAGGACCACGTAACAT CCGACGCTTTCTTCTTCCCT NM_131356.1 smad1 CCCTTCCCTTTACCCCGAAC GGAGGGGTTTCTGGCATCTG NM_001122700.1 smad4a CGGTAGTGTGCTCTCAGGAA GCTGGGGGTGAAGTTACTGT NM_212858.2 runx2a GTTCCCTTCCGATGCCTTGA TGCTCGGATCCCAGAAAAAGT NM_212863.2 sp7 GCGCTCGTCTTTACCAAACA TGAGGAGCAGAGAAAAGAGGAG NM_001115114.1 gapdh ACCCGTGCTGCTTTCTTGAC GACCAGTTTGCCGCCTTCT 1.4 数据分析
采用2–∆∆Ct法[17]评估6个骨骼发育相关基因的表达水平, 采用T检验评估肌间刺缺失突变型个体和野生型个体间6个基因在胚胎发育和胚后发育每个时期中的表达水平和时序表达差异(P<0.05)。
2. 结果
2.1 骨骼染色
染色结果显示, 斑马鱼野生型与突变型个体除肌间刺外, 其他骨骼的发育基本保持一致。
(1)8dpf: 耳石已经骨化; 头部骨骼、脊椎仍为软骨状态, 脊椎四周有规则的凹凸, 髓弓、脉弓和尾椎以软骨形式出现, 并由头部向尾部发展(图版Ⅰ-1、2)。(2)14dpf: 部分脊椎硬骨化, 并由头部向尾部发展, 硬骨化的椎体约5—8个; 头部骨骼如下咽骨开始出现部分硬骨化(图版Ⅰ-3、4)。(3)20dpf: 硬骨化的脊椎向尾部增加至20个左右, 头部下咽骨硬骨化范围增大, 前上颌骨和鳃盖边缘开始硬骨化(图版Ⅰ-5、6)。(4)26dpf: 脊椎硬骨化的范围扩大至约30个椎体, 前部骨节肋骨开始骨化, 尾鳍的鳍条基骨和鳍条骨也逐步开始硬骨化; 头部鳃弓, 眼眶骨, 开始硬骨化(图版Ⅰ-7、8)。(5)32dpf: 椎骨基本完成硬骨化, 肋骨、髓棘和脉棘骨化长度变大, 尾鳍鳍条骨骨化完成, 背鳍和臀鳍的鳍条骨也开始逐步骨化, 棘和支鳍骨仍呈软骨状态, 头部上颌弓、前鳃盖骨、鳃盖骨和方骨等基本完成骨化(图版Ⅰ-9、10)。(6)38dpf: 尾鳍骨化基本完成, 背鳍和臀鳍的鳍条和深入肌肉的棘硬骨化变长, 胸鳍开始骨化, 突变型腹鳍骨化早于野生型; 头部前上颌骨、下咽骨、上眶骨、泪骨、眶骨、方骨、鳃盖骨、下腮盖骨、鳃条骨、前鳃骨等均已骨化, 顶部额骨、颅顶骨、外枕骨等仍未完全骨化(图版Ⅰ-11、12)。(7)44dpf: 背鳍、臀鳍和腹鳍鳍条骨骨化基本完成, 仅余鳍条骨与支鳍骨连接的部位未骨化; 野生型个体头部仅剩颅顶骨未完全骨化, 突变型头部骨化基本完成; 野生型个体肌间刺由尾部向鱼体前部逐步骨化, 腹部骨化快于背部, 突变型斑马鱼无肌间刺骨化现象(图版Ⅰ-13、14)。(8)50dpf: 野生型个体颅顶骨完全硬骨化, 腹部肌间刺基本骨化完成, 背部肌间刺骨化至背鳍前, 突变型斑马鱼肌间刺未出现骨化现象(图版Ⅰ-15、16)。(9)56dpf: 全身骨骼基本骨化完成, 仅剩背鳍、臀鳍、尾鳍少数支鳍骨未骨化, 野生型斑马鱼的肌间刺骨化也基本完成(图版Ⅰ-17), 而突变型斑马鱼未有肌间刺形成(图版Ⅰ-18)。
![]() 图版 Ⅰ 野生型与突变型斑马鱼骨骼发育过程1. 8dpf野生型(体长6.12 mm); 2. 8dpf突变型(体长5.96 mm); 3. 14dpf野生型(体长7.32 mm); 4. 14dpf突变型(体长7.92 mm); 5. 20dpf野生型(体长9.87 mm); 6. 20dpf突变型(体长10.16 mm); 7. 26dpf野生型(体长11.27 mm); 8. 26dpf突变型(体长11.66 mm); 9. 32dpf野生型(体长12.38 mm); 10. 32dpf突变型(体长12.67 mm); 11. 38dpf野生型(体长15.42 mm); 12. 38dpf突变型(体长15.07 mm); 13. 44dpf野生型(体长17.02 mm); 14. 44dpf突变型(体长16.84 mm); 15. 50dpf野生型(体长17.98 mm); 16. 50dpf突变型(体长18.41 mm); 17. 56dpf野生型(体长19.04 mm); 18. 56dpf突变型(体长19.85 mm); Af: 臀鳍; Br: 鳃条骨; Ct: 椎体; Df: 背鳍; Fp: 支鳍骨; Fr: 鳍条骨; Fro: 额骨; Ga: 鳃弓; Hs: 脉棘; Hy: 下咽骨; Imb: 肌间刺; La: 泪骨; Na: 髓弓; Ns: 髓棘; Or: 眶骨; Op: 鳃盖骨; Ot: 耳石; Pa: 颅顶骨; Pef: 胸鳍; Pf: 腹鳍; Pr: 前上颌骨; Pra: 前鳃盖骨; R: 肋骨; Qu: 方骨; Sc: 上枕骨; So: 上眶骨; Su: 下鳃盖骨; Vc: 脊柱图版 Ⅰ. Development of the wildtype and mutant zebrafish skeleton1. 8dpf wildtype zebrafish (total length: 6.12 mm); 2. 8dpf mutant zebrafish (total length: 5.96 mm); 3. 14dpf wildtype zebrafish (total length: 7.32 mm); 4. 14dpf mutant zebrafish (total length: 7.92 mm); 5. 20dpf wildtype zebrafish (total length: 9.87 mm); 6. 20dpf mutant zebrafish (total length: 10.16 mm); 7. 26dpf wildtype zebrafish (total length: 11.27 mm); 8. 26dpf mutant zebrafish (total length: 11.66 mm); 9. 32dpf wildtype zebrafish (total length: 12.38 mm); 10. 32dpf mutant zebrafish (total length: 12.67 mm); 11. 38dpf wildtype zebrafish (total length: 15.42 mm); 12. 38dpf mutant zebrafish (total length: 15.07 mm); 13. 44dpf wild zebrafish (total length: 17.02 mm); 14. 44dpf mutant zebrafish (total length: 16.84 mm); 15. 50dpf wild zebrafish (total length: 17.98 mm); 16. 50dpf mutant zebrafish (total length: 18.41 mm); 17. 56dpf wild zebrafish (total length: 19.04 mm); 18. 56dpf mutant zebrafish (total length:19.85 mm). Af: anal fin; Br: branchiostegal ray; Ct: centrum; Df: dorsal fin; Fp: fin plate; Fr: fin ray; Fro: frontal bone; Ga: gill arch; Hs: haemal spine; Hy: hypopharyngeal bone; Imb:intermuscular bone; La: lacrimal bone; Na:neural arch; Ns: neural spine; Or: orbital bone; Op: Operculum; Ot: otolith; Pa: parietal bone; Pef: pectoral fin; pelvic fin; Pr: premaxillary bone; Pra: preopercular bone; R: rib; Qu: quadrate bone; Sc: supraoccipital bone; So: supra orbital; Su: suboperculum bone; Vc: vertebral column
图版 Ⅰ 野生型与突变型斑马鱼骨骼发育过程1. 8dpf野生型(体长6.12 mm); 2. 8dpf突变型(体长5.96 mm); 3. 14dpf野生型(体长7.32 mm); 4. 14dpf突变型(体长7.92 mm); 5. 20dpf野生型(体长9.87 mm); 6. 20dpf突变型(体长10.16 mm); 7. 26dpf野生型(体长11.27 mm); 8. 26dpf突变型(体长11.66 mm); 9. 32dpf野生型(体长12.38 mm); 10. 32dpf突变型(体长12.67 mm); 11. 38dpf野生型(体长15.42 mm); 12. 38dpf突变型(体长15.07 mm); 13. 44dpf野生型(体长17.02 mm); 14. 44dpf突变型(体长16.84 mm); 15. 50dpf野生型(体长17.98 mm); 16. 50dpf突变型(体长18.41 mm); 17. 56dpf野生型(体长19.04 mm); 18. 56dpf突变型(体长19.85 mm); Af: 臀鳍; Br: 鳃条骨; Ct: 椎体; Df: 背鳍; Fp: 支鳍骨; Fr: 鳍条骨; Fro: 额骨; Ga: 鳃弓; Hs: 脉棘; Hy: 下咽骨; Imb: 肌间刺; La: 泪骨; Na: 髓弓; Ns: 髓棘; Or: 眶骨; Op: 鳃盖骨; Ot: 耳石; Pa: 颅顶骨; Pef: 胸鳍; Pf: 腹鳍; Pr: 前上颌骨; Pra: 前鳃盖骨; R: 肋骨; Qu: 方骨; Sc: 上枕骨; So: 上眶骨; Su: 下鳃盖骨; Vc: 脊柱图版 Ⅰ. Development of the wildtype and mutant zebrafish skeleton1. 8dpf wildtype zebrafish (total length: 6.12 mm); 2. 8dpf mutant zebrafish (total length: 5.96 mm); 3. 14dpf wildtype zebrafish (total length: 7.32 mm); 4. 14dpf mutant zebrafish (total length: 7.92 mm); 5. 20dpf wildtype zebrafish (total length: 9.87 mm); 6. 20dpf mutant zebrafish (total length: 10.16 mm); 7. 26dpf wildtype zebrafish (total length: 11.27 mm); 8. 26dpf mutant zebrafish (total length: 11.66 mm); 9. 32dpf wildtype zebrafish (total length: 12.38 mm); 10. 32dpf mutant zebrafish (total length: 12.67 mm); 11. 38dpf wildtype zebrafish (total length: 15.42 mm); 12. 38dpf mutant zebrafish (total length: 15.07 mm); 13. 44dpf wild zebrafish (total length: 17.02 mm); 14. 44dpf mutant zebrafish (total length: 16.84 mm); 15. 50dpf wild zebrafish (total length: 17.98 mm); 16. 50dpf mutant zebrafish (total length: 18.41 mm); 17. 56dpf wild zebrafish (total length: 19.04 mm); 18. 56dpf mutant zebrafish (total length:19.85 mm). Af: anal fin; Br: branchiostegal ray; Ct: centrum; Df: dorsal fin; Fp: fin plate; Fr: fin ray; Fro: frontal bone; Ga: gill arch; Hs: haemal spine; Hy: hypopharyngeal bone; Imb:intermuscular bone; La: lacrimal bone; Na:neural arch; Ns: neural spine; Or: orbital bone; Op: Operculum; Ot: otolith; Pa: parietal bone; Pef: pectoral fin; pelvic fin; Pr: premaxillary bone; Pra: preopercular bone; R: rib; Qu: quadrate bone; Sc: supraoccipital bone; So: supra orbital; Su: suboperculum bone; Vc: vertebral column2.2 胚胎发育时期骨骼发育相关基因的表达
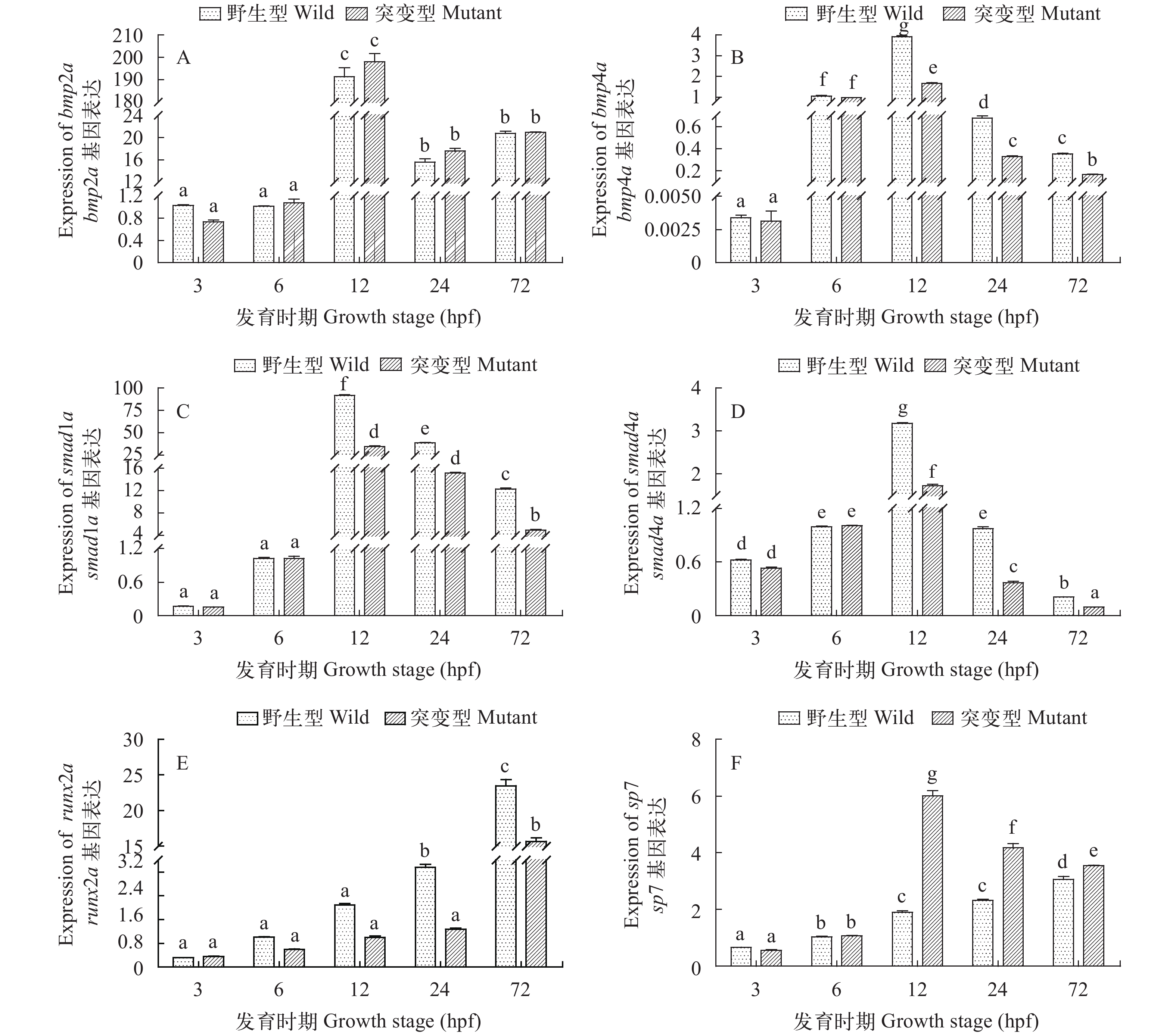
结果显示, bmp2a、bmp4、smad1、smad4a在野生型和突变性个体中的表达, 及sp7基因在突变型个体中的表达均呈现先升后降的变化趋势, 且在体节期(12hpf)达到最高表达水平; 而runx2a基因在野生型和突变型个体中的表达, 以及sp7基因在野生型个体中的表达则表现为逐渐上升的趋势。对6个基因在野生型和突变型胚胎发育时期的表达水平进行对比分析发现, 在囊胚期(3hpf)和原肠胚期(6hpf)6个基因在两种肌间刺表型间表达量无明显差异, 在体节期(12hpf)、咽囊期(24hpf)和孵化期(72hpf)bmp2a的表达水平在两种肌间刺表型间无明显差异, 野生型个体bmp4、smad1、smad4a、runx2a基因在体节期(12hpf)、咽囊期(24hpf)和孵化期(72hpf)的表达水平明显高于突变型, 而sp7基因则表现为突变型明显高于野生型(图 1)。
![]() 图 1 胚胎发育阶段不同肌间刺表型斑马鱼6个骨骼发育相关基因的表达以gadph为内参基因, 采用
图 1 胚胎发育阶段不同肌间刺表型斑马鱼6个骨骼发育相关基因的表达以gadph为内参基因, 采用${\bar x}\!\! \pm\!\! {\rm{SD}}$ (n=3)表示斑马鱼野生型和突变型6个骨骼发育相关基因表达水平; 不同小写字母表示差异显著(P<0.05); 下同Figure 1. Expression of 6 skeleton development related genes in different embryonic development stagesGene expression was normalized to the expression of the reference gene gapdh. Data are expressed as${\bar x}\! \!\pm\!\! {\rm{SD}}$ of 2–∆∆Ct (n=3). Different lowercase letters indicate significant differences (P<0.05). The same applies below2.3 胚后发育阶段骨骼发育相关基因的表达
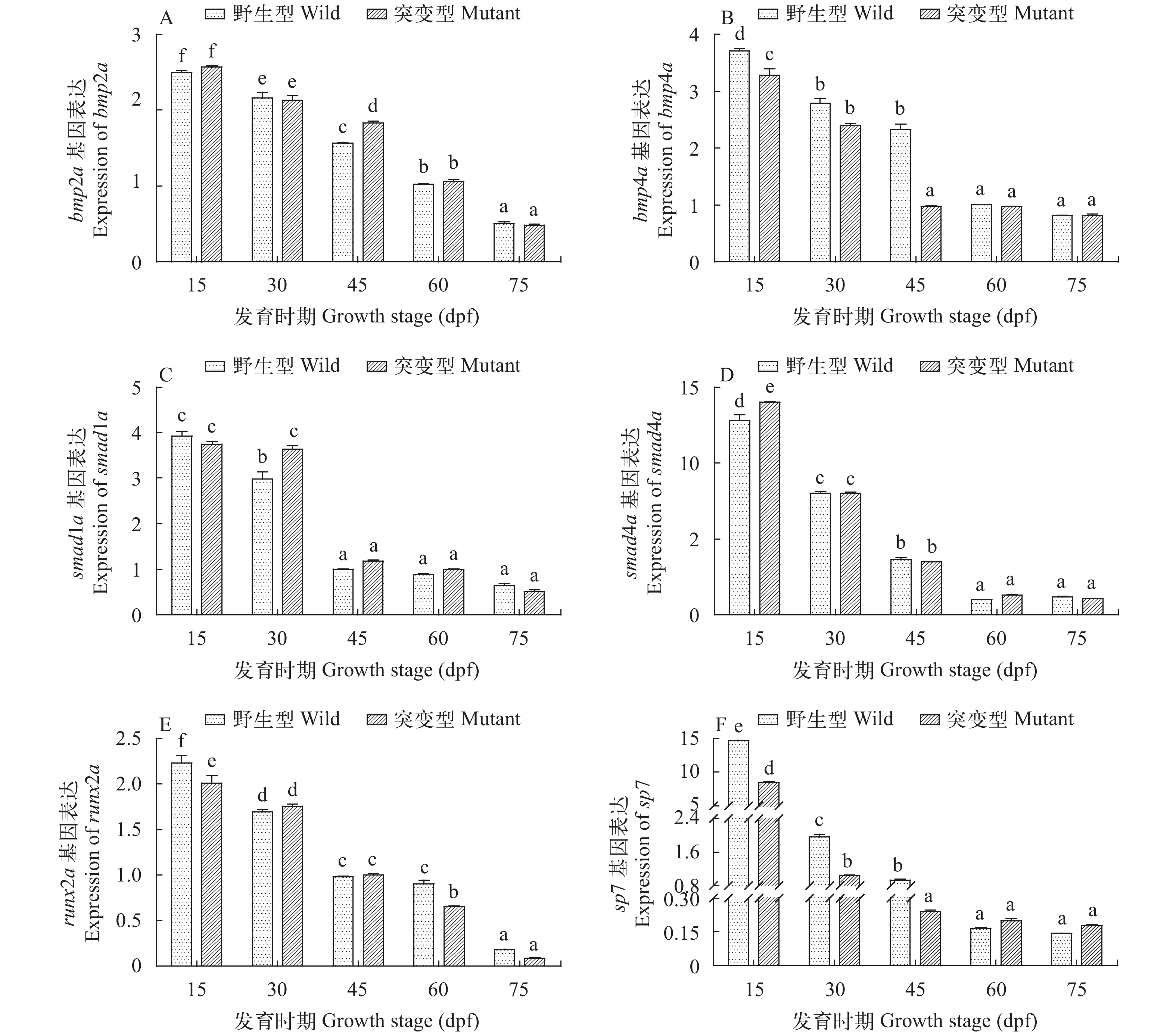
结果显示, bmp2a、bmp4、smad1、smad4a、runx2a和sp7基因在野生型和突变型斑马鱼个体5个胚后生长阶段(15、30、45、60和75dpf)的表达均基本呈现出逐渐下降的的趋势。两种肌间刺表型间6个基因的表达在个别时期存在差异, 其中, bmp2a在45dpf时野生型个体表达量明显高于突变型, 而bmp4则与之相反; smad1和smad4a则分别在30和15dpf表达量表现为野生型低于突变型; 此外, runx2a在15dpf时, 野生型个体在15和60dpf时的表达量表现为野生型高于突变型, 而sp7在15、30和45dpf 3个生长阶段亦表现为野生型个体表达量显著高于突变型(图 2)。
3. 讨论
本研究发现, 斑马鱼的骨骼发育具有特定的时空顺序, 头骨、脊椎骨和鱼鳍骨骼基本遵循由头部向尾部依次骨化的规律, 而肌间刺的发育则是由尾部向头部依次骨化, 且腹部肌间刺的骨化快于背部; 鳍条骨骼顺序为尾鳍、背鳍、臀鳍、腹鳍、胸鳍。斑马鱼骨骼的骨化方式与其他脊椎动物相同, 有软骨内骨化和膜内骨化两种方式[18-20], 斑马鱼的大部分骨骼(头骨、脊椎骨和鱼鳍骨骼等)均为需要经过软骨阶段的软骨内骨化, 肌间刺不经过软骨阶段而由骨膜直接骨化形成。对于斑马鱼骨骼发育的研究, 许多国内外研究人员已经做了大量的工作。Cubbage和Mabee[21]对斑马鱼幼鱼和成鱼头盖骨和侧鳞的骨化进行过了报道, Du等[18]对斑马鱼23dpf内个体纵轴骨骼的钙化进行了描述, Yao等[22]则对斑马鱼肌间刺的发育模式进行了观察。本研究观察分析了斑马鱼骨骼从8dpf到52dpf的连续发育过程, 结论与已有文献一致。此外, 本研究通过比较两种肌间刺表型骨骼的发育过程发现, 头骨、脊椎骨和鱼鳍骨骼的发育基本保持一致, 故初步推测肌间刺的缺失不影响斑马鱼其他骨骼的发育。
研究发现, 斑马鱼胚胎发育至48—52hpf的胚胎中就已存在未发育的由软骨因子组成的骨架, 具有基舌骨等头部骨骼, 脊索仅为轴向支撑结构[23, 24]。这与本研究中野生型斑马鱼6个骨骼发育相关基因的表达变化相一致。胚胎发育时, bmp2a、bmp4、smad1和smad4a基因相继激活并发挥作用[4, 13]。骨骼发育的结果发现, 野生型和突变型斑马鱼bmp2a、bmp4基因在胚胎发育5个发育阶段的变化趋势分别与smad1、smad4a相一致; 胚后发育过程5个生长阶段的变化趋势也基本呈现一致的变化趋势, 这一结果与已有文献一致[8, 25]。此外, 野生型斑马鱼个体中runx2a和sp7基因的表达也呈现持续上升的趋势, 虽然bmp2a基因的表达水平在12hpf后有所下降, 但仍保持较高的表达水平; 胚后发育过程中, runx2a与sp7基因的表达水平则随着BMPs家族基因和SMAD家族基因表达水平的降低而随之下降, 与已有文献报道一致[8, 9]。
胚胎发育阶段, 两种肌间刺表型6个基因在在囊胚期(3hpf)和原肠胚期(6hpf)表达量无明显差异, 在体节期(12hpf)、咽囊期(24hpf)和孵化期(72hpf)bmp2a基因表达无明显差异, bmp4、smad1、smad4a、runx2a基因表现为野生型明显高于突变型, 而sp7基因则表现为突变型明显高于野生型, 表明肌间刺的缺失对6个基因的表达存在一定程度的影响; 胚后生长阶段, 6个基因的表达水平仅在个别生长阶段差异显著。综合基因表达与骨骼染色情况发现, 虽然在胚胎发育和胚后发育阶段, 骨骼发育相关基因的表达在两种肌间刺表型间存在一定的差异, 但是骨骼染色结果显示两种表型骨骼发育并无明显差异, 推测肌间刺发育关键基因的突变对骨骼发育的影响主要在胚胎发育阶段。此外, 在胚胎发育过程中, runx2a的表达趋势为野生型个体高于突变型, 而sp7则刚好与之相反; 在胚后生长阶段个别时期(15dpf)则表现为表达趋势相同, 推测在胚胎发育过程肌间刺关键基因的突变导致的runx2a基因的表达下调由sp7的高表达进行了补偿; 而在胚后阶段runx2a和sp7基因在突变型中的低水平表达并未影响骨骼发育过程, 可能是由于其他调控途径激活了smad1和smad4a基因的上调, 补偿了runx2a和sp7基因的表达下调。综上, 肌间刺发育关键基因的突变对斑马鱼骨骼发育无显著影响, 而对于肌间刺关键基因的缺失的影响及表达调控仍需进一步研究证实。
-
图版 Ⅰ 野生型与突变型斑马鱼骨骼发育过程
1. 8dpf野生型(体长6.12 mm); 2. 8dpf突变型(体长5.96 mm); 3. 14dpf野生型(体长7.32 mm); 4. 14dpf突变型(体长7.92 mm); 5. 20dpf野生型(体长9.87 mm); 6. 20dpf突变型(体长10.16 mm); 7. 26dpf野生型(体长11.27 mm); 8. 26dpf突变型(体长11.66 mm); 9. 32dpf野生型(体长12.38 mm); 10. 32dpf突变型(体长12.67 mm); 11. 38dpf野生型(体长15.42 mm); 12. 38dpf突变型(体长15.07 mm); 13. 44dpf野生型(体长17.02 mm); 14. 44dpf突变型(体长16.84 mm); 15. 50dpf野生型(体长17.98 mm); 16. 50dpf突变型(体长18.41 mm); 17. 56dpf野生型(体长19.04 mm); 18. 56dpf突变型(体长19.85 mm); Af: 臀鳍; Br: 鳃条骨; Ct: 椎体; Df: 背鳍; Fp: 支鳍骨; Fr: 鳍条骨; Fro: 额骨; Ga: 鳃弓; Hs: 脉棘; Hy: 下咽骨; Imb: 肌间刺; La: 泪骨; Na: 髓弓; Ns: 髓棘; Or: 眶骨; Op: 鳃盖骨; Ot: 耳石; Pa: 颅顶骨; Pef: 胸鳍; Pf: 腹鳍; Pr: 前上颌骨; Pra: 前鳃盖骨; R: 肋骨; Qu: 方骨; Sc: 上枕骨; So: 上眶骨; Su: 下鳃盖骨; Vc: 脊柱
图版 Ⅰ. Development of the wildtype and mutant zebrafish skeleton
1. 8dpf wildtype zebrafish (total length: 6.12 mm); 2. 8dpf mutant zebrafish (total length: 5.96 mm); 3. 14dpf wildtype zebrafish (total length: 7.32 mm); 4. 14dpf mutant zebrafish (total length: 7.92 mm); 5. 20dpf wildtype zebrafish (total length: 9.87 mm); 6. 20dpf mutant zebrafish (total length: 10.16 mm); 7. 26dpf wildtype zebrafish (total length: 11.27 mm); 8. 26dpf mutant zebrafish (total length: 11.66 mm); 9. 32dpf wildtype zebrafish (total length: 12.38 mm); 10. 32dpf mutant zebrafish (total length: 12.67 mm); 11. 38dpf wildtype zebrafish (total length: 15.42 mm); 12. 38dpf mutant zebrafish (total length: 15.07 mm); 13. 44dpf wild zebrafish (total length: 17.02 mm); 14. 44dpf mutant zebrafish (total length: 16.84 mm); 15. 50dpf wild zebrafish (total length: 17.98 mm); 16. 50dpf mutant zebrafish (total length: 18.41 mm); 17. 56dpf wild zebrafish (total length: 19.04 mm); 18. 56dpf mutant zebrafish (total length:19.85 mm). Af: anal fin; Br: branchiostegal ray; Ct: centrum; Df: dorsal fin; Fp: fin plate; Fr: fin ray; Fro: frontal bone; Ga: gill arch; Hs: haemal spine; Hy: hypopharyngeal bone; Imb:intermuscular bone; La: lacrimal bone; Na:neural arch; Ns: neural spine; Or: orbital bone; Op: Operculum; Ot: otolith; Pa: parietal bone; Pef: pectoral fin; pelvic fin; Pr: premaxillary bone; Pra: preopercular bone; R: rib; Qu: quadrate bone; Sc: supraoccipital bone; So: supra orbital; Su: suboperculum bone; Vc: vertebral column
图 1 胚胎发育阶段不同肌间刺表型斑马鱼6个骨骼发育相关基因的表达
以gadph为内参基因, 采用
${\bar x}\!\! \pm\!\! {\rm{SD}}$ (n=3)表示斑马鱼野生型和突变型6个骨骼发育相关基因表达水平; 不同小写字母表示差异显著(P<0.05); 下同Figure 1. Expression of 6 skeleton development related genes in different embryonic development stages
Gene expression was normalized to the expression of the reference gene gapdh. Data are expressed as
${\bar x}\! \!\pm\!\! {\rm{SD}}$ of 2–∆∆Ct (n=3). Different lowercase letters indicate significant differences (P<0.05). The same applies below表 1 骨骼发育相关基因引物设计
Table 1 Skeletal development related gene primers for qRT-PCR
NCBI登录号NCBI accession number 基因Gene 序列Primer sequences (5′-3′) NM_131359.1 bmp2a GCCAGCAGAGCCAACACTAT GCACTTGCGTTGTTTAGCGA NM_131342.2 bmp4 CTGCCAGGACCACGTAACAT CCGACGCTTTCTTCTTCCCT NM_131356.1 smad1 CCCTTCCCTTTACCCCGAAC GGAGGGGTTTCTGGCATCTG NM_001122700.1 smad4a CGGTAGTGTGCTCTCAGGAA GCTGGGGGTGAAGTTACTGT NM_212858.2 runx2a GTTCCCTTCCGATGCCTTGA TGCTCGGATCCCAGAAAAAGT NM_212863.2 sp7 GCGCTCGTCTTTACCAAACA TGAGGAGCAGAGAAAAGAGGAG NM_001115114.1 gapdh ACCCGTGCTGCTTTCTTGAC GACCAGTTTGCCGCCTTCT -
[1] Agnes D B, Bjorn R O. Bone development [J]. Bone, 2015, 80(14): 14-18.
[2] Wu M R, Chen G Q, Li Y P. TGF-β and BMP signaling in osteoblast, skeletal development, and bone formation, homeostasis and disease [J]. Bone Research, 2016, 4(1): 10-30.
[3] DeLise A M, Fischer L, Tuan R S. Cellular interactions and signaling in cartilage development [J]. Osteoarthritis Cartilage, 2000, 8(5): 309-334. doi: 10.1053/joca.1999.0306
[4] Olsen B R, Reginato A M, Wang W. Bone development [J]. Annual Review of Cell and Developmental Biology, 2000, 16(1): 191-220.
[5] Shore E, Xu M Q, Shah P, et al. The human bone morphogenetic protein 4 (bmp4) gene: Molecular structure and transcriptional regulation [J]. Calcified Tissue International, 1998, 63(3): 221-229. doi: 10.1007/s002239900518
[6] 毛海峰. bmp4的生物学功能及其在运动损伤领域的应用 [J]. 宜春学院学报, 2009, 31(2): 145-147. doi: 10.3969/j.issn.1671-380X.2009.02.068 Mao H F. The biological function of bmp4 and its application in the field of sport injury [J]. Journal of Yichun College, 2009, 31(2): 145-147. doi: 10.3969/j.issn.1671-380X.2009.02.068
[7] Nojima J, Kanomata K, Takada Y, et al. Dual roles of smad proteins in the conservation from myoblasts to osteoblastic cells by bone morphogenetic proteins [J]. Journal of Biological Chemistry, 2010, 285(20): 15577-15586. doi: 10.1074/jbc.M109.028019
[8] Jeon E J, Lee K Y, Choi N S, et al. Bone morphogenetic protein-2 stimulates runx2 acetylation [J]. The Journal of Biological Chemistry, 2006, 24(24): 16502-16511.
[9] Liu T, Gao Y, Sakamoto K, et al. bmp2 promotes differentiation of osteoblasts and chondroblasts in runx2-deficient cell lines [J]. Journal of Cellular Physiology, 2007, 3(3): 728-735.
[10] Rosen V. bmp2a signaling in bone development and repair [J]. Cytokine & Growth Factor Review, 2009, 20(5): 475-480.
[11] Guzman A, Zelman F M, Boergermann J H, et al. smad versus non-smad signaling is determined by lateral mobility of bone morphogenetic protein (bmp) receptors [J]. Journal of Biological Chemistry, 2012, 287(47): 39492-39504. doi: 10.1074/jbc.M112.387639
[12] Wiegman E M, Blaese M A, Loeffler H, et al. TGFbeta-1 dependent fast stimulation of ATM and p53 phosphorylation following exposure to ionizing radiation does not involve TGF beta-receptor I signaling [J]. Radiotherapy and Oncology, 2007, 83(3): 289-295. doi: 10.1016/j.radonc.2007.05.013
[13] Nishimura R, Hata K, Ikeda F, et al. The role of Smads in bmp signaling [J]. Frontiers in Bioscience:a Journal and Virtual Library, 2003(8): 275-284.
[14] Komori T. Regulation of osteoblast differentiation by transcription factors [J]. Journal of Cellular Biochemistry, 2006, 99(5): 1233-1239. doi: 10.1002/jcb.20958
[15] Kitayner M, Rozenberg H, Rabinovieh D, et al. Structures of the DNA-bingding site of Runt-domain transcription regulators [J]. Acta Crystallographica. Section D:Biological Crystallography, 2005, 61(Pt3): 236-246.
[16] Charlrs B K, William W B, Seth R K, et al. Stages of embryonic development of the zebrafish [J]. Developmental Dynamics, 1995, 203(3): 253-310.
[17] Kenneth J L, Thomas D S. Analysis of relative gene expression data using real-time quantitative PCR and the 2–∆∆ Ct method [J]. Methods, 2001, 25(4): 402-408.
[18] Du SJ, Frenkel V, Kindschi G, et al. Visualizing normal and defective bone development in zebrafish embryos using the fluorescent chromophore calcein [J]. Developmental Biology, 2001, 238(2): 239-246.
[19] Bird N C and Mabee P M. Developmental morphology of the axial skeleton of the zebrafish, Danio redo (Ostariophysi: Cyprinidae) [J]. Developmental Dynamics, 2003, 228(3): 337-357. doi: 10.1002/dvdy.10387
[20] Walker M B, Miller C T, Talbot J C, et al. Zebrafish furin mutants reveal intricacies in regulating Endothelinl signaling in craniofacial patterning [J]. Developmental Biology, 2006, 295: 194-205. doi: 10.1016/j.ydbio.2006.03.028
[21] Cubbage C C, and Mabee P M. Development of the cranium and paired fins in the zebrafish Danio rerio (Ostadophysi, Cyprinidae) [J]. International Journal of Morphology, 1996, 229(2): 121-160.
[22] Yao W J, Lv Y P, Gong X L, et al. Different ossification patterns of intermuscular bones in fish with different swimming modes [J]. Biology Open, 2015, 12(4): 1727-1732.
[23] Enomoto H, Furuichi T, Zanma A, et al. runx2a deficiency in chondrocytes causes adipogenic changes in vitro [J]. Journal of Cell Science, 2004, 117(Pt3): 417-425.
[24] Zhang C. Molecular mechanisms of osteoblast-specific transcription factor Osterix effect on bone formation [J]. Journal of Peking University (
Health Science ) , 2012, 44(5): 659-665. [25] 陈兵, 鲁开智. Smad蛋白家族调控细胞分化的研究进展 [J]. 医学研究生学报, 2013, 26(5): 544-547. doi: 10.3969/j.issn.1008-8199.2013.05.024 Chen B, Lu K Z. Advances in researches on Smad proteins [J]. Journal of Medical Postgraduates, 2013, 26(5): 544-547. doi: 10.3969/j.issn.1008-8199.2013.05.024
-
期刊类型引用(10)
1. 孙怡,夏洪志,牛堃,李江波,朱宇雷,李古月,尹忠燕. 维生素K_2单独及与钙剂联合使用对斑马鱼骨骼健康的改善作用及机制研究. 食品工业科技. 2024(03): 320-327 .  百度学术
百度学术
2. 陈松林,王德寿,匡友谊,崔忠凯,李明辉. 中国鱼类基因组编辑育种研究现状及存在问题与展望. 水产学报. 2023(01): 13-26 .  百度学术
百度学术
3. 张静,迟彦艳,杨珩,宋雪,张健飞,隋鸿锦. 斑马鱼脊柱区的发育. 中国实验动物学报. 2023(04): 524-530 .  百度学术
百度学术
4. 杨笑星,佟广香,闫婷,董乐,孙志鹏,徐欢,唐国盘,匡友谊. Cilp基因对斑马鱼肌间骨和脊椎发育的影响. 上海海洋大学学报. 2023(03): 460-471 .  百度学术
百度学术
5. 张婷婷,佟广香,孙志鹏,闫婷,唐国盘,周慧杰,匡友谊. eomesa功能缺失对斑马鱼雌鱼生殖的影响. 淡水渔业. 2023(05): 86-96 .  百度学术
百度学术
6. 董乐,佟广香,闫婷,杨笑星,孙志鹏,徐欢,唐国盘,匡友谊. 斑马鱼ngs基因突变对骨骼发育的影响. 基因组学与应用生物学. 2022(07): 1403-1415 .  百度学术
百度学术
7. 贺瑜,陈淑娟,何胜,伍贤龙,蒲丽宇,彭亮跃,肖亚梅. SP600125孵育影响鲫骨骼发育基因表达. 水生生物学报. 2021(01): 22-28 .  本站查看
本站查看
8. 王旭东,聂春红,高泽霞. 鱼类肌间骨发育分子调控机制及遗传选育研究进展. 水生生物学报. 2021(03): 680-691 .  本站查看
本站查看
9. Bo Li,Yuan-Wei Zhang,Xiao Liu,Li Ma,Jun-Xing Yang. Molecular mechanisms of intermuscular bone development in fish: a review. Zoological Research. 2021(03): 362-376 .  必应学术
必应学术
10. 鲁翠云,匡友谊,郑先虎,孙志鹏,孙效文. 转化生长因子-β(TGF-β)基因家族在水产养殖中的潜在应用价值. 水产学杂志. 2020(06): 89-96 .  百度学术
百度学术
其他类型引用(4)



 下载:
下载: