MORPHOLOGY AND MOLECULAR PHYLOGENETIC ANALYSIS OF FRESHWATER HILDENBRANDIA IN CHINA
-
摘要: 以云南省玉溪市和河南省焦作市新采集的2株淡水胭脂藻标本为材料, 对其进行形态特征观察和分子系统发育分析, 联合我国已报道的其他胭脂藻序列信息, 构建该属植物可靠的系统发育关系。根据其现代地理分布模式, 对胭脂藻属进行了祖先地理起源重建。基于rbcL、psbA和UPA序列, 利用贝叶斯法、最大似然法和邻接法构建的系统发育树高度一致, 研究中的标本与鸡公山胭脂藻H. jigongshanensis聚合为一个独立分支, 并得到了很高的支持率, 根据分子生物学证据, 将其鉴定为鸡公山胭脂藻。通过研究中所采集2株鸡公山胭脂藻的形态特征比较, 发现传统的形态分类特征包括藻体高度和细胞直径, 在不同的环境条件下是可变的, 不适合作为胭脂藻属植物种类鉴定的依据。对于胭脂藻属这一形态结构较为简单的类群, 必须借助分子生物学证据和系统发育分析手段对其进行种类鉴定和系统发育分析。分子系统发育分析结果表明, 中国特有种鸡公山胭脂藻H. jigongshanensis形成单系类群, 其与日本胭脂藻H. japananense亲缘关系较近, 所有淡水胭脂藻种类形成一个独立的聚类群, 与海洋种类遗传差异较大。祖先地理重建的分析结果表明, 淡水胭脂藻的祖先起源地位于北美洲, 然后逐渐向东加勒比海区域、拉丁美洲和欧亚大陆扩散, 形成现代地理分布模式。胭脂藻属独特的种类地理分布特点, 可能与其较为古老的起源时间和漫长的进化历史相关, 同时淡水胭脂藻在北美洲区域起源时间较早, 进化历史漫长, 遗传多样性大, 这与该地理区域分布的种类H. angolensis为多系类群是相一致的。Abstract: This study explored morphological observation and molecular phylogenetic analysis of two freshwater Hildenbrandia specimens from Yuxi, Yunnan Province (encoded as YZYUNNAN) and Jiaozuo, Henan Province (encoded as YZHENAN) in China. Morphological observation and molecular phylogenetic analysis were conducted on these specimens. Phylogenetic relationship of genus Hildenbrandia was constructed based on the obtained gene sequence and related molecular data previously reported in China. Ancestral geographical origin of freshwater Hildenbrandia was inferred based on reliable phylogenetic relationship and modern distribution pattern of each sample. The results are consistent using Bayesian Inference, Maximum Likelihood and Neighbor-joining based on rbcL, psbA and UPA sequences. The genetic distances of three molecular sequences between specimens collected and H. jigongshanensis were smaller compared with another freshwater species. The uncorrected p-distances of rbcL sequences between specimens and H. jigongshanensis were within intraspecific divergence of freshwater Hildenbrandia species. Phylogenetic trees showed that specimens YZYUNNAN and YZHENAN formed an independent branch with H. jigongshanensis, and obtained high supporting values. Specimens YZYUNNAN and YZHENAN shared close relationship with H. jigongshanensis based on molecular phylogeny. The morphological measurements of collected specimens were in consistent with another freshwater Hildenbrandia species H. rivularis. It has been acknowledged that the widely reported freshwater species H. angolensis and H. rivularis are distinguished by morphometric measurements, with H. angolensis characterized by smaller mean cell and filament dimensions (cells 4.0×4.4 µm, filaments 46.5 µm) and H. rivularis by larger parameters (cells 5.8×6.6 µm, filaments 55.3 µm). H. jigongshanensis is separated from other freshwater members by significantly larger cell dimensions (9.8—19.6)×(9.9—10.4) µm and filament height (364—409 µm). The morphological measurements of H. japananense, the cell size (8.4×10.5 μm) and filament height (308—491 μm) were overlapping with H. jigongshanensis whereas identified as a new species based on molecular sequences. with (5.0—8.0)×(4.0—6.7) μm and (4.8—8.0)×(4.8—6.4) μm in cellular diameter and 42—50 μm in thallus height, respectively. There exits contradiction in species identification based on traditional morphological taxonomy and modern molecular methods. By referring the criteria of species identification in other freshwater red algal taxa, the specimens YZYUNNAN and YZHENAN were determined to be H. jigongshanensis based on molecular evidences. The molecular phylogenetic study indicated H. jigongshanensis was firstly described from specimens collected from Jigongshan Mountain, Henan Province, China and follow reported in Niangziguan, Shanxi Province, China. It was found from Jiaozuo, Henan Province and Yunnan Province for the first time. This study expands the geographical distribution and genetic diversity of genus Hildenbrandia in China. Additionally, the traditional morphological characters including thallus height and cellular diameter were found variable under different environments and thus not reliable taxonomic criteria. Molecular-assisted species identification and phylogenetic analysis were necessary for genus Hildenbrandia due to its simple morphological structures. There are 4 widely accepted freshwater Hildenbrandia species up to now and H. rivularis proved monophyletic whereas H. angolensis was paraphyletic. Molecular phylogenetics in this study showed the monophyly of H. jigongshanensis and its close relationship with another freshwater species H. japananense. All freshwater Hildenbrandia species formed an independent clade from the marine species, suggesting that the freshwater Hildenbrandia was derived from the marine populations. The 4 freshwater species of Hildenbrandia were special in geographical distribution, with populations distributed in Europe were mainly H. rivularis, populations distributed in North America were mainly H. angolensis, and H. jigongshanensis and H. japananense were only reported from China and Japan respectively. Ancestral geographical origin reconstruction showed the freshwater Hildenbrandia was derived in North America and dispersed to Eastern Caribbean, Latin America and Eurasia. Sexual reproduction has not been documented for freshwater forms of Hildenbrandia and they reproduced only by asexual modes including fragmentation or gemmae, resulting in rare genetic exchange among species. It was speculated that the special species-related geographical pattern of genus Hildenbrandia was formed after dispersal events and independent evolution in each geographical area. The freshwater Hildenbrandia in North America derived ancestrally and had a long evolutionary history and rich genetic diversity, consistent with the paraphyly of the species H. angolensis distributed in this area.
-
Keywords:
- Freshwater Hildenbrandia /
- Morphology /
- rbcL /
- psbA /
- UPA /
- Molecular phylogenetics /
- Ancestral geographical origin
-
能量是重要的营养指标, 是确定营养素精准供给的基础。能量供给水平与动物的生产性能和品质有密切关系。一般来说, 动物摄取能量越多, 日增重越快, 胴体脂肪含量也越多[1]。然而, 在人类或其他哺乳动物中, 摄入过高能量会引起体脂肪异常沉积, 进一步导致胰岛素抵抗和脂代谢紊乱等具“代谢综合征”的症状[2, 3], 也会引发炎症反应[4], 造成免疫抑制[5], 甚至引起癌症等其他严重疾病[6]。
鱼类的高能量摄入通常受到饲料能量密度或(和)投喂水平的影响[7]。饲料能量密度取决于饲料中三大主要营养物质—蛋白质、脂肪和碳水化合物(平均总能分别为23.6、39.5和17.2 kJ/g) [8]的组成。近年来, 为节约蛋白质, 饲料中脂肪和可消化碳水化合物水平有增加的趋势, 导致饲料能量密度提高[9]; 而在养殖过程中, 为追求鱼类快速增加体重, 饲料投喂水平过高的现象时有发生, 这均意味着鱼类摄入高能量的可能性变大。与人或其他哺乳动物类似, 高能量摄入也会引起鱼体脂肪异常沉积[7], 并进一步造成鱼类免疫力降低[10]和抗氧化能力减弱[11]等影响。
然而, 研究发现, 在等能投喂时, 高脂饲料(脂肪水平达到最适生长需要量的2倍)导致鱼体脂肪沉积超过20%, 但并未发现石斑鱼(Epinephelus malabaricus)免疫指标受到显著的影响[12]; 而另一些研究表明, 在不等能投喂时, 伴随高脂[13, 14]和高糖[15]所引起的高能摄入会导致试验鱼的抗氧化能力降低、免疫力受损和抗病力下降等问题。这些结果似乎表明与能量密度相比, 摄入能量水平是影鱼类健康的主要原因。因此, 有必要厘清饲料能量密度和投喂水平对鱼类生长和健康的影响。
罗非鱼是一种全球性的重要淡水经济鱼类, 其产量居世界淡水鱼第二位[16], 也是我国重要的出口水产品, 自2005年以来, 其养殖产量均维持在100×107 kg以上, 位居世界第一[17]。在罗非鱼的养殖过程中, 经常会发现易受病害侵袭的鱼具有可能与高能量摄入相关的腹腔和肝脏等部位脂肪异常沉积的表征。因此, 本研究以国内主养罗非鱼品系-吉富罗非鱼(GIFT, Oreochromis niloticus)为研究对象, 通过控制饲料能量密度和投喂水平, 饲养吉富罗非鱼, 研究不同时期其生长性能、体成分、血液学指标和抗无乳链球菌(Streptococcus agalactiae)感染能力的变化, 探讨摄入饲料能量的密度和水平对罗非鱼生长和健康的影响, 为鱼类的科学投喂提供理论依据。
1. 材料与方法
1.1 试验饲料
以罗非鱼营养需要[18]为依据, 以酪蛋白、明胶、糊精和大豆油等为原料, 配制成蛋白质水平为35%、脂肪水平为6%和糖水平为30%的对照组饲料; 另以同样原料, 配制成蛋白质水平为35%、脂肪水平为10%和糖水平为48%的高糖高脂饲料(配方见表 1)。各原料粉碎过60目筛, 称重后混匀, 少量的组分(<5%)采用逐级扩大法混合, 用饲料机制成直径为2 mm, 长约3 mm 的圆柱形颗粒, 100—105℃干燥10min (带式干燥机, DW型, 常州苏正干燥设备有限公司), 恢复室温后置于–20℃冰柜中冷藏备用。
表 1 试验饲料配方和营养成分Table 1. Formulation and composition of the experimental diets (%)原料成分
Ingredient饲料Diet 对照Control 高糖高脂High carbohydrate-high lipid 酪蛋白Casein 31.00 31.00 明胶Gelatin 7.00 7.00 糊精Dextrin 32.00 42.00 微晶纤维素Microcrystalline cellulose 16.65 0.65 大豆油Soybean oil 3.00 6.00 玉米油Corn oil 3.00 6.00 维生素预混料Vitamin premix* 1.00 1.00 矿物质预混料Mineral premix* 1.00 1.00 磷酸二氢钙Monocalcium phosphate 2.00 2.00 氯化胆碱Choline chloride 0.25 0.25 牛磺酸Taurine 1.00 1.00 沸石粉Zeolite powder 1.90 1.90 二氧化钛Titanium dioxide 0.20 0.20 成分分析Proximate composition (dry matter, %) 粗蛋白Crude protein 34.29 34.69 粗脂肪Crude lipid 6.26 12.63 灰分Ash 4.61 4.64 总能Total energy (kJ/g) 21.94 23.92 可消化能Digestible energy (kJ/g) 17.26 20.76 注: *维生素预混料由下列成分组成(g/kg预混料): 硫胺素盐酸盐. 5; 核黄素. 5; 泛酸钙. 10; D-生物素. 0.003; 盐酸吡哆醇. 4; 叶酸. 1.5; 肌醇. 200; L-维生素C-2-磷酸镁. 3.95; 烟酸. 6.05; α-维生素E醋酸酯. 50; 维生素K3. 4; 视黄醇乙酸酯. 0.4; 维生素D3. 160000 IU; 添加微晶纤维素至1 kg; *矿物质预混料由下列成分组成(g/kg 预混料): 磷酸二氢钙. 135; 乳酸钙. 327; 硫酸亚铁. 2.125; 硫酸镁. 137; 磷酸二氢钠. 87.2; 氯化钠. 43.5; 氯化铝. 0.15; 碘酸钾. 0.125; 氯化钾. 75; 氯化铜. 0.1; 硫酸锰. 0.8; 氯化钴. l; 硫酸锌. 3; 添加微晶纤维素至1 kgNote: * Vitamin premix consists of the following ingredients (g/kg premix): thiamine hydrochloride. 5; riboflavin. 5; calcium pantothenate. 10; d-biotin. 0.003; pyridoxine hydrochloride. 4; folic acid. 1.5; inositol. 200; magnesium L-vitamin C-2-phosphate. 3.95; niacin. 6.05; vitamin E acetate. 50; vitamin K3. 4; retinol acetate. 0.4; vitamin D3. 160000 IU; add microcrystalline cellulose to 1 kg; *Mineral premix consists of the following ingredients (g/kg premix): calcium dihydrogen phosphate. 135; calcium lactate. 327; ferrous sulfate. 2.125; magnesium sulfate. 137; sodium dihydrogen phosphate. 87.2; sodium chloride. 43.5; aluminium chloride. 0.15; potassium iodate. 0.125; potassium chloride. 75; copper chloride. 0.1; manganese sulfate. 0.8; cobalt chloride. 1; zinc sulfate. 3; add microcrystalline cellulose to 1 kg 1.2 试验鱼
试验用鱼来源于湖北英山罗非鱼原良种场。运回后, 暂养在循环水养殖系统中。先用商品料喂养, 使试验鱼恢复体质并适应养殖环境。正式试验前用对照组饲料暂养2周, 使试验鱼适应试验饲料, 每天投喂1次。
1.3 试验饲料能量表观消化率的测定(预试验)
选择规格整齐, 表观健康的罗非鱼, 分养于6个养殖桶中(有效容积450 L), 随机分为2组, 每桶放鱼60尾, 试验鱼的平均体重(5.28±0.08) g, 分别投喂1.1中的2种试验饲料。每天表观饱食投喂3次(8:30、12:30和16:30), 并记录投喂量。养殖期间水温保持在(30±0.5)℃, 溶氧>5 mg/L, 氨氮<0.5 mg/L, pH为6.5—7.3, 亚硝酸盐<0.1 mg/L。试验期间所有养殖桶连续充气。光照为自然光。在喂养2周后, 开始收集粪便。结果发现, 试验鱼对对照饲料的能量表观消化率为78.67%, 对高糖高脂饲料的能量表观消化率为86.77%。
能量表观消化率的计算公式如下:
能量表观消化率(ADCe, %)=100×[1–(Nf/Nd)×(Md/Mf)]
式中, Md为饲料中标记物含量(%), Mf为粪便中标记物含量(%), Nd为饲料中营养成分的含量(%), Nf为粪便中营养成分的含量(%)。
1.4 试验设计和养殖管理
采用2×2双因子试验设计, 设置2种饲料能量密度和2种投喂水平。试验饲料采用上述1.1中配制的2种饲料。以投喂对照饲料, 15min表观饱食的量, 作为正常投喂水平, 设置高投喂水平的能量为正常投喂水平的1.2倍, 以1.3预试验中取得的2种饲料的能量表观消化率为参考系数, 得出每组的投喂量。高能量密度饲料投喂量计算公式如下:
投喂量(DFR, g)=a×m×(100–Mc)×ADCc/ADCh/(100–Mh)
式中, a为投喂水平的转换系数1或1.2, m为试验鱼15min表观饱食对照饲料量(g), Mc和Mh分别为对照组和高糖高脂饲料水分(%), ADCc和ADCh为对照饲料和高糖高脂饲料能量表观消化率(%)。
选取体质健壮、规格整齐的720尾试验鱼, 放入1套循环水养殖系统的12个桶(有效容积450 L)中, 每桶放鱼60尾, 初始体重为(14.59±0.06) g。分别以对照组饲料或高糖高脂饲料, 并按照2种投喂水平饲养, 共分为4组, 即投喂对照组饲料+正常投喂水平的C组, 投喂对照组饲料+高投喂水平的DC组, 投喂高糖高脂饲料+正常投喂水平的HCL组, 以及投喂高糖高脂饲料+高投喂水平的DHCL组。每组3个平行, 每天投喂3次, 高投喂水平组投喂时间延长至30min。其余同1.3预试验。
1.5 样品采集及检测方法
试验分为2个周期, 每个周期40d。在每个周期结束后, 所有试验鱼禁食24h, 麻醉(MS-222, 100 mg/L)后, 对每桶试验鱼进行记数和称体重, 用于计算成活率、增重率和特定生长率, 并根据总饲料投喂量计算饲料效率。每桶随机取鱼3尾, 测量体长和体重, 用于计算肥满度; 随后于尾静脉取血, 其中0.5 mL放于肝素钠抗凝管中, 用于测定血液生理学指标, 剩余的血液放入2 mL聚乙烯离心管中, 4℃冰箱内静置2h, 以3000 r/min 的转速离心15min, 得到空腹血清, 保存于–20℃冰箱中, 用于测定血清生化和抗氧化指标; 而后取内脏和肝脏并称重, 测量肠道长度, 用于计算肝体比、脏体比和肠体比; 最后取背肌(背鳍下方侧线以上), 用于测定常规成分。另取全鱼3尾, 取肝脏和内脏, 并保留肝脏、内脏团和去内脏全鱼, 用于测定常规成分。
原计划在周期Ⅰ取样后, 每桶随机留取试验鱼30尾, 用于周期Ⅱ的试验。但是, 在周期Ⅱ的养殖试验进行至2周时, 因操作失误导致试验鱼逃逸, 造成生长和饲料利用数据难以准确统计。因此, 计数并称重后, 根据称重数据, 每桶留取大小均匀的试验鱼17尾, 并重新以此时为周期Ⅱ的开始。
采用直接干燥法测定水分含量(GB/T 5009.3-2003)、凯氏定氮法测定粗蛋白质含量(GB/T 5009.5-2003)、索氏抽提法测定粗脂肪含量(GB/T 5009.6-2003)和灼烧称重法测定灰分含量(GB/T 5009.4-2003)。能量的测定使用量热仪(SDACM4000, 湖南三德科技股份有限公司)测定。饲料和粪便中二氧化钛的测定参照Richter等[19]。血液中的红细胞和白细胞数量采用细胞计数板法, 血红蛋白采用沙利氏比色法测定, 血细胞比容采用离心法测定(2000×g, 10min), 血清生化指标全自动生化分析仪(CHEMIX-800, 日本希森美康株式会社)测定。血清抗氧化指标采用商用试剂盒测定, 购自南京建成生物工程研究所, 按照其提供的方法检测。其余各指标的计算公式如下:
增重率(WGR, %)=(Wf–Wi)/Wi×100
特定生长率(SGR, %/d)=(lnWf–lnWi)/t×100
饲料效率(FE)=(WF–WI+Wd)/WA
成活率(SR, %)=NF/NI×100
肥满度(CF, g/cm3)=W/L3×100
肝体比(HSI)=Wh/W×100
脏体比(VSI)=Wv/W×100
肠体比(ISI)=Li/L×100
蛋白质沉积率(PRE, %)=[Wa×Wp–(WF–WI+Wd)×Fp]×100/(Wa×Wp)
式中, t为每个周期的天数(d), Wf和Wi分别为每周期试验鱼的初、末均体重(g), WF、WI和Wd分别为每周期试验鱼的初、末总体重和死亡鱼体重(g), W为鱼体重(g), L为鱼体长(cm), NF和NI分别为每周期结束后和开始时鱼的尾数; Wh、Wv和Li分别为肝脏重(g)、内脏团重(g)和肠道长度(cm), Wa、WP和FP分别为投喂饲料总重(g)、 饲料粗蛋白含量(%)和全鱼粗蛋白含量(%)。
1.6 攻毒试验
养殖周期Ⅰ和周期Ⅱ结束后, 每桶取鱼10尾, 进行无乳链球菌(S. agalactiae)攻毒试验。根据之前试验[20], 从腹鳍基部按照每尾0.1 mL (1.0×108 cfu/mL) 注射病菌稀释液。注射24h后开始记录死亡数, 共计7d。攻毒期间, 记录死亡鱼的病症, 并取刚死亡鱼的肝脏, 进行划线培养, 进一步确定是否为注射菌造成的死亡。攻毒期间不投喂。
1.7 数据处理
所有数据采用平均值±标准误表示。用SPSS 22.0软件对试验数据进行统计分析。用Levene方法进行方差齐性检验, 当方差不齐时, 进行反正弦或对数(lg)转换。对饲料能量密度和投喂水平进行双因素方差分析(Two-way ANOVA), 检验2个因子间的相互作用。当主因素或相互作用显著时, 用单因素方差分析(One-way ANOVA) 中S-N-K法检验各试验组间的差异。所有分析取P<0.05为差异显著。
2. 结果
2.1 生长性能和饲料利用
由表 2可见, 在养殖周期Ⅰ和周期Ⅱ结束后, 试验鱼的成活率均高于95%, 并未受到饲料能量密度和投喂水平的影响(P>0.05)。双因素方差分析发现, 饲料能量密度和投喂水平对试验鱼的生长性能和饲料利用无显著交互作用(P>0.05); 在试验期内, 未发现饲料能量密度影响试验鱼的生长性能和饲料利用效率(P>0.05), 但饲料投喂水平显著影响试验鱼的末体重(P<0.05)。S-N-K法检验发现, 在周期Ⅰ, 摄入同一饲料能量密度, 高投喂水平显著提高了试验鱼的末体重、增重率和特定生长率(P<0.05); 在周期Ⅱ, DC组的蛋白质沉积率显著低于C组(P<0.05)。
表 2 饲料能量密度和投喂水平对试验鱼生长和饲料利用效率的影响Table 2. Effects of dietary energy density and feed ration on grow performance and feed utilization of GIFT (n=3)指标Index 组别Group 双因素方差分析Two way ANOVA C DC HCL DHCL 能量密度
Energy
density投喂量
Feed
ration交互作用
Interaction周期Ⅰ
Period Ⅰ初始平均体重Wi (g) 14.77±0.05 14.51±0.14 14.66±0.09 14.43±0.07 末平均体重Wf (g) 40.84±1.20a 46.39±0.99b 40.64±1.94a 47.82±1.19b 0.597 0.000 0.490 成活率SR (%) 98.99±1.11 96.67±3.33 96.11±0.56 95.56±1.11 0.327 0.477 0.667 特定生长率SGR (%/d) 3.39±0.10a 3.87±0.10b 3.40±0.11a 3.99±0.08b 0.533 0.001 0.595 增重率WGR (%) 176.56±8.22a 219.98±9.38b 177.43±9.36a 231.49±8.05b 0.500 0.001 0.561 饲料效率FE 1.02±0.03 1.01±0.05 1.02±0.06 1.08±0.05 0.529 0.594 0.436 蛋白质沉积率PRE (%) 49.49±1.16 49.27±3.04 49.80±3.21 51.53±1.42 0.605 0.760 0.695 周期Ⅱ
Period Ⅱ初始平均体重Wi (g) 62.41±0.73a 73.25±0.51b 62.57±0.62a 73.29±1.43b 0.916 0.000 0.949 末平均体重Wf (g) 121.10±1.82a 141.68±2.19b 121.12±3.37a 135.21±2.12b 0.224 0.000 0.221 成活率SR (%) 100 100 100 100 特定生长率SGR (%) 1.66±0.02 1.65±0.04 1.65±0.08 1.53±0.09 0.971 0.479 0.893 增重率WGR (%) 84.95±5.36 90.88±6.16 93.39±6.77 104.46±6.49 0.372 0.364 0.427 饲料效率FE 0.80±0.02 0.78±0.03 0.81±0.05 0.77±0.04 0.397 0.372 0.433 蛋白质沉积率PRE (%) 35.97±3.04b 27.78±0.38a 34.79±1.03ab 31.87±1.74ab 0.523 0.034 0.261 注: 表格中同行平均数上标不同表示差异显著(P<0.05); 下同Note: The mean values in the same row with different letters are significantly different (P<0.05). The same applies below 2.2 形体指标
由表 3可见, 双因素方差分析发现, 在试验期内, 肥满度未受饲料能量密度或投喂水平的影响(P>0.05)。在周期Ⅰ, 仅高能量密度饲料提高了试验鱼的脏体比(P<0.05); 可是, 在周期Ⅱ, 试验鱼的肠体比、脏体比同时受到饲料能量密度和投喂水平的影响(P<0.05), 而试验鱼的肝体比受到投喂水平的影响(P<0.05)。S-N-K法检验发现, 在周期Ⅰ, DHCL组的脏体比显著高于C和DC组(P<0.05), 但与HCL组的差异不显著(P>0.05); 在周期Ⅱ, DC组试验鱼的肠体比最高, 显著高于C组和HCL组(P<0.05); DHCL组的脏体比和肝体比最高, 且均显著高于C组和HCL组(P<0.05)。
表 3 饲料能量密度和投喂水平对试验鱼形体指标的影响Table 3. Effects of dietary energy density and feed ration on physical parameters of GIFT (n=3)指标Index 组别Group 双因素方差分析Two way ANOVA C DC HCL DHCL 能量密度
Energy density投喂水平
Feed ration交互作用
Interaction周期Ⅰ
Period Ⅰ肠体比ISI 7.41±0.31 8.40±0.47 7.54±0.29 7.69±0.40 0.461 0.165 0.299 肥满度CF (g/cm3) 3.43±0.01 3.51±0.05 3.58±0.08 3.58±0.08 0.105 0.520 0.530 脏体比VSI 9.49±0.40a 9.66±0.16a 10.14±0.19ab 10.89±0.08b 0.004 0.092 0.258 肝体比HSI 1.94±0.21 1.84±0.03 1.84±0.25 1.86±0.03 0.815 0.801 0.711 周期Ⅱ
Period Ⅱ肠体比ISI 7.89±0.26a 9.60±0.21b 7.91±0.43a 8.20±0.27ab 0.038 0.029 0.100 肥满度CF (g/cm3) 4.34±0.11 4.30±0.25 4.44±0.13 4.38±0.13 0.937 0.752 0.964 脏体比VSI 10.33±0.19a 13.68±0.14c 12.05±0.35b 15.08±0.26d 0.000 0.000 0.543 肝体比HSI 1.80±0.18a 3.69±0.09b 2.46±0.30a 3.95±0.37b 0.112 0.000 0.471 2.3 体成分
在周期Ⅰ(表 4), 双因素方差分析发现, 饲料能量密度和投喂水平并未对去内脏全鱼、肝脏、内脏团和肌肉的常规营养成分产生显著的交互作用(P>0.05)。可是, 高能量密度饲料不仅引起去内脏全鱼、内脏团粗脂肪水平的显著升高(P<0.05), 水分含量的显著降低(P<0.05), 而且也引起了去内脏全鱼粗灰分和肝脏的水分含量的显著减少(P<0.05); 而高投喂水平仅造成肝脏脂肪水平升高(P<0.05)。S-N-K法检验发现, 在去内脏全鱼的成分中, HCL与DHCL组的水分显著低于其他2组(P<0.05), 粗脂肪含量则相反; DHCL组的灰分含量显著低于DC组的(P<0.05)。在内脏团的成分中, 仅发现HCL与DHCL组的粗脂肪含量显著高于其他2组(P<0.05)。
表 4 饲料能量密度和投喂水平对周期Ⅰ试验鱼体成分的影响 (n=3, %湿重)Table 4. Effects of dietary energy density and feed ration on body composition of GIFT in period Ⅰ (n=3, % wet weight)指标Index 组别Group 双因素方差分析Two way ANOVA C DC HCL DHCL 能量密度
Energy density投喂量
Feed ration交互作用
Interaction去内脏全鱼
The eviscerated whole fish水分Moisture 72.36±0.19b 72.12±0.50b 70.06±0.28a 70.33±0.22a 0.000 0.963 0.438 粗脂肪Crude lipid 6.62±0.35a 6.44±0.54a 8.43±0.32b 8.66±0.10b 0.001 0.956 0.583 粗蛋白Crude protein 16.24±0.14 16.40±0.15 16.56±0.25 16.35±0.38 0.596 0.932 0.476 灰分Ash 4.35±0.11ab 4.53±0.17b 4.14±0.11ab 3.98±0.07a 0.014 0.907 0.199 肝脏Liver 水分Moisture 68.70±0.70 68.61±0.53 66.79±0.58 65.82±0.78 0.009 0.459 0.531 粗脂肪Crude lipid 9.98±0.91 13.74±0.07 11.94±0.37 13.47±1.40 0.351 0.015 0.229 粗蛋白Crude protein 12.93±0.47 12.76±0.70 11.78±0.83 12.13±0.36 0.191 0.886 0.684 内脏团
Visceral
mass*水分Moisture 74.26±1.88 74.17±2.71 68.07±2.54 66.05±2.41 0.018 0.673 0.700 粗脂肪Crude lipid 8.87±0.06a 9.08±0.50a 17.82±1.57b 19.84±1.88b 0.000 0.398 0.493 粗蛋白Crude protein 8.36±0.17 8.28±0.35 8.08±0.21 8.56±0.30 0.999 0.471 0.320 肌肉Muscle 水分Moisture 77.66±0.31 77.09±0.45 77.05±0.32 76.69±0.59 0.277 0.322 0.814 粗脂肪Crude lipid 0.94±0.10 1.06±0.31 1.13±0.11 1.19±0.18 0.501 0.597 0.818 粗蛋白Crude protein 17.48±0.20 17.72±0.21 18.20±0.69 18.44±0.51 0.154 0.620 0.999 注: *内脏团不包含肝脏; 下同Note: *Visceral masses do not contain the liver. The same applied below 在周期Ⅱ(表 5), 双因素方差分析发现, 饲料能量密度和投喂水平对肝脏粗脂肪含量有显著的交互作用(P<0.05); 高能量密度饲料摄入引起去内脏全鱼、内脏团的水分含量降低(P<0.05), 导致去内脏全鱼、肝脏和肌肉的粗脂肪含量升高(P<0.05), 但也提高了肌肉的粗蛋白含量(P<0.05); 而高投喂水平引起了去内脏全鱼的水分含量下降(P<0.05), 去内脏全鱼、肝脏、内脏团和肌肉的粗脂肪含量升高(P<0.05)。S-N-K法检验发现, 在去内脏全鱼中, C组的水分含量显著高于其他组(P<0.05), 而DHCL组的水分含量显著低于其他组(P<0.05), 摄食高糖高脂饲料的2组粗脂肪含量显著高于摄食对照组的(P<0.05); 在肝脏中, DHCL组粗脂肪含量显著高于其他3组(P<0.05); 在内脏团中, 摄食高糖高脂饲料的2组水分含量显著低于摄食对照组的(P<0.05), DC组和DHCL组的粗脂肪含量显著高于其他2组(P<0.05); 在肌肉中, C组的粗脂肪含量显著低于其他组(P<0.05), HCL组和DHCL组的粗蛋白含量显著高于其他2组(P<0.05)。
表 5 饲料能量密度和投喂水平对周期Ⅱ试验鱼体成分的影响 (n=3, %湿重)Table 5. Effects of dietary energy density and feed ration on body composition of GIFT in period Ⅱ (n=3, % wet weight)指标Index 组别Group 双因素方差分析Two way ANOVA C DC HCL DHCL 能量密度
Energy density投喂量
Feed ration交互作用
Interaction去内脏全鱼
The
eviscerated
whole fish水分Moisture 69.04±0.20c 67.69±0.55b 67.96±0.09b 66.13±0.19a 0.003 0.001 0.469 粗脂肪Crude lipid 8.64±0.16a 9.99±0.18a 11.49±0.24b 12.00±0.40b 0.000 0.008 0.148 粗蛋白Crude protein 17.55±0.35 16.69±0.58 16.77±0.21 16.72±0.46 0.461 0.314 0.366 灰分Ash 4.57±0.09 4.31±0.01 4.63±0.09 4.58±0.21 0.317 0.244 0.411 肝脏Liver 水分Moisture 69.36±2.92 67.47±0.70 64.78±0.02 65.02±1.26 0.228 0.626 0.531 粗脂肪Crude lipid 13.97±0.27a 15.11±0.26a 14.93±0.57a 18.51±0.13b 0.000 0.000 0.008 粗蛋白Crude protein 14.84±0.68 13.94±0.89 13.26±0.78 11.78±0.70 0.107 0.159 0.717 内脏团
Visceral
mass*水分Moisture 65.75±4.43a 67.54±2.54a 47.04±3.12b 43.36±2.87b 0.001 0.783 0.434 粗脂肪Crude lipid 19.05±0.64a 25.11±1.55b 20.36±0.17a 27.64±1.24b 0.131 0.000 0.606 粗蛋白Crude protein 6.99±0.43 6.26±0.23 5.32±0.38 5.78±0.45 0.071 0.730 0.157 肌肉Muscle 水分Moisture 77.38±0.37 77.13±0.27 76.87±0.27 76.20±0.15 0.077 0.139 0.468 粗脂肪Crude lipid 0.77±0.18a 1.63±0.15b 1.40±0.07b 1.82±0.07b 0.013 0.001 0.126 粗蛋白Crude protein 18.46±0.35a 18.21±0.05a 19.73±0.37b 20.66±0.40b 0.002 0.327 0.106 2.4 血液学指标
由表 6可见, 在试验鱼的血液生理指标中, 双因素方差分析发现, 饲料能量密度和投喂水平仅对周期Ⅱ试验鱼的白细胞计数(WBC)有显著的交互作用(P<0.05); 饲料能量密度或投喂水平对周期Ⅰ试验鱼的血细胞比容(HCT)和试验周期Ⅱ的WBC有显著的影响(P<0.05)。S-N-K法检验仅发现, 周期Ⅱ DHCL组的WBC显著低于其他3组(P<0.05)。
表 6 饲料能量密度和投喂水平对试验鱼血液生理指标的影响Table 6. Effects of dietary energy density and feed ration on blood physiological indices of GIFT (n=3)指标Index 组别Group 双因素方差分析Two way ANOVA C DC HCL DHCL 能量密度
Energy density投喂量
Feed ration交互作用
Interaction周期Ⅰ
Period Ⅰ血红蛋白HB (g/L) 187.33±18.67 236.67±5.46 231.33±8.11 230.67±3.71 0.114 0.209 0.558 红细胞数RBC (×1012) 14.00±3.94 15.112±1.67 19.05±2.82 14.82±1.56 0.401 0.129 0.627 白细胞数WBC (×1010) 23.50±2.02 14.33±1.45 22.50±3.33 19.33±12.11 0.763 0.426 0.189 血细胞比容HCT (%) 37.56±0.49 39.89±0.98 46.02±2.33 47.22±3.50 0.007 0.012 0.058 周期Ⅱ
Period Ⅱ血红蛋白HB (g/L) 179.67±13.72 188.33±13.86 182.67±5.46 180.33±2.03 0.927 0.764 0.604 红细胞数RBC (×1012) 14.38±1.23 11.27±3.50 11.43±0.80 17.35±1.85 0.215 0.526 0.065 白细胞数WBC (×1010) 51.00±4.36b 42.67±5.83b 49.00±0.76b 16.50±1.76a 0.006 0.001 0.012 血细胞比容HCT (%) 38.26±2.51 32.16±0.38 38.09±4.44 31.12±1.30 0.374 0.217 0.361 由表 7可见, 周期Ⅰ试验鱼的血清生化指标中, 双因素方差分析发现, 饲料能量密度和投喂水平对乳酸脱氢酶(LD)有显著的交互作用(P<0.05)。高能量密度饲料摄入造成试验鱼的血清碱性磷酸酶(ALP)和乳酸脱氢酶(LD)活性, 及甘油三酯(TGK)含量升高(P<0.05); 而高投喂水平造成LD活性、TGK和血糖(GLU)含量升高(P<0.05)。S-N-K法检验发现, C组血清的LD显著低于其他3组(P<0.05), DHCL组血清的TGK含量与DC组的差异不显著(P>0.05), 但显著高于其他2组(P<0.05)。
表 7 饲料能量密度和投喂水平对周期Ⅰ试验鱼血液生化指标的影响Table 7. Effects of dietary energy density and feed ration on blood biochemical indices of GIFT in period Ⅰ (n=3)指标Index 组别Group 双因素方差分析Two way ANOVA C DC HCL DHCL 能量密度
Energy density投喂量
Feed ration交互作用
Interaction谷草转氨酶AST (U/L) 170.33±5.55 161.33±2.33 171.00±10.79 179.33±6.06 0.212 0.963 0.243 谷丙转氨酶ALT (U/L) 54.67±4.10 54.00±4.36 57.00±4.36 58.67±3.92 0.428 0.908 0.788 碱性磷酸酶ALP (U/L) 30.33±1.45 34.00±1.53 42.00±3.51 41.67±3.84 0.009 0.569 0.497 乳酸脱氢酶LD (U/L) 7.00±1.53a 14.67±1.33b 17.33±0.33b 17.00±1.00b 0.001 0.012 0.008 甘油三酯TGK (mmol/L) 4.03±0.24a 5.44±0.35bc 4.82±0.08b 5.77±0.10c 0.036 0.001 0.330 胆固醇TCHO (mmol/L) 4.62±0.24 5.17±0.34 4.92±0.32 5.55±0.03 0.238 0.056 0.889 高密度脂蛋白胆固醇HDLC (mmol/L) 1.33±0.09 1.40±0.09 1.43±0.18 1.55±0.05 0.306 0.403 0.850 低密度脂蛋白胆固醇LDLC (mmol/L) 0.58±0.06 1.16±0.37 0.91±0.09 1.15±0.07 0.431 0.068 0.414 白蛋白ALB (g/L) 10.33±0.33 10.33±0.33 10.00±0.58 11.00±0.58 0.733 0.209 0.558 总蛋白TP (g/L) 40.33±1.20 41.67±0.33 38.00±3.21 39.50±1.23 0.291 0.129 0.627 尿素氮BUN (mmol/L) 0.56±0.04 0.68±0.04 0.69±0.07 0.53±0.07 0.887 0.426 0.189 血糖GLU (mmol/L) 7.84±0.87 8.11±0.49 7.44±0.78 8.57±0.22 0.968 0.012 0.058 由表 8可见, 周期Ⅱ试验鱼的血清生化指标中, 经双因素方差分析发现, 饲料能量密度和投喂水平对试验鱼血清的LD活性和白蛋白(ALB)含量有显著的交互作用(P<0.05); 高能量密度饲料摄入造成试验鱼的血清ALP和LD活性, TGK、胆固醇(TCHO)、ALB和GLU含量升高(P<0.05); 高饲料投喂水平造成LD活性, TGK含量升高(P<0.05)。S-N-K法检验发现, C组的血清LD活性显著低于其他组(P<0.05), 而DHCL组的血清TGK含量显著高于其他组(P<0.05); C组和DC组的血清TCHO含量显著低于HCL和DHCL组(P<0.05); DC组的血清ALB含量最低, 显著低于C和DHCL组(P<0.05); 而DHCL组GLU含量最高, 显著高于C组和DC组(P<0.05)。
表 8 饲料能量密度和投喂水平对周期Ⅱ试验鱼血清生化指标的影响Table 8. Effects of dietary energy density and feed ration on serum biochemical indices of GIFT in period Ⅱ (n=3)指标Index 组别Group 双因素方差分析Two way ANOVA C DC HCL DHCL 能量密度
Energy density投喂量
Feed ration交互作用
Interaction谷草转氨酶AST (U/L) 76.67±11.62 102.67±4.67 94.00±5.03 93.33±2.40 0.132 0.102 0.088 谷丙转氨酶ALT (U/L) 59.33±6.96 51.00±5.20 42.67±5.21 44.00±5.77 0.239 0.565 0.431 碱性磷酸酶ALP (U/L) 26.67±3.71 27.33±2.40 36.00±6.00 43.33±1.33 0.043 0.322 0.404 乳酸脱氢酶LD (U/L) 212.00±14.47a 452.00±26.86b 428.00±41.00b 455.33±26.39b 0.001 0.002 0.006 甘油三酯TGK (mmol/L) 2.91±0.49a 4.65±0.22b 5.49±0.39b 6.76±0.04c 0.000 0.002 0.498 胆固醇TCHO (mmol/L) 5.03±0.20a 5.50±0.23a 8.12±1.01b 7.73±0.62b 0.016 0.950 0.500 高密度脂蛋白胆固醇HDLC (mmol/L) 2.71±0.19 2.39±0.17 2.32±0.17 2.58±0.17 0.429 0.855 0.136 低密度脂蛋白胆固醇LDLC (mmol/L) 2.60±0.18 2.86±0.24 3.37±0.25 3.67±0.28 0.052 0.276 0.926 白蛋白ALB (g/L) 12.67±0.67b 10.00±0.00a 11.33±0.67ab 12.67±0.67b 0.032 0.282 0.009 总蛋白TP (g/L) 54.67±2.40 52.00±6.43 56.67±3.71 63.33±1.33 0.288 0.627 0.272 尿素氮BUN (mmol/L) 1.76±0.17 1.47±0.14 2.03±0.17 1.78±0.08 0.125 0.094 0.890 血糖GLU (mmol/L) 4.15±0.50a 4.38±0.09a 5.95±0.41ab 6.91±0.63b 0.008 0.225 0.445 由表 9可见, 在试验鱼的血清抗氧化指标中, 双因素方差分析发现, 饲料能量密度和投喂水平对周期Ⅰ试验鱼的血清超氧化物歧化酶(SOD)活性, 及周期Ⅱ的血清谷胱甘肽过氧化物酶(GSH-Px)活性和总抗氧化能力(TAOC)有显著的交互作用(P<0.05); 高能量密度饲料摄入造成周期Ⅰ试验鱼的血清过氧化氢酶(CAT)和GSH-Px活性降低(P<0.05), 周期Ⅱ的血清丙二醛(MDA)含量升高(P<0.05); 高饲料投喂水平造成周期Ⅱ的血清MDA含量升高(P<0.05)。S-N-K法检验发现, 在试验周期Ⅰ, C组和DC组的CAT活性显著高于HCL和DHCL组的(P<0.05), 而C组的GSH-Px活性显著高于其他3组(P<0.05); 在周期Ⅱ, C组血清的MDA含量显著低于其他3组(P<0.05)。
表 9 饲料能量密度和投喂水平对试验鱼血清抗氧化指标的影响Table 9. Effects of dietary energy density and feed ration on serum antioxidant indices of GIFT (n=3)指标Index 组别 Group 双因素方差分析Two way ANOVA C DC HCL DHCL 能量密度
Energy density投喂量
Feed ration交互作用
Interaction周期Ⅰ
Period ⅠSOD (U/mL) 47.93±0.95 51.81±7.92 44.91±4.75 55.08±4.41 0.981 0.053 0.048 CAT (U/mL) 148.43±22.48b 156.87±6.48b 84.01±5.49a 51.91±14.78a 0.000 0.364 0.652 GSH-Px (U/mL) 6.95±0.87b 3.27±0.65a 3.45±0.68a 2.76±0.43a 0.018 0.440 0.802 周期Ⅱ
Period ⅡSOD (U/mL) 47.38±5.14 41.43±1.36 46.32±5.86 43.76±4.51 0.795 0.377 0.720 GSH-Px (U/mL) 18.89±4.60 11.91±0.83 15.62±0.49 26.32±4.33 0.065 0.608 0.026 CAT (U/mL) 22.76±1.49 20.83±2.47 26.12±3.53 18.86±2.61 0.315 0.118 0.339 TAOC (U/mL) 6.49±0.84 3.51±0.54 3.99±0.73 4.80±0.68 0.073 0.163 0.028 MDA (nmol/mL) 9.37±1.24a 18.19±1.28b 14.94±1.00b 18.66±1.59b 0.003 0.001 0.084 注: SOD. 超氧化物歧化酶; CAT. 过氧化氢酶; GSH-Px. 谷胱甘肽过氧化物酶; TAOC. 总抗氧化能力; MDA. 丙二醛; 表格中同行平均数上标不同表示差异显著(P<0.05)Note: SOD. superoxide dismutase; CAT. catalase; GSH-Px. glutathione peroxidase; TAOC. Total antioxidant capacity; MDA. malondialdehyde. The mean values in the same row with different letters are significantly different (P<0.05) 2.5 攻毒成活率
由图 1可见, 在周期Ⅰ结束后, 对试验鱼攻毒后未发现各组间的成活率有显著差异(P>0.05), 且在攻毒5d以后发现鱼的活力较好, 未再发现死亡; 但是在周期Ⅱ结束后, 攻毒第5天表现差异(P<0.05), 且DC和DHCL组试验鱼的成活率显著低于C和HCL组的(P<0.05), 但也在5d以后发现鱼的活力较好, 亦未再发现死亡。
![]() 图 1 无乳链球菌攻毒中试验鱼的累计成活率A. 周期Ⅰ结束后攻毒结果; B. 周期Ⅱ结束后攻毒结果; 同一时间点具不同小写字母表示差异显著(P<0.05)Figure 1. Cumulative survival percentage of GIFT challenged by S. agalactiaeA. challenge results after period Ⅰ; B. challenge results after period Ⅱ. Different lowercase letters at the same time point indicate significant differences (P<0.05)
图 1 无乳链球菌攻毒中试验鱼的累计成活率A. 周期Ⅰ结束后攻毒结果; B. 周期Ⅱ结束后攻毒结果; 同一时间点具不同小写字母表示差异显著(P<0.05)Figure 1. Cumulative survival percentage of GIFT challenged by S. agalactiaeA. challenge results after period Ⅰ; B. challenge results after period Ⅱ. Different lowercase letters at the same time point indicate significant differences (P<0.05)3. 讨论
3.1 饲料能量密度和投喂水平对吉富罗非鱼生长性能和饲料利用的影响
本试验结果发现, 等能摄入不同能量密度的饲料未影响试验鱼的生长, 但高投喂水平提高了试验鱼的体重生长速度(表 2), 表明罗非鱼的生长与能量摄入正相关[21, 22], 这与高投喂水平增加了可利用代谢能[10], 进而会增加试验鱼的体重有关。在本试验的周期Ⅰ, 未发现饲料效率和蛋白质沉积率受到影响, 而发现周期Ⅱ的饲料效率和蛋白质沉积率均小于周期Ⅰ, 且高投喂水平造成蛋白质沉积率降低, 尤其是在投喂对照组饲料的2组间。这可能与试验鱼的规格变化有关, 因为鱼体越大用以维持自身的能量越多[8], 而且大规格鱼的适宜投喂率有所降低, 导致高水平投喂的营养物质有所浪费[23]。
高糖[9]和高脂[24]饲料更易造成动物体内脏脂肪沉积过多, 导致脏体比和肝体比升高[25]。这在本试验中有所表现, 根据形体指标的变化(表 3), 在周期Ⅰ, 仅发现高能量密度饲料导致了试验鱼的脏体比升高, 结合周期Ⅰ试验鱼的内脏成分可以看出(表 4), 这确实是脂肪积累的结果; 但肝体比未发生显著变化, 且肝脏粗脂肪含量也无差异(表 4), 这表明肝脏合成转运脂肪的功能未受到影响, 使得脂肪优先沉积于内脏[26]。在本试验中, 随着养殖时间的延长, 在周期Ⅱ结束后, 除肥满度无显著差异外, 肠体比、脏体比和肝体比均出现了显著差异, 结合周期Ⅱ试验鱼的体成分(表 5)可以看出, 脏体比和肝体比的升高是脂肪沉积的结果。然而, 一方面, 沉积在内脏的脂肪因不可食性, 造成能量浪费; 另一方面, 过多的脂肪沉积可能对鱼类的健康产生负面影响, 如对小鼠等实验动物的研究发现, 脂肪组织会分泌炎症因子, 引起代谢性疾病及其并发症的风险加大[27]。而在试验周期Ⅱ结束后, 低能量密度饲料或高投喂水平引起肠体比升高, 这应该是肠道的适应性变化, 肠道长度增加可延长营养物质在消化道中的时间, 以提高饲料利用率[28]。
3.2 饲料能量密度和投喂水平对吉富罗非鱼血液生理生化指标的影响
养殖鱼类的血液学特征可以表明其生理和健康状况[29]。在本试验期间, 发现饲料能量密度和投喂水平引起了部分指标出现显著的差异。在血液生理指标中, 发现高能量密度饲料显著升高了周期Ⅰ的HCT, 因红细胞参数(HCT、RBC和HB)是“代谢综合征(MS)”的独立危险因素, 与MS间存在正相关性[30], 这表明试验鱼的健康受到负面影响。可在周期Ⅱ, 各组间未发现红细胞参数出现显著差异, 这是否与试验鱼的适应性有关, 需要进一步研究; 但是, 机体中具免疫防卫作用的白细胞[31], 其数量在DHCL组显著降低, 则说明此处理试验鱼的免疫机能受到抑制。
在血清生化指标中, 表示肝脏健康状态的敏感指标转氨酶(AST和ALT)[32]活性未发生显著差异, 表明肝脏的健康状况尚未发生较大的改变; 而在周期Ⅱ, 高能量密度饲料或高投喂水平提高了与鱼体营养状况呈正相关的ALB、TGK或GLU水平, 表明鱼体蛋白质、脂肪和碳水化合物的代谢增强[33]。LD的主要作用是催化丙酮酸和乳酸间的相互转化, 丙酮酸进入线粒体, 氧化脱羧形成乙酰辅酶a(CoA)[34], 高LD活性意味着CoA合成量增加, 而CoA是脂肪合成的起始[34]。在2个周期的试验结束后, 均发现C组的LD和TGK显著低于其他组, 同时结合鱼体成分来看, 这应该与脂肪合成代谢有关。
高能量密度饲料或高水平投喂, 会增加机体能量代谢负担[35]。能量代谢过程中的副产物活性氧(ROS), 若产生过多会破坏细胞内的蛋白质、脂肪和核酸结构, 对细胞有害[36]。SOD、CAT和GSHPx是抗氧化初级防御系统, 可清除ROS[37]。在本试验中, 仅发现高能量密度饲料导致了周期Ⅰ试验鱼血清的CAT和GSHPx活性的降低, 减弱了试验鱼的抗氧化能力; 而在周期Ⅱ, 这3种抗氧化酶的活性并无显著差异, 这可能与其适应能力有关[38]。但在周期Ⅱ试验鱼的血清中, 发现高能量密度饲料或高投喂水平导致脂质过氧化的典型指标MDA[39]含量显著升高, 而MDA可导致细胞膜脂质过氧化促使细胞损伤[40]。
3.3 饲料能量密度和投喂水平对吉富罗非鱼攻毒成活率的影响
在本试验中, 周期Ⅰ结束后的攻毒并未影响试验鱼成活率, 这可能与试验期较短有关。因动物本身的调节能力[41], 试验鱼抵抗有害菌感染的能力尚未出现显著的差异, 类似的研究结果在杂交条纹鲈(Morone saxatilis ♂×M. chrysops ♀)[42]也有所表现。但周期Ⅱ结束后的攻毒发现, 在2种饲料能量密度下, 均是高投喂水平组的成活率显著下降, 这应该与高能量摄入降低了鱼类的免疫力有关[10]。
综上所述, 在本试验条件下, 高投喂水平可提高罗非鱼的生长速度, 但是会增加鱼体的脂肪沉积, 降低对病菌的抵抗力, 对鱼体健康产生负面影响; 而高能量密度饲料更易于鱼体脂肪沉积, 减弱抗氧化能力, 不利于鱼体健康。
-
图 1 采自河南焦作市的胭脂藻标本(YZHENAN)形态显微照片
a. 多层细胞藻体; b. 藻体横切面; c. 藻体多层细胞整齐排列; d. 藻体单层细胞纵切面
Figure 1. Morphological structures of specimen collected from Jiaozuo City, Henan Province, China (YZHENAN)
a. thallus of multiple cell layers; b. transection surface of thallus; c. cells of multiple layers arranged in order; d. cross section of cells in single layer
图 2 采自云南玉溪的胭脂藻标本(YZYUNNAN)形态显微照片
a. 藻体横切面; b-c. 多列细胞纵向排列; d. 细胞片状色素体周生
Figure 2. Morphological structures of specimen collected from Yuxi City, Yunnan Province, China (YZYUNNAN)
a. transection surface of thallus; b-c. multiserial cells arranged in vertical; d. a single chromoplast is parietal in cell
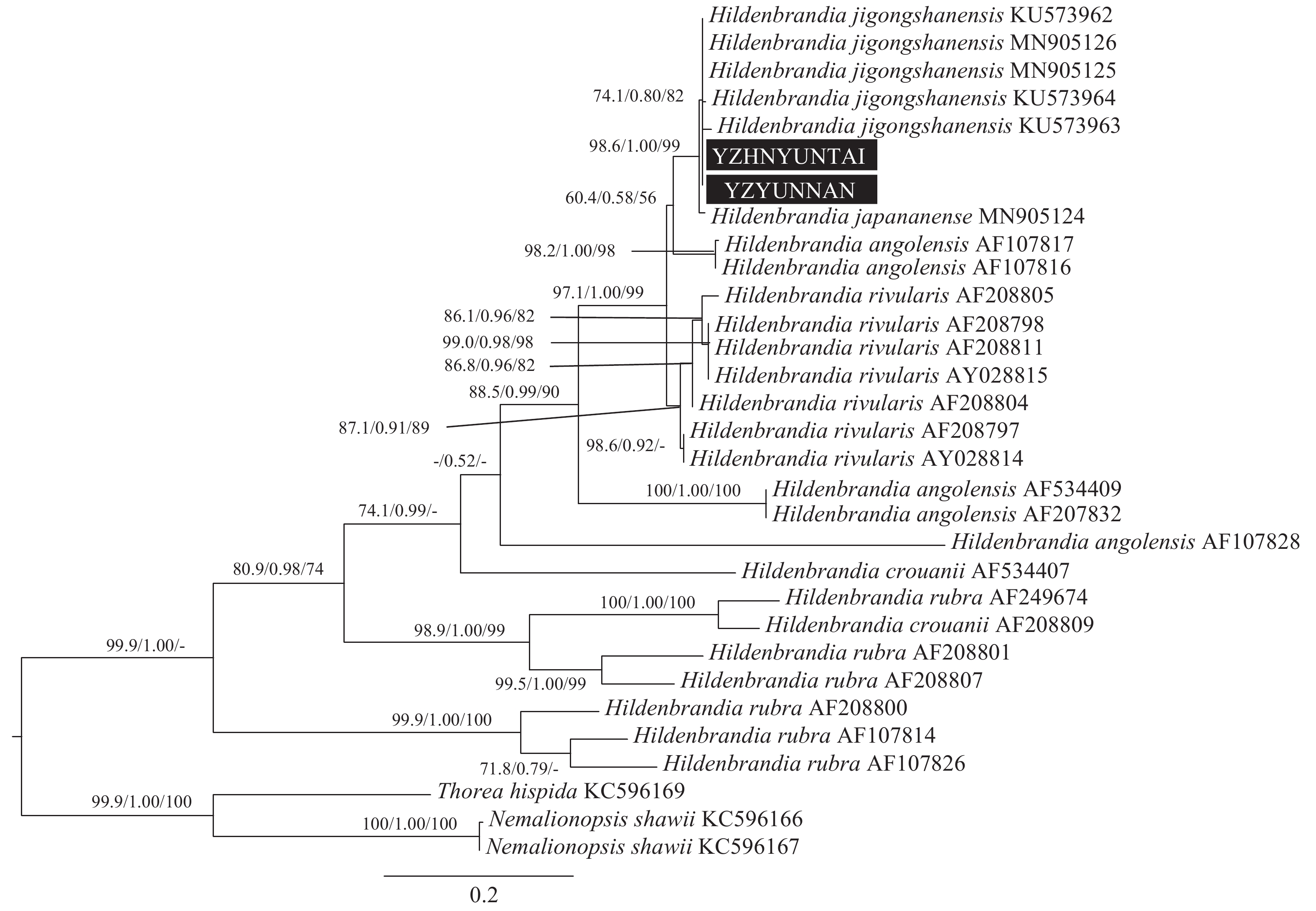
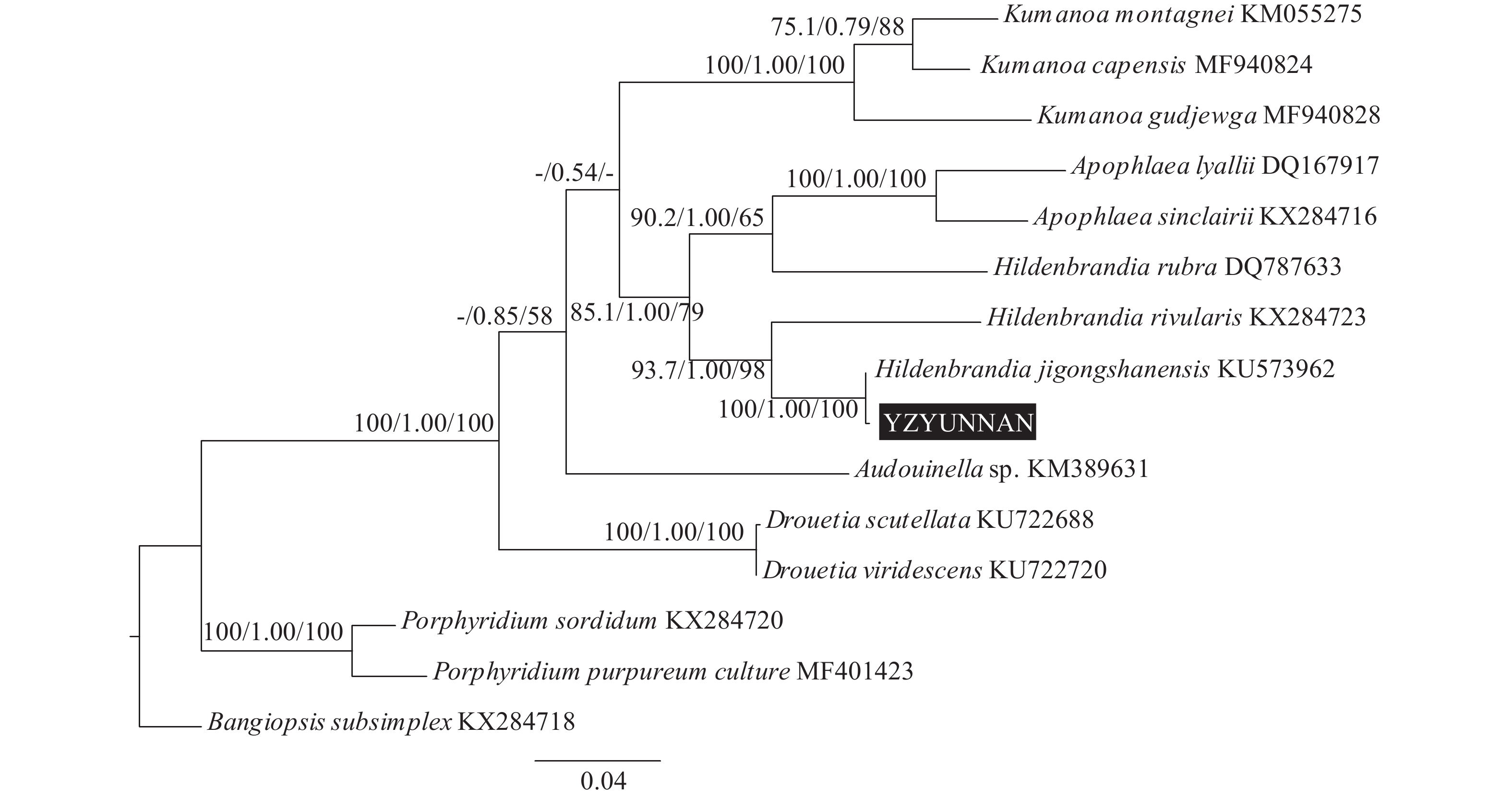
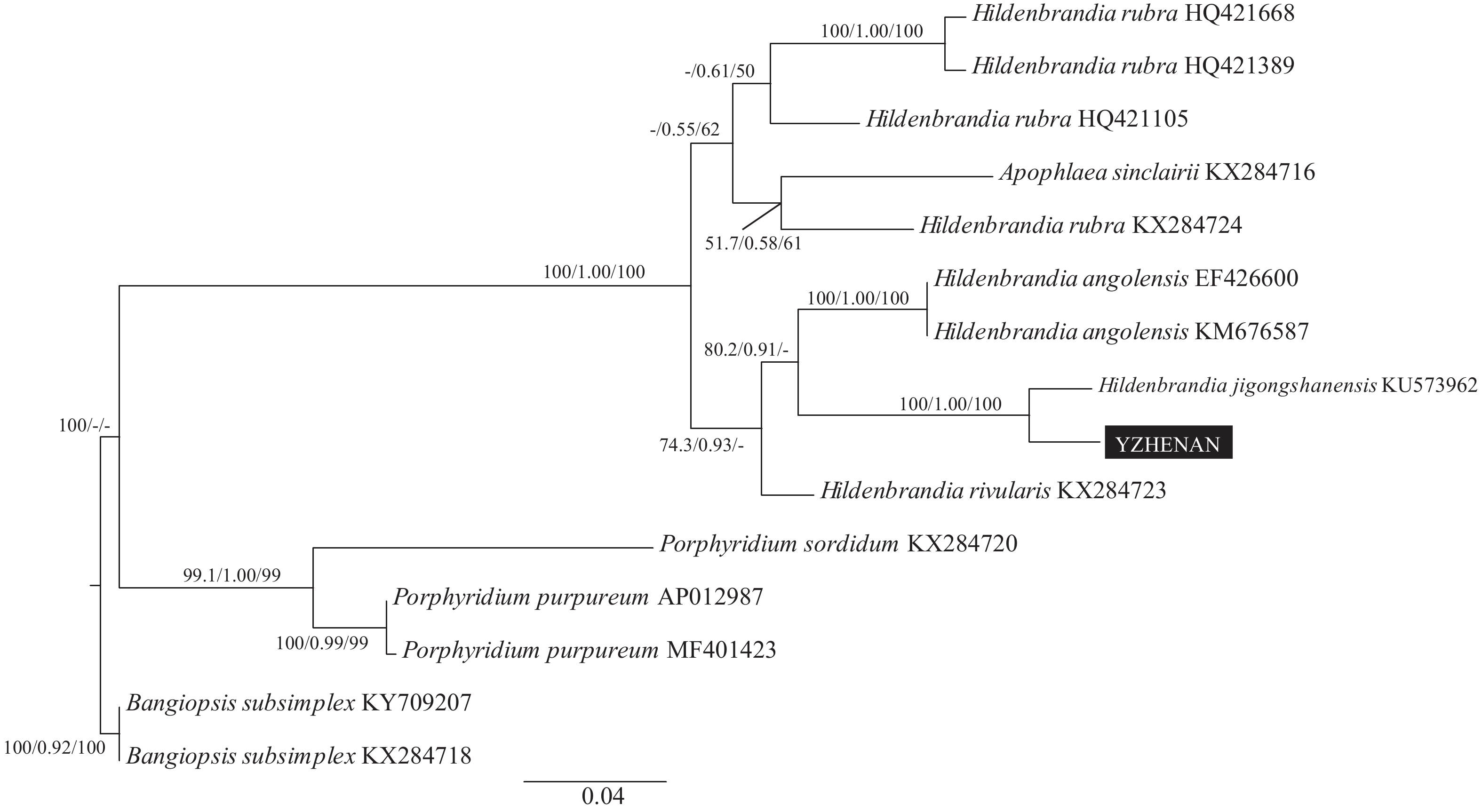
图 3 基于rbcL基因序列的系统树
各分支数字分别代表ML法支持率、贝叶斯法后验概率和NJ法支持率,“-”代表支持率低于50%; 下同
Figure 3. Phylogenetic tree based on rbcL gene sequence
Support values for all analyses are noted as: ML supporting values/Bayesian posterior probabilities/NJ distance bootstrap values, ‘-’ denotes supporting values lower than 50%. The same applies below
表 1 Modeltest 3.7分析获得的rbcL、psbA和UPA基因模型及相关参数
Table 1 Nucleotide substitution model parameter estimates of rbcL, psbA and UPA gene for Modeltest 3.7 analyses
基因类型 模型参数 碱基频率 矩阵参数 rbcL GTR+I+G-lnL=
3585.2925freqA=0.3337 R(a) [A-C]=6.0291 K=10 freqC=0.1206 R(b) [A-G]=9.0963 (I)=0.4854 freqG=0.2081 R(c) [A-T]=4.0643 (G)=1.0444 freqT=0.3375 R(d) [C-G]=4.2700 R(e) [C-T]=49.7748 R(f) [G-T]=1.0000 psbA GTR+I+G-lnL=
4302.8320freqA=0.2339 R(a) [A-C]=2.2366 K=10 freqC=0.1662 R(b) [A-G]=10.7395 (I)=0.5579 freqG=0.2176 R(c) [A-T]=13.9289 (G)=3.0916 freqT=0.3823 R(d) [C-G]=1.2210 R(e) [C-T]=39.8582 R(f) [G-T]=1.0000 UPA TIM+G-lnL=
1635.8729freqA=0.2972 R(a) [A-C]=1.0000 K=7 freqC=0.1730 R(b) [A-G]=6.4927 (I)=0 freqG=0.2750 R(c) [A-T]=1.6289 (G)=0.5960 freqT=0.2548 R(d) [C-G]=1.6289 R(e) [C-T]=10.1257 R(f) [G-T]=1.0000 表 2 淡水胭脂藻种类的关键分类特征
Table 2 Key taxonomic characters of freshwater Hildenbrandia
-
[1] 施之新. 中国淡水藻志 [M]. 第13卷, 红藻门和褐藻门. 北京: 科学出版社, 2006: 1-77. Shi Z X. Flora Algarum Sinicarum Aquae Dulcis [M]. Vol. 13, Rhodophyta and Phaeophyta. Beijing: Science Press, 2006: 1-77.
[2] Irvine L M, Pueschel C. M. Hildenbrandiales [M]//Irvine L M, Chamberlain Y M (Eds.), Seaweeds of the British Isles, Vol. 1, Rhodophyta, part 2B, Corallinales, Hildenbrandiales. London: the Natural History Museum, 1994: 235-241.
[3] Womersley H B S. The marine benthic flora of Southern Australia, Rhodophyta-Part IIIB [J]. Floras of Australia, 1996(5): 1-392.
[4] Silva P C, Basson P W, Moe R L. Catalogue of the Benthic Marine Algae of the Indian Ocean [M]. Oakland: University of California Press, 1996: 1-1259.
[5] Temniskova D, Stoyneva M P, Kirjakov I K. Red List of the Bulgarian algae. I. Macroalgae [J]. Phytologia Balcanica, 2008, 14(2): 193-206.
[6] Stoyneva M P, Stancheva R, Gärtner G. Heribaudiella fluviatilis (Aresch.) Sved. (Phaeophyceae) and the Hildenbrandia rivularis (Liebm.) J. AG. - Heribaudiella fluviatilis (Aresch.) Sved. association newly recorded in Bulgaria [J]. Berichte des Naturwissenschaftlich Medizinischen Verein in Innsbruck, 2003(90): 61-71.
[7] Liebman F. Bemœekninger og tillœg til den danske angeflora [J]. Naturhistorisk Tidsskrift, 1839(2): 464-494.
[8] Wolle F. Freshwater algae of the United States [M]. Bethlehem: Pennsylvania, 1887: 1-364.
[9] Guiry M D, Guiry G M. AlgaeBase. World-wide electronic publication, National University of Ireland, Galway. http://www.algaebase.org
[10] Sherwood A R, Sheath R G. Biogeography and systematics of Hildenbrandia (Rhodophyta, Hildenbrandiales) in Europe: Inferences from morphometrics and rbcL and 18S rRNA gene sequence analyses [J]. European Journal of Phycology, 2000(35): 143-152.
[11] Sherwood A R, Sheath R G. Systematics of the Hildenbrandiales (Rhodophyta): gene sequence and morphometric analyses of global collections [J]. Journal of Phycology, 2003(39): 409-422.
[12] Nan F, Feng J, Junping L V, et al. Hildenbrandia jigongshanensis (Hildenbrandiaceae, Rhodophyta), a new freshwater species described from Jigongshan Mountain, China [J]. Phytotaxa, 2017(292): 243-252.
[13] Nan F, Han J, Feng J, et al. Morphological and molecular investigation of freshwater Hildenbrandia (Hildenbrandiales, Rhodophyta) with a new species reported from Japan [J]. Phytotaxa, 2019(423): 68-74.
[14] Sherwood A R, Sheath R G. Biogeography and systematics of Hildenbrandia (Rhodophyta, Hildenbrandiales) in North America: inferences from morphometrics and rbcL and 18S rRNA gene sequence analyses [J]. European Journal of Phycology, 1999, 34(5): 523-532. doi: 10.1080/09541449910001718881
[15] Sherwood A R, Shea T B, Sheath R G. European freshwater Hildenbrandia (Hildenbrandiales, Rhodophyta) has not been derived from multiple invasions from marine habitats [J]. Phycologia, 2002, 41(1): 87-95. doi: 10.2216/i0031-8884-41-1-87.1
[16] Kahn M. On a freshwater Hildenbrandia Nardo from India [J]. Hydrobiologia, 1974, 44(2): 237-240.
[17] Zeller G. Algae collected by Mr. S. Kurz in Arracan and British Burma, determined and systematically arranged [J]. Journal of the Asiatic Society of Bengal, 1873(42): 175-193.
[18] Vis M L, Sheath R G. Biogeography of Batrachospermum gelatinosum (Batrachospermales, Rhodophyta) in North America based on molecular and morphological data [J]. Journal of Phycology, 1997, 33(3): 520-526. doi: 10.1111/j.0022-3646.1997.00520.x
[19] Vis M L, Saunders W, Sheath R G, et al. Phylogeny of the Batrachospermales (Rhodophyta) inferred from rbcL and 18S ribosomal DNA gene sequences [J]. Journal of Phycology, 2010, 34(2): 341-350.
[20] Salomaki E D, Kwandrans J, Eloranta P, et al. Molecular and morphological evidence for Sheathia gen. nov. (Batrachospermales, Rhodophyta) and three new species [J]. Journal of Phycology, 2014, 50(3): 526-542. doi: 10.1111/jpy.12179
[21] Hall T A. BioEdit: A user-friendly biological sequence alignment editor and analysis program for Windows 95/98/NT [J]. Nucleic Acids Symposium Series, 1999, 41(41): 95-98.
[22] Sudhir K, Glen S, Koichiro T. MEGA7: molecular evolutionary genetics analysis version 7.0 for bigger datasets [J]. Molecular Biology and Evolution, 2016(7): 1870.
[23] Posada D, Buckley T R. Model selection and model averaging in phylogenetics: advantages of Akaike information criterion and Bayesian approaches over likelihood ratio tests [J]. Systematic Biology, 2004, 53(5): 793-808. doi: 10.1080/10635150490522304
[24] Ronquist F, Huelsenbeck J P. MrBayes 3: Bayesian phylogenetic inference under mixed models [J]. Bioinformatics, 2003, 19(12): 1572-1574. doi: 10.1093/bioinformatics/btg180
[25] Guindon S, Dufayard J F, Lefort V, et al. New Algorithms and Methods to Estimate Maximum Likelihood Phylogenies: Assessing the Performance of PhyML 3.0 [J]. Systematic Biology, 2010, 59(3): 307-321. doi: 10.1093/sysbio/syq010
[26] Yu Y, Harris A, He X. RASP (reconstruct ancestral state in phylogenies) 2.0 beta [J]. WWW program. URLhttp://mnh.scu.edu.cn/soft/blog/RASP [accessed on 13 June 2011.]
[27] 南芳茹, 冯佳, 谢树莲. 中国熊野藻属植物系统发育分析—基于叶绿体UPA序列 [J]. 植物研究, 2014, 34(5): 584-591. doi: 10.7525/j.issn.1673-5102.2014.05.002 Nan F R, Feng J, Xie S L. Phylogenetic relationship of genus Kumanoa (Batrachospermales, Rhodophyta) based on chloroplast UPA gene [J]. Bulletin of Botanical Research, 2014, 34(5): 584-591. doi: 10.7525/j.issn.1673-5102.2014.05.002
[28] 南芳茹, 冯佳, 谢树莲. 基于叶绿体psaA和psbA基因的中国熊野藻属植物系统发育分析 [J]. 水生生物学报, 2015, 39(1): 155-163. doi: 10.7541/2015.20 Nan F R, Feng J, Xie S L. Phylogenetic relationship of genus Kumanoa based on chloroplast psaA and psbA genes [J]. Acta Hydrobiologica Sinica, 2015, 39(1): 155-163. doi: 10.7541/2015.20
[29] Necchi Jr O, West J A, Rai S K, et al. Phylogeny and morphology of the freshwater red alga Nemalionopsis shawii (Rhodophyta, Thoreales) from Nepal [J]. Phycological Research, 2016, 64(1): 11-18. doi: 10.1111/pre.12116
[30] Chapuis I S, Necchi Jr O, Zuccarello G C, et al. A new genus, Volatus and four new species of Batrachospermum sensu stricto (Batrachospermales, Rhodophyta) [J]. Phycologia, 2017, 56(4): 454-468. doi: 10.2216/16-73.1
[31] Skuja H. Comments on fresh-water Rhodophyceae [J]. Botanical Review, 1938, 4(12): 665-676. doi: 10.1007/BF02869845
[32] Nan F, Feng J, Lü J, et al. Origin and evolutionary history of freshwater Rhodophyta: further insights based on phylogenomic evidence [J]. Scientific Reports, 2017, 7(1): 1-12. doi: 10.1038/s41598-016-0028-x
[33] Sheath R G, Cole K M. Systematics of Bangia (Rhodophyta) in North America. I. Biogeographic trends in morphology [J]. Phycologia, 1984, 23(3): 383-396. doi: 10.2216/i0031-8884-23-3-383.1
[34] Yang E C, Boo S M, Bhattacharya D, et al. Divergence time estimates and the evolution of major lineages in the florideophyte red algae [J]. Scientific Reports, 2016, 6(1): 1-11. doi: 10.1038/s41598-016-0001-8
[35] 谢树莲, 凌元洁. 串珠藻目的现代地理分布和起源 [J]. 山西大学学报 (自然科学版), 2002(2): 149-155. Xie S L, Ling Y J. Modern geographical distribution and origin of Batrachospermales [J]. Journal of Shanxi University, 2002(2): 149-155.
-
期刊类型引用(5)
1. 徐立鸿,黄志尊,龙伟,蒋林华,童欣. 基于MobileViT-CBAM-BiLSTM的开放式养殖环境鱼群摄食强度分类模型. 农业机械学报. 2024(11): 147-153 .  百度学术
百度学术
2. 邵闯,秦守旺,朱波,张俊智,戴济鸿,戴振炎,胡毅,陈开健. 投喂策略对牛蛙蝌蚪生长发育及肝肠功能的影响. 水产学报. 2023(10): 72-83 .  百度学术
百度学术
3. 戴瑜来,王宇希,许宝青,戴杨鑫,林启存,蔡丽娟. 硫酸铜、敌百虫、聚维酮碘对吉富罗非鱼的急性毒性及组织病理学研究. 南方水产科学. 2023(06): 116-126 .  百度学术
百度学术
4. 王永帅,柏杨,孙凯,徐永健. 不同投喂频率对脊尾白虾生物钟基因表达、生长及肌肉成分组成的影响. 中国水产科学. 2023(08): 965-974 .  百度学术
百度学术
5. 邢书青. 基于随机森林回归的鱼饲料颗粒密度预测方法. 广东蚕业. 2022(07): 75-77 .  百度学术
百度学术
其他类型引用(4)



 下载:
下载: