MOLECULAR CHARACTERISTICS AND ANTIVIRAL EFFECTS OF ATG10 IN LARGE YELLOW CROAKER (LARIMICHTHYS CROCEA)
-
摘要: 为了研究自噬相关基因ATG10(Autophagy related gene 10)在鱼类免疫应答中的功能, 研究克隆了大黄鱼(Larimichthys crocea)ATG10基因(LcATG10)的cDNA序列, 其开放阅读框全长747个核苷酸, 编码248个氨基酸的蛋白, 包含1个Autophagy_act_C结构域。系统进化分析显示, LcATG10和其他硬骨鱼类ATG10聚成一支, 与金头鲷和石斑鱼ATG10亲缘关系最近。LcATG10在所检测的正常大黄鱼各组织中都有表达。在病毒类似物poly (I:C)刺激后, 大黄鱼脾脏和头肾组织中LcATG10的表达水平显著上调, 分别在12h和6h达到峰值(9.4和5.9倍)。LcATG10在大黄鱼头肾细胞系(LYCK)、原代巨噬细胞、淋巴细胞和粒细胞中也均有表达, 在原代粒细胞中的表达量相对较高; 在poly (I:C)刺激后, 大黄鱼原代头肾粒细胞和LYCK细胞中LcATG10的表达水平显著上调。过表达LcATG10的鲤上皮瘤(Epithelioma papulosum cyprinid, EPC)细胞受鲤春病毒血症病毒(Spring viremia of carp virus, SVCV)感染48h后, 细胞病变效应(Cytopathic effects, CPEs)明显低于对照组; 细胞培养上清中SVCV病毒滴度为103.55 TCID50/mL, 显著少于对照组; SVCV标志基因SVCV- G、SVCV-M和SVCV- P的表达水平也显著低于对照组, 分别是对照组的0.022、0.015和0.022倍。这些研究结果表明LcATG10在大黄鱼抗病毒免疫应答中发挥作用, 为深入研究自噬在大黄鱼抗病毒免疫中的分子机制奠定了基础。Abstract: Large yellow croaker (Larimichthys crocea) is an important economic marine fish species in China. In recent years, the frequent outbreaks of infectious diseases caused by bacteria or viruses have led to great economic losses to the large yellow croaker aquaculture. Thus, the understanding of immune mechanisms of large yellow croaker will contribute to prevent and control these diseases. Autophagy is an essential and widely conserved cellular degradation process that mediates the elimination of defective proteins and organelles. Autophagy is regulated by various autophagy-related genes (ATG), of which the ATG10 gene has been demonstrated to play a vital role in the immune response. To study the function of fish ATG10 in immune response, the ATG10 gene (LcATG10) was cloned from large yellow croaker (Larimichthys crocea). The open reading frame (ORF) of LcATG10 cDNA is 747 nucleotides long, encoding a protein of 248 amino acids with an Autophagy_act_C domain. Multiple amino acid sequence alignment showed that LcATG10 shared a high homology with ATG10 molecules in other known bony fishes. Phylogenetic analysis revealed that LcATG10 and other fish ATG10 molecules were clustered into a major clade, separated from the clade formed by the amphibian, avian, and mammalian ATG10s. Real-time qPCR results showed that the LcATG10 were widely expressed in tested tissues and immune-related cells of large yellow croaker. Poly (I:C) induced the mRNA levels of LcATG10 in the head kidney and spleen tissues with 5.9- and 9.4- fold, respectively, and it also increased LcATG10 in primary head kidney granulocytes and head kidney cell line (LYCK) cells of large yellow croaker. LcATG10-overexpression in epithelioma papulosum cyprinid (EPC) cells decreased the cytopathic effects (CPEs) caused by spring viremia of carp virus (SVCV) infection and reduced the viral titer of SVCV in the culture supernatant to 103.55 TCID50/mL. LcATG10-overexpression significantly down-regulated the expression levels of three viral genes (SVCV-G, SVCV-M, and SVCV-P) to 0.022-, 0.015- and 0.022-folds of those in control group, respectively. These results indicate that LcATG10 played an important role in the antiviral immune response of large yellow croaker, which provides a basis for in-depth study of the molecular mechanism of autophagy in the antiviral immunity of large yellow croaker.
-
Keywords:
- ATG10 /
- Immune-related cells /
- Antiviral immunity /
- Large yellow croaker
-
自噬(Autophagy)是一种依赖溶酶体对细胞内容物进行降解的过程, 在细胞分化、发育和免疫等多种生理过程中具有重要作用[1-3]。研究表明, 自噬作为细胞适应环境压力的自我保护机制, 参与机体的抗病毒先天免疫和特异性免疫反应[4]。自噬不仅可以直接清除病毒, 还参与调控天然和适应性抗病毒免疫应答的多个过程, 包括天然免疫细胞的分化发育、天然免疫信号通路的活化、淋巴细胞的稳态维持、抗原的加工提呈及抗体应答等[4, 5]。自噬相关基因(Autophagy-related genes, ATG)在自噬过程中发挥重要作用[6], 参与自噬的起始、自噬体膜的延伸、自噬体的成熟与融合及自噬体降解的全过程。目前在酵母(Saccharomyces cerevisiae)中已鉴定了30多个ATG基因, 其中15个(ATG1-10、ATG12-14、ATG16和ATG18)在哺乳动物中高度保守[7, 8]。
ATG10是招募其他自噬相关因子进行复杂共轭的重要接头分子, 在自噬体膜延伸的过程中起关键作用[9]。作为E2样泛素结合酶(E2-like ubiquitin conjugating enzyme), ATG10在E1样泛素活性酶(E1-like ubiquitin activating enzyme)ATG7的协助下, 招募ATG12形成ATG12-ATG10硫酯中间体, 进一步与ATG5结合形成ATG12-ATG5复合体[10]。在自噬发生时, ATG12-ATG5复合体与ATG16L1形成共轭蛋白复合体, 并定位于自噬小体形成过程中的隔离膜上, 具有E3样泛素连接酶(E3-like ubiquitin-protein ligase)活性, 参与微管相关蛋白LC3的脂化, 促进自噬体的形成[11-13]。研究表明, ATG10在动物抗病毒免疫过程中也具有重要作用[14]。在人肝癌细胞系Huh 7.5中过表达ATG10可促进自噬体与溶酶体的结合, 从而抑制丙肝病毒(Hepatitis C virus, HCV)的复制[15]。在太平洋牡蛎(Crassostrea gigas)中, 牡蛎外套膜中的CgATG10的转录水平在受到病毒类似物poly (I:C)刺激后显著上调, 表明CgATG10可能参与抗病毒免疫反应[9]。然而, 目前有关鱼类ATG10的研究还未见报道, 其在鱼类抗病毒免疫中的功能尚不清楚。
大黄鱼(Larimichthys crocea)在我国沿海地区养殖规模大, 经济价值高, 但近年来病害频发, 造成了重大的经济损失[16, 17]。由于自噬在动物抗病毒免疫中发挥重要作用, 因此解析大黄鱼自噬的分子基础及机制, 对于认识自噬在大黄鱼抗病毒免疫中的功能, 及大黄鱼病毒病的防治具有重要意义。为此, 我们研究了大黄鱼ATG10基因(LcATG10)在正常大黄鱼组织和免疫相关细胞中的表达水平及该基因对鱼类病毒复制的影响, 这些结果将为阐明ATG10在鱼类抗病毒免疫中的功能及其机制奠定基础。
1. 材料与方法
1.1 实验材料
实验所用大黄鱼均购自宁德富发水产有限公司, 将大黄鱼在流动的海水中适应性养殖10d, 水温为25℃。在暂养结束后, 将正常状态大黄鱼分为实验组和对照组, 每组30尾。实验组以2.5 μg/g大黄鱼的剂量腹腔注射poly (I:C), 对照组注射等体积的无菌磷酸盐缓冲液(PBS, pH=7.4), 分别于注射后3h、6h、12h和24h采集大黄鱼头肾和脾脏样品, 每个时间点各采集3尾。采集正常大黄鱼的心脏、肝脏、脾脏、头肾、胃、肠、血液、鳃、脑、皮肤和肌肉组织, 放入液氮中速冻, 再转入–80℃超低温冰箱保存。
1.2 大黄鱼免疫相关细胞分离与培养
取正常大黄鱼头肾组织, 放在70 μm细胞滤网上轻轻研磨, 制成细胞悬液, 将细胞悬液添加到新制备的34%和51% Percoll溶液上, 4℃, 650×g离心30min。离心后, 吸取中间层的细胞, 使用L-15培养基洗涤3次, 再接种到6孔板中, 每孔2.0×106个细胞, 28℃培养2h, 分别收集悬浮的原代淋巴细胞和贴壁的原代巨噬细胞。将研磨后的细胞悬液用移液枪加入到51%Percoll上, 4℃, 650×g离心30min, 收集离心管底部的原代粒细胞。
大黄鱼头肾细胞系(LYCK), 是本实验室建立并长期保存的细胞系[18], 使用L-15培养基(15% FBS)进行培养, 培养温度为28℃。
1.3 RNA提取和cDNA合成
采用Eastep® Super Total RNA Extraction Kit(Promega)分别提取大黄鱼各组织和免疫相关细胞的总RNA, 用Eastep® RT Master Mix Kit(Promega)合成cDNA, 具体方法参考试剂盒的说明书进行。
1.4 LcATG10基因克隆与序列分析
从NCBI上查找出大黄鱼ATG10基因序列(GenBank登录号: XM_019277201.2), 设计特异引物LcATG10-F和LcATG10-R(表 1), 以大黄鱼脾脏的cDNA为模板, PCR扩增ATG10基因的开放阅读框(Open reading frame, ORF)全长序列, 并测序验证。蛋白质结构域采用SMART软件进行预测, 其他物种ATG10序列来自GenBank数据库, 通过DNAMAN进行序列比对; 使用MEGA7.0 软件, 采用最大似然法构建进化树。
表 1 引物序列Table 1. Primers information引物名称Name 序列Sequence (5ʹ-3ʹ) 用途Usage LcATG10-F
LcATG10-R
PcDNA3.1-LcATG10-F
PcDNA3.1-LcATG10-R
RT-LcATG10-F
RT-LcATG10-R
RT-Lcβ-actin-F
RT-Lcβ-actin-R
RT-SVCV-G-F
RT-SVCV-G-R
RT-SVCV-M-F
RT-SVCV-M-R
RT-SVCV-P-F
RT-SVCV-P-R
RT-EPC-actin-F
RT-EPC-actin-RATGAGCTCGAGTGTCCTGGA
GTCTGGCTTGGTGCTGCTGA
ACTGTGCTGGATATCTG
CAGAATTCG
CCACCATGAGCTCGA
GTGTCCTGGA
GGGCCCAAGCTTGGT
ACCGTCTGGC
TTGGTGCTGCTGA
GGGTCCTGTGGTGGGTCTGG
CTGGCTTGGTGCTGCTGAGTG
GACCTGACAGACTACCTCATG
AGTTGAAGGTGGTCTCGTGGA
CGACCTGGATTAGACTTG
AATGTTCCGTTTCTCACT
TACTCCTCCCACTTACGA
CAAGAGTCCGAGAAGGTC
TTGGACCTGGGATAGTGA
CTTGCTTGGTTTGTGGG
TGTTCCAGCCATCCTTCTTG
TGATTTTCATTGTGCTGGGGORF扩增
真核表达载体构建
RT-PCR1.5 LcATG10在大黄鱼组织和免疫相关细胞中的表达分析
将采集的3尾大黄鱼的组织进行RNA提取, 利用特异性引物RT-LcATG10-F和RT-LcATG10-R(表 1)进行荧光定量PCR反应, 检测LcATG10在正常大黄鱼各组织中的表达水平。
分别收集4种大黄鱼免疫相关细胞, 用细胞计数仪(美国ORFLO公司)计数2.0 ×106个细胞进行总RNA提取和cDNA合成, 采用上述方法检测LcATG10在正常大黄鱼4种免疫相关细胞中的表达水平。
荧光定量PCR反应体系如下: 2×SYBR Green Ⅰ 10 μL, 上下游引物(10 μmol/L)各0.1 μL, cDNA模板0.2 μL, 无菌水9.6 μL。反应条件: 95℃预变性2min, 95℃变性15s, 57℃退火20s, 72℃延伸20s, 共40个循环。LcATG10的相对表达水平采用2–ΔΔCt方法计算, 并用SPSS 18.0软件进行统计学分析, P<0.05表示差异显著, 用“*”表示, P<0.01表示差异极显著, 用“**”表示。
1.6 poly (I:C)刺激后LcATG10在大黄鱼免疫组织和免疫相关细胞中的表达分析
将采集的大黄鱼头肾和脾脏组织分别进行总RNA提取和cDNA合成, 采用荧光定量PCR检测poly (I:C)刺激的大黄鱼各组织中LcATG10基因相对于对照组大黄鱼各组织的表达变化。荧光定量PCR和数据分析方法如1.5。
将大黄鱼LYCK细胞和原代粒细胞接种于6孔板中, 每种细胞各接种6个孔(实验组和对照组各3孔), 每孔2.0 ×106个细胞, 用L-15培养基于28℃进行培养。LYCK细胞培养12h后使用终浓度为50 μg/mL的poly (I:C)刺激, 原代粒细胞接种后立即进行poly (I:C)刺激, 同时用无菌PBS溶液处理的细胞作为对照。收集细胞后提取RNA并反转录为cDNA。以大黄鱼β-actin作为内参基因进行荧光定量PCR反应, 检测poly (I:C)刺激的LYCK和原代粒细胞中LcATG10基因相对于对照组细胞的表达变化。荧光定量PCR和数据分析方法如1.5。
1.7 免疫印迹
选择生长状态良好的鲤上皮瘤细胞系(EPC)接种于6孔板中, 每孔约1×106个细胞, 加入2 mL含10% FBS的L-15培养基, 28℃培养12h。利用转染试剂FuGENE® HD(Promega)将2 µg pcDNA3.1-LcATG10重组质粒转入EPC细胞, 以空载体pcDNA3.1作为对照。转染48h后, 加入裂解液使细胞裂解完全。离心取上清, SDS-PAGE电泳后转移到聚偏氟乙烯(PVDF)膜(Millipore)上。取出膜放入洗膜盒中, 加入5 mL TBST缓冲液[5%(w/v)脱脂奶粉], 放在摇床摇动1h, 然后与鼠抗人c-myc单克隆抗体(Thermo Fisher, 1﹕2000)室温孵育1h, TBST洗涤3次, 然后与辣根过氧化物酶标记的羊抗鼠IgG(H+L)多克隆抗体(Thermo Fisher, 1﹕4000)室温孵育1h, 再用TBST 洗涤3次, 每次5min, 最后用凝胶成像仪检测结果。
1.8 LcATG10抗病毒实验
借助鲤EPC细胞和鲤春病毒血症病毒(SVCV)感染模型分析LcATG10在病毒感染过程中的功能。生长状态良好的EPC细胞用胰酶消化下来, 加入L-15培养基并离心, 计数后接种于6孔板中, 每孔约1×106个细胞, 加入2 mL含10% FBS的L-15培养基, 放入28℃培养箱培养12h。将2 µg pcDNA3.1-LcATG10重组质粒转入EPC细胞作为实验组, 以空载体pcDNA3.1作为对照组。在转染24h后, 使用感染复数(Multiplicity of infection, MOI)为1.4的SVCV感染实验组和对照组EPC细胞。在感染24h和48h后, 使用显微镜观察细胞病变程度并拍照, 同时对感染48h的细胞用结晶紫染料进行染色观察。分别收集感染48h的细胞培养上清和细胞。培养上清用于测定病毒滴度, 收集的细胞提取总RNA, 并合成cDNA, 以大黄鱼β-actin作为内参基因, 采用荧光定量PCR检测病毒基因SVCV-G、SVCV-M和SVCV-P的相对表达水平。病毒基因SVCV-G、SVCV-M和SVCV-P的荧光定量PCR引物见表 1, 荧光定量PCR和数据分析方法如1.5。
2. 结果
2.1 大黄鱼LcATG10分子特征
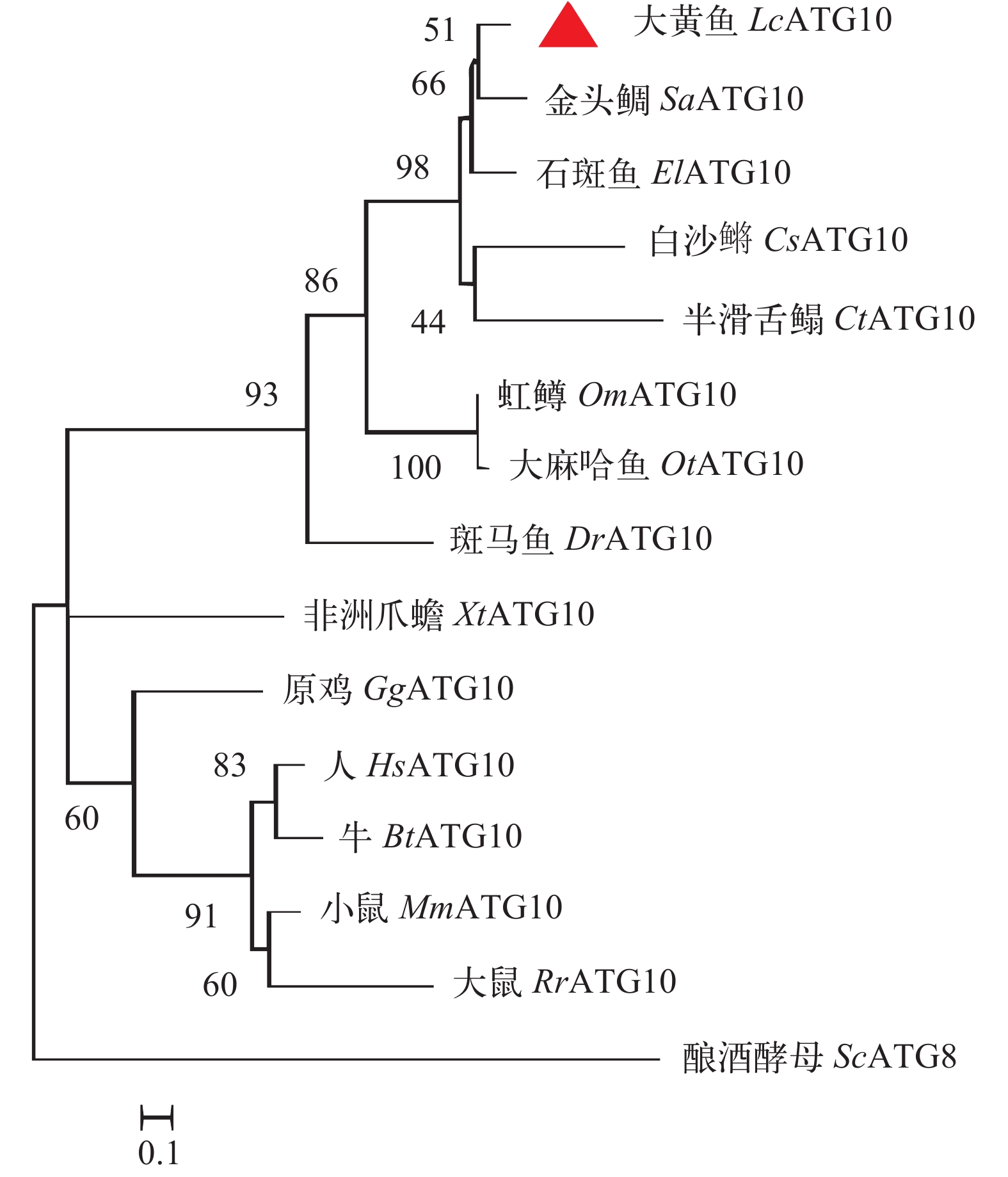
克隆的LcATG10基因ORF长747个核苷酸(GenBank登录号: XP_027143515.1), 该蛋白由248个氨基酸残基组成, 序列分析发现, LcATG10与哺乳动物ATG10蛋白序列特征相似, 不具有信号肽和跨膜区, 含有1个保守的Autophagy_act_C结构域(124—191位氨基酸), 该结构域含有与ATG12和ATG5结合的关键氨基酸位点, 包括亮氨酸(Leu135、Leu147、Leu149、Leu164、Leu180)、脯氨酸(Pro178、Pro189)、色氨酸(Trp153)和半胱氨酸(Cys190)。氨基酸序列同源性比对显示, LcATG10与金头鲷(Sparus aurata)ATG10的序列一致性最高(76.3%)其次为石斑鱼(Epinephelus lanceolatus)(74.2%)。系统进化分析显示, 所有物种的ATG10与酿酒酵母ATG8分为两大支, 其中LcATG10与其他鱼类的ATG10形成1个分支, 哺乳类、两栖类和禽类的ATG10聚为另外一支(图 1)。
![]() 图 1 大黄鱼与其他物种ATG10氨基酸序列构建的进化树基于大黄鱼和其他脊椎动物ATG10氨基酸序列构建了系统进化树, 使用的软件是MEGA 7.0, 计算方法: 最大似然法。所用氨基酸序列的GenBank登录号如下: 大黄鱼(XP_027143515.1); 金头鲷(XP_030257561.1); 石斑鱼(XP_033505554.1); 白沙鳉(XP_038133305.1); 半滑舌鳎(XP_024908216.1); 虹鳟(XP_036823990.1); 大马哈鱼(XP_035628463.1); 斑马鱼(NP_001032201.1); 非洲爪蟾(XP_031749390.1); 原鸡(XP_015136200.1); 人(NP_113670.1); 牛(NP_001077000.1); 小鼠(NP_080046.3); 大鼠(XP_032752943.1); 酿酒酵母(NP_009475.1)Figure 1. A phylogenetic tree was constructed based on the amino acid sequences of ATG10 from large yellow croaker and other vertebratesThe phylogenetic tree was constructed by MEGA 7.0 using Maximum Likelihood method. The GenBank accession numbers for protein sequences used here as followed, Larimichthys crocea (XP_027143515.1); Sparus aurata (XP_030257561.1); Epinephelus lanceolatus (XP_033505554.1); Cyprinodon tularosa (XP_038133305.1); Cynoglossus semilaevis (XP_024908216.1); Oncorhynchus mykiss(XP_036823990.1); Oncorhynchus keta (XP_035628463.1); Danio rerio (NP_001032201.1); Xenopus tropicalis (XP_031749390.1); Gallus gallus (XP_015136200.1); Homo sapiens (NP_113670.1); Bos Taurus (NP_001077000.1); Mus musculus (NP_080046.3); Rattus rattus (XP_032752943.1); Saccharomyces cerevisiae (NP_009475.1)
图 1 大黄鱼与其他物种ATG10氨基酸序列构建的进化树基于大黄鱼和其他脊椎动物ATG10氨基酸序列构建了系统进化树, 使用的软件是MEGA 7.0, 计算方法: 最大似然法。所用氨基酸序列的GenBank登录号如下: 大黄鱼(XP_027143515.1); 金头鲷(XP_030257561.1); 石斑鱼(XP_033505554.1); 白沙鳉(XP_038133305.1); 半滑舌鳎(XP_024908216.1); 虹鳟(XP_036823990.1); 大马哈鱼(XP_035628463.1); 斑马鱼(NP_001032201.1); 非洲爪蟾(XP_031749390.1); 原鸡(XP_015136200.1); 人(NP_113670.1); 牛(NP_001077000.1); 小鼠(NP_080046.3); 大鼠(XP_032752943.1); 酿酒酵母(NP_009475.1)Figure 1. A phylogenetic tree was constructed based on the amino acid sequences of ATG10 from large yellow croaker and other vertebratesThe phylogenetic tree was constructed by MEGA 7.0 using Maximum Likelihood method. The GenBank accession numbers for protein sequences used here as followed, Larimichthys crocea (XP_027143515.1); Sparus aurata (XP_030257561.1); Epinephelus lanceolatus (XP_033505554.1); Cyprinodon tularosa (XP_038133305.1); Cynoglossus semilaevis (XP_024908216.1); Oncorhynchus mykiss(XP_036823990.1); Oncorhynchus keta (XP_035628463.1); Danio rerio (NP_001032201.1); Xenopus tropicalis (XP_031749390.1); Gallus gallus (XP_015136200.1); Homo sapiens (NP_113670.1); Bos Taurus (NP_001077000.1); Mus musculus (NP_080046.3); Rattus rattus (XP_032752943.1); Saccharomyces cerevisiae (NP_009475.1)2.2 LcATG10在正常大黄鱼不同组织或器官及免疫相关细胞中表达分析
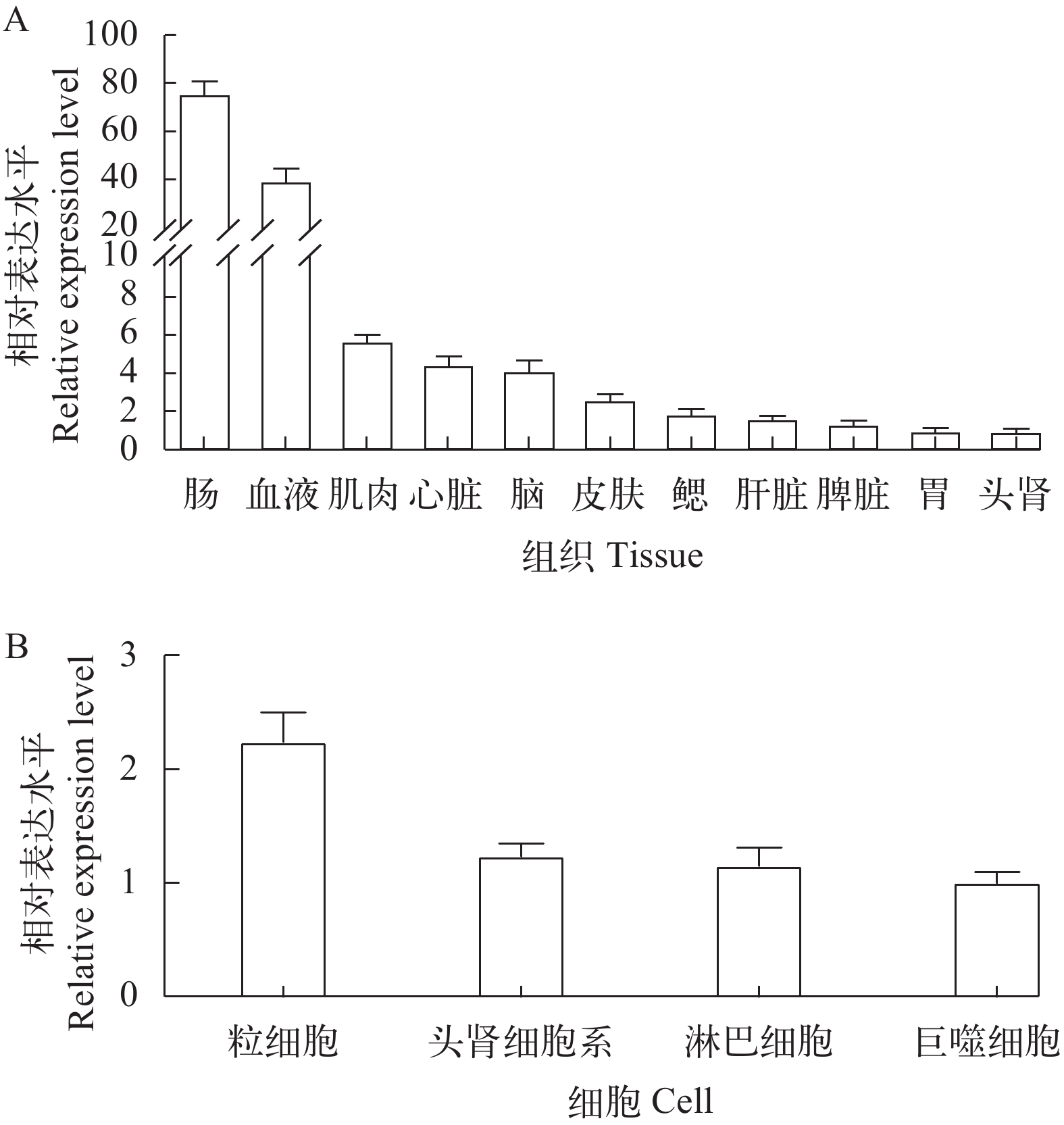
采用荧光定量PCR技术检测了正常大黄鱼心脏、肝脏、脾脏、头肾、胃、肠、血液、鳃、脑、皮肤和肌肉组织中LcATG10的表达水平。结果显示, LcATG10在所有检测的组织中呈组成型表达, 表达量最高的为肠道, 在头肾中最低(图 2A)。
![]() 图 2 LcATG10 在大黄鱼组织和免疫相关细胞中的表达模式A. 分别提取血液、肌肉、皮肤、肠道、脑、胃、鳃、脾脏、肝脏、心脏和头肾组织的RNA, qRT-PCR检测分析各种组织中LcATG10 mRNA的表达, β-actin为内参基因; B. LcATG10在大黄鱼头肾细胞系、原代巨噬细胞、淋巴细胞和粒细胞中的表达水平, β-actin为内参基因Figure 2. The relative expression of LcATG10 in tissues and immune-related cellsA. RT-PCR was performed to detect LcATG10 expression from different tissues include blood, muscle, skin, intestine, brain, stomach, gill, spleen, liver, heart and head kidney. β-actin was used as a positive control; B. The expression levels of LcATG10 in head kidney cell line, primary macrophage, lymphocytes and neutrophils of large yellow croaker were detected by fluorescence quantitative PCR, and β-actin was used as the internal reference gene
图 2 LcATG10 在大黄鱼组织和免疫相关细胞中的表达模式A. 分别提取血液、肌肉、皮肤、肠道、脑、胃、鳃、脾脏、肝脏、心脏和头肾组织的RNA, qRT-PCR检测分析各种组织中LcATG10 mRNA的表达, β-actin为内参基因; B. LcATG10在大黄鱼头肾细胞系、原代巨噬细胞、淋巴细胞和粒细胞中的表达水平, β-actin为内参基因Figure 2. The relative expression of LcATG10 in tissues and immune-related cellsA. RT-PCR was performed to detect LcATG10 expression from different tissues include blood, muscle, skin, intestine, brain, stomach, gill, spleen, liver, heart and head kidney. β-actin was used as a positive control; B. The expression levels of LcATG10 in head kidney cell line, primary macrophage, lymphocytes and neutrophils of large yellow croaker were detected by fluorescence quantitative PCR, and β-actin was used as the internal reference gene此外, 我们还检测了LcATG10在大黄鱼原代头肾淋巴细胞、巨噬细胞和粒细胞及头肾细胞系LYCK中的相对表达水平, 结果表明LcATG10能够在这些细胞中表达, 表达量最高的是原代粒细胞, 最低的是原代巨噬细胞(图 2B)。
2.3 poly(I:C)刺激对LcATG10表达的影响
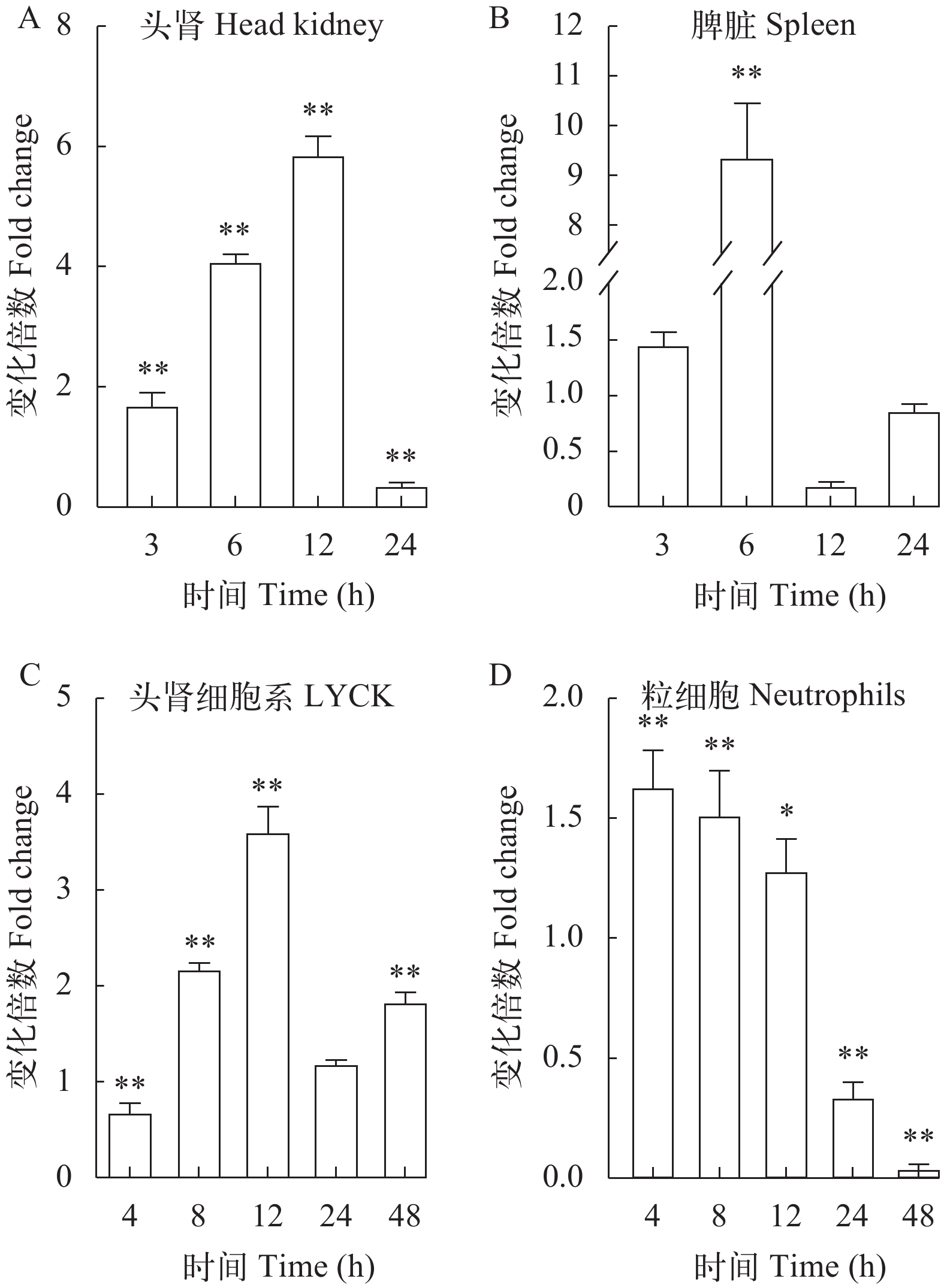
为了进一步了解LcATG10是否参与大黄鱼抗病毒免疫反应, 使用病毒类似物poly (I:C)刺激大黄鱼, 检测大黄鱼头肾和脾脏中LcATG10的转录水平变化。结果显示, poly (I:C)刺激后, 大黄鱼头肾中LcATG10的转录水平从3h开始上调, 在12h达到最高值, 是对照组的5.9倍, 而在24h表达量显著下降(图 3A); 在脾脏中, LcATG10的转录水平在刺激后3h开始上调, 6h 达到峰值, 为对照组的9.4倍, 随后下调(图 3B)。
![]() 图 3 大黄鱼组织和免疫相关细胞受poly(Ⅰ﹕C)刺激后LcATG10表达变化大黄鱼头肾(A)、脾脏(B)以及头肾细胞系(LYCK)细胞(C)和原代粒细胞(D)中LcATG10基因的时序表达分析。*代表显著性差异(P<0.05), **代表差异极显著(P<0.01)Figure 3. Expression levels of LcATG10 in tissues and immune-related cells of large yellow croaker after poly (I﹕C) stimulationRelative expression of LcATG10 gene in head kidney (A), spleen (B), LYCK cells (C) and primary neutrophils (D) of large yellow croaker stimulated with poly (I:C). * indicates significant difference (P<0.05); ** indicates highly significant difference (P<0.01)
图 3 大黄鱼组织和免疫相关细胞受poly(Ⅰ﹕C)刺激后LcATG10表达变化大黄鱼头肾(A)、脾脏(B)以及头肾细胞系(LYCK)细胞(C)和原代粒细胞(D)中LcATG10基因的时序表达分析。*代表显著性差异(P<0.05), **代表差异极显著(P<0.01)Figure 3. Expression levels of LcATG10 in tissues and immune-related cells of large yellow croaker after poly (I﹕C) stimulationRelative expression of LcATG10 gene in head kidney (A), spleen (B), LYCK cells (C) and primary neutrophils (D) of large yellow croaker stimulated with poly (I:C). * indicates significant difference (P<0.05); ** indicates highly significant difference (P<0.01)此外, 我们还分析了poly (I:C)刺激大黄鱼头肾细胞系LYCK和原代粒细胞中LcATG10的转录变化。结果显示, 在poly (I:C)刺激后, LcATG10的转录水平在LYCK细胞中先上升, 在12h达到最大值, 是对照组的3.6倍, 随后有所下降(图 3C); 在原代粒细胞中LcATG10的表达水平快速上调, 但在24h和48h显著下调(图 3D)。
2.4 LcATG10保护细胞免受病毒感染
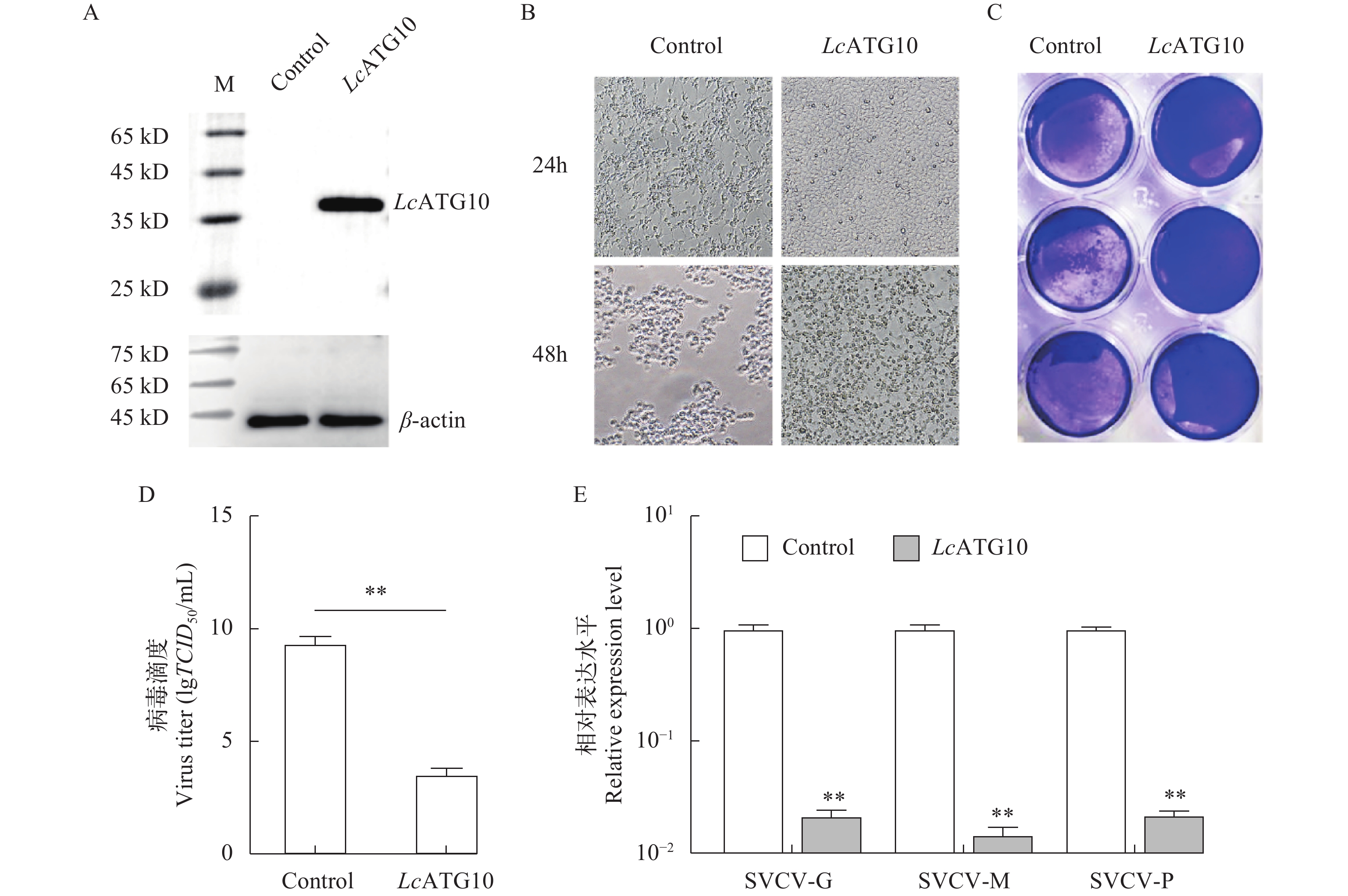
为了确定LcATG10在抗病毒免疫中的功能, 利用EPC细胞过表达LcATG10, 再分析LcATG10过表达对SVCV复制的影响。结果显示LcATG10在EPC细胞中得到了表达(图 4A), 在SVCV感染24h和48h后, 过表达LcATG10的EPC细胞中CPEs明显少于转染空载体的EPC细胞(图 4B和4C)。在感染48h后, 过表达LcATG10的EPC细胞上清中病毒滴度为103.55 TCID50/mL, 显著低于对照组的病毒滴度(109.36 TCID50/mL; 图 4D)。此外, 在过表达LcATG10的EPC细胞中, 感染48h后SVCV标志基因SVCV-G、SVCV-M和SVCV-P的表达量显著低于对照组, 分别是对照组的0.022、0.015和0.022倍(图 4E)。这些数据表明LcATG10具有抑制SVCV复制的功能。
![]() 图 4 LcATG10 过表达对病毒复制的影响A. 免疫印迹检测LcATG10在鲤上皮瘤细胞系(EPC)中的过表达, 空载体作为对照; B. pcDNA3.1-LcATG10 或 pcDNA3.1(作为对照)转染的EPC细胞感染 SVCV, 在感染后 24h 和 48h 显微镜下观察细胞病变效应(放大倍数: 63×); C. 结晶紫染色观察SVCV感染 48h 的细胞病变效应; D. 过表达LcATG10 的EPC 细胞或对照细胞培养上清中病毒滴度, 用50%组织细胞感染量表示; E. 荧光定量PCR检测LcATG10过表达的EPC细胞中SVCV基因的相对表达水平; 病毒基因相对表达水平表示为实验组细胞中SVCV基因的表达水平相对于对照组细胞中的倍数变化。*代表显著性差异(P<0.05), **代表差异极显著(P<0.01)Figure 4. Effects of LcATG10 overexpression on virus replicationA. Western blotting was used to detect the overexpression of LcATG10 in EPC cell lines; B. EPC cells transfected with pcDNA3.1-LcATG10 or pcDNA3.1 (as control) were infected with SVCV, and the CPEs were observed microscopically at 24h and 48h post-infection; C. Cells were stained with 1% crystal violet for detection of CPEs; D. The titers of SVCV in culture supernatants from LcATG10-overexpressed EPC cells or control cells, which was expressed as 50% tissue culture infectious dose (TCID50); E. The expression levels of the SVCV genes after overexpression of LcATG10 in EPC cells were detected by real-time PCR. * indicates significant difference (P<0.05); ** indicates highly significant difference (P<0.01)
图 4 LcATG10 过表达对病毒复制的影响A. 免疫印迹检测LcATG10在鲤上皮瘤细胞系(EPC)中的过表达, 空载体作为对照; B. pcDNA3.1-LcATG10 或 pcDNA3.1(作为对照)转染的EPC细胞感染 SVCV, 在感染后 24h 和 48h 显微镜下观察细胞病变效应(放大倍数: 63×); C. 结晶紫染色观察SVCV感染 48h 的细胞病变效应; D. 过表达LcATG10 的EPC 细胞或对照细胞培养上清中病毒滴度, 用50%组织细胞感染量表示; E. 荧光定量PCR检测LcATG10过表达的EPC细胞中SVCV基因的相对表达水平; 病毒基因相对表达水平表示为实验组细胞中SVCV基因的表达水平相对于对照组细胞中的倍数变化。*代表显著性差异(P<0.05), **代表差异极显著(P<0.01)Figure 4. Effects of LcATG10 overexpression on virus replicationA. Western blotting was used to detect the overexpression of LcATG10 in EPC cell lines; B. EPC cells transfected with pcDNA3.1-LcATG10 or pcDNA3.1 (as control) were infected with SVCV, and the CPEs were observed microscopically at 24h and 48h post-infection; C. Cells were stained with 1% crystal violet for detection of CPEs; D. The titers of SVCV in culture supernatants from LcATG10-overexpressed EPC cells or control cells, which was expressed as 50% tissue culture infectious dose (TCID50); E. The expression levels of the SVCV genes after overexpression of LcATG10 in EPC cells were detected by real-time PCR. * indicates significant difference (P<0.05); ** indicates highly significant difference (P<0.01)3. 讨论
ATG10作为自噬小体形成的核心因子之一, 介导了ATG12-ATG5复合体形成的最后一步反应[19, 20]。目前, ATG10基因在酵母[12]、人(Homo sapiens) [21]、小鼠(Mus musculus)[22]、牡蛎(Crassostrea gigas)[9]、拟南芥(Arabidopsis thaliana)[11]和小麦(Triticum aestivum)[23]等真核生物中得到了鉴定及功能研究, 但在鱼类中的研究尚未见报道。因此, 解析大黄鱼ATG10的分子特征及其在抗病毒免疫中功能, 有助于阐明鱼类ATG10在抗病毒免疫中的作用机制。
在系统进化树中, LcATG10和其他物种的ATG10与酿酒酵母ATG8分为两大支, 其中LcATG10与石斑鱼和金头鲷ATG10聚在一起, 处于硬骨鱼类分支中, 表明本研究获得的LcATG10基因确为ATG10的同源基因。大黄鱼ATG10蛋白含有一个Autophagy_act_c结构域, 该结构域是ATG10的一个重要功能域, 包含多个高度保守的氨基酸位点。在太平洋牡蛎中亮氨酸(Leu107和Leu159)、脯氨酸(Pro105和Pro161)、色氨酸(Trp125和Trp141)和半胱氨酸(Cys162)被认为是参与ATG12-ATG5结合的关键位点[19], 而大黄鱼Autophagy_act_c结构域同样包含这些保守氨基酸位点。此外, 在这些保守氨基酸残基中半胱氨酸Cys是ATG10和ATG12之间硫酯键的结构基础[10], 在人和小鼠ATG10中半胱氨酸Cys133残基周围序列高度保守, 被认为是活性位点[12], 同样在大黄鱼ATG10中半胱氨酸Cys190残基周围序列也高度保守, 提示大黄鱼ATG10蛋白可能也参与ATG12-ATG5结合过程。
为了研究LcATG10的功能特征, 本研究首先对LcATG10基因在大黄鱼组织中的表达谱进行分析。据报道, 目前对动物ATG10基因组织表达谱的分析较少, 仅在太平洋牡蛎中有类似的报道。在本研究中, LcATG10在所有被检测的大黄鱼组织中均有表达, 这种组成型表达模式不仅与太平洋牡蛎中CgATG10的表达模式相似[9], 而且与黄颡鱼ATG4和LC3(酵母ATG8同源基因)、太平洋鳕ATG5、草鱼Beclin1(酵母ATG6同源基因)等鱼类自噬相关基因组织表达谱类似[24-26], 推测自噬可能在大黄鱼多种生理功能中发挥作用。此外, LcATG10基因在LYCK细胞以及原代巨噬细胞、淋巴细胞和粒细胞中均有表达, 表明LcATG10可能参与大黄鱼免疫功能。
研究表明, 病原感染能够诱导宿主ATG10基因的上调表达, 进而激活细胞自噬发挥抗病原感染的功能, 其中ATG10在自噬小体的形成中具有重要作用, 在受到病毒感染时可以促进自噬小体的形成, 进而抑制病毒的复制[9, 14]。在人肝癌细胞系Huh7.5中, 过表达ATG10可以抑制人丙型肝炎病毒HCV的复制[15]。在本研究中, 病毒类似物poly (I:C)刺激后大黄鱼脾脏、头肾组织及LYCK细胞和原代粒细胞中LcATG10基因的转录水平均显著上升, 与poly(I:C)刺激后太平洋牡蛎中ATG10的表达上调相一致, 表明LcATG10可能参与抗病毒免疫反应。进一步在EPC细胞中过表达LcATG10可显著减少SVCV感染引起的CPEs现象, 同时还显著降低了感染细胞培养上清中SVCV滴度和SVCV标志基因的转录水平, 表明LcATG10具有抑制SVCV病毒在EPC细胞中复制的功能。Zhao等[15]在人肝癌细胞系HepG2中发现, 过表达ATG10可以促进自噬小体的形成, 并导致HCV亚基因组复制子的降解。因此, 我们推测LcATG10可能通过促进自噬小体形成来实现对病毒的抑制作用, 但这一推测还有待于进一步的证实。
综上所述, 本研究从大黄鱼中鉴定了一个具有保守Autophagy_act_c结构域的ATG10基因(LcATG10)。检测了LcATG10在大黄鱼组织和免疫相关细胞中的表达水平, 结果显示其均呈组成型表达。poly (I:C)刺激后LcATG10表达在大黄鱼免疫相关组织和免疫细胞中均显著上调。在EPC细胞中过表达LcATG10可抑制SVCV的复制, 提示LcATG10可能通过促进自噬小体的形成参与其抗病毒免疫反应, 然而具体机制有待阐明。这些研究结果将为进一步研究自噬在大黄鱼抗病毒免疫中的分子机制奠定了基础。
-
图 1 大黄鱼与其他物种ATG10氨基酸序列构建的进化树
基于大黄鱼和其他脊椎动物ATG10氨基酸序列构建了系统进化树, 使用的软件是MEGA 7.0, 计算方法: 最大似然法。所用氨基酸序列的GenBank登录号如下: 大黄鱼(XP_027143515.1); 金头鲷(XP_030257561.1); 石斑鱼(XP_033505554.1); 白沙鳉(XP_038133305.1); 半滑舌鳎(XP_024908216.1); 虹鳟(XP_036823990.1); 大马哈鱼(XP_035628463.1); 斑马鱼(NP_001032201.1); 非洲爪蟾(XP_031749390.1); 原鸡(XP_015136200.1); 人(NP_113670.1); 牛(NP_001077000.1); 小鼠(NP_080046.3); 大鼠(XP_032752943.1); 酿酒酵母(NP_009475.1)
Figure 1. A phylogenetic tree was constructed based on the amino acid sequences of ATG10 from large yellow croaker and other vertebrates
The phylogenetic tree was constructed by MEGA 7.0 using Maximum Likelihood method. The GenBank accession numbers for protein sequences used here as followed, Larimichthys crocea (XP_027143515.1); Sparus aurata (XP_030257561.1); Epinephelus lanceolatus (XP_033505554.1); Cyprinodon tularosa (XP_038133305.1); Cynoglossus semilaevis (XP_024908216.1); Oncorhynchus mykiss(XP_036823990.1); Oncorhynchus keta (XP_035628463.1); Danio rerio (NP_001032201.1); Xenopus tropicalis (XP_031749390.1); Gallus gallus (XP_015136200.1); Homo sapiens (NP_113670.1); Bos Taurus (NP_001077000.1); Mus musculus (NP_080046.3); Rattus rattus (XP_032752943.1); Saccharomyces cerevisiae (NP_009475.1)
图 2 LcATG10 在大黄鱼组织和免疫相关细胞中的表达模式
A. 分别提取血液、肌肉、皮肤、肠道、脑、胃、鳃、脾脏、肝脏、心脏和头肾组织的RNA, qRT-PCR检测分析各种组织中LcATG10 mRNA的表达, β-actin为内参基因; B. LcATG10在大黄鱼头肾细胞系、原代巨噬细胞、淋巴细胞和粒细胞中的表达水平, β-actin为内参基因
Figure 2. The relative expression of LcATG10 in tissues and immune-related cells
A. RT-PCR was performed to detect LcATG10 expression from different tissues include blood, muscle, skin, intestine, brain, stomach, gill, spleen, liver, heart and head kidney. β-actin was used as a positive control; B. The expression levels of LcATG10 in head kidney cell line, primary macrophage, lymphocytes and neutrophils of large yellow croaker were detected by fluorescence quantitative PCR, and β-actin was used as the internal reference gene
图 3 大黄鱼组织和免疫相关细胞受poly(Ⅰ﹕C)刺激后LcATG10表达变化
大黄鱼头肾(A)、脾脏(B)以及头肾细胞系(LYCK)细胞(C)和原代粒细胞(D)中LcATG10基因的时序表达分析。*代表显著性差异(P<0.05), **代表差异极显著(P<0.01)
Figure 3. Expression levels of LcATG10 in tissues and immune-related cells of large yellow croaker after poly (I﹕C) stimulation
Relative expression of LcATG10 gene in head kidney (A), spleen (B), LYCK cells (C) and primary neutrophils (D) of large yellow croaker stimulated with poly (I:C). * indicates significant difference (P<0.05); ** indicates highly significant difference (P<0.01)
图 4 LcATG10 过表达对病毒复制的影响
A. 免疫印迹检测LcATG10在鲤上皮瘤细胞系(EPC)中的过表达, 空载体作为对照; B. pcDNA3.1-LcATG10 或 pcDNA3.1(作为对照)转染的EPC细胞感染 SVCV, 在感染后 24h 和 48h 显微镜下观察细胞病变效应(放大倍数: 63×); C. 结晶紫染色观察SVCV感染 48h 的细胞病变效应; D. 过表达LcATG10 的EPC 细胞或对照细胞培养上清中病毒滴度, 用50%组织细胞感染量表示; E. 荧光定量PCR检测LcATG10过表达的EPC细胞中SVCV基因的相对表达水平; 病毒基因相对表达水平表示为实验组细胞中SVCV基因的表达水平相对于对照组细胞中的倍数变化。*代表显著性差异(P<0.05), **代表差异极显著(P<0.01)
Figure 4. Effects of LcATG10 overexpression on virus replication
A. Western blotting was used to detect the overexpression of LcATG10 in EPC cell lines; B. EPC cells transfected with pcDNA3.1-LcATG10 or pcDNA3.1 (as control) were infected with SVCV, and the CPEs were observed microscopically at 24h and 48h post-infection; C. Cells were stained with 1% crystal violet for detection of CPEs; D. The titers of SVCV in culture supernatants from LcATG10-overexpressed EPC cells or control cells, which was expressed as 50% tissue culture infectious dose (TCID50); E. The expression levels of the SVCV genes after overexpression of LcATG10 in EPC cells were detected by real-time PCR. * indicates significant difference (P<0.05); ** indicates highly significant difference (P<0.01)
表 1 引物序列
Table 1 Primers information
引物名称Name 序列Sequence (5ʹ-3ʹ) 用途Usage LcATG10-F
LcATG10-R
PcDNA3.1-LcATG10-F
PcDNA3.1-LcATG10-R
RT-LcATG10-F
RT-LcATG10-R
RT-Lcβ-actin-F
RT-Lcβ-actin-R
RT-SVCV-G-F
RT-SVCV-G-R
RT-SVCV-M-F
RT-SVCV-M-R
RT-SVCV-P-F
RT-SVCV-P-R
RT-EPC-actin-F
RT-EPC-actin-RATGAGCTCGAGTGTCCTGGA
GTCTGGCTTGGTGCTGCTGA
ACTGTGCTGGATATCTG
CAGAATTCG
CCACCATGAGCTCGA
GTGTCCTGGA
GGGCCCAAGCTTGGT
ACCGTCTGGC
TTGGTGCTGCTGA
GGGTCCTGTGGTGGGTCTGG
CTGGCTTGGTGCTGCTGAGTG
GACCTGACAGACTACCTCATG
AGTTGAAGGTGGTCTCGTGGA
CGACCTGGATTAGACTTG
AATGTTCCGTTTCTCACT
TACTCCTCCCACTTACGA
CAAGAGTCCGAGAAGGTC
TTGGACCTGGGATAGTGA
CTTGCTTGGTTTGTGGG
TGTTCCAGCCATCCTTCTTG
TGATTTTCATTGTGCTGGGGORF扩增
真核表达载体构建
RT-PCR -
[1] Klionsky D J, Emr S D. Autophagy as a regulated pathway of cellular degradation [J]. Science, 2000, 290(5497): 1717-1721. doi: 10.1126/science.290.5497.1717
[2] Dunn W A Jr. Autophagy and related mechanisms of lysosome-mediated protein degradation [J]. Trends in Cell Biology, 1994, 4(4): 139-143. doi: 10.1016/0962-8924(94)90069-8
[3] Virgin H W, Levine B. Autophagy genes in immunity [J]. Nature Immunology, 2009, 10(5): 461-470. doi: 10.1038/ni.1726
[4] 雷泽慧, 汪静, 刘翠华. 自噬在抗感染免疫中的作用机制研究进展 [J]. 中国免疫学杂志, 2020, 36(12): 1409-1418. doi: 10.3969/j.issn.1000-484X.2020.12.001 Lei Z H, Wang J, Liu C H. Research progress of regulatory roles and mechanisms of autophagy in anti-infection immunity [J]. Chinese Journal of Immunology, 2020, 36(12): 1409-1418. doi: 10.3969/j.issn.1000-484X.2020.12.001
[5] Ahmad L, Mostowy S, Sancho-Shimizu V. Autophagy-virus interplay: from cell biology to human disease [J]. Frontiers in Cell and Developmental Biology, 2018(6): 155.
[6] Klionsky D J. Autophagy revisited: a conversation with Christian de Duve [J]. Autophagy, 2008, 4(6): 740-743. doi: 10.4161/auto.6398
[7] Klionsky D J, Codogno P, Cuervo A M, et al. A comprehensive glossary of autophagy-related molecules and processes [J]. Autophagy, 2010, 6(4): 438-448. doi: 10.4161/auto.6.4.12244
[8] Jordan T X, Randall G. Manipulation or capitulation: virus interactions with autophagy [J]. Microbes Infect, 2012, 14(2): 126-139. doi: 10.1016/j.micinf.2011.09.007
[9] Han Z, Wang W, Lü X, et al. ATG10 (autophagy-related 10) regulates the formation of autophagosome in the anti-virus immune response of pacific oyster (Crassostrea gigas) [J]. Fish & Shellfish Immunology, 2019(91): 325-332.
[10] Kaiser S E, Qiu Y, Coats J E, et al. Structures of Atg7-Atg3 and Atg7-Atg10 reveal noncanonical mechanisms of E2 recruitment by the autophagy E1 [J]. Autophagy, 2013, 9(5): 778-780. doi: 10.4161/auto.23644
[11] Phillips A R, Suttangkakul A, Vierstra R D. The ATG12-conjugating enzyme ATG10 Is essential for autophagic vesicle formation in Arabidopsis thaliana [J]. Genetics, 2008, 178(3): 1339-1353. doi: 10.1534/genetics.107.086199
[12] Shintani T, Mizushima N, Ogawa Y, et al. Apg10p, a novel protein-conjugating enzyme essential for autophagy in yeast [J]. EMBO Journal, 1999, 18(19): 5234-5241. doi: 10.1093/emboj/18.19.5234
[13] Fujita N, Saitoh T, Kageyama S, et al. Differential involvement of Atg16L1 in Crohn disease and canonical autophagy: analysis of the organization of the Atg16L1 complex in fibroblasts [J]. Journal of Biological Chemistry, 2009, 284(47): 32602-32609. doi: 10.1074/jbc.M109.037671
[14] Shoji-Kawata S, Levine B. Autophagy, antiviral immunity, and viral countermeasures [J]. Biochimica et Biophysica Acta, 2009, 1793(9): 1478-1484. doi: 10.1016/j.bbamcr.2009.02.008
[15] Zhao Q, Hu Z Y, Zhang J P, et al. Dual roles of two isoforms of autophagy-related gene ATG10 in HCV-Subgenomic replicon mediated autophagy flux and innate immunity [J]. Scientific Reports, 2017, 7(1): 11250. doi: 10.1038/s41598-017-11105-3
[16] Li C, Wang S, Ren Q, et al. An outbreak of visceral white nodules disease caused by Pseudomonas plecoglossicida at a water temperature of 12℃ in cultured large yellow croaker (Larimichthys crocea) in China [J]. Journal of Fish Diseases, 2020, 43(11): 1353-1361. doi: 10.1111/jfd.13206
[17] Mu Y, Li M, Ding F, et al. De novo characterization of the spleen transcriptome of the large yellow croaker (Pseudosciaena crocea) and analysis of the immune relevant genes and pathways involved in the antiviral response [J]. PLoS One, 2014, 9(5): e97471. doi: 10.1371/journal.pone.0097471
[18] Wang X H, Wang K R, Nie P, et al. Establishment and characterization of a head kidney cell line from large yellow croaker Pseudosciaena crocea [J]. Journal of Fish Biology, 2014, 84(5): 1551-1561. doi: 10.1111/jfb.12386
[19] Ohsumi Y. Molecular dissection of autophagy: two ubiquitin-like systems [J]. Nature Reviews Molecular Cell Biology, 2001, 2(3): 211-216. doi: 10.1038/35056522
[20] Jounai N, Takeshita F, Kobiyama K, et al. The Atg5 Atg12 conjugate associates with innate antiviral immune responses [J]. Proceedings of the National Academy of Sciences of the United States of America, 2007, 104(35): 14050-14055. doi: 10.1073/pnas.0704014104
[21] Jo Y K, Kim S C, Park I J, et al. Increased expression of ATG10 in colorectal cancer is associated with lymphovascular invasion and lymph node metastasis [J]. PLoS One, 2012, 7(12): e52705. doi: 10.1371/journal.pone.0052705
[22] Mizushima N, Yoshimori T, Ohsumi Y. Mouse Apg10 as an Apg12-conjugating enzyme: analysis by the conjugation-mediated yeast two-hybrid method [J]. FEBS Letters, 2002, 532(3): 450-454. doi: 10.1016/S0014-5793(02)03739-0
[23] 张微, 孙鸿, 邢莉萍, 等. 小麦自噬相关基因 ATG10 的克隆及白粉菌侵染诱导的ATG10的表达 [J]. 作物学报, 2014, 40(8): 1392-1402. doi: 10.3724/SP.J.1006.2014.01392 Zhang W, Sun H, Xing L P, et al. Cloning of autophagy-related genes, ATG10s, in wheat and their expression characteristics induced by Blumeria graminis f. sp. tritici [J]. Acta Agronomica Sinica, 2014, 40(8): 1392-1402. doi: 10.3724/SP.J.1006.2014.01392
[24] Wei C C, Luo Z, Song Y F, et al. Identification of autophagy related genes LC3 and ATG4 from yellow catfish Pelteobagrus fulvidraco and their transcriptional responses to waterborne and dietborne zinc exposure [J]. Chemosphere, 2017(175): 228-238.
[25] 何丽, 阮记明, 刘毅, 等. 草鱼自噬相关基因Beclin1的克隆及其在MC-LR 胁迫下的表达特征 [J]. 水生生物学报, 2019, 43(3): 479-485. doi: 10.7541/2019.059 He L, Ruan J M, Liu Y, et al. Cloning of Beclin1, an autophagy gene, and it’s expression under microcystin-lr stress in grass carp (Ctenopharyngodon idella) [J]. Acta Hydrobiologica Sinica, 2019, 43(3): 479-485. doi: 10.7541/2019.059
[26] 孙航, 毛明光, 蒋洁兰, 等. 太平洋鳕 ATG5 基因的克隆及表达分析 [J]. 大连海洋大学学报, 2015, 30(5): 478-483. Sun H, Mao M G, Jiang J L, et al. Cloning and expression of ATG5 gene in Pacific cod Gadus macrocephalus [J]. Journal of Dalian Ocean University, 2015, 30(5): 478-483.
-
期刊类型引用(0)
其他类型引用(1)



 下载:
下载: