THE ROLE OF FUNCTIONAL AMINO ACIDS IN AQUATIC CRUSTACEANS
-
摘要: 传统氨基酸根据其在体内合成能力, 一般分为必需氨基酸和非必需氨基酸。目前最新研究认为, 部分氨基酸除了合成蛋白质以外, 也能够合成一系列功能性物质, 并对动物营养代谢和免疫功能具有十分重要的调节作用, 为此提出功能性氨基酸这一概念。功能性氨基酸在甲壳类促生长、提高免疫和存活率等方面效果显著。近些年来, 甲壳类动物养殖病害严重, 对高效抗病功能性饲料需求较高。功能性氨基酸将在未来甲壳类配合饲料升级中扮演着重要的角色。文章总结功能性氨基酸在甲壳类蜕壳、抗应激、增强饲料诱食性及提高繁殖和幼体培育等方面的具体作用, 为相关功能性饲料技术开发提供参考。Abstract: Traditionally, amino acids are classified as essential amino acids and non-essential amino acids based on their ability of syntheses from metabolic intermediates. Currently, many scientists gave a new concept of functional amino acids, which are defined as those amino acids that participate in and regulate key metabolic pathways and immune systems. These amino acids not only provide blocks for protein synthesis, but also as substrates for many functional compounds. It has been reported that these amino acids can improve health, survival, growth, development, and reproduction of organisms. Crustaceans (e.g., shrimp and crabs) are the second largest aquaculture species worldwide, their feed development play a vital role in industry development. Functional amino acids hold great promise in prevention and treatment of metabolic diseases, intrauterine growth restriction, and infectious diseases (including viral infections). However, there are still some technical difficulties and challenges in the use of crystalline amino acids for research and practical production. At present, the knowledge about amino acid metabolism and functions in crustaceans is still limited, and much of them are based on studies of mammals and fish species. This article highlights current knowledge about the functions of amino acids on molt, adaptation of stress, immune, and antioxidant responses, spawning and larval development of crustaceans. It will help to advance the field of protein nutrition and guide the development of future crustacean feeds.
-
Keywords:
- Amino acids /
- Functional /
- Health /
- Crustaceans
-
甲壳类是重要水产养殖种类, 主要包括十足类虾蟹种类。甲壳动物含有丰富的蛋白质、脂肪酸和矿物盐等多种营养物质, 深受市场欢迎。我国甲壳类水产品资源丰富, 种类繁多, 是世界甲壳类水产品主要供给国。根据2021年中国渔业统计年鉴数据, 2020年我国甲壳类的养殖和捕捞产量分别为603万吨和197万吨。甲壳类水产动物在我国社会经济发展和食品良性供应上发挥着重要的作用。我国主要养殖的甲壳类品种(如南美白对虾 Litopenaeus vannamei、斑节对虾Penaeus monodon、中华绒螯蟹Eriocheir sinensis和三疣梭子蟹Portunus trituberculatus等)均为杂食性或肉食性动物, 能够摄食鱼、虾、贝、藻, 甚至同类相食, 个别种类喜腐食, 对蛋白质和氨基酸要求较高。大部分养殖品种已能够做到利用人工配合饲料进行养殖, 并且效果显著。个别品种, 如三疣梭子蟹和青蟹, 仍以投喂冰鲜杂鱼为主, 由于冰鲜杂鱼品质不稳定, 极易引起污染环境、浪费严重、饲料系数高、易诱发疾病及破坏资源等问题[1]。另一方面, 采用配合饲料养殖甲壳类, 不仅可避免上述缺点, 也能提高养殖动物产品品质与营养价值。
过去几十年里, 我国甲壳类水产养殖产业(尤其对虾产业)得到较好的发展, 相关配套产业(如饲料加工和开发)也比较成熟。但是, 目前主要存在以下几点问题: (1)养殖问题: 个别甲壳类(如对虾)养殖密度高, 且病害严重, 例如南美白对虾的白便问题一直未能得到解决; (2)环境问题: 甲壳类养殖地区水体盐度温度变化大, 养殖密度大, 且养殖池塘底部有害物质沉积严重, 养殖动物长期应对不同养殖胁迫条件, 导致蜕壳和生长受阻; (3)饲料问题: 对虾摄食快慢是决定养殖效果的关键因素之一, 如何在营养方面提高饲料诱食性是关键; (4)产品品质: 我国对个别甲壳类品种(如蟹类)的品质要求较高, 如大众对“红膏蟹”比较青睐。近些年来, 国内外许多研究也报道了甲壳类的基本营养需求, 这在一定程度上为该品种配合饲料的发展提供一定的基础。在三大类营养物质中, 蛋白质(氨基酸)在甲壳类生长、发育和免疫中起到了关键性的作用, 它不仅提供甲壳类所需的能量, 也是其功能性物质的重要成分或前体。因此, 最近几年国内外研究者相继提出“功能性氨基酸”这一概念, 指除了合成蛋白质外还具有其他特殊功能的氨基酸, 其不仅对动物的正常生长及维持是必需的, 而且对多种生物活性物质的合成也是必需的[2]。近些年, 相关工作在甲壳类中得到一定开展。因此, 本文通过总结相关研究工作, 为甲壳类水产养殖动物的饲料开发和技术升级提供理论依据。
1. 提供组织能量
相比较于猪和家禽动物, 鱼类对饲料蛋白质需求量高, 其中主要原因之一是鱼类大量利用氨基酸为能量物质, 而对脂肪酸和葡萄糖作为能源利用相对较低[3, 4]。与鱼类相似, 甲壳类的蛋白质需求量较高, 大多在30%—50%, 例如南美白对虾幼虾蛋白质需求量在40%左右[5-8]。此外, 甲壳类对饲料非蛋白能利用相对有限, 对脂肪和淀粉的需求分别为≤10%和≤20%[9, 10]。另一方面, 甲壳类的饲料氮保留率整体不高, 在17%—30%, 甚至低于一些肉食性鱼类[11-13]。这也间接证明大量饲料氨基酸未能成为体蛋白, 而是直接作为能源被降解。此外, 甲壳类(如南美白对虾和中华绒螯蟹)的耗氧: 氮排率普遍小于40, 也证明氨基酸是其重要的能量底物[14-16]。Rosas 等[17]指出, 南美白对虾能够较好适应以蛋白质为主要能量来源的饲料, 而非基于淀粉基础的饲料。我们同位素示踪实验结果也证明, 氨基酸是南美白对虾的主要能量物质, 当然在各个器官中所占比重有所不同[18]。例如, 谷氨酰胺和天冬氨酸是肌肉重要能量底物, 其氧化效率显著高于其他能量底物 (如葡萄糖和棕榈酸)。南美白对虾鳃部对葡萄糖氧化效率最高, 其次是谷氨酰胺和天冬氨酸。对虾在应对不同胁迫情况下, 往往需要更多能量或功能物质去调节体内生理平衡。例如, 研究发现环境低温及高温均会导致ATP含量增加, 表明南美白对虾在应对温度胁迫的过程中可能需要更多能量[19]。早期研究已表明, 氨基酸(如丙氨酸)是非常重要的功能和能量物质, 在应对环境急性渗透压的变化中起到非常重要的作用[20]。由此可见, 氨基酸作为部分器官或组织的重要能源, 能够保障甲壳类适应不同环境, 也是发挥氨基酸功能性的重要机制之一。另一方面, 关于甲壳类利用氨基酸作为能源的研究相对有限, 相关结论仍存在一定争议, 未来需要大量工作进一步验证。氨基酸也是糖类、脂类和其他功能物质的前体物, 在生理上扮演重要的功能, 这里不做详细介绍。
2. 促进蜕壳
众所周知, 蜕壳是甲壳类养殖非常重要的一个生理环节, 其主要作用是: (1) 生长需要, 蜕去旧壳有利于生长; (2) 繁殖需要; (3) 除去旧壳上的寄生虫和细菌。蜕壳后期水的摄入非常重要, 因为这一过程决定下一生长阶段的身体大小[21]。蜕壳是一种复杂生理活动, 氨基酸在各个阶段中扮演着重要的作用(表 1)。例如, 蜕壳后期是能量和矿物盐的急需期, 需要注意营养物质的充足提供。一般认为, 蜕壳后对钙需求大, 需要根据各个水环境不同盐度和硬度调整钙的补充。但值得注意的是, 虾壳通常含有25%—40%蛋白质、15%—20%几丁质、45%—50%碳酸钙, 15—40 mg/kg虾青素, 其中蛋白质中含有60%胶原蛋白[22, 23]。因此, 氨基酸和蛋白质的补充对蜕壳的成功和新壳的形成起到非常重要的作用。蜕壳和生长并不是完全相关, 在某些非正常条件下, 如温度和盐度刺激可提高蜕壳频率, 但对生长反而无帮助[29, 30]。通过环境因子改变而促进的蜕壳能否带来总体养殖效率的提高还不得而知。已有部分证据表明, 这种方式会引起蜕壳成功率下降, 导致不必要的损失[31-33] 。 与此相反, 通过功能性氨基酸添加, 强化饲料营养而提高蜕壳成功率和生长是比较可取之道。氨基酸在甲壳类蜕壳中扮演的作用已得到一定的研究, 虾体内游离氨基酸的组成也从侧面反映出虾对饲料氨基酸的需求。例如, 游离脯氨酸和甘氨酸被证明是蜕壳期间的重要能量物质, 也是在蜕壳前期合成新壳的重要底物[29, 30]。研究结果表明, 中华绒螯蟹的血清蜕壳激素和蜕皮甾酮随着饲料添加1%—2%精氨酸而增加, 并且可提高蜕壳频率[31]。在表 1中, 我们总结氨基酸在不同蜕壳期间的作用, 相关研究相对有限, 需要进一步验证。
表 1 氨基酸在甲壳类不同蜕壳时期的作用Table 1. Main functions of amino acids at different stages of the molt cycle in shrimp蜕壳时期
Molt cycle阶段
Stage时间
Duration壳状态
Exoskeleton摄食
Feeding氨基酸作用
Main functions
of amino acids后期
PostmoltA 1—2h 软壳 无 调节渗透压,
参与蛋白合成B 2—5h 微硬 微量 间期
IntermoltC 8—10d 外壳完
全硬正常 能量来源和
蛋白合成前期
PremoltD0 1—2d 外壳开
始分解正常 胶原蛋白合成,
渗透压调节,
荷尔蒙释放D1 1—2d 新内壳
未成形下降 D2 2d 新壳形成 下降 D3 1d 旧壳新壳之
间形成裂缝下降 D4 1d 大量吸水、
旧壳裂开无 蜕壳
MoltE 15min 蜕壳 无 提供能量、
渗透压调节注: 蜕壳各个时期分类参考自Rao 等[50]Note: The stages of molt cycle adapted from Rao et al.[50] 3. 抵抗环境胁迫
由于养殖环境复杂多变, 甲壳类动物往往面临环境盐度、温度和氨氮变化等的胁迫。其中, 渗透压调节能力是甲壳类养殖成功的重要因素[32]。相比较于脊椎动物, 甲壳类动物体内含有较高的游离氨基酸, 主要为甘氨酸、谷氨酸、丙氨酸、精氨酸和牛磺酸[33, 34]。研究证实, 血淋巴游离氨基酸水平会随着外界应激条件刺激而产生变动[31]。值得注意的是, 游离谷氨酸、脯氨酸、甘氨酸、丙氨酸、牛磺酸和精氨酸已被证明是海洋无脊椎动物渗透压调节的重要物质[35-39]。例如, 对三疣梭子蟹研究表明, 体内游离氨基酸(主要包括丙氨酸、甘氨酸、天冬氨酸和谷氨酸)在适应环境盐度骤变中发挥着重要的作用[40]。有研究表明, 适当提高饲料蛋白水平是应对盐度应激的有效办法[41]。南美白对虾幼虾投喂含有额外添加的2.26%—2.70%甘氨酸能够有效提高急性盐度刺激下的存活率[42]。在应激条件下, 动物往往需要更多能量去适应新的生活环境。作为甲壳类动物重要的能量物质, 氨基酸在抵抗其他应激中也扮演着比较重要的作用。过去研究结果表明, 氨基酸在提升甲壳类抵抗其他各类胁迫(如低温、饥饿和高氨氮)过程中扮演着重要的角色[36, 43-45]。例如, 高温与氨氮复合胁迫对南美白对虾游离氨基酸含量影响显著, 从而造成南美白对虾渗透压生理调节功能紊乱[38]。此外, 肝胰腺中脯氨酸和丙氨酸的积累是甲壳类适应低温胁迫的主要手段之一[46-48]。对南美白对虾的研究表明, 低鱼粉基础饲料通过添加额外脯氨酸提升饲料脯氨酸从2.02%—2.6%能够显著性增加幼虾抵御高氨氮环境[49]。由此可见, 氨基酸作为能量和渗透压调节物质在抵御各种胁迫中发挥重要的作用。
4. 诱食剂
游离氨基酸已被证明是鱼虾的重要诱食剂。例如, 真龙虾(Panulirus argus)的嗅觉和味觉对牛磺酸及其衍生物非常敏感[51]。对罗氏沼虾的研究表明, 复合氨基酸(甘氨酸+丙氨酸)的诱食效果好于单一氨基酸和中草药, 且氨基酸类诱食剂比中草药更有助于提高罗氏沼虾肝胰腺消化酶的活性[52]。对中华绒螯蟹的研究表明, 各个单体氨基酸(苯丙氨酸除外)都具有一定的诱食效果[53]。值得注意的是, 同一氨基酸在不同种类中的刺激性有一定差别, 甚至起到相反的作用。因此, 相关氨基酸的诱食性在不同甲壳类养殖品种中应该谨慎对待。此外, 酵母粉、乌贼膏、鱼溶浆和磷虾粉等也被认为具有较好的诱食效果[54], 可以和氨基酸配合使用。另一方面, 虽然很多原料或氨基酸对幼虾有较好的摄食刺激性, 但考虑到加工加热等因素, 可能导致有效游离氨基酸减少, 作用减弱。相关研究表明, 乌贼粉和乌贼膏对南美白对虾摄食无显著性提高[55], 这可能与饲料加工方式有关。国外研究者基于氨基酸诱食性原理, 利用金枪鱼副产品水解物加黏合剂与已完成制粒的饲料搅拌混匀, 然后投喂南美白对虾, 诱食效果明显[56]。氨基酸的诱食作用也可能与养殖动物消化能力的提升有关。例如, 微胶囊和晶体蛋氨酸有助于提高南美白对虾肝胰腺蛋白酶的活性[57]。
5. 提高免疫力和抗氧化性
环境胁迫可造成甲壳类的免疫力降低和机体自由基代谢紊乱。氨基酸作为细胞和组织的主要营养成分, 在维护动物的免疫力和抗氧化中发挥着重要的作用[58, 59]。甲壳类没有特异性免疫系统, 而主要依赖非特异性免疫系统抵抗病菌的侵入[60]。研究表明, 南美白对虾受弧菌感染后, 各个组织的氨基酸代谢得到一定改变以应对感染后能量需求的增加。例如, 酪氨酸在鳃和肝胰腺中的代谢均表现出显著变化[61]。目前关于各个氨基酸在甲壳类动物中的作用尚未全面展开, 但个别报道已证实相关氨基酸具有一定增加免疫的作用。例如, 精氨酸代谢可产生NO、多胺和磷酸精氨酸, 能够提高机体免疫力[28]。对南美白对虾的研究表明, NO介导的信号传导可能在应对高温胁迫中起着重要作用[19]。对中华绒螯蟹的研究表明, 饲料添加1%—2%精氨酸能够提高生长、存活率及抗病力[31]。另一个研究也表明, 饲料添加0.47%或者0.73%的色氨酸能够提高抗病力和存活率[62]。对斑节对虾的研究表明, 复合植物蛋白源并添加包膜赖氨酸和蛋氨酸可降低饲料中20%的鱼粉用量, 并增强对虾非特异性免疫力[63]。如表 2所示, 近些年已有研究表明, 相关传统非必需氨基酸(如甘氨酸、脯氨酸和谷氨酸)及其代谢产物具有相关功能作用, 尤其可提高免疫力和抗应激能力, 从而促进生长。考虑到近些年对虾养殖病害频发, 养殖成功率较低, 在原有配方基础之上, 适当添加相关功能性氨基酸意义重大。相关研究工作亟待开展。
表 2 不同氨基酸及其代谢产物在水产甲壳类动物中的作用Table 2. Nutritional and physiological functions of amino acids and their metabolites in crustaceans氨基酸Amino acid 代谢物Metabolite 主要作用Main fuction 品种Species 参考文献Reference 精氨酸Arg NO和多胺 提高抗氧化和免疫力 中国对虾; 日本囊对虾; 南美白对虾 [76] 精氨酸Arg 磷酸精氨酸 能量储存物质, 参与渗透压调节 蓝蟹和岸蟹 [77, 78] 精氨酸、鸟氨酸和蛋氨酸Arg, Orn and Met NO、多胺、牛磺酸和
磷酸精氨酸参与渗透压和离子调节 蓝蟹 [79] 谷氨酰胺、甘氨酸和天冬
氨酸Gln, Gly and Asp核苷酸和ATP 抗氧化和提高生长 斑节对虾 [80, 81] 赖氨酸和蛋氨酸
Lys and Met肉碱、牛磺酸和多胺 提高免疫力、抗氧化和能量代谢 南美白对虾和窄爪小龙虾 [82, 83] 谷氨酰胺Gln 氨基葡萄糖、谷氨酸、
ATP作为性识别糖蛋白合成底物; 提
高伤口愈合速度和维持正常健
康养殖鞭藻虾 [84, 85] 甘氨酸Gly 谷胱甘肽 提高生长、抗氧化和免疫力 南美白对虾 [86] 脯氨酸Pro 1-吡咯啉-5-羧酸 提高生长、抗氧化力和免疫力 南美白对虾 [49] 谷氨酸Glu GABA和ATP 提高生长、抗氧化系统和抗应激能量 南美白对虾 [85] 色氨酸Try 血清素, 褪黑素 调节生长、繁殖和残杀行为 斑节对虾和青蟹 [87, 88] 牛磺酸Tau 牛磺胆酸和羟乙基磺酸 提高免疫力、生长和脂肪利用 日本沼虾和南美白对虾 [89—91] 注: GABA, γ-氨基丁酸Note: GABA, γ-aminobutyric acid 活性氧自由基(ROS)具有很强的化学反应活性, 使蛋白质失活, 造成生物膜系统和生物结构的损坏, 也可引起细胞DNA和RNA在结构和功能上的损伤, 并进一步造成器官的损害[64]。内源性抗氧化是控制自由基和组织氧化损伤的重要防御体系, 主要包括超氧化物歧化酶、谷胱甘肽、谷胱甘肽过氧化物酶、谷胱甘肽还原酶、过氧化氢酶(一种含血红素的酶)和抗氧化性营养素。氨基酸及其衍生物是甲壳类重要的抗氧化剂。例如, 谷胱甘肽由谷氨酸、胱氨酸和甘氨酸合成, 是一种具有较强抗氧化性的营养物质。饲料添加0.2 g/kg谷胱甘肽能够有效提高南美白对虾免疫力和抗氧化能力[65]。另一个实验研究表明, 饲料甘氨酸水平高于2.44%能够有效提高对虾在高盐度刺激下的抗氧化和抗病力[42]。
6. 提高繁殖和幼体培育
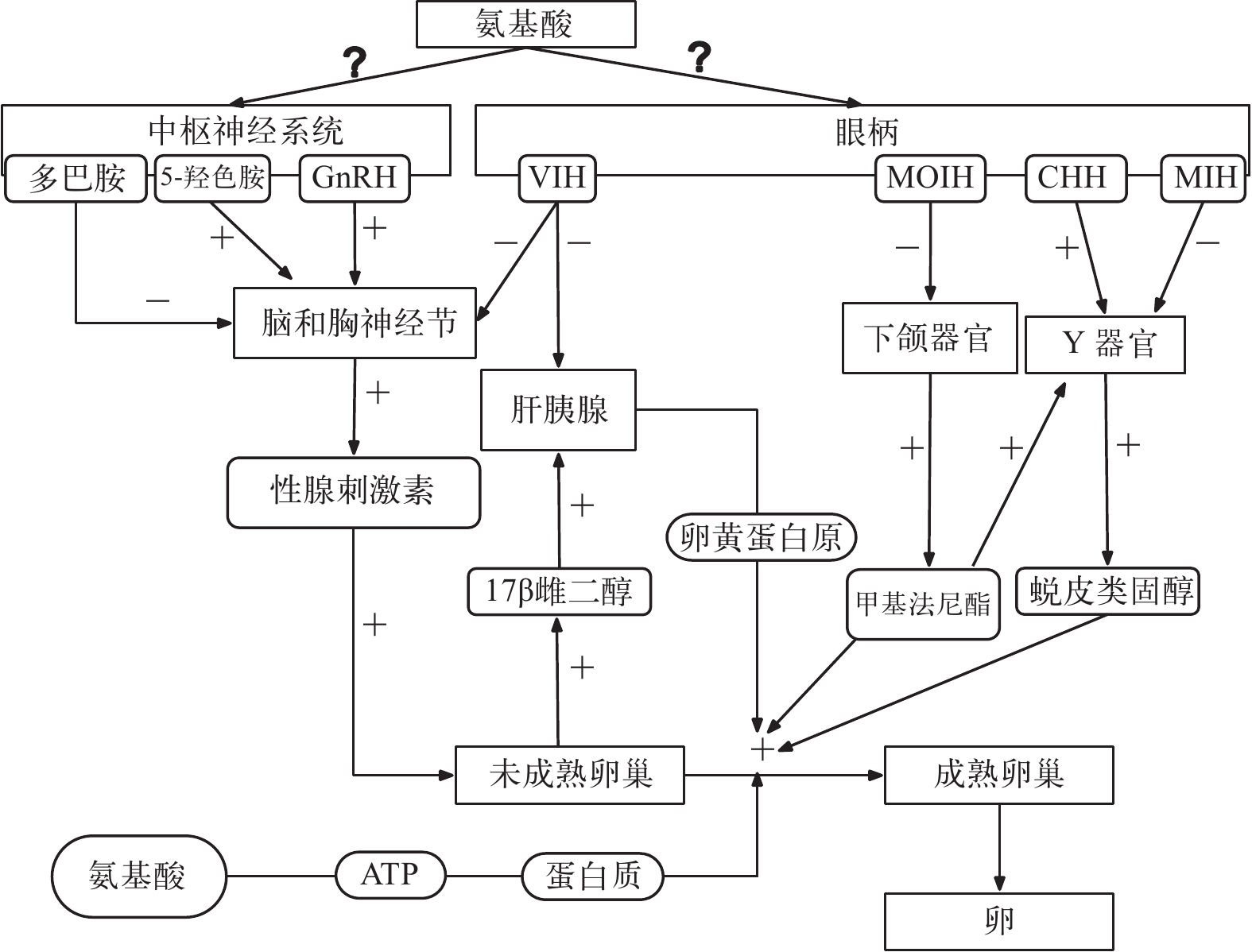
已有证据表明氨基酸在性腺发育中扮演重要角色, 进而影响甲壳类的繁殖。此外, 养殖蟹类的卵巢是重要的可食用部位, 其发育好坏也决定了商品的价值。卵黄原蛋白生成是其卵巢发育的重要步骤, 该蛋白主要合成于肝胰腺和卵巢, 受一系列激素调控, 并在卵巢积累(图 1)。 温为庚等[66]通过分析野生斑节对虾卵巢发育过程中不同组织的氨基酸组成发现, 随着卵巢发育, 野生斑节对虾卵巢的氨基酸总量逐渐上升, 但到临产时下降, 而必需氨基酸总量整体逐渐上升。早期卵巢氨基酸积累主要受大量卵黄蛋白积累影响, 而总氨基酸后期下降可能原因之一是大量非必需氨基酸作为能源被消耗。通过同位素示踪技术, 我们在蓝蟹(Callinectes sapidus)中的研究(相关数据暂未发表)表明, 谷氨酸和天冬氨酸在卵巢中的氧化效率分别为5.62和2.09 [nmol CO2/(mg 组织·2h)], 远高于葡萄糖和棕榈酸的氧化效率, 分别为0.08和0.74 [nmol CO2/(mg 组织·2h)]。由此可见, 卵巢可能主要以氨基酸(谷氨酸和天冬氨酸)作为能量底物, 而非葡萄糖和脂肪酸。此外, 处于卵巢中期发育阶段的野生斑节对虾中, 卵巢的天冬氨酸、 谷氨酸、脯氨酸、酪氨酸和赖氨酸质量分数达到极大值, 总和占总氨基酸 的 42.5%[66]。这点印证了在实际生产中, 养殖户往往为了促使对虾卵巢发育, 会投喂沙蚕、乌贼和牡蛎等作为饵料, 其中以沙蚕的效果最好。这可能与饵料中富含相关氨基酸有关。此外, 部分实验已证明, 氨基酸可对甲壳类动物的激素分泌产生调控作用。例如, 中华绒螯蟹血清的生长激素和肝胰腺的IGF2激素会随着饲料精氨酸的添加而增加[31]。氨基酸可能通过调控激素分泌而控制卵巢发育, 相关研究相对有限, 大量研究亟待展开。
![]() 图 1 甲壳类雌性卵巢发育调控机制以及氨基酸可能存在的作用CHH. 甲壳类高血糖激素; GnRH. 促性腺激素释放激素; MOIH. 下颌器官抑制激素; MIH. 蜕皮抑制激素; VIH. 抑制卵黄生成素; ‘+’ 和‘−’ 分别代表激活和抑制; 参考自 Pamuru [73] 和 Subramoniam[74, 75]Figure 1. Roles of internal and external factors in the regulation of reproduction in female crustaceansCHH. Crustacean hyperglycemic hormone, GnRH. Gonadotropin-releasing hormone, MOIH. Mandibular organ-inhibiting hormone, MIH. Molt-inhibiting hormone, VIH. Vitellogenesis-inhibiting hormone, ‘+’ and ‘−’ denotes activation and inhibition, respectively (Adapted from Pamuru [73] and Subramoniam [74, 75])
图 1 甲壳类雌性卵巢发育调控机制以及氨基酸可能存在的作用CHH. 甲壳类高血糖激素; GnRH. 促性腺激素释放激素; MOIH. 下颌器官抑制激素; MIH. 蜕皮抑制激素; VIH. 抑制卵黄生成素; ‘+’ 和‘−’ 分别代表激活和抑制; 参考自 Pamuru [73] 和 Subramoniam[74, 75]Figure 1. Roles of internal and external factors in the regulation of reproduction in female crustaceansCHH. Crustacean hyperglycemic hormone, GnRH. Gonadotropin-releasing hormone, MOIH. Mandibular organ-inhibiting hormone, MIH. Molt-inhibiting hormone, VIH. Vitellogenesis-inhibiting hormone, ‘+’ and ‘−’ denotes activation and inhibition, respectively (Adapted from Pamuru [73] and Subramoniam [74, 75])蛋白质和氨基酸也是甲壳类卵和幼体的主要组成成分, 在其发育和生长中扮演着十分重要的角色[67, 68]。繁殖亲本的营养状态往往影响卵的营养组成并影响其质量。例如, 相比较于35%蛋白组, 投喂45%蛋白饲料的白滨对虾(Litopenaeus setiferus)拥有更好的精子质量[69]。此外, 甲壳类幼体的游离氨基酸不但提供能量, 还能刺激蛋白合成, 从而促进生长和发育[70]。例如, 南白对虾幼体投喂牛磺酸强化轮虫能提高其存活率和发育[71]。类似的, 通过强化卤虫的赖氨酸含量投喂南美白对虾幼体, 可提高幼体的存活率、生长和抗逆性[70]。因此, 在早期甲壳类动物生长和发育中, 足量的氨基酸补充发挥十分关键的作用。例如, 通过优化藻类培养方式, 可以提升氨基酸含量和质量, 从而达到甲壳类幼体开口饵料营养的强化[72]。
7. 研究现状和前景
综上所述, 氨基酸在甲壳类发育、生长和繁殖过程中扮演着十分重要的作用(表 2)。因此, 合适的饲料氨基酸添加对养殖甲壳类的生长、健康和产品品质具有重要的影响。当前, 商业饲料的氨基酸使用主要集中在传统必需氨基酸(如赖氨酸和蛋氨酸)的添加, 主要评价指标仍然以生长和饲料利用率为主。近些年来, 养殖环境越发恶劣, 养殖动物健康问题频发, 通过传统生长实验得出的氨基酸适宜添加量满足不了功能性的额外需求。因此, 通过额外补充一定形式的氨基酸来调控甲壳类健康养殖是未来发展途径之一。近些年来, 富含功能性氨基酸小肽类原料也越来越受行业关注, 但相关应用效果在不同条件和品种中有一定差异。通过了解相关功能性氨基酸作用及需求量, 也有助于我们进一步精细化使用这些功能性原料。
目前, 关于甲壳类相关功能性氨基酸代谢和作用的研究仍然十分薄弱, 大量工作亟待开展。主要问题集中于以下几个方面: (1)氨基酸在不同养殖甲壳类动物中的代谢特征尚未阐明, 导致研究基础相对薄弱, 大量理论参考于鱼类甚至是哺乳类动物; (2)甲壳类动物特殊的摄食行为方式可能导致游离氨基酸出现一定的溶失, 影响应用效果, 相关数据薄弱; (3)不同地区或种类的甲壳类养殖环境差异较大, 如何发挥特定条件下的功能性氨基酸的应用技术是未来重点工作之一。
-
图 1 甲壳类雌性卵巢发育调控机制以及氨基酸可能存在的作用
CHH. 甲壳类高血糖激素; GnRH. 促性腺激素释放激素; MOIH. 下颌器官抑制激素; MIH. 蜕皮抑制激素; VIH. 抑制卵黄生成素; ‘+’ 和‘−’ 分别代表激活和抑制; 参考自 Pamuru [73] 和 Subramoniam[74, 75]
Figure 1. Roles of internal and external factors in the regulation of reproduction in female crustaceans
CHH. Crustacean hyperglycemic hormone, GnRH. Gonadotropin-releasing hormone, MOIH. Mandibular organ-inhibiting hormone, MIH. Molt-inhibiting hormone, VIH. Vitellogenesis-inhibiting hormone, ‘+’ and ‘−’ denotes activation and inhibition, respectively (Adapted from Pamuru [73] and Subramoniam [74, 75])
表 1 氨基酸在甲壳类不同蜕壳时期的作用
Table 1 Main functions of amino acids at different stages of the molt cycle in shrimp
蜕壳时期
Molt cycle阶段
Stage时间
Duration壳状态
Exoskeleton摄食
Feeding氨基酸作用
Main functions
of amino acids后期
PostmoltA 1—2h 软壳 无 调节渗透压,
参与蛋白合成B 2—5h 微硬 微量 间期
IntermoltC 8—10d 外壳完
全硬正常 能量来源和
蛋白合成前期
PremoltD0 1—2d 外壳开
始分解正常 胶原蛋白合成,
渗透压调节,
荷尔蒙释放D1 1—2d 新内壳
未成形下降 D2 2d 新壳形成 下降 D3 1d 旧壳新壳之
间形成裂缝下降 D4 1d 大量吸水、
旧壳裂开无 蜕壳
MoltE 15min 蜕壳 无 提供能量、
渗透压调节注: 蜕壳各个时期分类参考自Rao 等[50]Note: The stages of molt cycle adapted from Rao et al.[50] 表 2 不同氨基酸及其代谢产物在水产甲壳类动物中的作用
Table 2 Nutritional and physiological functions of amino acids and their metabolites in crustaceans
氨基酸Amino acid 代谢物Metabolite 主要作用Main fuction 品种Species 参考文献Reference 精氨酸Arg NO和多胺 提高抗氧化和免疫力 中国对虾; 日本囊对虾; 南美白对虾 [76] 精氨酸Arg 磷酸精氨酸 能量储存物质, 参与渗透压调节 蓝蟹和岸蟹 [77, 78] 精氨酸、鸟氨酸和蛋氨酸Arg, Orn and Met NO、多胺、牛磺酸和
磷酸精氨酸参与渗透压和离子调节 蓝蟹 [79] 谷氨酰胺、甘氨酸和天冬
氨酸Gln, Gly and Asp核苷酸和ATP 抗氧化和提高生长 斑节对虾 [80, 81] 赖氨酸和蛋氨酸
Lys and Met肉碱、牛磺酸和多胺 提高免疫力、抗氧化和能量代谢 南美白对虾和窄爪小龙虾 [82, 83] 谷氨酰胺Gln 氨基葡萄糖、谷氨酸、
ATP作为性识别糖蛋白合成底物; 提
高伤口愈合速度和维持正常健
康养殖鞭藻虾 [84, 85] 甘氨酸Gly 谷胱甘肽 提高生长、抗氧化和免疫力 南美白对虾 [86] 脯氨酸Pro 1-吡咯啉-5-羧酸 提高生长、抗氧化力和免疫力 南美白对虾 [49] 谷氨酸Glu GABA和ATP 提高生长、抗氧化系统和抗应激能量 南美白对虾 [85] 色氨酸Try 血清素, 褪黑素 调节生长、繁殖和残杀行为 斑节对虾和青蟹 [87, 88] 牛磺酸Tau 牛磺胆酸和羟乙基磺酸 提高免疫力、生长和脂肪利用 日本沼虾和南美白对虾 [89—91] 注: GABA, γ-氨基丁酸Note: GABA, γ-aminobutyric acid -
[1] 方怀义, 林海涵, 王秀娟, 等. 青蟹营养需求的研究进展 [J]. 饲料研究, 2019, 497(10): 108-111. doi: 10.13557/j.cnki.issn1002-2813.2019.10.025 Fang H Y, Lin H H, Wang X J, et al. Advances in the nutritional requirements for mud crab (Scylla serrata) [J]. Feed Research, 2019, 497(10): 108-111. doi: 10.13557/j.cnki.issn1002-2813.2019.10.025
[2] 孔祥峰, 印遇龙, 伍国耀. 猪功能性氨基酸营养研究进展 [J]. 动物营养学报, 2009, 21(1): 1-7. doi: 10.3969/j.issn.1006-267x.2009.01.001 Kong X F, Yin Y L, Wu G Y. Research advances in functional amino acid nutrition of pigs [J]. Chinese Journal of Animal Nutrition, 2009, 21(1): 1-7. doi: 10.3969/j.issn.1006-267x.2009.01.001
[3] Li X L, Zheng S X, Jia S C, et al. Oxidation of energy substrates in tissues of largemouth bass (Micropterus salmoides) [J]. Amino Acids, 2020, 52(6-7): 1017-1032. doi: 10.1007/s00726-020-02871-y
[4] Jia S, Li X, Zheng S, et al. Amino acids are major energy substrates for tissues of hybrid striped bass and zebrafish [J]. Amino Acids, 2017, 49(12): 2053-2063. doi: 10.1007/s00726-017-2481-7
[5] Cuzon G, Lawrence A, Gaxiola G, et al. Nutrition of Litopenaeus vannamei reared in tanks or in ponds [J]. Aquaculture, 2004(235): 513-551.
[6] Unnikrishnan U, Paulraj R. Dietary protein requirement of giant mud crab Scylla serrata juveniles fed iso-energetic formulated diets having graded protein levels [J]. Aquaculture Research, 2010, 41(2): 278-294. doi: 10.1111/j.1365-2109.2009.02330.x
[7] Jin M, Zhou Q C, Zhang W, et al. Dietary protein requirements of the juvenile swimming crab, Portunus trituberculatus [J]. Aquaculture, 2013(414): 303-308.
[8] Mente E. Protein nutrition in crustaceans [J]. CAB Reviews: Perspectives in Agriculture, Veterinary Science, Nutrition and Natural Resources, 2006, 1(43): 1—5.
[9] NRC. Nutrient requirements of fish and shrimp, Animal Nutrition Series, National Research Council of the National Academies [M]. Washington, DC, 2011: The National Academies Press
[10] Wang X, Li E, Chen L (2016). A review of carbohydrate nutrition and metabolism in crustaceans [J]. North American Journal of Aquaculture, 2016, 78(2): 178-187. doi: 10.1080/15222055.2016.1141129
[11] Bulbul M, Kader M A, Asaduzzaman M, et al. Can canola meal and soybean meal be used as major dietary protein sources for kuruma shrimp, Marsupenaeus japonicus [J]? Aquaculture, 2016(452): 194-199.
[12] Panini R L, Freitas L E L, Guimarães A M, et al. Potential use of mealworms as an alternative protein source for Pacific white shrimp: digestibility and performance [J]. Aquaculture 2017 (473): 115-120.
[13] Qiu X, Davis D A. Effects of dietary phytase supplementation on growth performance and apparent digestibility coefficients of Pacific white shrimp Litopenaeus vannamei [J]. Aquaculture Nutrition, 2017, 23(5): 942-951. doi: 10.1111/anu.12462
[14] Coelho R T I, Yasumaru F A, Passos M J A C R, et al. Energy budgets for juvenile Pacific whiteleg shrimp Litopenaeus vannamei fed different diets [J]. Brazilian Journal of Oceanography, 2019, (67):1—8.
[15] Comoglio L I, Gaxiola G, Roque A, et al. The effect of starvation on refeeding, digestive enzyme activity, oxygen consumption and ammonia excretion in juvenile white shrimp Litopenaeus vannamei [J]. Journal of Shellfish Research, 2004, 23(1): 243-250.
[16] Zhang C, Zhang Q, Song X, et al. L-tryptophan promotes the cheliped regeneration of Chinese mitten crab (Eriocheir sinensis) through melatonin, serotonin and dopamine involvement [J]. Aquaculture, 2019(511): 734205.
[17] Rosas C, Cuzon G, Gaxiola G, et al. An energetic and conceptual model of the physiological role of dietary carbohydrates and salinity on Litopenaeus vannamei juveniles [J]. Journal of Experimental Marine Biology and Ecology, 2002, 268(1): 47-67. doi: 10.1016/S0022-0981(01)00370-7
[18] Li X Y and Wu G Y. Oxidation of Energy Substrates in Tissues of Whiteleg Shrimp [C]. Abstracts Book. Aquaculture America, 2020: 273.
[19] 朱孟凯, 姚翠鸾. 温度胁迫对凡纳滨对虾肝胰腺氧代谢及能量代谢的影响 [J]. 水产学报, 2015, 39(5): 670-679. Zhu M K, Yao C L. The impact of temperature stress on the oxygen metabolism and energy metabolism in the hepatopancreas of shrimp Litopenaeus vannamei [J]. Journal of Fisheries of China, 2015, 39(5): 670-679.
[20] Pressley T A, Graves J S. Increased amino acid oxidation in the gills of blue crabs acclimated to dilute seawater [J]. Journal of Experimental Zoology, 1983, 226(1): 45-51. doi: 10.1002/jez.1402260107
[21] Chang E. Endocrinology [M]//Fast A W, Lester L J (Eds.), Marine Shrimp Culture: Principles and Practices, Amsterdam: Elsevier, 1992: 53-91.
[22] Ong L K, Danujatmiko Z, Aylianawati, et al. The prospect of shrimp shell waste as raw material in the gelatin production [J]. ARPN Journal of Engineering and Applied Sciences, 2014, 9(11): 2035-2038.
[23] Rødde R H, Einbu A, Vårum K M. A seasonal study of the chemical composition and chitin quality of shrimp shells obtained from northern shrimp (Pandalus borealis) [J]. Carbohydrate Polymers, 2008, 71(3): 388-393. doi: 10.1016/j.carbpol.2007.06.006
[24] Allan G L, Maguire G B. Effects of pH and salinity on survival, growth and osmoregulation in Penaeus monodon Fabricius [J]. Aquaculture, 1992(107): 33-47.
[25] Chen J C, Lin M N, Lin J L, et al. Effect of salinity on growth of Penaeus chinensis juveniles [J]. Comparative Biochemistry and Physiology, 1992(102A): 343-346.
[26] Mugnier C, Soyez C. Response of the blue shrimp Litopenaeus stylirostris to temperature decrease and hypoxia in relation to molt stage [J]. Aquaculture, 2005(244): 315-322.
[27] Jia X, Ding S, Wang F, et al. A comparative study on the nonspecific immunity of juvenile Litopenaeus vannamei ever inhabiting freshwater and seawater [J]. Journal of Ocean University of China, 2014(13): 472-478.
[28] Li X, Han T, Zheng S, et al. Nutrition and Functions of Amino Acids in Aquatic Crustaceans [M]. Amino Acids in Nutrition and Health. Springer, Cham. 2021: 169-198.
[29] Claybrook D L. Nitrogen metabolism L. H. Mantel (Eds.), The Biology of Crustacea, 5, Academic Press, N. Y., 1983: 163-213.
[30] Yamaoka L H, Skinner D M. Free amino acid pools in muscle and hemolymph during the molt cycle of the land crab, Gecarcinus lateralis [J]. Comparative Biochemistry and Physiology-Part A:Physiology, 1976, 55(2): 129-134. doi: 10.1016/0300-9629(76)90080-3
[31] Qi C, Wang X, Han F, et al. Arginine supplementation improves growth, antioxidant capacity, immunity and disease resistance of juvenile Chinese mitten crab, Eriocheir sinensis [J]. Fish & Shellfish Immunology, 2019(93): 463-473.
[32] Romano N, Zeng C. Osmoregulation in decapod crustaceans: implications to aquaculture productivity, methods for potential improvement and interactions with elevated ammonia exposure [J]. Aquaculture, 2012(334): 12-23.
[33] Shinji J, Wilder M N. Dynamics of free amino acids in the hemolymph of Pacific whiteleg shrimp Litopenaeus vannamei exposed to different types of stress [J]. Fisheries Science, 2012, 78(6): 1187-1194. doi: 10.1007/s12562-012-0542-0
[34] Miyagawa M, Tabuchi Y, Yamane K, et al. Changes in the free amino acid profile of snow crab Chionoecetes opilio muscle during storage in ice [J]. Agricultural and Biological Chemistry, 1990, 54(2): 359-364.
[35] Tan C H, Choong K Y. Effect of hyperosmotic stress on hemolymph protein, muscle ninhydrin-positive substances and free amino acids in Macrobrachium rosenbergii (De Man) [J]. Comparative Biochemistry and Physiology Part A: Physiology, 1981, 70(4): 485-489. doi: 10.1016/0300-9629(81)92559-7
[36] Chen J M, Chen J C. Study on the free amino acid levels in the hemolymph, gill, hepatopancreas and muscle of Penaeus monodon exposed to elevated ambient ammonia [J]. Aquatic Toxicology, 2000, 50(1-2): 27-37. doi: 10.1016/S0166-445X(99)00095-8
[37] Liu H Y, Sun W W, Tan B P, et al. Molecular cloning and expression of hepatopancreas glutamine synthetase in the Pacific white shrimp, Litopenaeus vannamei, induced by acute hypo-osmotic stress [J]. Aquaculture, 2012(362): 80-87.
[38] Chakrapani V, Rasal K D, Mohapatra S D, et al. Molecular characterization, computational analysis and transcript profiling of glutamate dehydrogenase (gdh) gene of Macrobrachium rosenbergii exposed to saline water [J]. Gene Reports, 2017(8): 37-44.
[39] 黄凯, 蒋焕超, 吴宏玉, 等. 盐度对凡纳滨对虾肌肉中游离氨基酸含量的影响 [J]. 海洋渔业, 2010, 32(4): 422-426. doi: 10.3969/j.issn.1004-2490.2010.04.012 Huang K, Jiang H C, Wu H Y, et al. Salinity responses of free amino acids in the muscle of Litopenaeus vannamei [J]. Marine Fisheries, 2010, 32(4): 422-426. doi: 10.3969/j.issn.1004-2490.2010.04.012
[40] Fu P, Liu P, Li J, et al. Effects of different salinity level on free amino acid composition in muscle and hemolymph of the swimming crab Portunus trituberculatus. Journal of Fisheries of China, 2017, 41(3): 374-381.
[41] Li E, Wang X, Chen K, et al. Physiological change and nutritional requirement of Pacific white shrimp Litopenaeus vannamei at low salinity [J]. Reviews in Aquaculture, 2015, 9(1): 57-75.
[42] Xie S W, Tian L X, Jin Y, et al. Effect of glycine supplementation on growth performance, body composition and salinity stress of juvenile Pacific white shrimp, Litopenaeus vannamei fed low fishmeal diet [J]. Aquaculture, 2014, 418: 159-164.
[43] 熊大林, 段亚飞, 陈成勋, 等. 高温与氨氮复合胁迫对凡纳滨对虾渗透调节的影响 [J]. 水产科学, 2021, 40(4): 475-482 Xiong D L, Duan Y F, et al. Combined effects of high temperature and ammonia stress on osmoregulation of pacific white shrimp Litopenaeus vannamei [J]. Fisheries Science, 2021, 40(4): 475-482.
[44] Chen J C, Cheng S Y, Chen C T. Changes of haemocyanin, protein and free amino acid levels in the haemolymph of Penaeus japonicus exposed to ambient ammonia [J]. Comparative Biochemistry and Physiology - Part A, 1994 (109): 339–347.
[45] Zhou M, Wang A L, Xian J A. Variation of free amino acid and carbohydrate concentrations in white shrimp, Litopenaeus vannamei: effects of continuous cold stress [J]. Aquaculture, 2011(317): 182-186.
[46] Hanzal R, Jegorov A. Changes in free amino acid composition in haemolymph of larvae of the wax moth, Galleria mellonella L., during cold acclimation [J]. Comparative Biochemistry and Physiology - Part A, 1991(100): 957-962.
[47] Fields P G, Fleurat-Lessard F, Lavenseau L, et al. The effect of cold acclimation and deacclimation on cold tolerance, trehalose and free amino acid levels in Sitophilus granarius and Cryptolestes ferrugineus (Coleoptera) [J]. Journal of Insect Physiology, 1998(44): 955-965.
[48] Liu Z, Zhou Z, Wang L, Li M, et al. Dopamine and serotonin modulate free amino acids production and Na+/K+ pump activity in Chinese mitten crab Eriocheir sinensis under acute salinity stress [J]. Frontiers in Physiology, 2018(9): 1080.
[49] Xie S W, Tian L X, Li Y M, et al. Effect of proline supplementation on anti-oxidative capacity, immune response and stress tolerance of juvenile Pacific white shrimp, Litopenaeus vannamei [J]. Aquaculture, 2015(448): 105-111.
[50] Rao M S, Rajitha B, Pavitra E, et al. Changes of copper and protein profiles in hepatopancreas and hemolymph tissues during different molt stages of white shrimp, Litopenaeus vannamei (Boone, 1931). Biotechnology, 2008 (7): 153-156.
[51] Fuzessery Z M, Carr W E, Ache B W. Antennular chemosensitivity in the spiny lobster, Panulirus argus: studies of taurine sensitive receptors [J]. The Biological Bulletin, 1978, 154(2): 226-240. doi: 10.2307/1541124
[52] 叶陈静, 杨霞, 沈小燕, 等. 五种诱食剂对罗氏沼虾生长性能及消化酶活性的影响 [J]. 湖州师范学院学报, 2016, 38(8): 75-80. doi: 10.3969/j.issn.1009-1734.2016.08.013 Ye C J, Yang X, Shen X Y, et al. Effect of five attractants on growth performance and digestive enzyme activities of freshwater prawn, Macrobrachium Rosenbergii [J]. Journal of Huzhou University, 2016, 38(8): 75-80. doi: 10.3969/j.issn.1009-1734.2016.08.013
[53] 杨学华. 河蟹饲料用新型诱食剂的比较研究 [D]. 苏州: 苏州大学, 2009: 21-29. Yang X Y. A new comparative study of Eriocheir sinensis phagostimulant [D]. Suzhou: Suzhou University, 2009: 21-29
[54] Hernández C, Olvera-Novoa M A, Smith D M, et al. Enhancement of shrimp Litopenaeus vannamei diets based on terrestrial protein sources via the inclusion of tuna by-product protein hydrolysates [J]. Aquaculture, 2011(317): 117-123.
[55] Zhou Y, Thirumurugan R, Wang Q, et al. Use of dry hydrolysate from squid and scallop product supplement in plant based practical diets for Pacific white shrimp Litopenaeus vannamei [J]. Aquaculture, 2016(465): 53-59. doi: 10.1016/j.aquaculture.2016.08.028
[56] Cobos J V. and Farías C V. Study about the use of aquaculture binder with tuna attractant in the feeding of white shrimp (Litopenaeus vannamei) [J]. Revista Mexicana de Ingeniería Química, 2000, 19(1): 355-361.
[57] Guo J, Zhou W, Liu S, et al. Efficacy of crystalline methionine and microencapsulation methionine in diets for Pacific white shrimp Litopenaeus vannamei [J]. Aquaculture Research, 2020, 51(10): 4206-4214. doi: 10.1111/are.14762
[58] Trichet V V. Nutrition and immunity: an update [J]. Aquaculture Research, 2010, 41(3): 356-372. doi: 10.1111/j.1365-2109.2009.02374.x
[59] Li P, Yin Y L, Li D, et al. Amino acids and immune function [J]. British Journal of Nutrition, 2007, 98(2): 237-252. doi: 10.1017/S000711450769936X
[60] Vazquez L, Alpuche J, Maldonado G, et al. Immunity mechanisms in crustaceans [J]. Innate Immunity, 2009, 15(3): 179-188. doi: 10.1177/1753425909102876
[61] Ma S, Kim A, Lee W, et al. Vibrio harveyi infection significantly alters amino acid and carbohydrate metabolism in whiteleg shrimp, litopenaeus vannamei [J]. Metabolites, 2020, 10(6): 265. doi: 10.3390/metabo10060265
[62] Yang X, Xu M, Huang G, et al. Effect of dietary L-tryptophan on the survival, immune response and gut microbiota of the Chinese mitten crab, Eriocheir sinensis [J]. Fish & Shellfish Immunology, 2019(84): 1007-1017.
[63] 张加润, 林黑着, 黄忠, 等. 饲料中用混合植物蛋白并添加氨基酸替代鱼粉对斑节对虾生长及免疫力的影响 [J]. 南方水产科学, 2013, 9(5): 44-50. Zhang J R, Lin H Z, Huang Z, et al. Effects of plant proteins supplemented with amino acids on growth and non-specific immunity of Penaeus monodon [J]. South China Fisheries Science, 2013, 9(5): 44-50.
[64] Fang Y Z, Yang S, Wu G. Free radicals, antioxidants, and nutrition [J]. Nutrition, 2002(18): 872-879.
[65] Xia Z, Wu S. Effects of glutathione on the survival, growth performance and non-specific immunity of white shrimps (Litopenaeus vannamei) [J]. Fish & Shellfish Immunology, 2018(73): 141-144.
[66] 温为庚, 林黑着, 牛津, 等. 野生斑节对虾卵巢发育过程中不同组织的氨基酸组成 [J]. 南方水产科学, 2013, 9(5): 32-36. doi: 10.3969/j.issn.2095-0780.2013.05.006 Wen W G, Lin H Z, Niu J et al. Amino acid composition of different tissues of wild female Penaeus monodon broodstock during ovarian development [J]. South China Fisheries Science, 2013, 9(5): 32-36. doi: 10.3969/j.issn.2095-0780.2013.05.006
[67] Heras H, Gonzalez-Baró MR, Pollero RJ. Lipid and fatty acid composition and energy partitioning during embryo development in the shrimp Macrobrachium borellii [J]. Lipids, 2000, 35(6): 645-651. doi: 10.1007/s11745-000-0569-z
[68] Xu X, Liu X, Tao J. Changes in biochemical composition and digestive enzyme activity during the embryonic development of the marine crab, Charybdis japonica (Crustadea: Decapoda) [J]. Zoological Science, 2013, 30(3): 160-166. doi: 10.2108/zsj.30.160
[69] Goimier Y, Pascual C, Sánchez A, et al. Relation between reproductive, physiological, and immunological condition of Litopenaeus setiferus pre-adult males fed different dietary protein levels (Crustacea; Penaeidae) [J]. Animal Reproduction Science, 2006, 92(1-2): 193-208. doi: 10.1016/j.anireprosci.2005.05.034
[70] Bahabadi N M, Mozanzadeh M T, Agh N, et al. Enriched artemia with L-lysine and DL-methionine on growth performance, stress resistance, and fatty acid profile of Litopenaeus vannamei postlarvae [J]. Journal of Applied Aquaculture, 2018(30): 325-336.
[71] Jusadi D, Ruchyani S, Ekasari J. Improvement of survival and development of Pacific white shrimp Litopenaeus vannamei larvae by feeding taurine enriched rotifers [J]. Jurnal Akuakultur Indonesia, 2011, 10(2): 131-136.
[72] 高金伟, 张文慧, 窦勇, 等. 培养方式对纤细裸藻脂肪酸与氨基酸含量的影响 [J]. 水生生物学报, 2020, 44(3): 631-637. doi: 10.7541/2020.077 Gao J W, Zhang W H, Dou Y et al. Effects of culture mode on fatty acids and amino acids in Euglena gracilis [J]. Acta Hydrobiologica Sinica, 2020, 44(3): 631-637. doi: 10.7541/2020.077
[73] Pamuru R R. Endocrinology of Reproduction in Crustaceans [J]. In Comparative Endocrinology of Animals. IntechOpen. 2019.
[74] Subramoniam T. Mechanisms and control of vitellogenesis in crustaceans [J]. Fisheries Science, 2011, 77(1): 1-21. doi: 10.1007/s12562-010-0301-z
[75] Subramoniam T. Steroidal control of vitellogenesis in Crustacea: a new understanding for improving shrimp hatchery production [J]. Proceedings of the Indian National Science Academy, 2017, 83(3): 595-610.
[76] Jiang G, Yu R, Zhou M. Studies on nitric oxide synthase activity in haemocytes of shrimps Fenneropenaeus chinensis and Marsupenaeus japonicus after white spot syndrome virus infection [J]. Nitric Oxide, 2006(14): 219-227.
[77] Holt S M, Kinsey S T. Osmotic effects on arginine kinase function in living muscle of the blue crab Callinectes sapidus [J]. Journal of Experimental Biology, 2002(205): 1775-1785. doi: 10.1242/jeb.205.12.1775
[78] Kotlyar S, Weihrauch D, Paulsen R S, et al. Expression of arginine kinase enzymatic activity and mRNA in gills of the euryhaline crabs Carcinus maenas and Callinectes sapidus [J]. Journal of Experimental Biology, 2000(203): 2395-2404. doi: 10.1242/jeb.203.16.2395
[79] Lovett D L, Watts S A. Changes in polyamine levels in response to acclimation salinity in gills of the blue crab Callinectes sapidus Rathbun [J]. Comparative Biochemistry and Physiology Part B, 1995(110): 115-119. doi: 10.1016/0305-0491(94)00133-F
[80] Do Huu H, Tabrett S, Hoffmann K, et al. Dietary nucleotides are semiessential nutrients for optimal growth of black tiger shrimp (Penaeus monodon) [J]. Aquaculture, 2012(366): 115-121.
[81] Do Huu H, Tabrett S, Hoffmann K, et al. The purine nucleotides guanine, adenine and inosine are a dietary requirement for optimal growth of black tiger prawn, P. monodon [J]. Aquaculture, 2013(408): 100-105.
[82] Safari O, Atash MMS, Paolucci M. Effects of dietary L-carnitine level on growth performance, immune responses and stress resistance of juvenile narrow clawed crayfish, Astacus leptodactylus leptodactylus Eschscholtz, 1823 [J]. Aquaculture, 2015(439): 20-28. doi: 10.1016/j.aquaculture.2015.01.019
[83] Zhou M, Wu Z, Liang R, et al. Effects of dietary taurine, carnitine and cholesterol supplementation on growth performance and immunological status of Litopenaeus vannamei under cold exposure [J]. Aquaculture Research, 2017(48): 1279-1290. doi: 10.1111/are.12970
[84] Caskey J L, Watson G M, Bauer R T. Studies on contact sex pheromones of the caridean shrimp Palaemonetes pugio: Ⅱ. The role of glucosamine in mate recognition [J]. Invertebrate Reproduction & Development, 2009(53): 105-116.
[85] Martin G G, Castro C, Moy N, et al. N-acetyl-Dglucosamine in crustacean hemocytes; possible functions and usefulness in hemocyte classification [J]. Invertebrate Biology, 2003(122): 265-270.
[86] Xie S W, Li Y T, Zhou W W, et al. Effect of γ-aminobutyric acid supplementation on growth performance, endocrine hormone and stress tolerance of juvenile Pacific white shrimp, Litopenaeus vannamei, fed low fishmeal diet [J]. Aquaculture Nutrition, 2015(23): 54-62.
[87] Wongprasert K, Asuvapongpatana S, Poltana P, et al. Serotonin stimulates ovarian maturation and spawning in the black tiger shrimp Penaeus monodon [J]. Aquaculture, 2006(261): 1447-1454. doi: 10.1016/j.aquaculture.2006.08.044
[88] Laranja J L Q Jr, Quinitio E T, Catacutan M R, et al. Effects of dietary L-tryptophan on the agonistic behavior, growth and survival of juvenile mud crab Scylla serrata [J]. Aquaculture, 2010(310): 84-90. doi: 10.1016/j.aquaculture.2010.09.038
[89] 刘媛, 王维娜, 王安利, 等. 牛磺酸对日本沼虾生长及酚氧化酶活性的影响 [J]. 淡水渔业, 2005, 35(2): 28-30. Liu Y, Wang W N, Wang A L, et al. Effects of taurine on growth of Macrobrachium nipponense and activity of phenoloxidase [J]. Freshwater Fisheries, 2005, 35(2): 28-30.
[90] To V A, Chyng H L, Shuenn D Y. Can dietary with a taurine supplement improve lipid utilization, growth performance, haemolymph parameters and immune responses of white shrimp (Litopenaeus vannamei) [J]? Aquaculture Research, 2021: 6612—6625.
[91] Yue Y R, Liu Y J, Tian L X, et al. The effect of dietary taurine supplementation on growth performance, feed utilization and taurine contents in tissues of juvenile white shrimp (Litopenaeus vannamei, Boone, 1931) fed with low-fishmeal diets [J]. Aquaculture Research, 2013, 44(8): 1317-1325. doi: 10.1111/j.1365-2109.2012.03135.x
-
期刊类型引用(3)
1. 高思惠,马玉芯,刘秀军,夏广清,郭鑫. 鱼鳔氨基酸组成分析及抗氧化活性研究. 粮食与食品工业. 2024(02): 28-32 .  百度学术
百度学术
2. 章梦丹,张俊杰,黄鸿兵,许志强,徐宇,袁孝春,张美琴,邵俊杰. 不同低温循环水暂养时间对克氏原螯虾肌肉品质和健康状况的影响. 江苏农业学报. 2024(05): 905-912 .  百度学术
百度学术
3. 王硕,吴华,李金铭,沈童,武小庆. 天然提取物在影响动物氧化应激中的研究进展. 饲料研究. 2023(18): 145-149 .  百度学术
百度学术
其他类型引用(4)



 下载:
下载: