TRANSCRIPTOME ANALYSIS OF TWO DIFFERENT MORPHOLOGICAL POPULATIONS OF SCYLLA PARAMAMOSAIN UNDER COLD STRESS
-
摘要: 为研究拟穴青蟹(Scylla paramamosain)不同形态群体对温度变化的适应差异, 以Sp1群体(腕节外缘中部都不具有发达的刺)和Sp2群体(至少一只螯足腕节外缘中部具有发达的刺)为研究对象, 选用低温胁迫组(8℃)和对照组(20℃)拟穴青蟹肝胰腺为实验材料, 进行转录组测序。结果显示, 测序共获得81853个Unigene, 平均长度为420 bp, N50为1460 bp, 其中22.33%为已知基因。差异表达基因筛选发现Sp1群体在低温胁迫下共有15773个Unigene显著差异表达, 其中15628个Unigene表达下调, 145个Unigene表达上调, 这些Unigene显著富集于细胞质基质等生物学过程和RNA结合、核糖体结构组分等分子功能, 并进一步富集在核糖体、剪接体和内质网蛋白质加工等信号通路。Sp2群体在低温胁迫下共有323个Unigene显著差异表达, 其中上调114个, 下调209个。这些Unigene显著富集于DNA整合等生物学过程和甾体羟化酶活性、碳酸氢盐跨膜转运体活性等分子功能, 并进一步富集在赖氨酸降解、甘氨酸、丝氨酸和苏氨酸的代谢、精氨酸和脯氨酸的代谢等代谢通路。以上结果表明, 水温从20℃骤降至8℃, Sp1群体大量基因表达下调, 生理活动大幅度降低, 这可能与寒冷的冬季青蟹停止摄食、穴居不动等行为相对应; 而Sp2群体仅调整了物质代谢, 表明Sp2群体可能对温度骤降的响应较为迟缓。利用RT-qPCR验证了转录组数据, 结果证明基于转录组分析比较两种形态群体拟穴青蟹对低温胁迫的响应是可行的, 研究结果将应用于拟穴青蟹耐寒优质品种的选育。Abstract: Scylla paramamosain is an economically important crab species mainly distribute in the southern reaches of the Yangtze River. Based on many years of breeding experience, it is speculated that different morphological populations of Scylla paramamosain have acquired different adaptations to temperature changes. In this study, Sp1 populations, with “one spine on the outer margin of the carpus of cheliped ” and Sp2 populations, with “two spines” were designated research objects, and 8℃ low temperature stress and 20℃ control groups were established. The hepatopancreas was used as a transcriptome source, and an Illumina Hiseq4000 platform was used for sequencing. A total of 81853 Unigenes were obtained by sequencing, with an average length of 420 bp, and an N50 of 1460 bp. Among these, 22.33% were known genes. Screening for differentially expressed genes identified 15773 Unigenes displaying significant differential expression in the Sp1 population under low temperature stress. Of these, 15628 Unigenes were down-regulated, and 145 Unigenes were up-regulated. Functional enrichment analysis revealed that the differentially expressed genes encode abundant cytosolic, RNA binding, and ribosome structural constituent proteins, and were further enriched in signal pathway components including ribosome, spliceosome, and protein processing components in the endoplasmic reticulum. 323 Unigenes were significantly differentially expressed in the Sp2 population under low temperature stress, of which, 209 Unigenes were down-regulated, and 114 Unigenes were up-regulated. Functional enrichment analysis revealed that the differentially expressed genes include abundant contributors to steroid hydroxylase activity, DNA integration, and bicarbonate transmembrane transporter activity, and were also enriched in signal pathways including lysine degradation, glycine, serine, and threonine metabolism, and arginine and proline metabolism. The above results indicated that as water temperature droped from 20℃ to 8℃, expression of a large number of genes was down-regulated in the Sp1 population, and physiological activities were drastically reduced. This may correspond to winter behaviors of Scylla paramamosain, including fasting and dwelling in burrows. By contrast, the Sp2 population mainly adjusted its material metabolism, indicating that the Sp2 population was relatively slow to respond to sudden temperature drops. Transcriptome data has been verified by RT-qPCR, supporting the feasibility of comparing responses of two morphological populations to low temperature stress based on transcriptome analysis. This study will inform selection of cold-tolerant and high-quality varieties for breeding of Scylla paramamosain.
-
Keywords:
- Cold challenge /
- Population /
- Transcriptome analysis /
- Scylla paramamosain
-
黄颡鱼(Tachysurus fulvidraco Richardson)隶属于鲶形目、鲿科、黄颡鱼属[1], 广泛分布于我国长江、黄河和黑龙江等水域, 是我国重要的淡水名优鱼类, 因其肉质细嫩鲜美, 无肌间刺, 营养价值高, 养殖周期短等优点, 一直受到养殖者和消费者的青睐。黄颡鱼2018年全国总产量51.0×107 kg, 从2012年开始年平均增长16.4%, 是我国淡水名优鱼类中增长速度最快、增长速率最稳定的养殖品种[2], 2018年全国淡水鱼类养殖产量排名第9位, 是我国名副其实的淡水名优第一鱼。黄颡鱼生长具有明显的性别二态性, 前期研究我们发现, 在相同养殖环境下, 雄鱼生长速度比雌鱼快120%[3], 达上市规格时雄鱼体重可达雌鱼的2—3倍[4]。
为了提高黄颡鱼养殖群体的生长速度与养殖效益, 我国科研人员做了大量工作, 培育出了2个黄颡鱼新品种, 黄颡鱼“全雄1号”(2010年认定)和杂交黄颡鱼“黄优1号”(2019年认定), 推动了黄颡鱼产业的稳步增长。在新品种的培育过程中, 科研人员对黄颡鱼的性别决定与性别分化机制、性别特异分子标记、性别控制技术、两性生长异形进行了大量深入的研究, 取得了较大的进展[3—14]。黄颡鱼遗传性别决定类型为雄性配子异形(XX-XY), 但是研究发现黄颡鱼性别分化易受到环境因素的影响。虽然黄颡鱼Y染色体上存在潜在性别决定基因pfpdz1[6], 但本研究发现, 在性别分化关键时期, 短期的高温(33℃)处理能诱导部分XX个体发生性逆转。高温诱导遗传型雌鱼性逆转的机制尚不清楚。
研究发现, 高温[4, 15, 22—25]、高密度[26, 27]等应激条件下引起鱼苗雄性化的同时都伴随着皮质醇水平的升高, 使鱼类的性腺都朝着雄性方向分化[20, 28]。Hattori等[15]高温处理银汉鱼(Odontesthes bonariensis)幼鱼中有相当大比例的雌鱼逆转为雄鱼, 与对照组相比, 在高温饲养的幼鱼中检测到较高的皮质醇; Van den Hurk等[29]用皮质醇和皮质酮处理虹鳟(Oncorhynchus mykiss)仔鱼30d, 虹鳟仔鱼出现明显的雄性化, 未发生性逆转雌鱼卵巢发育受到抑制; Hayashi等[21]报道高温(33℃)处理青鳉(Oryzias latipes)仔鱼引起皮质醇水平升高, 抑制原始生殖细胞分化和fshr mRNA表达, 青鳉仔鱼高温处理过程中加入皮质醇合成酶抑制剂(美替拉酮, metyrapone), 雄性化完全被药物所抵消。此外, XX青鳉孵化后暴露于高温和皮质醇中(0—5日龄)抑制雌性生殖细胞的增值和卵巢芳香化酶(cyp19a1)的表达, 而这些影响在高温和皮质醇处理中加入雌二醇(17β-estradiol, E2)后雄性化被抵消[22]。高温[15—18, 20, 24, 30]和皮质醇[15, 26, 29, 31]处理对性别调控的作用在许多鱼类中得到证实, 我们将这些证据总结如下: (1)环境应激条件在鱼类性别分化关键时期诱导雄性化过程中无一例外地导致皮质醇水平升高; (2)皮质醇处理也能诱导雄性化; (3)而皮质醇合成酶抑制剂能抵消高温等应激条件诱导的雄性化; (4)雌二醇处理能解救皮质醇或高温诱导的雄性化。这4个方面的证据表明, 皮质醇很可能是环境应激诱导雄性化过程的关键因子。因此我们推测皮质醇参与环境诱导雄性化的过程。
本研究以我国重要经济鱼类黄颡鱼为研究对象, 开展高温与皮质醇诱导黄颡鱼XX个体雄性化组织学进程研究, 以期为解密环境应激诱导鱼类雄性化的遗传学与生理学机制提供基础资料, 并为建立环境友好型全雄黄颡鱼的生产方法提供初步的实践支持。
1. 材料与方法
1.1 实验材料与实验鱼养殖
实验鱼亲本均来自湖北省黄优源渔业发展有限公司, 雌鱼亲本来源于江苏地区, 雄性亲本来源于湖北本地。选取规格大体一致、无损伤和体质健壮的黄颡鱼亲本, 进行人工催产, 实验鱼苗经人工授精孵化所得, 出膜后3d用丰年虫开口(天津丰年水产养殖有限公司), 然后逐渐转食成微粒配合饲料(山东升索渔用饲料研究中心, 主要成分: 粗蛋白质≥50.0%, 粗脂肪>8.0%, 粗纤维≤3.0%, 灰分≤16.5%, 水分≤12.0%, 钙≤5.0%, 总磷≥1.0%, 赖氨酸≥2.0%)。每100 g饲料拌30 mL 95%乙醇溶液, 将皮质醇溶于乙醇溶液, 浓度为300 mg每kg饲料, 对照组和高温组不添加药物直接与乙醇混合, 每100 g饲料伴入30 mL乙醇, 均匀地喷洒在微粒配合饲料中, 通风厨中过夜晾干, 使酒精充分挥发, 将配好的饲料置于4℃条件下备用。实验期间鱼苗饲养在60 L的水箱中, 在12—35日龄每天投喂3次, 36日龄后每天投喂2次, 每天清理残饵粪便并及时换注清水。
1.2 实验设计
实验共3个组: 对照组(CR)、高温组(HT)和皮质醇组(CS), 每组3个平行, 每个平行随机放入500尾鱼苗。本次实验在12—35日龄期间, 皮质醇处理组投喂伴入皮质醇的饲料, 对照组和高温组仅加入95%乙醇伴入的饲料, 皮质醇和对照组平均水温为26℃, 高温组平均水温为33℃。35日龄之后所有实验鱼转喂未经处理的颗粒饲料, 水温全部设置为26℃(高温组水温每天降低1℃)。实验养殖阶段分别在22、32、42、62、122日龄设置取样点, 每个平行随机捞取相同或相近数量的实验鱼, 用MS-222麻醉后测量全长(精确到0.1 mm), 取每尾鱼鳍条保存于95%乙醇中, 取躯干部分(鳃盖后缘之后, 肛门之前)或性腺组织于Bouin’s液中固定, 48h后转入70%乙醇常温保存。
1.3 性别鉴定
采用通用型柱式基因组试剂盒提取鳍条DNA(康为世纪), 利用Dan等[5]开发的黄颡鱼性别特异性分子标记(XY-F: 5′-GATTGTAGAAGCCATCTCCTTAGCGTA-3′; XY-R: 5′-CATGTAGATCACTGTACAATCCCTG-3′), 来鉴定每尾鱼的遗传型性别。PCR反应体系为10 μL: 上下游引物各0.5 μL; 模板DNA 1.0 μL; 2×Taq PCR Master Mix 5.0 μL(康为世纪); ddH2O 3.0 μL。PCR反应程序为: 95℃预变性3min, 34个循环(95℃变性30s, 59℃退火30s, 72℃延伸40s), 72℃延伸5min。扩增完成后, 取PCR产物3 µL, 以DL2000 Marker作为参照, 利用凝胶成像系统依据片段长度鉴别出XY和XX, XY为2条带(826和955 bp), XX为一条带(955 bp)。
1.4 性腺组织学观察
性腺组织学样品通过梯度乙醇脱水、二甲苯透明、石蜡包埋后, 连续切片(切片厚度5—6 μm), 用于苏木精伊红染色(HE染色), 中性树胶封片, 组织切片在光学显微镜下用成像系统进行检查和拍照(Olympus DP73, Japan)。各阶段性腺中生殖细胞的鉴别参照前人对黄颡鱼性腺分化的组织学观察研究[31-33]。
1.5 数据分析
实验数据采用SPSS 软件(version 20.0)进行单因素方差分析(One-way ANOVA)差异显著性检验, 方差分析前进行数据正态性和方差齐性检验, 如不符合方差分析的条件, 将数据进行对数或正弦转换。用Duncan’s多重比较来确定组间差异的显著性, P<0.05时视为显著性差异。文中的数据均以均值±标准差(Mean±SD)表示。
2. 结果
2.1 性别鉴定
黄颡鱼遗传性别决定类型为雄性配子异形(XX-XY)。利用黄颡鱼性别特异性的分子标记, 以黄颡鱼基因组为模板扩增出两段不同大小的片段(X-955 bp; Y-826 bp), 电泳检测结果扩增出两条带(955和826 bp)的为雄鱼, 只有一条带(955 bp)的为雌鱼。
图 1A显示的是对照组62日龄利用黄颡鱼性别特异性分子标记的琼脂糖凝胶电泳图(部分), 检测结果可以清楚地鉴定出每一尾鱼的遗传型性别, 并无模糊条带, 跟我们前期研究结果一致[3]。因此利用黄颡鱼性别特异性的分子标记可以100%准确鉴定遗传型性别。部分结果如下: 62日龄取样组织学观察发现1、3、4、5、6、7、8、9为雌鱼, 2、10、11、12、13、14为雄鱼, 与图 1A所表现的遗传型性别完全一致。
图 1B显示的是高温组62日龄琼脂糖凝胶电泳图(部分), 62日龄取样组织学观察发现5、8、9、11、14为雌性, 1、2、3、4、6、7、10、12、13为雄性, 说明4、12、13个体XX雌鱼性逆转为XX伪雄鱼, 其中7是YY超雄鱼。
我们统计了62日龄时各处理组的存活率, 对照组存活率(79.4±3.2)%显著高于高温组(63.6±1.5)%, 而高温组显著高于皮质醇处理组(59.0±0.6)%。
2.2 高温和皮质醇处理对黄颡鱼生长的影响
利用黄颡鱼性别特异分子标记和组织学结合的方法, 我们分别在各处理组间和各处理组之内比较了XX伪雄鱼、XX雌鱼与XY雄鱼生长方面的差异(表 1)。高温或皮质醇处理结束4周, 即黄颡鱼幼鱼62日龄时, 我们发现不论是高温组还是皮质醇组, XX伪雄鱼全长均显著大于XX雌鱼, 也较XY雄鱼大。这种生长优势一直延续至122日龄, 但这种优势没有统计学上的显著差异。
表 1 高温和皮质醇处理对黄颡鱼幼鱼生长的影响Table 1. The effects of high temperature and cortisol treatments on the growth of yellow catfish全长Total length (cm) 高温组HT 对照组CR 皮质醇组CS XX♀XX Female XX♂XX Male XY♂XY Male XX♀XX Female XX♂XX Male XY♂XY Male XX♀XX Female XX♂XX Male XY♂XY Male 22 DPH 1.35±0.25a — 1.20±0.25ab 1.24±0.34ab — 1.28±0.29ab 1.14±0.20b — 1.23±0.25ab 32 DPH 2.18±0.51ab — 2.41±0.65b 1.85±0.33ac — 1.85±0.30ac 1.69±0.52c — 1.55±0.22c 42 DPH 3.22±1.00a — 2.78±0.66ab 2.19±0.40cd — 2.12±0.42cd 2.61±0.64bc — 1.78±0.36d 62 DPH 4.47±0.63ac 5.45±0.53b 5.16±0.72bc 4.40±0.79ac — 4.94±0.89bc 3.85±0.36a 5.51±1.27b 4.40±0.76ac 122 DPH 6.70±0.33a 7.16±0.62a 6.70±0.59ab 7.16±0.29ab — 7.62±0.88ab 7.85±1.40ab 8.24±1.25ab 7.39±0.76b 注: 表中数据为平均值±标准差; 同一行不同上标表示显著性差异(P<0.05); DPH. 日龄Note: Data are displayed as Mean±SD; Different superscript letters indicate significant differences in each line (P<0.05); DPH: days post-hatching; HT. High Temperature; CR. Control; CS. Cortisol 2.3 高温和皮质醇对黄颡鱼性腺发育和性别分化的影响
我们将每一尾黄颡鱼个体通过性别特异性分子标记进行遗传性别鉴定, 并对相应的性腺进行组织学观察, 22日龄性腺组织学如图 2所示。22日龄皮质醇和高温处理组均未发现XX个体发生性逆转。高温组、对照组和皮质醇组中的卵巢组织与精巢组织可明显区分, 标志着卵巢解剖学上分化的开始。高温组卵巢组织由卵原细胞组成, 精巢组织仍处在发育最初期(由少量原始生殖细胞及体细胞组成)。对照组卵巢(图 2C、2c)和皮质醇组卵巢(图 2E、2e), 卵原细胞细胞核染色较浅, 细胞质呈网状或丝状, 卵圆形或椭圆形, 细胞处于有丝分裂期, 高温组卵巢(图 2A、2a)发育比对照组(图 2C、2c)和皮质醇组(图 2E、2e)快。高温组(图 2B、2b)、对照组(图 2D、2d)和皮质醇组(图 2F、2f)精巢由原始生殖细胞(Primordial germ cells)和性腺体细胞(Somatic gonadal cells)组成。
![]() 图 2 黄颡鱼XX与XY遗传型幼鱼22日龄性腺组织学A, a. 高温组XX, 卵原细胞; B, b. 高温组XY, 原始生殖细胞; C, c. 对照组XX, 卵原细胞; D, d. 对照组XY, 原始生殖细胞; E, e. 皮质醇组XX, 原始生殖细胞; F, f. 皮质醇组XY, 原始生殖细胞; PGC. 原始生殖细胞; OG. 卵原细胞. 图中三角形指向性腺所在的位置; 箭头指向生殖细胞; 下同Figure 2. Representative gonadal histology at 22 days post-hatching (DPH) of XX and XY yellow catfishA, a. High temperature group XX, oogonium; B, b. High temperature group XY, primordial germ cells; C, c. Control group XX, oogonium; D, d. Control XY, primordial germ cells; E, e. Cortisol group XX, primordial germ cells; F, f. Cortisol group XY, primordial germ cells; PGC: primordial germ cells; OG: oogonium. Triangles indicate the position of gonad; arrows indicate germ cells. The same applies below
图 2 黄颡鱼XX与XY遗传型幼鱼22日龄性腺组织学A, a. 高温组XX, 卵原细胞; B, b. 高温组XY, 原始生殖细胞; C, c. 对照组XX, 卵原细胞; D, d. 对照组XY, 原始生殖细胞; E, e. 皮质醇组XX, 原始生殖细胞; F, f. 皮质醇组XY, 原始生殖细胞; PGC. 原始生殖细胞; OG. 卵原细胞. 图中三角形指向性腺所在的位置; 箭头指向生殖细胞; 下同Figure 2. Representative gonadal histology at 22 days post-hatching (DPH) of XX and XY yellow catfishA, a. High temperature group XX, oogonium; B, b. High temperature group XY, primordial germ cells; C, c. Control group XX, oogonium; D, d. Control XY, primordial germ cells; E, e. Cortisol group XX, primordial germ cells; F, f. Cortisol group XY, primordial germ cells; PGC: primordial germ cells; OG: oogonium. Triangles indicate the position of gonad; arrows indicate germ cells. The same applies below黄颡鱼32日龄性腺组织学如图 3所示, 我们观察到, 高温组、对照组和皮质醇组中的卵巢组织与精巢组织可明显区分。高温和皮质醇处理诱导了一部分XX遗传型雌鱼雄性化, 并且这些XX雄鱼保留了原有的卵巢腔结构; 而另一部分雌鱼保持了原有的卵巢结构和细胞。在对照组(图 3D、3d)中观察到卵原细胞, 在高温组(图 3A、3a)部分XX雌鱼(未性逆转)中观察到较大的初级卵母细胞, 初级卵母细胞的出现标志着卵巢细胞学上分化的开始, 因此高温促进了卵巢发育。皮质醇组(图 3F、3f)部分XX雌鱼(未性逆转)中也观察到卵原细胞和初级卵母细胞, 在发生性逆转的XX个体性腺中(图 3G、3g), 性腺中充满大量原始生殖细胞。高温组(图 3C、3c)与皮质醇组(图 3H、3h)XY个体精巢与对照组(图 3E、3e)XY个体相比, 形态上无明显区别。
![]() 图 3 黄颡鱼XX与XY遗传型幼鱼32日龄性腺组织学G, g. 皮质醇组XX♂,卵原细胞;H, h. 皮质醇组XY♂,原始生殖细胞;OC. 卵巢腔; PO. 初级卵母细胞; XX♀. XX雌性; XX♂. XX雄性; XY♂. XY雄性. 图中三角形指向性腺所在的位置, 箭头指向生殖细胞Figure 3. Representative gonadal histology at 32 days post-hatching (DPH) of XX and XY yellow catfishG, g. Cortisol group XX♂, oogonium; H, h. Cortisol group XY♂, primordial germ cells; OC. ovarian cavity; PO. primary oocyte; XX♀: XX female; XX♂. XX male; XY♂. XY male. Triangles indicate the position of gonad; arrows indicate germ cells
图 3 黄颡鱼XX与XY遗传型幼鱼32日龄性腺组织学G, g. 皮质醇组XX♂,卵原细胞;H, h. 皮质醇组XY♂,原始生殖细胞;OC. 卵巢腔; PO. 初级卵母细胞; XX♀. XX雌性; XX♂. XX雄性; XY♂. XY雄性. 图中三角形指向性腺所在的位置, 箭头指向生殖细胞Figure 3. Representative gonadal histology at 32 days post-hatching (DPH) of XX and XY yellow catfishG, g. Cortisol group XX♂, oogonium; H, h. Cortisol group XY♂, primordial germ cells; OC. ovarian cavity; PO. primary oocyte; XX♀: XX female; XX♂. XX male; XY♂. XY male. Triangles indicate the position of gonad; arrows indicate germ cells图 4是黄颡鱼62日龄组织学, 在结束处理4周之后(35日龄处理结束), 高温组(图 4B、4b)和皮质醇组(图 4G、4g)性逆转的XX伪雄鱼精巢结构仍然保留32日龄时观察到的卵巢腔结构。对照组XY雄鱼(图 4E、4e)精原细胞有丝分裂大量增值充满整个精巢, 精小叶的形成标着着精巢解剖学水平上的分化。高温组(图 4C、4c)、对照组(图 4E、4e)和皮质醇组(图 4H、4h)XY雄鱼精巢处于发育的第Ⅰ期, 精巢中精原细胞细胞核较大, 位于细胞中央。高温组(图 4B、4b)和皮质醇组(图 4G、4g)性逆转的XX伪雄鱼精巢组织较大, 精巢组织充满大量无明显核仁的初级精母细胞, 说明性逆转XX伪雄鱼精巢比正常XY雄鱼大。高温组(图 4A、4a)和皮质醇组(图 4F、4f)XX雌鱼与对照组XX雌鱼(图 4D、4d)相比, 初级卵母细胞的形态结构、大小等无明显差异。
![]() 图 4 黄颡鱼XX与XY遗传型幼鱼62日龄性腺组织学G, g. 皮质醇组XX♂, 初级精母细胞; H, h. 皮质醇组XY♂, 精原细胞; PO: 初级卵母细胞; OC. 卵巢腔; SG. 精原细胞; PS. 初级精母细胞Figure 4. Representative gonadal histology at 62 days post-hatching (DPH) of XX and XY yellow catfishG, g. Cortisol group of XX♂, primary spermatocyte; H, h. Cortisol group XY♂, spermatogonia. PO. primary oocyte; OC. ovarian cavity; SG. spermatogonia; PS. primary spermatocyte
图 4 黄颡鱼XX与XY遗传型幼鱼62日龄性腺组织学G, g. 皮质醇组XX♂, 初级精母细胞; H, h. 皮质醇组XY♂, 精原细胞; PO: 初级卵母细胞; OC. 卵巢腔; SG. 精原细胞; PS. 初级精母细胞Figure 4. Representative gonadal histology at 62 days post-hatching (DPH) of XX and XY yellow catfishG, g. Cortisol group of XX♂, primary spermatocyte; H, h. Cortisol group XY♂, spermatogonia. PO. primary oocyte; OC. ovarian cavity; SG. spermatogonia; PS. primary spermatocyte图 5是黄颡鱼122日龄组织学, 在结束处理11周之后, 高温组(图 5B、5b)和皮质醇组(图 5G、5g)性逆转的XX伪雄鱼并未观察到32日龄和62日龄时观察到的卵巢腔结构, 而具有典型精小叶和精小囊结构。对照组XY雄鱼(图 5E、5e)精巢处于发育第Ⅲ期, 精原细胞和精母细胞有丝分裂大量增值充满整个精巢。高温组(图 5C、5c)和皮质醇组(图 5H、9h)XY雄鱼精巢处于发育的第Ⅳ期, 精巢的精小囊内除了有精原细胞外, 还有大量的精母细胞, 并向腹壶腔内推进, 腹壶腔中央充满大量精子细胞。高温组(图 5B、5b)性逆转的XX伪雄鱼精巢处于发育的第Ⅳ期, 精巢中充满大量的精子细胞。皮质醇组(图 5G、5g)性逆转的XX伪雄鱼精巢处于发育第Ⅲ期, 精细小管出现管腔, 精细小管内充满大量精原细胞和精母细胞, 细胞圆形或椭圆形, 细胞质嗜碱性。高温组(图 5A、5a)、对照组XX雌鱼(图 5D、5d)和皮质醇组(图 5F、5f)卵巢发育至第Ⅱ期, 细胞呈圆形或椭圆形, 处于初级卵母细胞小生长期细胞, 细胞核中核仁数量增多, 靠近核膜内侧分布, 卵母细胞膜外包围一层由滤泡细胞构成的滤泡膜。
![]() 图 5 黄颡鱼XX与XY遗传型幼鱼122日龄性腺组织学G, g. 皮质醇组XX♂;H, h. 皮质醇组XY♂; OC. 卵巢腔; N. 核; Nu. 核仁; FM. 滤泡膜; PO. 初级卵母细胞; SG. 精原细胞;ST. 精子细胞; SC. 精母细胞Figure 5. Representative gonadal histology at 122 days post-hatching (DPH) of XX and XY yellow catfishG, g. Cortisol group of XX♂; H, h. Cortisol group XY♂; OC. ovarian cavity; N. nucleus; Nu. nucleolus; FM. follicle membrane; PO. primary oocyte; SG. spermatogonia; ST. spermatid; SC. spermatocytes
图 5 黄颡鱼XX与XY遗传型幼鱼122日龄性腺组织学G, g. 皮质醇组XX♂;H, h. 皮质醇组XY♂; OC. 卵巢腔; N. 核; Nu. 核仁; FM. 滤泡膜; PO. 初级卵母细胞; SG. 精原细胞;ST. 精子细胞; SC. 精母细胞Figure 5. Representative gonadal histology at 122 days post-hatching (DPH) of XX and XY yellow catfishG, g. Cortisol group of XX♂; H, h. Cortisol group XY♂; OC. ovarian cavity; N. nucleus; Nu. nucleolus; FM. follicle membrane; PO. primary oocyte; SG. spermatogonia; ST. spermatid; SC. spermatocytes此外, 我们逐条检查了具有生殖突的个体21尾, 利用性别特异分子标记鉴定发现, 其中10尾鱼为XX基因型。表明XX伪雄鱼具有雄鱼特有的生殖突结构, 可能具有正常的生殖能力。
2.4 温度和皮质醇处理对黄颡鱼性比的影响
黄颡鱼幼鱼发育至62和122日龄, 通过组织学鉴定生理型性别, 并统计各处理组雌雄性别比例。如图所示(图 6A、6B)对照组没有个体发生性逆转, 高温和皮质醇处理组中均有一定比例的XX雌鱼性逆转为XX伪雄鱼, 62日龄高温组中幼鱼雄性率为63.3%, 其中XX雌性个体中有26.7%发生性逆转, 皮质醇组中幼鱼的雌、雄比例为1﹕29, 其中皮质醇组XX雌性个体中有96.7%发生性逆转。122日龄高温组中幼鱼的雌、雄比例为1﹕5.3, 其中XX雌性个体中有62.5%发生性逆转, 皮质醇组中幼鱼的雄性率为77.8%, 其中皮质醇组XX雌性个体中有55.6%发生性逆转。
3. 讨论
3.1 皮质醇可能在高温诱导XX遗传型雌鱼性逆转中起关键作用
高等脊椎动物, 性别通常由基因决定, 而在鱼类中, 性别由基因或环境或它们共同决定[35]。鱼类的性别分化极易受到环境因素的影响, 包括温度、密度[26, 27, 41]、pH[42, 43]、饵料丰度、环境背景色[31]、溶氧水平[44]和盐度[45]等, 因此, 对于很多鱼类来说, 性别最终是遗传基因和环境因素相互作用的结果[46]。研究表明, 几乎在所有的应激条件下, 鱼类的性腺都朝着雄性方向分化[47]。应激条件主要通过以下三个方面引起鱼类雄性化[8, 9]: (1)提高雄激素水平及相关基因表达; (2)抑制卵巢分化通路; (3)抑制原始生殖细胞的增值。研究发现, 高温和皮质醇处理会导致鱼类芳香化酶活性升高, 抑制生殖细胞的增殖和卵母细胞的发育, 同时导致体内皮质醇、11-甲基睾酮(11-KT)和睾酮(Testosterone, T)水平升高, 使鱼类雄性化[15, 21, 24, 29, 30]。通过4个方面的证据: (1)环境应激条件在鱼类性别分化关键时期诱导雄性化过程中无一例外地导致皮质醇水平升高[47]; (2)皮质醇处理也能诱导雄性化[15]; (3)而皮质醇合成酶抑制剂能抵消高温等应激条件诱导的雄性化[22], (4)雌二醇处理能解救皮质醇或高温诱导的雄性化[23], 我们推测皮质醇很有可能是环境应激诱导雄性化过程中的关键因子。同时, 从单细胞动物偶尔通过有性生殖来抵御不良环境, 到水生甲壳类通过无性生殖转变为有性生殖来渡过环境压力[48], 再到环境应激普遍性诱导鱼类与爬行动物雄性化[47], 这些证据将个体抵御环境应激的通路与性起源与维持联系在一起, 而皮质醇作为个体最主要的抗应激激素, 在其中可能起到关键作用。
本实验高温和皮质醇处理黄颡鱼幼鱼有部分XX遗传型雌鱼性逆转为XX伪雄鱼, 皮质醇组雌性个体中85.7%发生性逆转, 高温组中有39.2%发生雄性化, 说明部分XX遗传型雌鱼个体对皮质醇与高温处理并不敏感。这种同样基因型个体存在温度敏感性差异现象, 在斑马鱼(Danio rerio)[26]和罗非鱼(Oreochromis niloticus)[49]中有报道, 但是这其中的机制却不得而知。我们发现, 对照组32日龄雌性性腺中观察到卵原细胞, 而此时高温组未发生性逆转的XX雌性个体中观察到较大的初级卵母细胞, 且高温处理组的细胞数量较对照组更多。刘菲菲[50]将孵化后5d的尼罗罗非鱼(Nile Tilapia)高温(36±1)℃处理12d, 25日龄高温组未发生性逆转的个体也同样观察到较大的卵母细胞, 与本实验结果相似, 说明高温对未发生性逆转个体的生殖细胞的发育具有促进作用, 使卵巢发育比对照温度提前。同样是XX基因型个体, 同样在高温处理下, 一部分个体卵巢发育加快, 而另一部分卵巢发育受到抑制继而发育成精巢, 这背后的机制需要我们进一步挖掘。温度型性别决定两大问题还未知: (1)温度型性别决定的遗传机制; (2)温度如何进行信号传递从而决定性别或者引起性逆转。而遗传-环境共同性别决定的鱼类如黄颡鱼、罗非鱼等是研究这一问题的最好材料。我们推测, 相同基因型的XX个体对温度处理表现出完全相反的表型, 是因为它们在遗传上存在差异, 因此寻找这些差异是我们应当重点关注的研究方向, 是解开性别决定进化与性别决定机制转换的重要途径。
3.2 XX遗传型个体中存在温度敏感型与温度不敏感型
目前, 温度对于黄颡鱼性别分化的报道存在分歧, 游鑫等[33]发现32℃处理黄颡鱼受精卵至60日龄能显著提高雄鱼比例, 而Zhang等[51]报道称, 用高温32℃和34℃处理黄颡鱼幼鱼45d对性比没有显著影响; 而Xiong等[52]报道称32℃和34℃能导致XX全雌种群(芳香化酶抑制剂诱导的XX雄鱼与XX雌鱼的后代)的雄性化, 并且在Zhang等[51]研究结果的基础上, 推测人工诱导性逆转可能导致黄颡鱼从GSD转变成了TSD。我们的研究结果与这种推测不相符。同一种鱼类不同地理种群对温度的敏感性具有较大的差异[53, 54], 可能是造成实验不同结果的原因, 后续实验我们也将关注这方面的问题, 区分不同种群对于温度处理的敏感性。在本研究中, 通过对每尾实验鱼进行遗传型性别鉴定(性别特异分子标记)和生理型性别鉴定(组织学切片), 明确在我们实验种群中, 一定比例的XX遗传型个体性腺发育为精巢样结构。并且在122日龄时可明显观察到高温组(图5B、5b)和皮质醇组(图5G、5g)性逆转的XX伪雄鱼具有雄性特有的生殖突, 组织学显示其具有典型精小叶和精小囊结构, 精巢的精小囊内除了有精原细胞外, 还有大量的精母细胞和精子细胞。因此, 我们用确切的证据证明, 高温处理能导致XX遗传型个体性逆转为生理型雄鱼, 并且推测XX伪雄鱼可能具有生殖能力, 这些XX伪雄鱼生殖能力有待进一步研究确认。
在之前的报道中, 经皮质醇(26℃)和高温(33℃)处理XX青鳉仔鱼, 皮质醇处理组中48%的XX雌性个体性逆转为XX伪雄鱼, 而高温组中只有25%雌性发生性逆转, 皮质醇处理过的青鳉仔鱼皮质醇水平明显高温处理组[22]。此外, 用不同浓度的皮质醇(0、100、300 mg/kg)处理Southern flounder(Paralichthys lethostigma)幼鱼, 性逆转的比例具有明显的浓度依赖性[27]。血浆中皮质醇激素的清除依赖于结合蛋白、靶组织受体等, 外源激素在体内消除相对较慢[28, 55], 因此, 外源皮质醇激素比鱼体内应激而导致皮质醇激素具有更明显的性逆转作用, 这可能是外源皮质醇处理黄颡鱼比高温更能引起鱼类雄性化的原因之一。青鳉仔鱼用皮质醇和高温处理均可引起雌鱼向雄鱼的性别逆转, 组织学观察表明性逆转的XX雄鱼具有典型的精巢[21]。黄颡鱼62日龄组织学, 高温组和皮质醇组性逆转的XX伪雄鱼精巢结构仍然保留32日龄时观察到的卵巢腔结构, 说明高温和皮质醇处理对黄颡鱼性腺分化具有持续性。在高温和皮质醇处理组中, 62日龄时XX伪雄鱼的精巢与对照组XY雄鱼相比性腺较大, 精巢中充满着无明显核仁的初级精母细胞, 但细胞排列疏松, 存在较多的体细胞, 而此时对照组XY雄鱼精巢组织充满大量的精原细胞。122日龄时, 精巢中并未观察到之前32日龄和62日龄时观察到的卵巢腔结构。我们对比发现, 62日龄时, XX伪雄鱼的卵巢腔较32日龄时明显缩减, 精巢结构朝卵巢腔内延展, 开始出现黄颡鱼精巢典型的分枝状结构, 这可能是122日龄时卵巢巢消失的主要原因。Kitano等[23]在早期报道中表示高温和皮质醇处理能使XX青鳉发生性逆转, 性逆转的XX伪雄鱼精巢生殖细胞数目少于正常XY雄鱼, 高温和皮质醇诱导鱼类雄性化, 性逆转的个体性腺细胞发育比对照组快, 说明XX伪雄鱼精巢发育比正常XY雄鱼快, 但性逆转性腺中体细胞较多而生殖细胞较少。
3.3 个体生长取决于生理型性别而非遗传型性别
本实验中高温和皮质醇组性逆转XX伪雄鱼全长高于XX雌鱼和XY雄鱼, 表明高温或皮质醇诱导的XX伪雄鱼生长比正常XY雄鱼快。在此之前的报道中虹鳟仔鱼用皮质醇处理, 性逆转的XX虹鳟伪雄鱼的平均体重和平均性腺重明显增加[29], 在尼罗罗非鱼也发现高温处理XX雄鱼比正常XY雄鱼生长快[50], 说明高温和皮质醇的作用并不局限性腺, 对鱼类的生长也有一定的促进作用。研究发现, 高温处理抑制cyp19a1 mRNA表达, 导致雄激素和皮质醇水平显著升高[16], 外源皮质醇和皮质酮激素可以转化为雄激素[15, 29], 精巢分泌雄激素对鱼类的生长有促进作用[56]。此外, 皮质醇作为一种糖皮质激素可以直接作用于肾上腺, 加强肾上腺皮质细胞类固醇合成能力[57], 这些可能是导致XX雄鱼比正常XY雄鱼生长快的原因。另一方面, 我们发现, 62日龄时XX伪雄鱼精巢组织远比正常XY雄鱼大(图 4), 可能产生更多的雄激素和生长激素, 表明性腺大小也可能是决定同一性别个体大小的重要因素。在罗非鱼的研究中发现, 性腺切除显著抑制雌雄个体生长, 而这种抑制作用可以通过性腺植入而获得挽救[58], 表明性腺在生长中的重要作用。
鱼类的性腺发育有2种类型: 一种是性腺直接发育为卵巢或精巢; 另一种性腺最初是雌性同体, 但随后发育为卵巢或者精巢[59]。斑马鱼属于第二种类型, 性腺最初发育为卵巢, 随后一部分个体卵巢组织退化, 卵母细胞凋亡, 最终发育为雄性, 卵母细胞凋亡是斑马鱼卵巢-精巢转化的重要原因[60]。本实验黄颡鱼32日龄性腺组织学我们观察到高温和皮质醇处理诱导了一部分XX遗传型雌鱼雄性化, 一部分未发生性逆转的XX雌鱼正常发育为生理型雌鱼, 有趣的是另一部分性逆转的XX伪雄鱼保留了原有的卵巢腔结构, 内部结构却是雄性生殖细胞。32日龄组织学观察皮质醇组未发生性逆转的个体中也观察到卵原细胞和部分初级卵母细胞, 其中有部分未发生性逆转的XX雌鱼性腺中, 卵巢含有空泡化组织, 细胞边缘皱缩, 无论从大小还是形状上, 似乎是卵原细胞退化而形成的, 可能是退化的卵巢向精巢分化的过渡阶段。在性别分化时期将青鳉仔鱼暴露在高温(33℃)下, 通过提高皮质醇水平, 抑制雌性生殖细胞的增值和fshr mRNA的表达, 从而导致XX雌性发生性逆转[22]。研究发现, 高温导致雌性斑马鱼雄性化是由于抑制芳香化酶表达[19], 从而诱导早期卵母细胞凋亡。高温处理尼罗罗非鱼性腺具有很强的凋亡信号[50], 孵化后的青鳉暴露于高温和皮质醇下会抑制雌性生殖细胞的增值和cyp19ala表达, 此结果也在Olive flounder (Paralichthys olivaceus)[21, 30]、虹鳟[29]有相应报道。因此, 抑制雌性性别分化相关通路, 抑制原始生殖细胞发育或诱导其凋亡, 在应激条件诱导雄性化过程中起关键作用。
本实验主要研究高温和皮质醇处理对黄颡鱼性别分化的影响, 研究表明高温和皮质醇处理通过抑制卵母细胞发育, 导致性腺细胞发生凋亡, 启动精巢发育通路, 从而诱导XX遗传型个体雄性化。XX遗传型个体受到高温处理后, 一部分个体性腺发育进程加快, 一部分个体原始生殖细胞受到抑制甚至凋亡继而发育成生理型雄鱼, 它们之间的遗传差异值得我们进一步研究。环境友好型应激条件(如高温、高密度等)诱导鱼类雄性化的研究, 将为建立鱼类环境友好型单性种群生产提供重要的理论与生产实践意义。
-
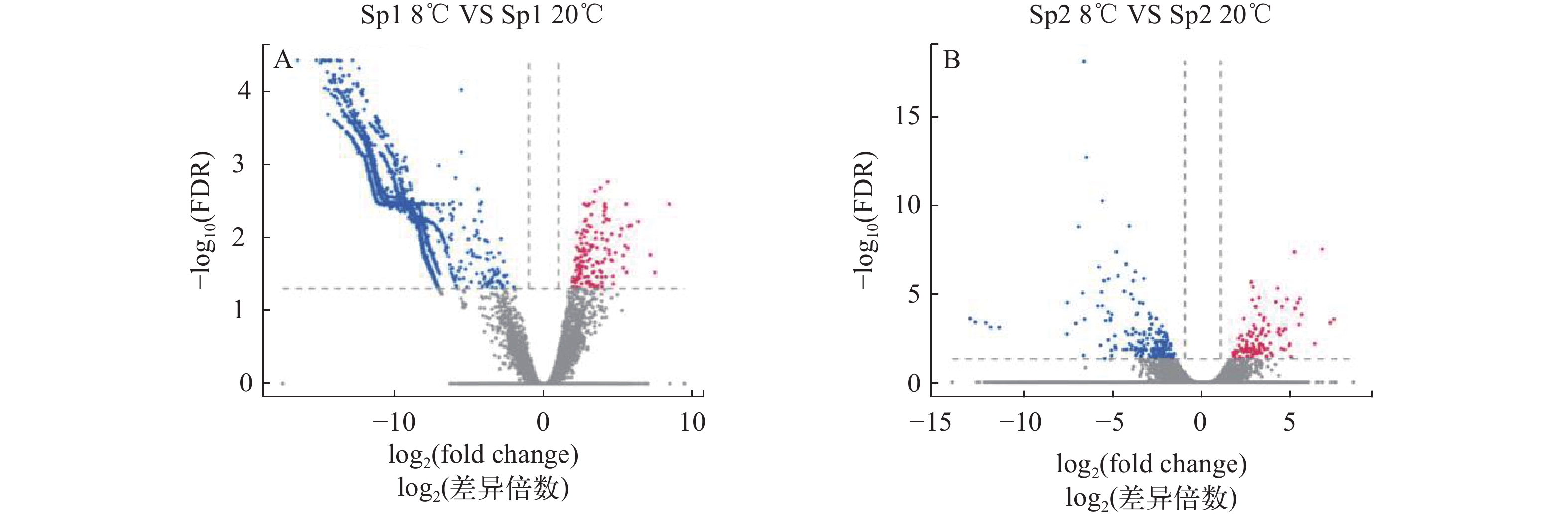
图 1 低温胁迫下不同形态群体拟穴青蟹肝胰腺基因表达差异火山图
A. 低温胁迫下Sp1群体基因表达差异火山图; B. 低温胁迫下Sp2群体基因表达差异火山图。横轴为样本的log2(差异倍数)均值, 纵轴为-lg (FDR)。图中每个点代表一个基因, 其中红色表示上调基因, 蓝色表示下调基因, 灰色表示非差异基因
Figure 1. The ‘volcano plot’ picture of differentially expressed genes of Scylla paramamosain with different morphological populations under cold challenge
A. The ‘volcano plot’ picture of differentially expressed genes of Sp1 population under cold challenge; B. The ‘volcano plot’ picture of differentially expressed genes of Sp2 population under cold challenge. The horizontal axis is the average log2 (fold change) of the sample, and the vertical axis is -lg (FDR). The red dot indicates the up-regulated gene, the blue dot indicates the down-regulated gene, and the gray dot indicates the non-differentially expressed gene
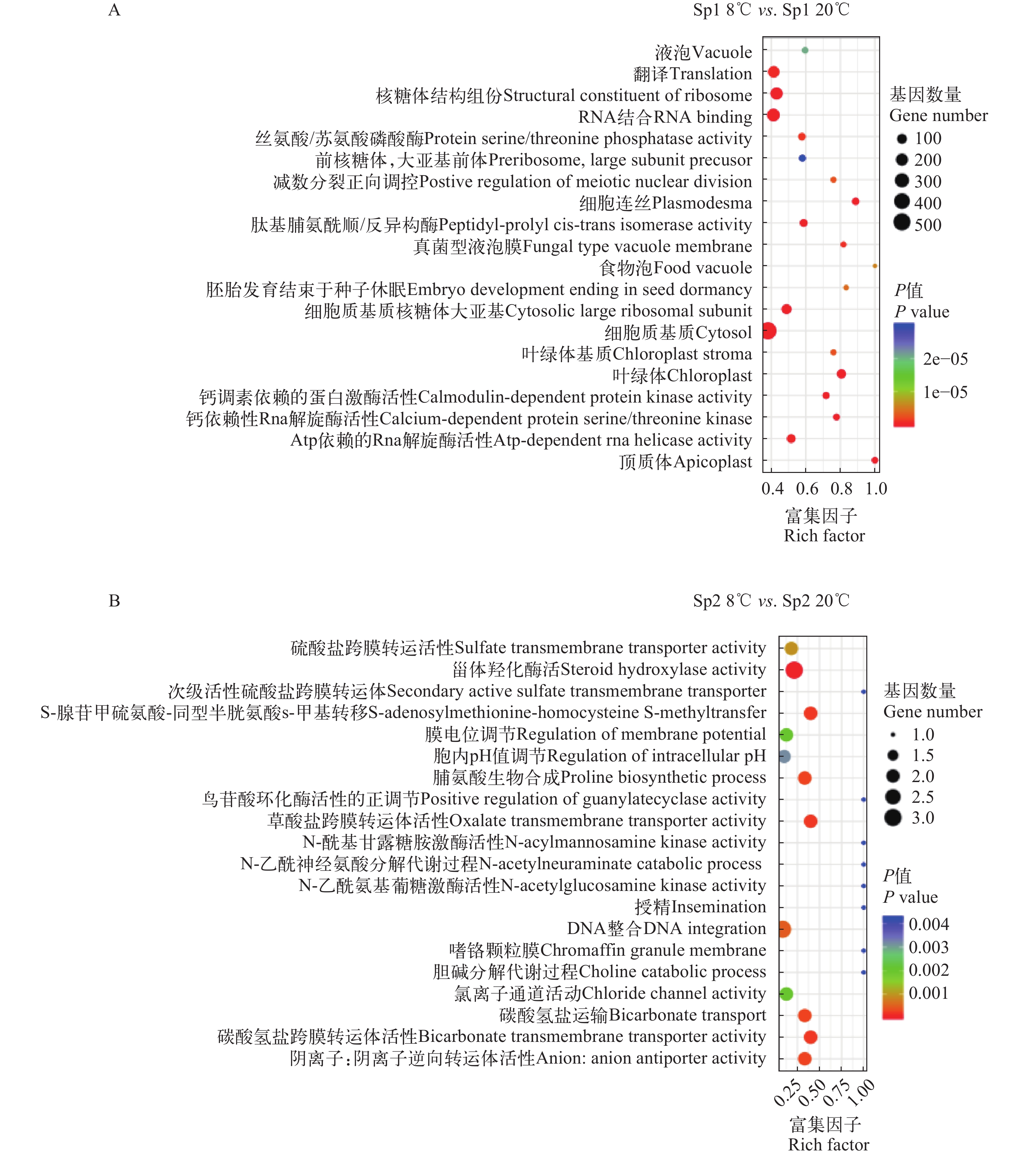
图 2 差异表达基因的GO富集分布散点图
A. 低温胁迫下Sp1群体差异表达基因的GO富集分布散点图; B. 低温胁迫下Sp2群体差异表达基因的GO富集分布散点图
Figure 2. GO enrichment results of differentially expressed genes
A. GO enrichment results of differentially expressed genes of Sp1 population under cold challenge; B. GO enrichment results of differentially expressed genes of Sp2 population under cold challenge
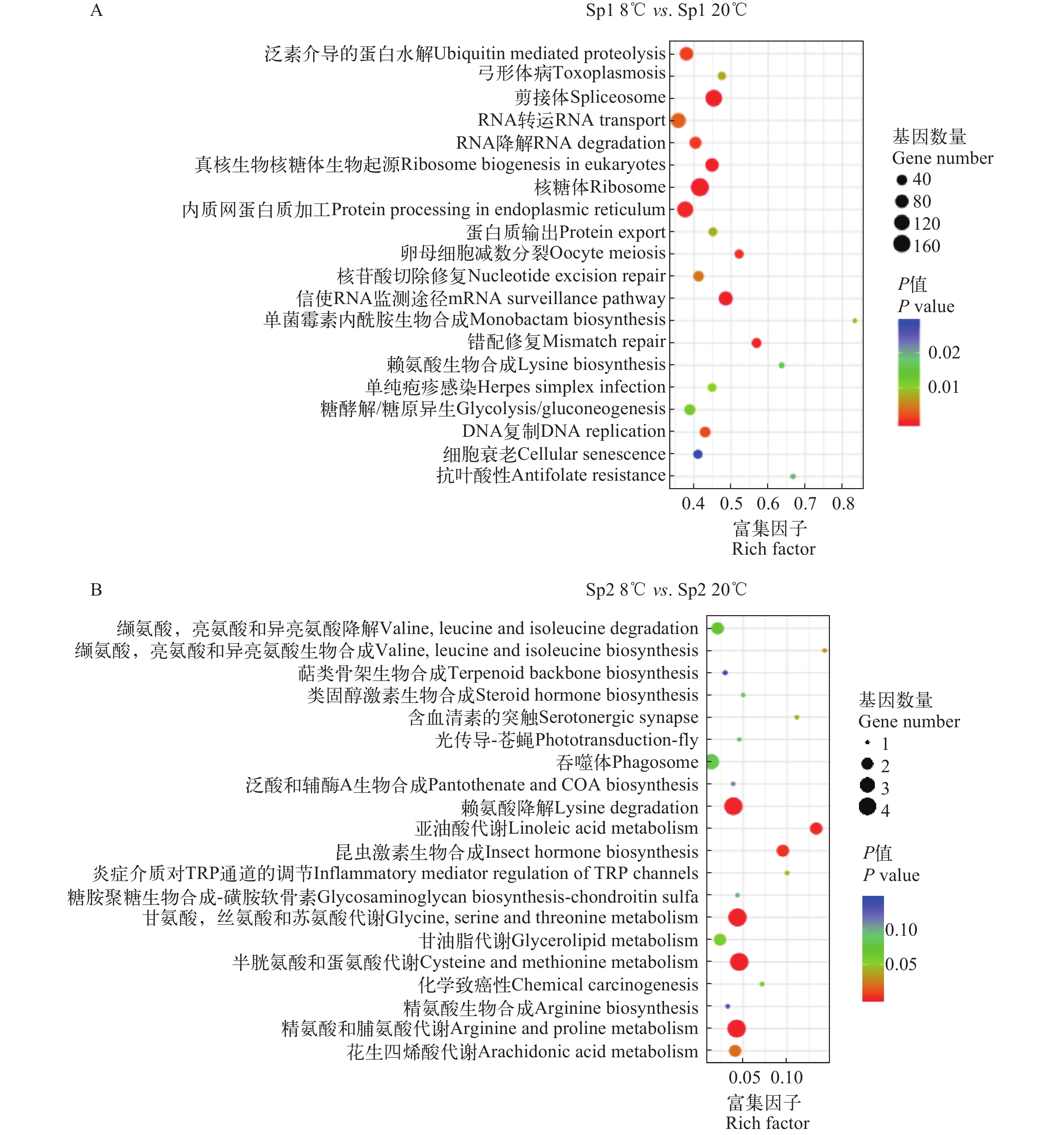
图 3 差异表达基因的KEEG富集分布散点图
A. 低温胁迫下Sp1群体差异表达基因的KEEG富集分布散点图; B. 低温胁迫下Sp2群体差异表达基因的KEEG富集分布散点图
Figure 3. KEGG enrichment results of differentially expressed genes
A. KEGG enrichment results of differentially expressed genes of Sp1 population under cold challenge; B. KEGG enrichment results of differentially expressed genes of Sp2 population under cold challenge
表 1 引物序列
Table 1 Primers used in this study
基因ID
Gene ID序列
Sequence (5′—3′)扩增子
Amplicon (bp)描述
DescriptionDN31044_c0_g3 TGATCTACGACAT
GGGAGGC158 下调表达基因 TTTGCGCTTGAA
GTCTTGCTDN26570_c1_g10 CGAAAAGAAAGA
GGGCGAGG175 下调表达基因 TTCGTCACTTCCT
CTGCCTTDN30086_c1_g4 TTCCCTCTCGAAA
CATGCCT195 下调表达基因 TGCGGCCATGGTA
GAAATTGDN31551_c2_g5 CCTCCTCATCAA
GTGCCTCA227 下调表达基因 CTTCCTCTTGCAA
CTCACGGDN31035_c0_g1 CTGCACGTGGAAA
TCTGCTT189 下调表达基因 CGCGACCTCTTCA
TCCAAAGDN31746_c1_g9 CCTGATTCAAGAT
GCGGGTG234 上调表达基因 CACTGCTCCACAA
TAGACGCDN32164_c1_g4 CCTCCATGACAA
GCTGCATC182 上调表达基因 TGTTGGTGGGGA
TAATGCCTDN31085_c1_g3 TGAAAAGGAACC
AAGCACCG153 上调表达基因 GTTGGACGGAGCT
ATGCATGDN26955_c0_g4 ATAAAGAGGTGGT
GGAGGGC245 上调表达基因 CTCCGTCTTGACC
AGTCTGTDN21811_c0_g1 GGCTTTGCTGTC
CTTTTCCA191 上调表达基因 CATGGTCTCTGG
AAGGTCGT18S rRNA TGATTACGTCCCT
GCCCTTT162 内参基因 ACATCTTTCCGT
CAGCTCGA表 2 不同形态群体拟穴青蟹肝胰腺转录组数据
Table 2 Hepatopancreatic transcriptome data of Scylla paramamosain with different morphological populations
样品
Sample有效数据
Valid data
(Gb)有效读长数
Number of
valid reads匹配读长数
Mapped ReadsQ20
(%)GC
(%)Sp1 20℃-a 5.73 40997180 36712207 98.24 48.89 Sp1 20℃-b 5.22 37302044 33850351 98.29 50.02 Sp1 20℃-c 5.89 42149974 37375442 98.28 50.01 Sp1 8℃-a 4.71 33665342 30041579 98.37 51.30 Sp1 8℃-b 5.15 36857374 33248660 98.29 50.46 Sp1 8℃-c 5.80 41444206 36790048 98.35 51.62 Sp2 20℃-a 5.61 40138790 35549897 98.25 49.82 Sp2 20℃-b 6.33 45264650 40529976 98.32 50.54 Sp2 20℃-c 5.83 41729606 37554633 98.24 48.93 Sp2 8℃-a 4.66 33335922 30397607 98.22 50.09 Sp2 8℃-b 5.96 42601794 37791107 98.28 50.41 Sp2 8℃-c 5.11 36564424 32509406 98.28 50.12 表 3 DIAMOND注释结果
Table 3 DIAMOND annotation results
数据库
Database数量
Number注释率
Annotation rate (%)swissprot 12556 15.34 KEGG 12848 15.70 GO 13951 17.04 Pfam 14119 17.25 eggNOG 16646 20.34 NR 18278 22.33 表 4 低温胁迫下两种不同形态群体拟穴青蟹差异表达最显著的前10个基因
Table 4 The top 10 differentially expressed genes of Scylla paramamosain with different morphological populations under cold challenge
Sp1 8℃ vs. Sp1 20℃ 基因ID Gene ID Nr注释 NR annotation log2(差异倍数) log2(fold change) DN26767_c0_g2 肌动蛋白3 X2异构体
Actin-3-like isoform X2–14.31 DN31044_c0_g3 热休克蛋白70 X6异构体
Heat shock 70 kDa protein-like isoform X6–13.89 DN29152_c1_g1 热休克蛋白82
Heat shock protein HSP82-like–14.74 DN26570_c1_g10 热休克蛋白90
Heat shock protein 90-like–13.69 DN30086_c1_g4 60S核糖体蛋白L21
60S ribosomal protein L21–14.41 DN31551_c2_g5 60S核糖体蛋白L12
60S ribosomal protein L12–14.31 DN31035_c0_g1 延伸因子2
Elongation factor 2-like–14.97 DN31846_c0_g1 40S核糖体蛋白
S13-2 40S ribosomal protein S13-2-like–13.63 DN24607_c0_g13 60S核糖体蛋白L5
PREDICTED: 60S ribosomal protein L5-like–12.38 DN25988_c0_g1 60S核糖体蛋白L2-A
60S ribosomal protein L2-A-like–14.13 Sp2 8℃ vs. Sp2 20℃ 基因ID Gene ID Nr注释 NR annotation log2(差异倍数) log2(fold change) DN28300_c0_g2 甜菜碱同型半胱氨酸甲基转移酶
Betaine homocysteine methyl transferase-like protein–6.51 DN31746_c1_g9 吡咯啉-5-羧酸合成酶
Pyrroline-5-carboxylate synthetase2.78 DN25548_c0_g1 甘氨酸-N-甲基转移酶异构体X1
Glycine N-methyltransferase-like isoform X1–3.54 DN28628_c0_g6 蛋白质二硫化物异构酶2
Protein disulfide-isomerase 2-like–5.63 DN32164_c1_g4 自水解酶结构域3蛋白
Abhydrolase domain-containing protein 32.95 DN31085_c1_g3 ATP依赖性解旋酶PF08_0048
Probable ATP-dependent helicase PF08_00483.19 DN26955_c0_g4 乙醛脱氢酶家族3成员A1
Aldehyde dehydrogenase, dimeric NADP-preferring-like3.45 DN24644_c1_g1 脱氢酶/还原酶(SDR家族)蛋白11
Dehydrogenase/reductase SDR family member 11-like–2.59 DN29326_c0_g2 碱性氨基酸转运载体2
Cationic amino acid transporter 2–2.96 DN21811_c0_g1 Kruppel样因子
Kruppel-like factor2.32 -
[1] 马凌波, 张凤英, 乔振国, 等. 中国东南沿海青蟹线粒体COI基因部分序列分析 [J]. 水产学报, 2006, 30(4): 463-468. Ma L B, Zhang F Y, Qiao Z G, et al. Sequence analysis of mitochondrial COI gene of Scylla spp. along coast of southeastern China [J]. Journal of Fisheries of China, 2006, 30(4): 463-468.
[2] 高天翔, 王玉江, 刘进贤, 等. 基于线粒体12S rRNA序列探讨4种青蟹系统发育关系及中国沿海青蟹的分类地位 [J]. 中国海洋大学学报(自然科学版), 2007, 37(1): 57-60. Gao T X, Wang Y J, Liu J X, et al. Study on phylogenetic relationships of four Scylla species and taxonomic status of mud crab in China based on mitochondrial 12S rRNA sequences [J]. Periodical of Ocean University of China, 2007, 37(1): 57-60.
[3] 林琪, 李少菁, 黎中宝, 等. 中国东南沿海青蟹属不同种类的mtDNA COI基因序列分析及其系统发育 [J]. 厦门大学学报(自然科学版), 2008, 47(2): 268-273. Lin Q, Li S J, Li Z B, et al. Sequence analysis of mtDNA COI gene and molecular phylogeny of four spcies in Scylla from the coast of southeast China [J]. Journal of Xiamen University (
Natural Science ) , 2008, 47(2): 268-273. [4] Liu Z M, Zhu X L, Lu J, et al. Effect of high temperature stress on heat shock protein expression and antioxidant enzyme activity of two morphs of the mud crab Scylla paramamosain [J]. Comparative Biochemistry and Physiology Part A: Molecular & Integrative Physiology, 2018(223): 10-17.
[5] Liu Z M, Wang G Z, Wu L S, et al. Seasonal change in mitochondrial function and metabolic enzyme activity of different populations of the mud crab, Scylla paramamosain, from China [J]. Aquaculture, 2013(376-379): 68-75. doi: 10.1016/j.aquaculture.2012.11.007
[6] Kong X, Wang G, Li S. Seasonal variations of ATPase activity and antioxidant defenses in gills of the mud crab Scylla serrata (Crustacea, Decapoda) [J]. Marine Biology, 2008, 154(2): 269-276. doi: 10.1007/s00227-008-0920-4
[7] Kong X, Wang G, Li S. Effects of low temperature acclimation on antioxidant defenses and ATPase activities in the muscle of mud crab (Scylla paramamosain) [J]. Aquaculture, 2012(370-371): 144-149. doi: 10.1016/j.aquaculture.2012.10.012
[8] Saranyan P V, Ross N W, Benfey T J. Erythrocyte heat shock protein responses to chronic (in vivo) and acute (in vitro) temperature challenge in diploid and triploid salmonids [J]. Comparative Biochemistry and Physiology Part A: Molecular & Integrative Physiology, 2017(206): 95-104.
[9] Zheng J, Li L, Dong H, et al. Molecular cloning of heat shock protein 60 from Marsupenaeus japonicus and its expression profiles at early developmental stages and response to heat stress [J]. Aquaculture Research, 2018, 49(1): 301-312. doi: 10.1111/are.13461
[10] Houde A L S, Akbarzadeh A, Günther O P, et al. Salmonid gene expression biomarkers indicative of physiological responses to changes in salinity and temperature, but not dissolved oxygen [J]. The Journal of Experimental Biology, 2019, 222(Pt 13): jeb198036.
[11] Huang A M, Geng Y, Wang K Y, et al. Molecular cloning and expression analysis of heat shock protein 90 (Hsp90) of the mud crab, Scylla paramamosain [J]. Journal of Agricultural Science, 2013, 5(7): 1-11.
[12] Yang Y N, Ye H, Huang H, et al. Expression of Hsp70 in the mud crab, Scylla paramamosain in response to bacterial, osmotic, and thermal stress [J]. Cell Stress & Chaperones, 2013, 18(4): 475-482.
[13] Yang Y N, Ye H, Huang H, et al. Characterization and expression of SpHsp60 in hemocytes after challenge to bacterial, osmotic and thermal stress from the mud crab Scylla paramamosain [J]. Fish & Shellfish Immunology, 2013, 35(4): 1185-1191.
[14] Ding J, Chen F Y, Ren S Y, et al. Molecular characterization and promoter analysis of crustacean heat shock protein 10 in Scylla paramemosain [J]. Genome, 2013, 56(5): 273-281. doi: 10.1139/gen-2013-0002
[15] Grabherr M G, Haas B J, Yassour M, et al. Full-length transcriptome assembly from RNA-Seq data without a reference genome [J]. Nature Biotechnology, 2011, 29(7): 644-652. doi: 10.1038/nbt.1883
[16] Mortazavi A, Williams B A, McCue K, et al. Mapping and quantifying mammalian transcriptomes by RNA-seq [J]. Nature Methods, 2008, 5(7): 621-628. doi: 10.1038/nmeth.1226
[17] Robinson M D, McCarthy D J, Smyth G K. edgeR: a Bioconductor package for differential expression analysis of digital gene expression data [J]. Bioinformatics (Oxford, England)
, 2010, 26(1): 139-140. doi: 10.1093/bioinformatics/btp616 [18] Young M D, Wakefield M J, Smyth G K, et al. Gene ontology analysis for RNA-seq: accounting for selection bias [J]. Genome Biology, 2010, 11(2): R14. doi: 10.1186/gb-2010-11-2-r14
[19] Kanehisa M, Araki M, Goto S, et al. KEGG for linking genomes to life and the environment [J]. Nucleic Acids Research, 2008(36): D480-D484.
[20] Livak K J, Schmittgen T D. Analysis of relative gene expression data using real-time quantitative PCR and the 2−ΔΔ CT method [J]. Methods, 2001, 25(4): 402-408. doi: 10.1006/meth.2001.1262
[21] Hsieh S L, Chiu Y C, Kuo C M. Molecular cloning and tissue distribution of ferritin in Pacific white shrimp (Litopenaeus vannamei) [J]. Fish & Shellfish Immunology, 2006, 21(3): 279-283.
[22] Xu Z, Liu A, Li S, et al. Hepatopancreas immune response during molt cycle in the mud crab, Scylla paramamosain [J]. Scientific Reports, 2020(10): 13102. doi: 10.1038/s41598-020-70139-2
[23] 孔祥会, 王桂忠, 王克坚, 等. 低温驯化下锯缘青蟹肝胰腺蛋白质表达及脂肪酸组成的变化 [J]. 水生生物学报, 2005, 29(5): 524-532. doi: 10.3321/j.issn:1000-3207.2005.05.009 Kong X H, Wang G Z, Wang K J, et al. Changes of protein expression and fatty acid composition in hepatopancreas of Scylla serrata under low temperature acclimation [J]. Acta Hydrobiologica Sinica, 2005, 29(5): 524-532. doi: 10.3321/j.issn:1000-3207.2005.05.009
[24] 刘子明, 王桂忠, 李少菁, 等. 低温季节不同种群拟穴青蟹线粒体呼吸速率和酶活性的差异 [J]. 厦门大学学报(自然科学版), 2018, 57(3): 354-362. Liu Z M, Wang G Z, Li S J, et al. Mitochondrial respiration rate and enzyme activity of two populations of Scylla paramamosain during low temperature seasons [J]. Journal of Xiamen University (
Natural Science ) , 2018, 57(3): 354-362. [25] Guderley H, St-Pierre J. Going with the flow or life in the fast lane: contrasting mitochondrial responses to thermal change [J]. The Journal of Experimental Biology, 2002, 205(Pt 15): 2237-2249.
[26] Yan Y, Xie X. Liver mitochondrial and whole-animal level metabolic compensation in a catfish during seasonal acclimatization [J]. Current Zoology, 2011, 57(1): 109-115. doi: 10.1093/czoolo/57.1.109
[27] Berner N J, Bessay E P. Correlation of seasonal acclimatization in metabolic enzyme activity with preferred body temperature in the Eastern red spotted newt (Notophthalmus viridescens viridescens) [J]. Comparative Biochemistry and Physiology Part A: Molecular & Integrative Physiology, 2006, 144(4): 429-436.
[28] 董丽君, 孟宪红, 孔杰, 等. 基于转录组分析筛选凡纳滨对虾低温胁迫下的差异表达基因 [J]. 中国水产科学, 2019, 26(1): 161-171. doi: 10.3724/SP.J.1118.2019.18061 Dong L J, Meng X H, Kong J, et al. Screening of differentially expressed genes related to the cold tolerance in Litopenaeus vannamei based on high-throughput transcriptome sequencing [J]. Journal of Fishery Sciences of China, 2019, 26(1): 161-171. doi: 10.3724/SP.J.1118.2019.18061
[29] Shi M, Zhang Q, Li Y, et al. Global gene expression profile under low-temperature conditions in the brain of the grass carp (Ctenopharyngodon idellus) [J]. PLoS One, 2020, 15(9): e0239730. doi: 10.1371/journal.pone.0239730
[30] Liu L, Zhang R, Wang X, et al. Transcriptome analysis reveals molecular mechanisms responsive to acute cold stress in the tropical stenothermal fish tiger barb (Puntius tetrazona) [J]. BMC Genomics, 2020, 21(1): 737. doi: 10.1186/s12864-020-07139-z
-
期刊类型引用(8)
1. 刘佳南,王巍,吴立新,胡红霞. 性逆转在硬骨鱼类中的研究现状及育种应用. 农业生物技术学报. 2025(01): 200-207 .  百度学术
百度学术
2. 程蔓,麻艳群,程光平,司楠,古昌辉,韦云勇. 不同催产剂型对人工培育巴马拟缨鱼性腺及性激素水平的影响. 水产养殖. 2024(03): 19-24 .  百度学术
百度学术
3. 丁洋,鲁子怡,刘娅,曹霄,王亚,梁浩文,任旌雷,邓翔,何焱,樊启学,牟长军,沈志刚. 黄颡鱼XX伪雄鱼制备与全雌种群规模化繁育. 水生生物学报. 2024(08): 1365-1377 .  本站查看
本站查看
4. 汪小旵,武尧,肖茂华,施印炎. 水产养殖中智能识别技术的研究进展. 华南农业大学学报. 2023(01): 24-33 .  百度学术
百度学术
5. 鲁子怡,丁洋,刘娅,胡晨昊,任旌雷,梁浩文,陈可云,胡俊豪,樊启学,沈志刚. 左炔诺孕酮对XX遗传型黄颡鱼雄性化的影响. 水生生物学报. 2023(10): 1595-1608 .  本站查看
本站查看
6. 徐思琪,张世勇,张文平,刘洪岩,王明华,钟立强,边文冀,陈校辉. 温度诱导斑点叉尾鮰雌性化研究. 福建农业学报. 2022(06): 741-747 .  百度学术
百度学术
7. 刘娅,于跃,鲁子怡,丁洋,樊启学,沈志刚. 黄颡鱼XX伪雄鱼诱导与全雌种群规模化繁育. 水生生物学报. 2022(12): 1939-1948 .  本站查看
本站查看
8. 孙旋辉,邴旭文,丁炜东,段金荣,薛婷,赵金良. 高温应激对鳜幼鱼血清生化指标及肝脏sod基因和热休克蛋白基因表达的影响. 南方农业学报. 2022(12): 3539-3547 .  百度学术
百度学术
其他类型引用(10)




 下载:
下载: