FEEDING LIVE BAIT AND FEED ON THE PEPTIDASE ACTIVITY, TRANSPORT AND ABSORPTION OF SMALL PEPTIDES IN JUVENILE MANDARIN FISH
-
摘要:
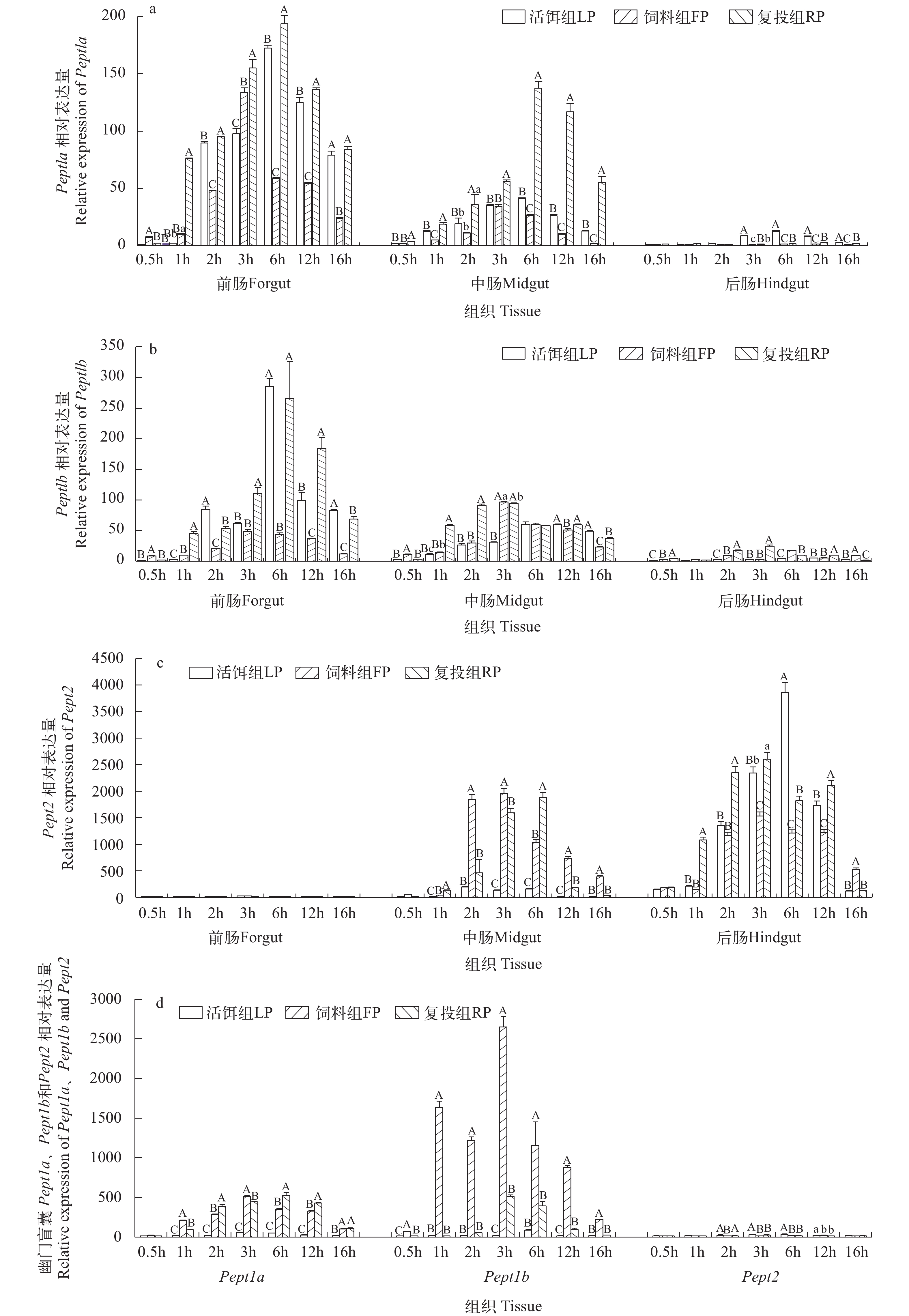
以初始体重(6.77±0.64) g的鳜(Siniperca chuatsi)为实验对象, 从消化道肠肽酶活力和小肽转运吸收方面比较研究鳜对活饵与饲料消化吸收能力的差异。实验采用3种分组投食策略, 将鳜分活饵组(仅投喂活饵鱼)、饲料组(仅投喂饲料)、复投活饵组(以下简称复投组, 先投喂饲料后活饵鱼)。活饵组、饲料组分别饲养22d, 复投组经5d驯饲、15d饲料和2d活饵喂养。饲养结束时在各组进食0.5h、1h、2h、3h、6h、12h、16h时分别取样肠和幽门盲囊, 测定氨肽酶和羧肽酶含量与活力, 小肽转运载体基因Pept1a、Pept1b和Pept2 mRNA表达水平, 及进食12h后肠内容物及粪便中残余小肽含量。结果表明: 各组羧肽酶、氨肽酶含量变化无显著性规律, 酶活力总体呈先升后降趋势; 活饵组肽酶活力峰值显著高于复投组高于饲料组(P<0.01), 复投组由饲料转喂活饵后, 肠道肠肽酶活力显著上升; 各组前肠、中肠及幽门盲囊Pept1a、Pept1b mRNA表达显著高于后肠(P<0.01), 后肠则以Pept2 mRNA高表达(P<0.01)。在复投组摄食活饵后, 小肽转运载体基因表达水平较饲料组迅速回升(P<0.01); 摄食12h, 复投组肠内容物小肽含量显著高于活饵组和饲料组, 小肽吸收效率随消化时间延长而上升。饲料组粪便中小肽含量显著高于活饵组与复投组, 未转运的小肽中含必需氨基酸居高。综上所述, 投喂鳜配合饲料, 对肠肽酶活力、小肽转运载体基因表达和小肽吸收速率均产生不利影响, 鳜对饲料蛋白的分解和小肽转运吸收效率显著低于活饵鱼。
Abstract:In this study, we examined Siniperca chuatsi with an initial weight of (6.77±0.64) g to explore the difference of digestive and absorption ability between live bait and feed from the aspects of digestive tract peptidase activity and small peptide transport and absorption. Overall, fish were divided into three groups by random: live bait group (the following group was fed with live bait only for 22d), feeding group (the following group was fed with feed only for 22d) and re-feeding group (the following group was fed with 5d of domestication, 15d of feed and 2d of live bait). At 22d post feeding, the isolated intestinal and pyloric caecum sampled at 0.5h, 1h, 2h, 3h, 6h, 12h and 16h after eating were used to measure activities of aminopeptidase and carboxypeptidase and gene expression of mall peptide transport vector genes: Pept1a, Pept1b and Pept2. Besides, the content of residual small peptides in intestinal contents and feces 12h after eating were measured. The results showed that there was no significant change in the contents of carboxypeptidase and aminopeptidase in each group, and the enzyme activity increased first and then decreased; The peak value of peptidase activity in the live bait group was significantly higher than that in the re-feeding group (P<0.01); In foregut, midgut and pyloric caecum, the mRNA expression of Pept1a and Pept1b was significantly higher while that of Pept2 was comparatively lower than those in hindgut (P<0.01); After feeding live bait, the gene expression level of small peptide transport vector in the re-feeding group increased rapidly compared with that in the feed group (P<0.01); At 12h post feeding, the content of small peptides in intestinal contents in the re-feeding group was significantly higher than that in the live bait group and feed group, and the absorption efficiency of small peptides increased with the extension of digestion time. However, the content of small peptides in feces of feed group was significantly higher than that of live bait group and re-feeding group, and the content of essential amino acids in small peptides not transported was higher. In conclusion, feeding S. chuatsi compound feed has adverse effects on the activity of intestinal peptidase, small peptide transporter gene expression and small peptide absorption rate. The decomposition of protein and the efficiency of small peptide transport and absorption of mandarin fish which intake artificial feed are significantly lower than those that intake live bait.
-
Keywords:
- Live bait /
- Feedstuff feeding /
- Intestinal peptidase /
- Small peptide /
- Transport and absorption /
- Siniperca chuatsi
-
虹鳟(Oncorhynchus mykiss)是世界广泛养殖的肉食性冷水鱼类之一。三倍体虹鳟细胞内拥有三套完整染色体, 具有生长快、肉质好和无基因污染等优点[1], 目前已在青海、新疆、甘肃和重庆等省(自治区)推广和养殖。主要养殖模式以水库大水面网箱养殖、陆基工厂化循环水养殖及利用山间溪流的流水池塘养殖为主。
随着产业的不断发展以及人民美好生活的需要, 鱼类品质成为关注的重点。鱼类品质是一个较为复杂的概念, 一般体现在表观、肉质、气味及营养价值方面[2]。目前关于鱼肉品质影响因素的研究主要集中在环境[3—5]、饲料[6—8]、种质[9—11]、规格[12—14]和屠宰方式[15—17]等。对罗非鱼(Oreochromis spp.)[18, 19]、大黄鱼(Larimichthys crocea)[20, 21]和草鱼(Ctenopharyngodon idella)[22, 23]的研究表明, 不同养殖模式对鱼肉品质影响显著, 而关于不同养殖模式三倍体虹鳟鱼肉品质差异对比却鲜见报道。
因此, 本研究通过比较网箱养殖、工厂化循环水养殖及流水池塘养殖三种模式下三倍体虹鳟在表观、肉质、气味及营养价值方面的差异, 系统研究三种养殖模式下三倍体虹鳟品质特点, 为三倍体虹鳟养殖产业可持续发展提供基础数据。
1. 材料与方法
1.1 实验材料
网箱、工厂化循环水和流水池塘养殖三倍体虹鳟分别购自于青海[体重为(3.99±0.17) kg]、新疆[体重为(4.07±0.15) kg]和重庆[体重为(4.39±0.15) kg], 依次命名为W、G和C养殖模式。每个养殖模式随机取12尾冰鲜去脏商品鱼并于宰杀72h内完成鱼肉pH、肉色、质构和持水力等物理品质指标的测定, 去皮分割特定部位的鱼肉置于入–80℃冰箱保存, 用于后续化学品质指标的测定, 不同指标的测定部位如图 1所示。
![]() 图 1 鱼肉品质指标测定区域分布图A. 检测肉色、质构和pH; B. 检测肌间隔宽度、汁液流失率、失水率和失脂率; C. 检测羟脯氨酸、水/盐溶性蛋白和肌糖原; D. 检测挥发性气味物质; E. 检测水分、灰分、脂肪、脂肪酸、总蛋白、氨基酸和矿物元素Figure 1. Sampling segments for measurements of the quality parameters in the fillet of triploid rainbow troutA. Segment is used to assay muscle color, texture, pH; B. Segment is used to assay myoseptum thickness, liquid losses, water losses and fat losses; C. Segment is used to assay hydroxyproline, water/salt soluble protein and fillet glycogen; D. Segment is used to assay volatile odor compounds; E. Segment is used to assay moisture, ash content, lipid content, fatty acids, total protein, amino acids and mineral elements
图 1 鱼肉品质指标测定区域分布图A. 检测肉色、质构和pH; B. 检测肌间隔宽度、汁液流失率、失水率和失脂率; C. 检测羟脯氨酸、水/盐溶性蛋白和肌糖原; D. 检测挥发性气味物质; E. 检测水分、灰分、脂肪、脂肪酸、总蛋白、氨基酸和矿物元素Figure 1. Sampling segments for measurements of the quality parameters in the fillet of triploid rainbow troutA. Segment is used to assay muscle color, texture, pH; B. Segment is used to assay myoseptum thickness, liquid losses, water losses and fat losses; C. Segment is used to assay hydroxyproline, water/salt soluble protein and fillet glycogen; D. Segment is used to assay volatile odor compounds; E. Segment is used to assay moisture, ash content, lipid content, fatty acids, total protein, amino acids and mineral elements1.2 实验方法
表观指标测定分析 测量每条鱼的体重、体长、内脏重和剖下的鱼片重, 并计算肥满度、去脏率和出肉率, 计算公式如下:
$ \begin{array}{c}肥\; 满\; 度(g/{\rm{cm}}^{3}) = W/L^{3} × 100 \;\; \end{array} $


(1) $ \begin{array}{c}去\; 脏\; 率(\text{%}) = (W - W_{v})/W \times 100 \end{array} $


(2) $ \begin{array}{c}出\; 肉\; 率(\text{%}) = W_{ f}/W × 100 \qquad\; \end{array} $


(3) 式中, W为鱼体质量(g), Wv为内脏质量(g), Wf为鱼片质量(g), L为鱼体长(cm)。
使用体式显微镜(P2-DBL, 尼康, 日本)对三倍体虹鳟腹部特定部位鱼肉进行拍照, 之后使用Image-J软件统计三倍体虹鳟鱼肉肌间隔宽度。
采用色彩色差仪(CR-400, 柯尼卡美能达, 日本)测定三倍体虹鳟鱼肉的特定两个点的肉色, 并由L*(亮度值)、a*(红色值-绿色值轴)、b*(黄色值-蓝色值轴)、Cab*(色度值)和Hab°(色调角)表示。参考Nickell等[24]和Yeşilayer等[25]方法, 按式(4)-(5)分别计算Cab*(色度值)和Hab°(色调角)。
$ Cab^*(色\; 度\; 值) = \sqrt {a^{*2} + b^{*2}}$


(4) $ {{Hab}}^\circ (色\; 调\; 角) = {\rm{ta}}{{\rm{n}}^{{\rm{ - 1}}}} \left(\frac{{b^*}}{{a^*}}\right) \left( {a^* > 0} \right) $


(5) 肉质指标测定分析 在肉色测定点采用食品物性分析仪(TMS-PRO, FTC, 美国)的TPA(texture profile analysis)模式对鱼肉质构进行测定, 相关参数为: 圆柱形探头直径8 mm; 力量单元25 kg; 起始力0.1 N; 形变量60%; 检测速度60 mm/min。之后在对应点使用带有固态电极的pH计(S220, 梅特勒, 瑞士)进行鱼肉pH测定。
参照Schubring等[26]的方法, 将鱼肉放入提前烘干的三层滤纸(定量滤纸ϕ12.5 cm)中, 使用食品物性分析仪(TMS-PRO, FTC, 美国)进行挤压处理, 将滤纸放入75℃烘箱烘24h, 称重, 计算鱼肉汁液流失率、失水率和失脂率。
$ \begin{array}{c}汁\; 液\; 流\; 失\; 率(\text{%}) = (m _{1} - m _{0}) /m × 100\end{array} $


(6) $ 失\; 脂\; 率(\text{%}) = (m _{2} - m _{0})/m × 100 \qquad$


(7) $ \begin{array}{c}失\; 水\; 率(\text{%}) = (m _{1} - m _{2})/m × 100 \qquad \end{array} $


(8) 式中, m为样品的重量(g), m0为滤纸的重量(g), m1为挤压样品后滤纸的重量(g), m2为烘24h后滤纸的重量(g)。
采用AOAC标准方法[27]检测鱼肉中总蛋白和灰分含量。鱼肉总蛋白含量采用凯氏定氮法(N×6.25)测定(2300-Auto-analyzer, FOSS, 丹麦); 鱼肉灰分含量采用550℃燃烧法测定。鱼肉脂肪含量采用氯仿甲醇提取法[28]测定。鱼肉水分采用冻干法测定。
鱼肉碱溶性、碱不溶性羟脯氨酸和总羟脯氨酸含量及水溶性蛋白和盐溶性蛋白含量的测定方法参考马睿[29]。肌糖原含量的测定采用南京建成试剂盒(货号: A043-1-1)。
气味指标测定分析 挥发性气味物质测定参考Ma[1]方法。采用气相色谱-质谱联用仪(GC-MS; QP2020, 岛津, 日本)测定。
挥发性气味物质的评价方法: 用气味活度值(OAV, Odor activity value)来描述单个挥发性气味物质对整体气味的贡献。当该物质OAV≥1时, 为气味活性物质, 对鱼肉整体风味有贡献。
$ {\rm{OAV}} = C/OT$


(9) 式中, C为挥发性气味物质的相对浓度, OT为挥发性气味物质的阈值。
营养价值指标测定分析 鱼肉结合态氨基酸含量的测定方法参照GB5009.124—2016并略有改动, 使用HPLC(HP1260, 安捷伦, 美国)进行测定。检测参数: 采用Agilent 1260 HPLC自动进样器, 对氨基酸标准品和样品氨基酸进行OPA-FMOC在线衍生。硼酸缓冲液(pH 10.4)2.5 μL, 氨基酸标准品或样品液0.5 μL, 混合2次, 等待0.5min, 洗针, 邻苯二甲醛(OPA)0.5 μL, 混合6次, 洗针, 9-芴甲基氯甲酸酯(FMOC)0.5 μL, 混合6次, 洗针, 衍生。色谱条件: G7121A荧光检测器(FLD); 色谱柱: ZORBAX Eclipse-AAA(4.6 mm×150 mm, 3.5 μm); 柱温: 40℃; FLD检测波长: 0.00—15.00min(λEx=340 nm, λEm=450 nm), 15.00—26.00min(λEx=266 nm, λEm=305 nm)。流动相A: 40 mmol/L Na2HPO4(pH 7.8); 流动相B: 乙腈﹕甲醇﹕水=(45﹕45﹕10, v/v/v); 泵设置: 流速为2.0 mL/min, 柱温为40℃, 停止时间为26min。
测定鱼肉脂肪时用氯仿-甲醇提取的脂质用于测定脂肪酸组成, 参照Ma等[30]方法将脂肪酸甲酯化, 而后通过GC-MS(QP2020, 岛津, 日本)分离测定样品中脂肪酸甲酯和添加已知浓度的内标(十七烷甲酯)。气相参数: 色谱柱为Rxi—5 sil MS(30 mm×0.25 mm, 0.25 μm); 色谱柱升温程序为以15℃/min速度从150℃升温到200℃, 而后以2℃/min速度从200℃升温到250℃; 载气为氦气, 1 mg/min; 接口温度为250℃, 采用分流模式(分流比: 20﹕1)。质谱参数: 电子轰击离子源, 离子源温度为230℃, 接口温度为280℃, 电子能量为70 eV, 质量扫描范围: 45—500 m/z。每个脂肪酸甲酯定性通过外标(Supelco, 美国)确定, 定量根据内标浓度及目标脂肪酸甲酯和内标的峰面积之比计算。参照Ulbricht等[31], 计算致动脉粥样硬化指数(AI)和血栓形成指数(TI), 具体计算公式如下:
$ \begin{array}{c}{\rm{AI}} = ({\rm{C}}12:0 + {\rm{C}}14:0 + {\rm{C}}16:0)/\\({\rm{Sum PUFAs}} + {\rm{Sum MUFAs}}) \end{array}$


(10) $ \begin{array}{c} {\rm{TI}} = ({\rm{C}}14:0 + {\rm{C}}16:0 + {\rm{C}}18:0)/\\(0.5 × {\rm{Sum\;PUFAs}} + 0.5 × {\rm{Sum }}\\{\rm{n}}\text{-}6\; {\rm{PUFAs}} + 3 × {\rm{Sum\; n}}\text{-}3 \;{\rm{PUFAs}} + \\{\rm{n}}\text{-}3\; {\rm{PUFAs}}/{\rm{n}}\text{-}6 \;{\rm{PUFAs}}) \end{array} $


(11) 式中, C12:0为十二烷酸, C14:0为十四烷酸, C16:0为十六烷酸, C18:0为十八烷酸, MUFA为单不饱和脂肪酸, PUFA为多不饱和脂肪酸, n-3 PUFA为n-3系列多不饱和脂肪酸, n-6 PUFA为n-6系列多不饱和脂肪酸。
鱼肉中矿物元素测定方法参考GB5009.268—2016, 采用电感耦合等离子体质谱法(ICP-MS; iCAP RQ, 赛默飞, 美国)进行测定。
1.3 统计分析
实验数据均采用平均值 ± 标准误(mean±SE)表示, 使用SPSS 25.0统计软件进行单因素方差分析, 当差异显著时(P<0.05), 采用Tukey’s检验进行多重比较; 使用SPSS 25.0统计软件进行主成分分析和聚类分析, 用Origin 2019软件绘图。
2. 结果
2.1 表观指标
由表 1可知, 不同养殖模式三倍体虹鳟的去脏率和肌间隔宽度差异不显著(P>0.05); 不同养殖模式三倍体虹鳟的肥满度差异显著(P<0.05), 从大到小分别是G>W>C。W组和G组三倍体虹鳟出肉率差异不显著(P>0.05), 但都显著低于C组(P<0.05)。
表 1 不同养殖模式三倍体虹鳟表观品质指标对比Table 1. Comparison of biometrical parameters of triploid rainbow trout cultured under different modes (n=12)指标Indicator 网箱养殖模式
Cage culture工厂化循环水
养殖模式
Recirculating aquaculture system流水池塘
养殖模式
Flowing pond肥满度Condition factor (g/cm3) 2.08±
0.06b2.61±
0.12c1.61±
0.05a去脏率Gutted yield (%) 85.64±
0.3786.96±
0.9386.58±
0.48出肉率Fillet yield (%) 60.51±
2.33a63.22±
0.75a76.53±
1.41b肌间隔宽度
Myoseptum thickness (mm)0.76±
0.030.78±
0.060.73±
0.05亮度值L* 47.30±
0.79b44.65±
0.37a46.16±
0.82ab红色值a* 16.20±
0.37a22.58±
0.72b14.59±
0.67a黄色值b* 24.20±
0.90b26.22±
0.66b18.59±
1.04a色度值Cab* 28.47±
1.07b34.62±
0.91c23.64±
1.22a色调角Hab° 59.02±
1.89b49.32±
0.57a51.72±
0.54a注: 表中数据表示为平均值±标准误(n=12); 同行数据上标不同表示组间存在显著差异(P<0.05); 下同Note: Data present mean±SE (n=12); Values in each row with different superscripts are significantly different (P<0.05), the same applies below 在肉色方面, W组和G组三倍体虹鳟鱼肉的亮度值(L*)和C组差异不显著(P>0.05), 但W组鱼肉的亮度值(L*)显著高于G组鱼肉的亮度值(L*)(P<0.05); W组和C组三倍体虹鳟鱼肉的红色值(a*)差异不显著(P>0.05), 但都显著低于G组(P<0.05); W组和G组三倍体虹鳟鱼肉的黄色值(b*)差异不显著(P>0.05), 但都显著高于C组(P<0.05); 不同养殖模式三倍体虹鳟的色度值(Cab*)差异显著(P<0.05), 从大到小分别是G>W>C; G组和C组三倍体虹鳟色调角(Hab°)差异不显著(P>0.05), 但都显著低于W组(P<0.05)。
2.2 肉质指标
如表 2所示, 在物理性状方面, 不同养殖模式三倍体虹鳟鱼肉的破裂力和pH差异不显著(P>0.05); G组和C组三倍体虹鳟鱼肉的硬度、内聚性、弹性和咀嚼性差异不显著(P>0.05), 但均显著低于W组(P<0.05); 不同养殖模式三倍体虹鳟的鱼肉的黏附性差异显著(P<0.05), 从大到小分别是C>G>W。在持水力方面, 不同养殖模式三倍体虹鳟鱼肉的失脂率差异不显著(P>0.05); G组和C组三倍体虹鳟鱼肉的汁液流失率和失水率差异不显著(P>0.05), 但均显著低于W组(P<0.05)。
表 2 不同养殖模式三倍体虹鳟鱼肉肉质指标对比Table 2. Comparison of fillet texture of triploid rainbow trout cultured under different modes指标Indicator 网箱养殖
模式
Cage culture工厂化循环
水养殖模式
Recirculating
aquaculture
system流水池塘
养殖模式
Flowing pond物理性状Physical property 质构Texture 硬度Hardness (N) 11.34±
0.31b8.62±
0.42a7.91±
0.48a破裂力Fracture (N) 8.01±
0.767.24±
0.635.44±
0.55黏附性Adhesiveness (mJ) 2.82±
0.26a4.22±
0.30b5.70±
0.23c内聚性Cohesiveness 0.22±
0.01b0.19±
0.01a0.19±
0.01a弹性Springness (mm) 9.05±
0.43b6.65±
0.44a5.81±
0.22a咀嚼性Chewiness (mJ) 21.63±
1.51b10.53±
1.13a7.93±
0.54a持水力Water holding capacity (%) 汁液流失率Liquid losses 16.04±
0.69b11.04±
0.40a12.15±
0.33a失脂率Fat losses 6.32±
0.564.98±
0.435.41±
0.20失水率Water losses 9.73±
0.39b6.06±
0.21a6.73±
0.31apH 6.28±
0.036.25±
0.026.18±
0.03化学成分Chemical component (g/kg) 水分Moisture 592.30±
3.50a590.80±
7.10a618.10±
5.10b灰分Ash 13.50±
0.50b10.50±
0.70a12.10±
0.50ab脂肪Lipid 189.70±
3.47b206.93±
5.34b163.35±
4.84a总蛋白Total protein 182.34±
5.29173.80±
2.88183.19±
0.99胶原蛋白Collagen 碱溶性羟脯氨酸
Alkali soluble hydroxyproline0.04±
0.01b0.01±
0.00a0.03±
0.01b碱不溶性羟脯氨酸
Alkali insoluble hydroxyproline0.07±
0.000.08±
0.010.07±
0.01总羟脯氨酸
Total hydroxyproline0.11±
0.010.09±
0.020.10±
0.01水溶性蛋白
Water soluble protein50.16±
1.89a69.03±
1.69b66.05±
2.89b盐溶性蛋白
Salt soluble protein54.10±
1.94a77.69±
2.25b56.37±
4.03a肌糖原Fillet glycogen 0.64±
0.06b0.41±
0.03a0.98±
0.08c在化学成分方面, 不同养殖模式三倍体虹鳟鱼肉的总蛋白、碱不溶性羟脯氨酸和总羟脯氨酸的含量差异不显著(P>0.05); W组和G组三倍体虹鳟鱼肉的水分和脂肪含量差异不显著(P>0.05), 但均显著高于C组(P<0.05); W组和G组三倍体虹鳟鱼肉的灰分和C组差异不显著(P>0.05), 但G组三倍体虹鳟鱼肉的灰分显著高于W组(P<0.05); W组和C组三倍体虹鳟鱼肉的碱溶性羟脯氨酸含量差异不显著(P>0.05), 但均显著高于G组(P<0.05); G组和C组三倍体虹鳟鱼肉的水溶性蛋白含量差异不显著(P>0.05), 但均显著高于W组(P<0.05); W组和C组三倍体虹鳟鱼肉的盐溶性蛋白差异不显著(P>0.05), 但均显著低于G组(P<0.05); 不同养殖模式三倍体虹鳟鱼肉的肌糖原含量差异显著(P<0.05), 从大到小分别是C>W>G。
2.3 气味指标
如表 3所示, W组、G组和C组分别检测到20、21和23种气味活性物质, 其中醇类3种、酮类3类、醛类15类和呋喃类2种。不同养殖模式三倍体虹鳟鱼肉气味活性物质的总OAV、庚醛和辛醛的OAV差异显著(P<0.05), 从小到大分别是C>G>W; 2-辛烯-1-醇、2,3-戊二酮和3,5-辛二烯-2-酮在W组三倍体虹鳟鱼肉中未检测出; (E)-2-庚烯醛、(E,E)-2,4-庚二烯醛在G组三倍体虹鳟鱼肉中未检测出; G组和C组三倍体虹鳟鱼肉的1-庚醇、壬醛的OAV差异不显著(P>0.05), 但均显著高于W组(P<0.05); W组和G组三倍体虹鳟鱼肉的1-辛烯-3-醇、2,3-辛二酮、戊醛、己醛和(E)-2-葵烯醛的OAV差异不显著(P>0.05), 但均显著低于C组(P<0.05); 不同养殖模式三倍体虹鳟鱼肉中(Z)-4-庚烯醛、(E,Z)-2,6-壬二烯醛、2-乙基呋喃和2-戊基呋喃的OAV差异不显著(P>0.05); W组和C组三倍体虹鳟鱼肉中(E)-2-辛烯醛的OAV差异不显著(P>0.05), 但均显著高于G组(P<0.05); W组和C组三倍体虹鳟鱼肉中(E)-2-壬烯醛、癸醛、十一醛的OAV和G组差异不显著(P>0.05), 但C组三倍体虹鳟鱼肉中(E)-2-壬烯醛、癸醛和十一醛的OAV显著高于W组(P<0.05); G组和C组三倍体虹鳟鱼肉中(E,E)-2,4-壬二烯醛的OAV和G组差异不显著(P>0.05), 但C组三倍体虹鳟鱼肉中(E,E)-2,4-壬二烯醛的OAV显著高于W组(P<0.05)。
表 3 不同养殖模式三倍体虹鳟鱼肉气味活性物质的气味活度值对比Table 3. Comparison of odor activity values (OAVs) of odor active substances in the muscles of triploid rainbow trout cultured under different modes气味活性物质
Odor-active compound气味描述Odor description 阈值Threshold
(μg/kg)OAVs 网箱养殖
模式
Cage culture工厂化循环
水养殖模式
Recirculating
aquaculture system流水池塘养殖模式
Flowing pond1-庚醇1-Heptanol 青绿味、坚果味、发酵味[32] Green, nutty, fermented 5.4[33] 6.84±0.45a 12.35±1.17b 14.39±0.87b 1-辛烯-3-醇1-Octen-3-ol 泥土味、蘑菇味、发酵味[34, 35] Earthly, mushroom, fermented 1.5[36] 99.57±5.86a 129.35±12.27a 203.40±13.57b 2-辛烯-1-醇2-Octen-1-ol 泥土味、蘑菇味[37] Earthly, mushroom 40[38] nd. 1.21±0.00 1.46±0.09 2,3-戊二酮
2,3-Pentanedione黄油味、焦糖味、果香[32] Buttery, caramel, fruity 30[35] nd. 1.18±0.00 1.28±0.10 2,3-辛二酮2,3-Octanedione 金属味[39] Metallic 12[40] 8.05±0.61a 11.00±0.74a 18.14±1.57b 3,5-辛二烯-2-酮
3,5-Octadien-2-one青绿味、花香味、类黄瓜味[35] Green, floral, cucumber 150[40] nd. 1.22±0.16 1.30±0.10 戊醛Pentanal 辛辣味、类乙醛味[32] Pungent, acetaldehyde-like 9[40] 2.42±0.15a 2.97±0.31a 4.26±0.33b 己醛Hexanal 青草味、鱼腥味、脂香、辛辣味[32] Grassy, fishy, fatty, pungent 4.5[38] 102.88±2.97a 118.13±10.50a 183.05±12.74b (Z)-4-庚烯醛
(Z)-4-Heptenal鱼腥味、煮土豆味[34] Fishy, boiled potato 4.2[40] 6.96±0.65 7.00±0.95 6.24±0.64 庚醛Heptanal 青绿味、鱼腥味、可可味、坚果味、脂香、蘑菇味[32, 41] Green, fishy, floral, chocolate, nutty, fatty, mushroom 2.8[36] 20.66±1.60a 35.19±3.12b 54.43±3.25c (E)-2-庚烯醛
(E)-2-Heptenal烤肉味、熟鱼味[39, 41] Roast meat, cooked fish 13[36] 1.61±0.21 nd. 3.87±0.79 辛醛Octanal 青绿味、花香、橙香、脂香[32] Green, floral, orange, fatty 0.7[38] 165.64±8.49a 257.36±21.52b 354.60±17.98c (E,E)-2,4-庚二烯醛
(E,E)-2,4-Heptadienal青草味、鱼腥味[42] Grassy, fishy, 15.4[36] 1.87±0.10 nd. 1.38±0.34 (E)-2-辛烯醛
(E)-2-Octenal类黄瓜味、辛辣味、脂香、蘑菇味[41, 43] Cucumber, pungent, fatty, mushroom 3[38] 12.13±1.10ab 10.05±0.99a 15.08±1.20b 壬醛Nonanal 青绿味、鱼腥味、脂香、橙香[41] Green, fishy, fatty, orange 1.1[36] 126.56±8.98a 305.23±41.16b 314.01±47.69b (E,Z)-2,6-壬二烯醛
(E,Z)-2,6-Nonadienal类黄瓜味、花香[35] Cucumber, floral 0.8[40] 31.57±3.01 31.82±5.43 34.42±3.75 (E)-2-壬烯醛
(E)-2-Nonenal青绿味、木质味、花香、果香[41, 43] Green, woody, floral, fruity 0.08[38] 168.51±20.15a 207.08±35.73ab 376.06±68.64b 癸醛Decanal 青绿味、花香、脂香、类黄瓜味[32] Green, floral, fatty, cucumber 2[38] 4.80±0.54a 8.70±1.15ab 12.68±1.52b (E,E)-2,4-壬二烯醛
(E,E)-2,4-Nonadienal脂香[39] Fatty 0.09[38] 87.35±10.18ab 51.26±8.73a 105.17±13.01b (E)-2-癸烯醛
(E)-2-Decenal脂香、橙香[39] Fatty, orange 0.3[38] 28.81±0.34a 36.39±3.99a 112.94±14.76b 十一醛Undecanal 青绿味、果香、薄荷味[32, 43] Green, fruity, minty 5[40] 1.33±0.17a 1.86±0.25ab 2.60±0.32b 2-乙基呋喃
2-Ethyl-furan橡胶味、辛辣味、绿豆味[36, 41] Rubber, pungent, green bean 2.3[36] 2.88±0.45 2.86±0.54 3.86±0.55 2-戊基呋喃
2-Pentyl-furan甘草味, 橙香[39] Liquorice, orange 6[38] 1.32±0.14 1.55±0.17 2.75±0.47 气味活度总值Total OAVs 780.74±8.77a 1029.90±85.53b 1602.66±182.54c 注: nd. 表示没有检测出; 下同Note: nd. not detected; the same applies below 2.4 营养价值指标
由表 4可知, 不同养殖模式三倍体虹鳟鱼肉中检测了17种结合态氨基酸, 其中必需氨基酸8种, 非必需氨基酸9种。W组和G组三倍体虹鳟鱼肉的组氨酸含量和C组差异不显著(P>0.05), 但W组三倍体虹鳟鱼肉的组氨酸含量显著高于G组(P<0.05); G组和C组三倍体虹鳟鱼肉的精氨酸和脯氨酸含量差异不显著(P>0.05), 但均显著低于W组(P<0.05); G组和C组三倍体虹鳟鱼肉的胱氨酸含量差异不显著(P>0.05), 但均显著高于W组(P<0.05); 其他各种氨基酸、必需氨基酸、非必需氨基酸及总氨基酸含量在3组间无显著差异(P>0.05)。
表 4 不同养殖模式三倍体虹鳟鱼肉结合态氨基酸含量对比Table 4. Comparison of fillet bound amino acids contents of triploid rainbow trout cultured under different modes (mg/100g)氨基酸Amino acid 网箱养殖
模式
Cage culture工厂化循环水
养殖模式
Recirculating aquaculture system流水池塘
养殖模式
Flowing pond必需氨基酸Essential amino acid 组氨酸His 547.71±
94.86b278.90±
32.06a490.49±
25.61ab异亮氨酸Ile 786.61±
25.98748.40±
56.87760.48±
6.69亮氨酸Leu 1323.88±
34.851257.51±
104.261283.39±
19.49赖氨酸Lys 1467.77±
34.551453.17±
110.921464.08±
15.57蛋氨酸Met 550.88±
15.81475.00±
33.40508.71±
14.02苯丙氨酸Phe 753.48±
17.03699.03±
63.83708.69±
4.47苏氨酸Thr 794.92±
19.31738.59±
57.52763.98±
13.10缬氨酸Val 946.59±
31.93872.81±
72.66892.77±
15.61总必需氨基酸
Total essential amino acids7171.84±
239.906511.12±
394.196872.59±
95.45非必需氨基酸Non-essential amino acid 丙氨酸Ala 1158.05±
33.59994.43±
83.641019.78±
17.29精氨酸Arg 1268.84±
30.32b977.43±
82.25a995.46±
18.93a天冬氨酸Asp 1720.26±
56.341578.91±
91.581669.87±
31.07胱氨酸Cys 1201.85±
82.39a1716.80±
108.74b1693.81±
88.37b谷氨酸Glu 2425.12±
49.712288.63±
154.936300.06±
3940.64甘氨酸Gly 1034.27±
80.58929.99±
54.85935.57±
39.11丝氨酸Ser 711.12±
10.51644.98±
53.45662.35±
11.82酪氨酸Tyr 626.25±
17.42556.05±
47.31570.16±
9.28脯氨酸Pro 936.95±
11.78b526.27±
24.17a564.66±
26.12a非必需氨基酸
Total non-essential amino acids11082.70±
213.3810182.32±
612.3210471.16±
193.33总氨基酸Total amino acids 18254.54±
328.8916661.60±
1069.7117343.74±
265.86由表 5可知, 不同养殖模式三倍体虹鳟鱼肉中均检测出20种脂肪酸, 其中饱和脂肪酸(SFA)7种, 单不饱和脂肪酸(MUFA)6种, 多不饱和脂肪酸(PUFA)7种。W组和C组三倍体虹鳟鱼肉的C12:0、C16:0、C18:1n-9(Z)、C20:1n-9、C22:1n-9、饱和脂肪酸(SFA)、单不饱和脂肪酸(MUFA)、总脂肪酸含量(TFA)及n-3/n-6的比值差异不显著(P>0.05), 但均显著低于G组(P<0.05); 不同养殖模式三倍体虹鳟鱼肉的C14:0、C24:1n-9、C20:5n-3(EPA)、C22:6n-3(DHA)和n-3系列脂肪酸(n-3)含量差异显著(P<0.05), 从大到小分别是G>W>C; G组和C组三倍体虹鳟鱼肉的C18:0含量和W组差异不显著(P>0.05), 但G组三倍体虹鳟鱼肉的C18:0含量显著高于C组(P<0.05); W组和G组三倍体虹鳟鱼肉的C20:0、C18:1n-9(E)含量和C组差异不显著(P>0.05), 但G组三倍体虹鳟鱼肉的C20:0、C18:1n-9(E)含量显著高于W组(P<0.05); W组和G组三倍体虹鳟鱼肉的C22:0、C24:0、C18:2n-6、C20:2n-6、多不饱和脂肪酸(PUFA)和n-6系列脂肪酸(n-6)含量差异不显著(P>0.05), 但均显著高于C组(P<0.05); G组和C组三倍体虹鳟鱼肉的C16:1n-7、C20:3n-6和C20:4n-6(ARA)含量差异不显著(P>0.05), 但均显著高于W组(P<0.05); W组和G组三倍体虹鳟鱼肉的C18:3n-3含量差异不显著(P>0.05), 但均显著低于C组(P<0.05); W组和C组三倍体虹鳟鱼肉的动脉粥样硬化指数(AI)和G组差异不显著(P>0.05), 但W组三倍体虹鳟鱼肉的动脉粥样硬化指数(AI)显著高于C组(P<0.05); G组和C组三倍体虹鳟鱼肉的致血栓指数(TI)和W组差异不显著(P>0.05), 但C组三倍体虹鳟鱼肉的致血栓指数(TI)显著高于G组(P<0.05)。
表 5 不同养殖模式三倍体虹鳟鱼肉脂肪酸含量对比Table 5. Comparison of fillet fatty acids contents of triploid rainbow trout cultured under different modes (mg/100g)脂肪酸
Fatty acid网箱养殖模式
Cage culture工厂化循环水
养殖模式
Recirculating
aquaculture system流水池塘
养殖模式
Flowing pondC12:0 1.76±0.10a 2.82±0.03b 1.51±0.11a C14:0 113.90±6.77b 138.06±3.73c 87.16±2.33a C16:0 882.87±40.40a 1022.16±13.39b 791.47±17.87a C18:0 413.95±
28.92ab478.59±
5.40b346.86±
10.88aC20:0 19.68±
5.15a34.38±
0.51b24.94±
2.34abC22:0 15.64±
0.76b17.38±
0.14b11.22±
0.83aC24:0 5.12±
0.33b4.49±
0.30b2.84±
0.24aC16:1n-7 226.57±
12.25a290.38±
4.76b266.97±
7.49bC18:1n-9(Z) 1967.25±
28.93a2896.49±
102.61b2445.83±
164.53abC18:1n-9(E) 230.32±
17.70a340.69±
8.16b255.98±
11.65aC20:1n-9 236.45±
10.19a357.67±
7.84b232.38±
20.26aC22:1n-9 25.80±
0.90a37.14±
1.20b24.77±
2.39aC24:1n-9 19.56±
0.98b30.24±
0.97c13.04±
0.91aC18:2n-6 1508.88±
56.43b1554.06±
41.23b1166.24±
49.30aC20:2n-6 121.46±
8.38b140.23±
1.64b85.95±
9.29aC20:3n-6 30.94±
2.41a44.04±
0.33b46.24±
3.47bC20:4n-6(ARA) 51.55±
1.47a60.71±
2.38b66.90±
1.15bC18:3n-3 20.05±
0.26a20.86±
0.97a42.90±
0.31bC20:5n-3(EPA) 85.07±
3.35b122.95±
3.69c65.18±
4.52aC22:6n-3(DHA) 349.09±
23.52b489±
9.34c258.58±
7.38aSFA 1452.92±
80.10a1697.87±
16.00b1266.00±
29.74aMUFA 2705.95±
60.85a3952.61±
120.73b3238.97±
197.57aPUFA 2448.86±
100.26b2856.89±
47.30b1927.53±
141.07aPUFA/SFA 1.69±
0.041.68±
0.031.52±
0.08n-3 454.21±
27.01b632.81±
13.30c366.66±
9.57an-6 1712.84±
67.37b1799.03±
40.15b1365.33±
52.25an-3/n-6 0.27±
0.01a0.35±
0.00b0.27±
0.02aTFA 6325.92±
220.81a8082.32±
153.27b6236.96±
266.44aAI 0.26±
0.01b0.23±
0.00ab0.22±
0.01aTI 0.41±
0.01ab0.38±
0.01a0.44±
0.00b注: SFA. 饱和脂肪酸; MUFA. 单不饱和脂肪酸; PUFA. 多不饱和脂肪酸; n-3. n-3系列脂肪酸; n-6. n-6系列脂肪酸; TFA. 总脂肪酸; AI. 动脉粥样硬化指数; TI. 致血栓指数Note: SFA. Saturated fatty acids. MUFA. Mono-unsaturated fatty acids. PUFA. Poly-unsaturated fatty acids. n-3. n-3 fatty acids. n-6. n-6 fatty acids. TFA. Total fatty acids. AI: Atherosclerosis index. TI. Thrombosis index 由表 6可知, 不同养殖模式三倍体虹鳟鱼肉中均检测出8种矿物元素。不同养殖模式三倍体虹鳟鱼肉的钾、磷、镁、钙、锌和铜含量差异不显著(P>0.05); W组和G组三倍体虹鳟鱼肉的铁含量和C组差异不显著(P>0.05), 但W组三倍体虹鳟鱼肉的铁含量显著高于G组(P<0.05); 不同养殖模式三倍体虹鳟鱼肉的硒含量差异显著(P<0.05), 从大到小分别是W>G>C。
表 6 不同养殖模式三倍体虹鳟鱼肉矿物元素含量对比Table 6. Comparison of fillet mineral elements contents in muscle of triploid rainbow trout cultured under different modes (mg/100g)矿物元素
Mineral
element网箱养殖
模式
Cage culture工厂化循环水
养殖模式
Recirculating
aquaculture system流水池塘
养殖模式
Flowing pond钾K 367.92±5.43 367.87±3.70 368.65±0.04 磷P 83.80±4.08 72.90±0.01 76.81±1.92 镁Mg 16.30±1.06 13.99±0.75 15.82±1.05 钙Ca 3.99±0.85 1.64±0.16 3.56±0.04 铁Fe 1.00±0.09b 0.49±0.10a 0.60±0.04ab 锌Zn 0.27±0.01 0.24±0.01 0.23±0.01 铜Cu 0.04±0.00 0.03±0.00 0.03±0.00 硒Se 0.04±0.00c 0.02±0.00b 0.02±0.00a 2.5 主成分分析
图 2所示, 本研究将111个品质指标的数据进行主成分分析。图 2a中每个箭头代表一个品质指标, 箭头与箭头之间越近表示它们之间存在正相关关系, 而箭头与箭头方向相反表示它们之间存在负相关关系。由图 2b可知, 网箱养殖、工厂化循环水养殖和流水池塘养殖三倍体虹鳟鱼肉品质轮廓差异明显, 均能独立成组。
3. 讨论
3.1 表观方面
鱼类的表观品质指标不仅取决于遗传因素, 更与其养殖环境具有紧密联系[44]。肥满度是衡量形体的重要指标, 可以一定程度反映鱼类的肥瘦程度和生长情况。出肉率是衡量鱼类生产能力的重要指标, 可以反映鱼类可食用部分的商用价值。研究表明鱼肉脂肪含量越高, 肥满度越大, 出肉率越小[45]。本研究通过主成分分析也发现脂肪含量和肥满度呈正相关, 而和出肉率呈负相关关系。在本研究中, 流水池塘养殖三倍体虹鳟出肉率具有明显优势, 可能的原因与该养殖模式下鱼呈现细长的体型, 便于鱼片剖取有关。
肉色和“大理石”纹理是感知鲑科鱼类品质的最重要属性之一, 与消费者接受或拒绝产品直接相关[46]。其中鱼类肉色可以通过色差仪L*、a*、b*值衡量, L*表示亮度值, L*值越大表明颜色越明亮; a*表示红绿程度(–a*表示绿, +a*表示红); b*表示黄蓝程度(–b*表示蓝, +b*表示黄)[44]。在本研究中, 循环水养殖的三倍体虹鳟鱼肉具有较高的红色值和黄色值, 这可能由于循环水箱内水体积较小, 饲料中色素类物质不易流失[47], 同时脂肪含量高, 有利于虾青素的沉积[24]。色度值(Cab*)表示颜色的饱和度、密度或亮度, 是颜色的强度和清晰度的表达; 色调角(Hab°)是鱼片的红色和黄色之间的关系, 红色调0°, 黄色调在90°, 绿色调在180°和蓝色调在270°[48]。一般来说, 色度值(Cab*)越大、色调角(Hab°)越大, 表示鱼肉饱和度高, 肉色偏橘。研究表明呈现高饱和度且肉色偏橘色的鲑科鱼肉更具有商业价值[49]。在本研究中, 工厂化循环水养殖和网箱养殖三倍体虹鳟鱼肉均呈现出的偏橘色, 其中网箱养殖鱼鱼肉在此基础上饱和度更高, 因此具有更高的商业价值。“大理石”纹理主要指鲑鳟鱼肉片红白相间的排布, 本研究通过测定肌间隔宽度作为衡量鱼肉白色纹理的品质指标, 结果表明不同养殖模式三倍体虹鳟鱼肉肌间隔宽度无显著差异。在陆生动物中肌间隔宽度可以在一定程度上反应动物胴体品质, 与肌肉脂肪含量呈正相关[50, 51]。本研究中网箱养殖和工厂化循环水养殖三倍体虹鳟鱼肉具有较高的脂肪含量, 但肌间隔宽度并没有增加, 可能的原因与养殖环境影响了鱼肉脂肪沉积, 需进一步研究。
3.2 肉质方面
水产品质构是鱼类组织特性的一项重要指标[52]。硬度是鲑鳟鱼肉品质的重要组成部分, 消费者倾向于坚实度较高的鱼肉[53, 54]。本研究结果表明, 网箱养殖三倍体虹鳟鱼肉的硬度、咀嚼性、内聚性、弹性最大而黏附性最小, 因此其鱼肉较为坚实。通过主成分分析发现, 三倍体虹鳟坚实度与鱼肉胶原蛋白成正相关, 与鱼肉水溶性蛋白负相关。但网箱养殖的三倍体虹鳟肌肉中羟脯氨酸含量与其他养殖模式没有显著性差异。质地的影响因素可能较多, Ma等[30]在研究大黄鱼中同样发现鱼肉坚实度与羟脯氨酸含量没有存在显著线性关系。
在鱼死后, 鱼肉中糖原无氧降解产生大量乳酸进而降低pH[55], 因此pH是判断肉质的重要指标[56]。此外, 研究表明, pH的迅速降低会显著影响鱼肉的坚韧度、持水力和感官品质[53]。本研究通过主成分分析发现鱼肉pH与糖原含量呈负相关关系, 但本研究中流水池塘养殖三倍体虹鳟肌糖原含量最高, 工厂化循环水最低, 但不同养殖模式鱼肉并未表现出pH的差异, 其原因可能与鱼肉pH的影响因素较多有关。
持水力可以体现鱼肉保持其本身水分的能力, 对鱼类的质构和风味等指标有着重要的影响[57]。持水力越高则汁液流失率、失脂率和失水率越低。研究表明, 鱼类鱼肉盐溶性蛋白含量与鱼肉保水力呈正相关[58]。本研究通过主成分分析也发现鱼肉盐溶性蛋白与汁液流失率和失水率均呈负相关关系。因此, 网箱养殖三倍体虹鳟汁液流失率和失水率较高原因可能与盐溶性蛋白含量较低相关。
3.3 气味方面
风味是鱼类品质的重要组成部分, 挥发性气味物质不仅是风味的重要组成部分, 也是鱼类品质的重要衡量标准[59]。气味的形成与人类嗅觉阈值有关。嗅觉阈值是指引起人嗅觉最小刺激的物质浓度, 嗅觉阈值越低的化合物越容易被感知, 而在挥发性气味物质中, 酮类和醛类化合物的嗅觉阈值相对较低[60], 容易被人类感知。此外研究表明, 三倍体虹鳟鱼肉中醛类物质的种类和含量都远高于其他几类物质, 可能是影响其气味的主要物质种类[1, 61]。气味活度值(OAV)用来描述单个挥发性气味物质对整体气味的贡献, 当OAV≥1时, 对鱼肉整体风味有贡献[41]。本团队之前已通过气味活度值(OAV)构建了网箱养殖三倍体虹鳟气味轮廓并确定了主体气味化合物, 主要包括醇类、酮类和醛类等21种气味活性物质[1]。本研究发现工厂化循环水养殖和流水池塘养殖三倍体虹鳟鱼肉比之前研究多了3,5-辛二烯-2-酮和2-辛烯-1-醇两种气味活性物质, 但OAV较低, 不同养殖模式三倍体虹鳟鱼肉气味仍以青绿味、脂香和果香为主。在所有气味活性物质中, 按对三倍体虹鳟气味贡献较大的前五种分别是1-辛烯-3-醇、己醛、辛醛、壬醛及(E)-2-壬烯醛, 与本团队之前所得出的结论一致[1], 通过查阅文献发现, 这些物质主要是通过油酸和亚油酸氧化裂解产生[62-64]。此外, 本研究测定鱼肉中脂肪酸组成也发现三倍体虹鳟鱼肉中油酸和亚油酸含量占总脂肪酸含量50%以上, 因此油酸和亚油酸的氧化产物可能是形成虹鳟气味的重要原因, 其作用机制有待进一步研究。本研究中流水池塘养殖三倍体虹鳟鱼肉气味活性物质的总OAV最高, 主要对鱼肉气味有贡献的物质为(E)-2-壬烯醛、辛醛、壬醛、1-辛烯-3醇和己醛, 其OAV占总值的80%以上, 主要呈现为青绿味、果香和脂香。网箱和工厂化循环水养殖三倍体虹鳟气味强度较低, 但对鱼肉整体气味有贡献的主要气味活性物质相同, 故不同养殖模式三倍体虹鳟鱼肉的气味特征一致。
3.4 营养价值方面
鱼类鱼肉营养价值主要与总蛋白含量、脂肪含量、氨基酸组成及含量、脂肪酸组成及含量、矿物元素组成及含量等有关。必需氨基酸的组成及含量对于蛋白质营养价值起重要作用, 3个养殖模式三倍体虹鳟鱼肉必需氨基酸组成相对均衡, 含量丰富, 具有较高营养价值, 为优质的动物蛋白源。在本研究中, 不同养殖模式三倍体虹鳟鱼肉中总氨基酸及总蛋白含量无显著性差异, 且含量与张殿福等[65]和朱龙等[10]研究结果相近。
脂肪含量对于鱼肉风味及适口性影响巨大[66]。而鱼肉中的不饱和脂肪酸, 尤其是n-3 PUFA包括EPA和DHA具有很多生理学功能, 例如抗心血管疾病、促进发育和免疫调节作用[67]。在本研究中, 三个养殖模式三倍体虹鳟鱼肉中MUFA含量最高, 其次是PUFA和SFA, 类似结果在Celik等[68]的研究中发现。AI和TI用于评估三倍体虹鳟鱼肉对人类心血管疾病发生的影响, AI和TI值越高, 危险性越高。在本研究中, 三组三倍体虹鳟鱼肉的AI和TI均远低于牛肉、羊肉及猪肉(AI为0.72、1.00、0.60; TI为1.06、1.58、1.37)[31], 说明三倍体虹鳟鱼肉具有较高的食用和保健价值。对比不同养殖模式发现, 工厂化循环水养殖三倍体虹鳟鱼肉中粗脂肪、TFA、SFA、MUFA、PUFA、n-3、n-6、n-3/n-6、EPA、DHA、ARA及C18: 1n-9含量最高, 其原因可能受到养殖环境的影响。由于工厂化循环水系统场地有限, 三倍体虹鳟运动受限因此脂肪更易沉积于肌肉中。脂肪酸组成与含量和张雯等[69]对养殖虹鳟的研究结果相近。
4. 结论
通过评估表观品质、肉质、气味和营养价值相关111个品质指标发现网箱养殖、工厂化循环水养殖及流水池塘养殖三倍体虹鳟鱼肉品质存在明显差异, 各具特色: 网箱养殖三倍体虹鳟鱼肉质地坚实富有弹性, 工厂化循环水养殖三倍体虹鳟具有较红的肉色并富含不饱和脂肪酸, 流水池塘养殖三倍体虹鳟形体优美且出肉率相对较高, 挥发性风味物质含量丰富。
-
表 1 引物序列
Table 1 Primer sequence
引物名称
Primer引物序列
Primer sequence
(5′—3′)扩增产物大小
Amplification
product
size (bp)退火温度
Annealing
temperature (℃)Pept1a-F AAGACATCGAGCCCAACTCG 235 64 Pept1a-R ATGTACTCTGCCCACCGTTC Pept1b-F GGCAGACAAAGGCGAGAT 193 56 Pept1b-R ATGGTAGATAGTGGTGGC Pept2-F GACGCTCTACTTCCTCAC 199 58 Pept2-R AATGGCTCCAACCGACTT β-actin-F GCGTGACATCAAGGAGAA 181 β-actin-R CATACCGAGGAAGGAAGG 表 2 活饵组、饲料组和复投组的肠道与幽门盲囊的氨肽酶含量
Table 2 The content of aminopeptidase in the intestine and pyloric caeca of live bait group, feed group and re-injection group (ng/mL)
时间
Time
(h)肠氨肽酶含量
Content of aminopeptidase in the intestine幽门盲囊氨肽酶含量
Content of aminopeptidase in thepyloric caeca饲料组 活饵组 复投组 饲料组 活饵组 复投组 0.5 10.28±0.23bc 10.39±0.19a 10.11±0.13 6.53±0.79b 10.72±0.25a 10.03±0.62a 1 10.44±0.45b 10.42±0.71a 8.29±1.88 9.87±0.19a 9.76±0.17ab 7.47±0.06b 2 11.70±0.16a 10.23±0.15ab 10.09±0.32 8.57±0.11a 9.70±0.89ab 8.60±0.15ab 3 10.47±0.43b 10.17±0.03ab 10.89±0.16 9.82±0.18a 10.22±0.21a 8.37±0.47ab 6 9.52±0.29c 8.96±0.31b 9.67±0.71 5.65±0.32b 8.35±0.32b 7.70±0.38b 12 10.75±0.38ab 10.22±0.50ab 10.33±0.18 8.74±0.30a 9.81±0.56ab 7.27±0.03b 16 9.58±0.23c 10.16±0.04ab 9.73±0.15 9.65±0.42a 9.28±0.07ab 7.82±1.14b 注: 同一列数据上标注不同小写字母表示差异显著(P<0.05), 标注不同大写字母表示差异极显著(P<0.05), 下同Note: Different lowercase letters marked on the same row indicate significant difference (P<0.05). Different uppercase letters indicate extremely significant difference (P<0.05). The same applies below 表 3 活饵组、饲料组和复投组的肠道与幽门盲囊的羧肽酶含量
Table 3 The content of carboxypeptidase in the intestine and pyloric caeca of the live bait group, feed group and re-injection group (ng/mL)
时间
Time
(h)肠羧肽酶含量
Content of carboxypeptidase in the intestine幽门盲囊羧肽酶含量
Content of carboxypeptidase in the pyloric caeca饲料组 活饵组 复投组 饲料组 活饵组 复投组 0.5 130.26±3.54bc 128.74±1.01bc 141.09±4.25a 72.87±6.88c 130.77±2.83ab 138.06±1.42a 1 126.32±0.61bc 152.94±13.46a 152.02±9.72a 112.75±6.68ab 123.08±0.61ab 104.55±2.73bc 2 124.29±1.62bc 124.19±0.71c 97.67±16.30b 107.69±2.02ab 124.70±2.02ab 111.54±7.89ab 3 117.31±3.74c 120.55±1.52c 123.12±0.56ab 127.83±3.74a 113.77±4.45b 104.55±18.52bc 6 152.13±8.00a 145.65±6.17ab 141.19±0.51a 109.62±6.17ab 141.80±11.03a 128.14±2.43ab 12 131.38±0.81b 128.24±0.91bc 123.68±10.53ab 104.25±10.53b 122.47±1.62ab 94.13±12.75b 16 127.83±0.30bc 119.03±0.20c 125.81±6.58ab 116.19±2.43ab 124.70±13.16ab 60.22±0.71c 表 4 鳜肠道内容物与粪便中肽含量
Table 4 Peptide content of intestinal contents and excrement of S. chuatsi (μg/mL)
项目Item 分类
Category活饵组
Live bait group饲料组
Feed group复投组
Repeat
feeding group肠内容物
Intestinal contents短肽 1567.21 2767.05 16581.92 小肽 1001.70 2106.22 11234.14 小肽占比 (%) 63.92 76.12 67.75 含必需AA小肽 404.93 1295.08 8347.72 含必需AA小肽占比 (%) 40.42 61.49 74.31 粪便
Excrement短肽 19209.10 40013.89 16311.32 小肽 13401.33 20383.24 11287.71 小肽占比 (%) 69.77 50.94 69.20 含必需AA小肽 9329.88 17583.97 8188.71 含必需AA小肽占比 (%) 69.62 86.27 72.55 注: 本试验短肽特指由2—5个AA缩合组成的肽链; 小肽特指由2—3个AA缩合组成的肽链; 含必需AA小肽特指由2或3个NEAA组成的肽链Note: The short peptide refers to the peptide chain composed of 2—5 AA condensation in this test; Small peptide refers to the peptide chain composed of 2—3 AA condensation; Small peptides containing essential AA are especially those containing 2 or 3 NEAA chains -
[1] Daniel H, Kottra G. The proton oligopeptide cotransporter family SLC15 in physiology and pharmacology [J]. Pflugers Archiv: European Journal of Physiology, 2004, 447(5): 610-618. doi: 10.1007/s00424-003-1101-4
[2] Wang J L, Yan X, Lu R H, et al. Peptide transporter 1 (PepT1) in fish: a review [J]. Aquaculture and Fisheries, 2017, 2(5): 193-206. doi: 10.1016/j.aaf.2017.06.007
[3] Maffia M, Rizzello A, Acierno R, et al. Characterisation of intestinal peptide transporter of the Antarctic haemoglobinless teleost Chionodraco hamatus [J]. Journal of Experimental Biology, 2003, 206(Pt4): 705-714.
[4] Con P, Nitzan T, Slosman T, et al. Peptide transporters in the primary gastrointestinal tract of pre-feeding Mozambique tilapia larva [J]. Frontiers in Physiology, 2019(10): 808. doi: 10.3389/fphys.2019.00808
[5] 马燕梅, 梅景良, 林树根. 鳜胃肠道和肝脏主要消化酶活性的研究 [J]. 江西农业大学学报, 2004, 26(4): 584-588. Ma Y M, Mei J L, Ling S G. Studies on the main digestive enzyme activities in stomach Intestine and Liver of Siniperca chautsi [J]. Acta Agriculturae Universitatis Jiangxiensis, 2004, 26(4): 584-588.
[6] 曾萌冬, 徐俊, 宋银都, 等. 饲料替代活饵对鳜生长、消化及小肽转运载体基因表达的影响 [J]. 南方农业学报, 2021, 52(1): 228-237. Zeng M D, Xu J, Song Y D, et al. Effects of replacing live bait with compound feed on growth, digestion and expression of small peptide transporter (PepT1) gene of Siniperca chuatsi [J]. Journal of Southern Agriculture, 2021, 52(1): 228-237.
[7] 李燕, 李永强, 李建忠, 等. 配合饲料完全替代鲜活饵料对翘嘴鳜生长、体成分及消化能力的影响 [J]. 水产科技情报, 2016, 43(3): 164-168. Li Y, Li Y Q, Li J Z, et al. Effects of replacing fresh bait with compound feed completely on growth, body composition and digestion ability of Siniperca chuatsi [J]. Fisheries Science & Technology Information, 2016, 43(3): 164-168.
[8] 梁旭方, 何珊. 鳜鱼遗传育种与饲料养殖 [M]. 北京: 科学出版社, 2018. Liang X F, He S. Genetic Breeding and Feed Breeding of Mandarin Fish [M]. Beijing: Science Press, 2018.
[9] 曾萌冬, 宋银都, 吴红岩, 等. 鳜不同驯食方式的效果比较 [J]. 渔业研究, 2020, 42(2): 160-166. Zeng M D, Song Y D, Wu H Y, et al. Comparison on the effects of different domestication methods of Mandarin fish Siniperca chuatsi [J]. Journal of Fisheries Research, 2020, 42(2): 160-166.
[10] Nakanishi K, Yaoi K, Nagino Y, et al. Aminopeptidase N isoforms from the midgut of Bombyx mori and Plutella xylostella-their classification and the factors that determine their binding specificity to Bacillus thuringiensis Cry1A toxin [J]. Federation of European Biochemical Societies letter, 2002, 519(1-3): 215-220. doi: 10.1016/S0014-5793(02)02708-4
[11] 吴婷婷, 朱晓鸣. 鳜鱼、青鱼、草鱼、鲤、鲫、鲢消化酶活性的研究 [J]. 中国水产科学, 1994, 1(2): 10-17. Wu T T, Zhu X M. Studies on the activity of digestive enzymes in mandarin fish, black carp, grass carp, common carp, crucian carp and silver carp [J]. Journal of Fishery Sciences of China, 1994, 1(2): 10-17.
[12] Zambonino Infante J L, Cahu C L. Ontogeny of the gastrointestinal tract of marine fish larvae [J]. Comparative Biochemistry and Physiology Part C:Toxicology & Pharmacology, 2001, 130(4): 477-487.
[13] Srichanun M, Tantikitti C, Kortner T M, et al. Effects of different protein hydrolysate products and levels on growth, survival rate and digestive capacity in Asian seabass (Lates calcarifer Bloch) larvae [J]. Aquaculture, 2014(428-429): 195-202. doi: 10.1016/j.aquaculture.2014.03.004
[14] Tlak Gajger I, Nejedli S, Kozarić Z. Histochemical distribution of digestive enzymes in the intestine of the common two-banded SeaBream, Diplodus vulgaris, geoffroy st-hilaire 1817 [J]. Anatomia, Histologia, Embryologia, 2013, 42(3): 161-167. doi: 10.1111/j.1439-0264.2012.01179.x
[15] 李武辉. 鲂鲌品系和鲌鲂品系遗传特性及食性研究 [D]. 长沙: 湖南师范大学, 2018: 13. Li W H. Genetics and diet traits of reciprocal hybrids lineage derived from hybridization between Megalobrama amblycephala and Culter alburnus [D]. Changsha: Hunan Normal University, 2018: 13.
[16] 周景祥, 余涛, 黄权, 等. 鲤鱼、黄颡鱼和大眼鰤鲈消化酶活性的比较研究 [J]. 吉林农业大学学报, 2001, 23(1): 94-96. Zhou J X, Yu T, Huang Q, et al. Comparison studies on the activities of the digestive enzymes of common carp, Huangsang cat-fish and walleye [J]. Journal of Jilin Agricultural University, 2001, 23(1): 94-96.
[17] 高云红, 景琦琦, 黄滨, 等. 云龙石斑鱼胃排空特征和摄食消化特性研究 [J]. 渔业科学进展, 2021, 42(1): 92-99. Gao Y H, Jing Q Q, Huang B, et al. Characteristics of gastric evacuation and feeding digestion in “Yunlong” groupers (Epinephelus moara ♀ × E. lanceolatus ♂) [J]. Progress in Fishery Sciences, 2021, 42(1): 92-99.
[18] 逯尚尉, 刘兆普, 余燕. 不同饵料对点带石斑鱼幼鱼生长、营养成分及组织消化酶活性的影响 [J]. 上海海洋大学学报, 2010, 19(5): 648-653. Lu S W, Liu Z P, Yu Y. Effect of different diets on growth, nutritive composition and digestive enzyme activities of juvenile Epinephelus malabaricus [J]. Journal of Shanghai Ocean University, 2010, 19(5): 648-653.
[19] 曹崇海. 乌鳢饲喂冰鲜鱼和配合饲料消化道组织及消化酶差异的研究 [D]. 浙江: 浙江大学, 2011. Cao C H. Study on the differences of digestive tract tissues and digestive enzymes of snakehead fed chilled fish and compound feed [J]. Zhejiang: Zhejiang University: 2011.
[20] 王立波, 刘伟, 陈军, 等. 怀头鲇幼鱼摄食前后消化酶活性的变化 [J]. 水产学杂志, 2007, 20(1): 36-41. Wang L B, Liu W, Chen J, et al. Changes in digestive enzyme activities of northern sheatfish after feeding [J]. Chinese Journal of Fisheries, 2007, 20(1): 36-41.
[21] 翁祖桐. 2个养殖水温下罗非鱼食后肠道消化酶活性的动态变化 [J]. 渔业研究, 2018, 40(5): 374-379. Weng Z T. The variations of digestive enzyme activities after feeding in intestinal canal of tilapia at two water temperatures [J]. Journal of Fisheries Research, 2018, 40(5): 374-379.
[22] Kamaszewski M, Ostaszewska T, Napora-Rutkowski L, et al. The role of dipeptide on fish growth and digestive enzyme activity modulation in common carp (Cyprinus carpio L.) [J]. Animal Science Papers and Reports, 2019, 37(1): 75-85.
[23] 姜柯君, 王际英, 张利民, 等. 饲料中添加小肽对星斑川鲽幼鱼生长性能、体组成及血清生化指标的影响 [J]. 动物营养学报, 2013, 25(1): 222-230. Jiang K J, Wang J Y, Zhang L M, et al. Effects of small peptides supplementation on growth performance, body composition and serum biochemical indices of juvenile starry flounder (Platichthys stellatus) [J]. Chinese Journal of Animal Nutrition, 2013, 25(1): 222-230.
[24] 许培玉, 周洪琪. 小肽制品对凡纳滨对虾蛋白酶和淀粉酶活力的影响 [J]. 上海水产大学学报, 2005, 14(2): 133-137. Xu P Y, Zhou H Q. Effects of small peptides on the protease and amylase activities of Litopenaeus vannamei [J]. Journal of Shanghai Fisheries University, 2005, 14(2): 133-137.
[25] 夏薇, 刘文斌, 乔秋实, 等. 棉粕酶解蛋白肽对建鲤生产性能和生化指标的影响 [J]. 淡水渔业, 2012, 42(1): 46-51. Xia W, Liu W B, Qiao Q S, et al. Effects of cottonseed meal hydrolysate on growth performance and biochemical indices of Cyprinus carpio var. Jian [J]. Freshwater Fisheries, 2012, 42(1): 46-51.
[26] 邓敦, 李铁军, 黄瑞林, 等. 小肽转运蛋白(PepT1)及其活性调控 [J]. 广西农业生物科学, 2005, 24(4): 352-358. Deng D, Li T J, Huang R L, et al. Peptide-transporters (PepT1) and it’s activity regulation [J]. Journal of Guangxi Agricultural and Biological Science, 2005, 24(4): 352-358.
[27] Amberg J J, Myr C, Kamisaka Y, et al. Expression of the oligopeptide transporter, PepT1, in larval Atlantic cod (Gadus morhua) [J]. Comparative Biochemistry and Physiology Part B, 2008, 150(2): 177-182. doi: 10.1016/j.cbpb.2008.02.011
[28] Con P, Nitzan T, Cnaani A. Salinity-dependent shift in the localization of three peptide transporters along the intestine of the Mozambique tilapia (Oreochromis mossambicus) [J]. Frontiers in Physiology, 2017(8): 8. doi: 10.3389/fphys.2017.00008
[29] 汪建华, 李玉珑, 陈敦学, 等. 饥饿再投喂对鳜肌FSRP-1、FSRP-3和肠道PepT1基因表达的影响 [J]. 广西师范大学学报(自然科学版), 2016, 34(1): 144-149. doi: 10.16088/j.issn.1001-6600.2016.01.023 Wang J H, Li Y L, Chen D X, et al. Effect of starvating and refeeding on relative expression of FSRP-1, FSRP-3 and PepT1 gene in mandarin fish (Siniperca chuatsi) [J]. Journal of Guangxi Normal University (Natural Science Edition), 2016, 34(1): 144-149. doi: 10.16088/j.issn.1001-6600.2016.01.023
[30] Rubio-Aliaga I, Frey I, Boll M, et al. Targeted disruption of the peptide transporter Pept2 gene in mice defines its physiological role in the kidney [J]. Molecular and Cellular Biology, 2003, 23(9): 3247-3252. doi: 10.1128/MCB.23.9.3247-3252.2003
[31] Ahmed M, Liang H L, Kasiya H C, et al. Complete replacement of fish meal by plant protein ingredients with dietary essential amino acids supplementation for juvenile blunt snout bream (Megalobrama amblycephala) [J]. Aquaculture Nutrition, 2019, 25(1): 205-214. doi: 10.1111/anu.12844
[32] Ostaszewska T, Dabrowski K, Kamaszewski M, et al. The effect of plant protein-based diet supplemented with dipeptide or free amino acids on digestive tract morphology and Pept1 and PepT2 expressions in common carp (Cyprinus carpio L.) [J]. Comparative Biochemistry and Physiology Part A:Molecular & Integrative Physiology, 2010, 157(2): 158-169.
[33] Xu D, He G, Mai K, et al. Expression pattern of peptide and amino acid genes in digestive tract of transporter juvenile turbot (Scophthalmus maximus L.) [J]. Journal of Ocean University of China, 2016, 15(2): 334-340. doi: 10.1007/s11802-016-2768-4
[34] Bogé G, Rigal A, Pérès G. Rates of in vivo intestinal absorption of glycine and glycylglycine by rainbow trout (Salmo gairdneri R.) [J]. Comparative Biochemistry and Physiology. Part A: Physiology, 1981, 69(3): 455-459. doi: 10.1016/0300-9629(81)93004-8
[35] Jia Y D, Gao Y H, Jing Q Q, et al. Gastric evacuation and changes in postprandial blood biochemistry, digestive enzymes, and appetite-related genes in juvenile hybrid grouper (Epinephelus moara ♀ × E. lanceolatus ♂) [J]. Aquaculture, 2021(530): 735721. doi: 10.1016/j.aquaculture.2020.735721
[36] 乐国伟, 施用晖, 杨凤. 肽在动物蛋白质营养中的作用——小肽在动物氨基酸吸收中的作用 [J]. 四川农业大学学报, 1996, 14(S1): 19-26. Yue G W, Shi Y H, Yang F. The role of small peptides in the intestinal absorption of amino acids [J]. Journal of Sichuan Agricultural University, 1996, 14(S1): 19-26.
-
期刊类型引用(12)
1. 喻亚丽,李清,张浪,孙艳红,鲁晓蓉,魏辉杰,陈见,李佩,高银爱,王贵英. 短期微流水处理对池塘养殖杂交鲌“先锋1号”肌肉品质的影响. 渔业科学进展. 2024(02): 245-256 .  百度学术
百度学术
2. 龚雅婷,王兰梅,朱文彬,傅建军,罗明坤,董在杰. 不同体色福瑞鲤2号的肌肉品质. 水产学报. 2024(04): 289-297 .  百度学术
百度学术
3. 宁可源,李永雄,玄一凡,梁萧,王茂林,王伟. 海水驯化对鲟肌肉品质的影响研究. 水产养殖. 2024(07): 11-14 .  百度学术
百度学术
4. 陈丽霞,曹嵩靖,孟玉琼,孙国梁,李长忠,马睿. 饲料蛋白质和脂肪水平对三倍体虹鳟生长性能、生理代谢和感官品质的影响. 水生生物学报. 2024(08): 1279-1291 .  本站查看
本站查看
5. 李积萍,刘扬,王辰,陶馨,都慧芳,李月. 三倍体虹鳟幼鱼对过饱和总溶解气体的耐受能力. 水产学杂志. 2024(04): 1-8 .  百度学术
百度学术
6. 汤伟,王祺,李佳欣,张军,吴春光,何增国. 饲料中添加褐藻寡糖、红藻寡糖对虹鳟生长性能、肌肉营养成分及血清免疫功能的影响. 农业生物技术学报. 2024(09): 2100-2111 .  百度学术
百度学术
7. 刘阳,马睿,田海宁,管玲玲,刘小红,姜晓明,孟玉琼. 不同规格三倍体虹鳟鱼肉品质差异的研究. 淡水渔业. 2024(05): 69-80 .  百度学术
百度学术
8. 王英英,马睿,武泽众,田海宁,姜晓明,孟玉琼. 三倍体虹鳟鱼片不同部位品质差异. 广东海洋大学学报. 2024(05): 76-84 .  百度学术
百度学术
9. 李温蓉,安玥琦,陶玲,温利,刘茹,李谷,熊善柏. 传统养殖与组合湿地-池塘循环水养殖黄颡鱼的品质比较. 现代食品科技. 2023(05): 14-24 .  百度学术
百度学术
10. 冉鹏程,赵松龄,李选凯,刘巧,赵柳兰,杨淞. 鱼肉品质评价及改善研究进展. 水产养殖. 2023(06): 14-19 .  百度学术
百度学术
11. 任艳丽,罗杰儿,王人开,周芷晴,吴紫倩,谢瑞涛,杨远廷,周萌,舒绪刚. 不同锌源对珍珠龙胆石斑鱼肠道形态、消化酶、抗氧化能力以及全鱼矿物元素沉积的影响. 广东饲料. 2023(05): 31-34 .  百度学术
百度学术
12. 武燕霓,安玥琦,熊善柏. 鱼汤风味的形成与调控研究进展. 食品科学. 2023(15): 251-260 .  百度学术
百度学术
其他类型引用(4)




 下载:
下载: