HARVESTING HAEMATOCOCCUS PLUVIALIS USING PH-INDUCED DISSOLVED AIR FLOTATION (DAF)
-
摘要: 为提高雨生红球藻(Haematococcus pluvialis)收获效率, 文章发现一种通过pH调控诱导雨生红球藻絮凝-气浮收获方法。通过与自然沉降对比发现, 在不添加混凝药剂的情况下, 调节藻液的pH可以诱导雨生红球藻细胞自发团聚形成絮体, 显著提高其沉降或气浮收获效率。pH小于3或大于11.5时, 气浮可在2min内实现95%左右的收获效率, 而自然沉降则需要30min, 才能达到80%—90%的收获效率。气浮收获后的生物质含固率要显著高于沉降收获, 当初始浓度为3.2 g/L时, pH诱导絮凝-气浮收获后的雨生红球藻生物质含固率可达到17%, 实现了53倍浓缩。另外, 与化学混凝剂(硫酸铝)和生物混凝剂(壳聚糖)混凝-气浮对比发现, pH诱导絮凝-气浮不仅可以实现传统药剂混凝-气浮的高收获效率, 还可以有效避免混凝剂对生物质的污染(如金属离子残留等), 且不会对雨生红球藻中虾青素提取产生影响。因此, pH调控诱导絮凝-气浮可以实现雨生红球藻的快速、高效和无污染收获, 为雨生红球藻的收获提供新的解决方案。Abstract: As an important raw material for the extraction of natural astaxanthin, Haematococcus pluvialis is usually harvested by natural sedimentation or centrifugation. However, these harvesting methods either take a long time or consume a lot of energy. This study proposed an efficient method for the harvesting H. pluvialis using pH-induced induced dissolved air flotation (DAF). Harvesting efficiency and solid content, as well as their kinetic curves, were adopted to investigate the influence of pH on the pH-induced DAF harvesting. In addition, the harvesting performances of pH-induced DAF was compared with those of pH-induced sedimentation, chemical coagulant (aluminum sulfate)- and biological coagulant (chitosan)-induced DAF, based on the efficiency and residual metal contents in the harvested biomass. Whether pH treatment affects the astaxanthin content in the harvested biomass was also evaluated, comparing with the content in centrifugation harvested biomass. The results showed that auto-flocculation occurred when the pH of the media was decreased or increased, facilitating the flotation harvesting and sedimentation harvesting of H. pluvialis. pH-induced DAF obtained higher harvesting efficiency and required less separation time, comparing with pH-induced sedimentation. When pH was adjusted to less than 3 or greater than 11.5, the harvesting efficiency of 95% was achieved in 2min using pH-induced DAF, while that took 30min for pH-induced sedimentation to achieve 80%—90% harvesting efficiency. When the initial concentration was 3.2 g/L, the solid content of biomass harvested by pH-induced DAF can reach 17%, realizing 53 times concentration, which was much higher than those harvested by pH-induced sedimentation. Most importantly, pH-induced DAF performed as well as aluminum sulfate and chitosan coagulants induced DAF, while avoiding the impurity of biomass caused by chemical such as Al3+. The astaxanthin contents in H. pluvialis biomass harvested by pH-induced DAF were not affected by the pH treatment. Therefore, harvesting H. pluvialis by pH-induced DAF proved to be a rapid, efficient and environmental sustainable technique, which shed a light on the process development of mass production of H. pluvialis biomass.
-
Keywords:
- Harvest /
- Air floatation /
- Flocculation /
- pH induction /
- Haematococcus pluvialis
-
虾青素由于其抗氧化性能被广泛应用到食品、化妆品、营养保健和医药、水产养殖等行业[1]。虾青素的抗氧化性是类胡萝卜素的10倍, 是维生素E的550倍, 被誉为“超级抗氧”, 有利于预防癌症、糖尿病、心血管疾病、溃疡、免疫反应和炎症等[2, 3]。同时由于虾青素是一种鲜红色的类胡萝卜素, 是鲑、虾和小龙虾等水产品的肉和壳红色的重要色素[4], 因此, 在水产品饲料中常会添加虾青素以改善水产品的体色、肉质和营养价值[5]。虾青素可以从天然原料中提取, 也可以合成获得。但是人工合成的虾青素由于其原材料固有的毒性等问题而使用较少, 占整个商业化份额不到1%, 大部分虾青素来源于天然原料的提取[6]。在天然原料中, 雨生红球藻(Haematococcus pluvialis)被认为是自然界中虾青素含量最高的生物, 被称为天然虾青素的“浓缩品”[7], 使其成为高附加值经济微藻技术研究的热点。
雨生红球藻是一种单细胞淡水绿藻, 和其他微藻细胞特征类似, 如细胞个体小(10—30 μm), 密度与水接近, 因表面带负电荷而稳定悬浮在培养液中等, 从而使得雨生红球藻的收获难, 收获过程能耗高, 成为其产业化过程的技术难题之一[8]。常用的雨生红球藻收获方式有沉降和过滤等方法。沉降法虽然经济性高, 但其收获时间长, 且收获的雨生红球藻生物质的含固率通常只有0.5%—1.5%, 仍需要高能耗的脱水等才能进入下一步的干燥环节[9]。离心法是快速、可靠的收获方式, 但由于较高的能耗和投资运行成本, 且高转速离心时, 藻细胞在离心机内壁摩擦导致破裂, 致使虾青素等营养成分溶出, 也不具备大规模应用的潜力[10]。过滤法仅在分离丝状藻时成本较低, 对于非丝状藻, 容易造成膜污染, 造成膜过滤堵塞, 也不是高效、低成本的收获方式[11]。
虽然沉降法是一种经济的固液分离方法, 已应用于微藻的收获或藻水分离, 但是藻细胞的沉降性能与其大小与密度密切相关。自然状态下由于藻细胞个体小, 密度与水接近, 使其自然沉降性能较差, 因此, 为了达到好的沉降效果, 通常添加混凝剂使藻细胞预先混凝, 生成大的絮体, 从而实现快速沉降[12]。由于藻细胞的密度与水接近, 即使混凝预处理, 其絮体沉降也相对较慢, 通常需要30min[13]; 气浮相对沉降在处理速度上具有明显优势, 尤其是针对藻细胞这种密度小的颗粒物, 一般5min就可以达到一个较理想的收获效率, 已广泛应用于微藻生物质的收获和水体中藻类的去除[14]。然而, 通常所采用的化学混凝剂(Al盐或Fe盐)预处理均会导致藻类生物质或水体中的金属离含量过高, 进而造成污染, 影响藻类生物质和水体的进一步使用[15], 从而限制了沉降或气浮法在微藻收获上的应用。
本文提出一种不需要添加混凝剂的pH诱导藻细胞絮凝-气浮收获雨生红球藻的新方法, 通过系统对比pH诱导絮凝后气浮与沉降的收获效率、含固率和二者的动力学曲线, 以及与混凝剂絮凝-气浮间的差异, 论证pH诱导絮凝-气浮收获雨生红球藻的技术优势; 并通过收获后雨生红球藻生物质中金属离子的残留和虾青素含量进一步证明了该收获方法的可行性, 为雨生红球藻的高效率、低成本收获提供了新的解决方案。
1. 材料与方法
1.1 实验材料
This page contains the following errors:
error on line 1 at column 1: Start tag expected, '<' not foundBelow is a rendering of the page up to the first error.
1.2 pH诱导絮凝-沉降收获
本文采用六联混凝搅拌仪(DBT6, EC Engineering, 美国)进行雨生红球藻的pH诱导絮凝-沉降收获批次试验。具体步骤如下: 取500 mL的雨生红球藻液加入1 L的混凝杯中, 通过加入NaOH或HCl调节藻液的pH, 先以100 r/min (速度梯度G=200s–1)快速搅拌2min, 再以30 r/min (速度梯度G=30/s)慢速搅拌10min, 使藻细胞絮凝, 形成团聚体或絮体, 然后静止沉降30min, 取50 mL上清液用于分析收获效率, 同时去掉上清后取50 mL底部堆集生物质用于分析含固率, 对照组不调节pH。
1.3 pH诱导絮凝-气浮收获
本文采用六联混凝搅拌仪(DBT6, EC Engineering, 美国)进行雨生红球藻的絮凝-气浮收获批次试验。pH诱导絮凝-气浮实验中的调节pH步骤与絮凝-沉降实验中相同, 调节pH后藻液絮凝, 此时通入100 mL的由压力溶气系统在0.55 MPa产生的溶气水, 加入比例为20%, 气泡通入后立即停止搅拌, 静止10min后, 取50 mL下清液用于分析收获效率, 并取50 mL表层的浮渣用于分析生物质含固率, 对照组不调节pH。
1.4 分析方法
絮体粒径分布 将不同预处理后生成的絮体转移至载玻片上, 利用显微镜(OLYMPUS BX53, 日本)图像识别及拍照系统, 随机拍取50张以上不同视野的照片, 保证每张照片至少20个絮体, 利用Adobe Photoshop (2019版)将50张照片进行合并, 再利用Image-J (1.4.3.67版)图像处理软件对图片上的絮体进行提取分析, 并利用标尺对分析的尺寸进行校准, 提取每个絮凝的等效直径, 并利用Origin (2021版)软件分析絮体粒径大小分布, 并绘制直方图[17]。
收获效率与含固率 根据干重法分析雨生红球藻的收获前的初始浓度(C0, g/L), 以及收获后的上清液、下清液的藻细胞浓度(CR, g/L)。通过气浮杯刻度读取收获前的初始体积(V0, L), 以及收获后最终藻层的体积(Vf, L), R(%)为气浮溶气水的加入比例, 根据生物质收获前后质量守恒定律结合气浮溶气水加入比例对最终浓度影响的校正[18, 19], 通过公式(1)计算收获后最终藻类生物质浓度(Cf, g/L), 通过公式(2)计算收获效率(HE, %), 然后通过公式(3)(4)计算收获后生物质的含固率(S, m/m, %)和浓缩倍率(CF), 根据多次实验比较, 通过此方法计算的藻层生物质浓度与通过干重法分析的生物质浓度误差在5%以内。
$ {C}_{f}=\frac{{C}_{0}{V}_{0}-{C}_{R}[{V}_{0}\left(1+R\right)-{V}_{f}]}{{V}_{F}} $
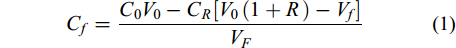
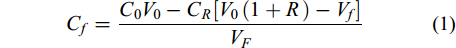
(1) $ HE = \frac{{C}_{f}{V}_{f}}{{C}_{0}{V}_{0}} = \left\{1 - \frac{{C}_{R}[{V}_{0}\left(1 + R\right)-{V}_{f}]}{{C}_{0}{V}_{0}}\right\} \times 100\text{%} $
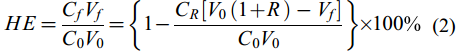
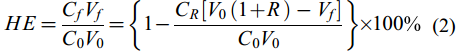
(2) $ S=\frac{{C}_{f}}{{\rho }_{水}} \times 100\text{%} $
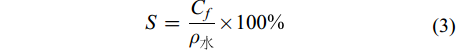
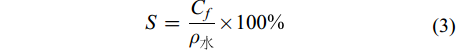
(3) $ CF=\frac{{C}_{f}}{{C}_{0}} $
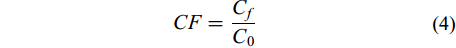
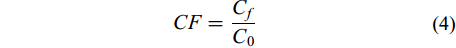
(4) 式中, 絮凝-气浮收获试验R=20%, 絮凝-沉淀收获试验R=0。
气浮与沉降动力学 在气浮或沉降过程中, 在设定的时间点(0、1min、2min、5min、10min、20min、30min和60min)读取气浮杯刻度得到Vf, 通过公式(2)计算收获效率, 通过公式(1)(3)计算含固率, 并绘制收获效率随时间变化的动力学曲线和含固率随时间变化的动力学曲线。
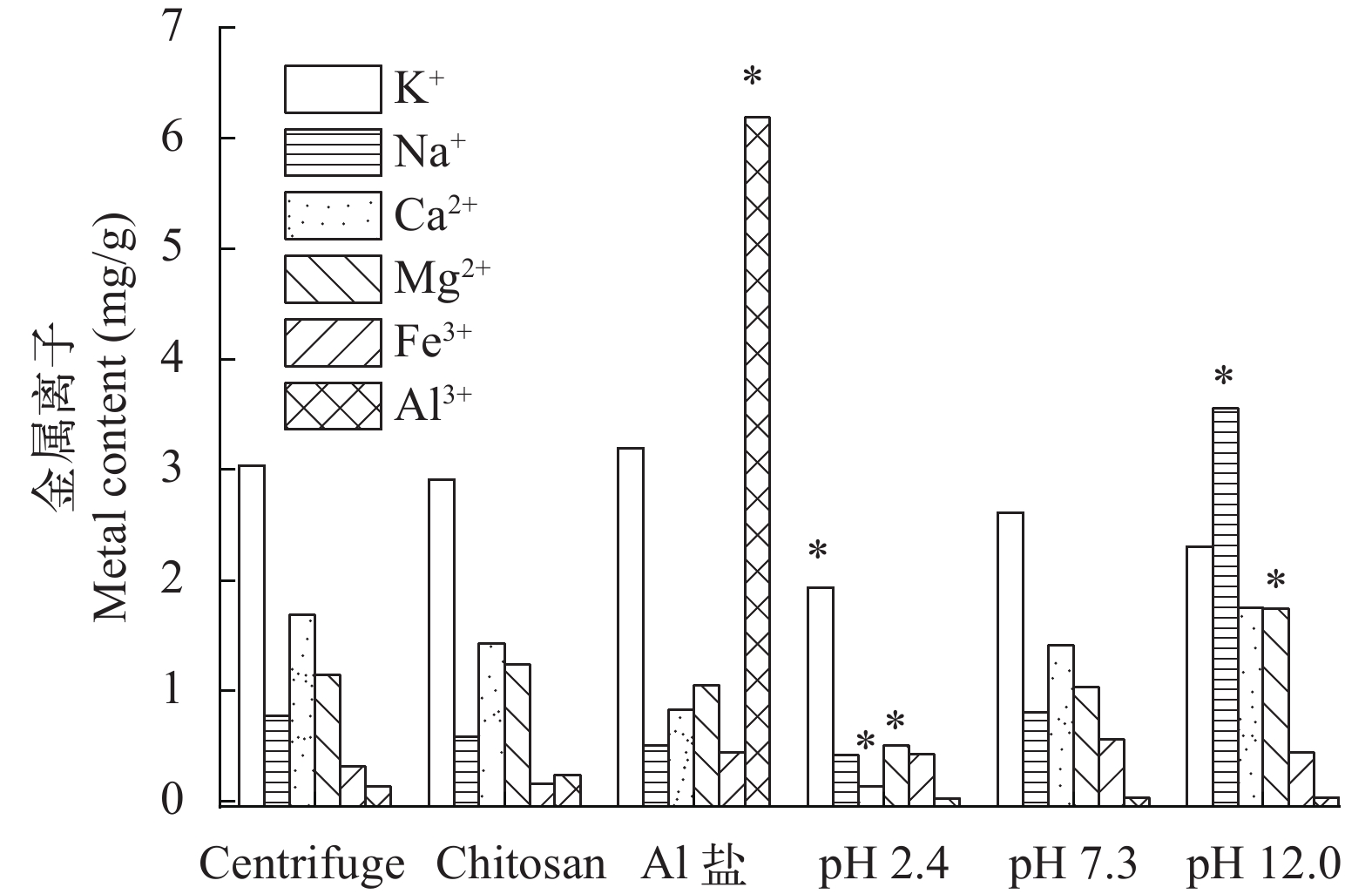
收获生物质中金属离子含量 将不同方式收获的微藻生物质于105℃烘箱中烘干后, 称取一定量的样品置于四氟乙烯消解管中, 加入7 mL浓硝酸和1 mL氢氟酸, 利用微波萃取消解仪(ETHOSUP, 意大利)在180℃下消解25min, 得到消解液, 然后利用赶酸仪(上海博通BHW, 中国), 在160℃去除多余的残留酸至样品体积为0.5—1.0 mL, 再加入2%硝酸定容至25 mL。消解后样品利用0.22 μm水系滤膜(MREDA聚醚砜, 美国)过滤, 并利用2%的硝酸稀释样品, 使金属离子含量低于200 mg/L, 再通过OPTIMA 8000DV电感耦合等离子体发射光谱(ICP-OES, PekinElmer, MA, 美国)测定各生物质中阳离子(Na+、K+、Ca2+、Mg2+、Fe3+和Al3+)含量。
虾青素提取与含量分析 采用超声辅助提取法从雨生红球藻中提取虾青素: 将10 mg冷冻干燥的雨生红球藻粉放入15 mL的离心管中, 加入8 mL丙酮进行充分混合, 样品置于冰浴中, 在20 kHz频率和375 w的超声(CPX 500, Cole- Parmer)下对样品进行脉冲模式(声波3s, 停止冷却3s)处理10min, 再通过离心(4000 r/min, 5min)收集上清液, 上述提取过程重复5次。所收集到的上清液在通过氮吹的方式蒸发, 然后再利用1 mL丙酮溶解, 得到含有虾青素的溶液, –20℃冷冻避光保存。取一定量含有虾青素溶液使用高效液相色谱(Waters 2695, 美国)测定, 通过与色素标准品的光谱特征和最大吸收波长的比较, 对雨生红球藻中的虾青素进行定量分析。
2. 结果
2.1 pH对雨生红球藻絮凝过程絮体大小的影响
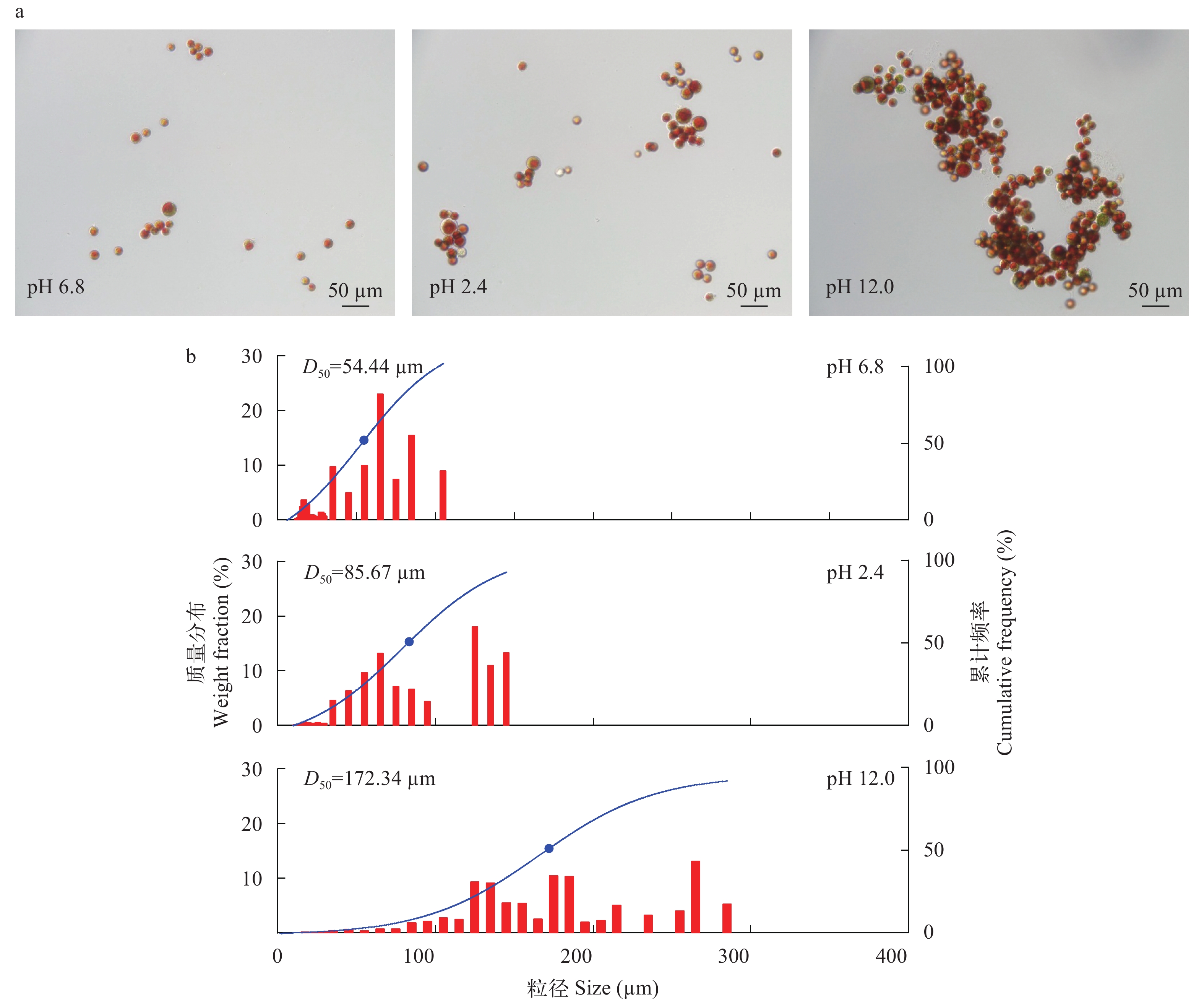
如图 1所示, 自然状态(pH 6.8)下的雨生红球藻细胞较为分散, 主要以单细胞或两三个细胞聚集体(10—100 μm)形式存在, 其质量比例占总数的91.10%, 而只有不到10%的藻细胞形成大于100 μm以上的絮体。而当藻液pH被调节到2.4时, 粒径在10—100 μm单细胞或两三个细胞聚集体明显减少, 占絮体总数量的57.78%, 100 μm以上的絮体数量增多, 占总数的42.22%。当藻液pH 12.0时, 藻细胞相互聚集明显增加, 絮体粒径增大, 100 μm以上的絮体比例达到了92.55%。进一步通过累计频率拟合曲线中可知, 原藻液中值粒径D50为54.44 μm, 当pH 2.4、pH 12.0的D50明显增大, 分别达到了85.67和172.34 μm。
2.2 pH对沉降收获效率与含固率的影响
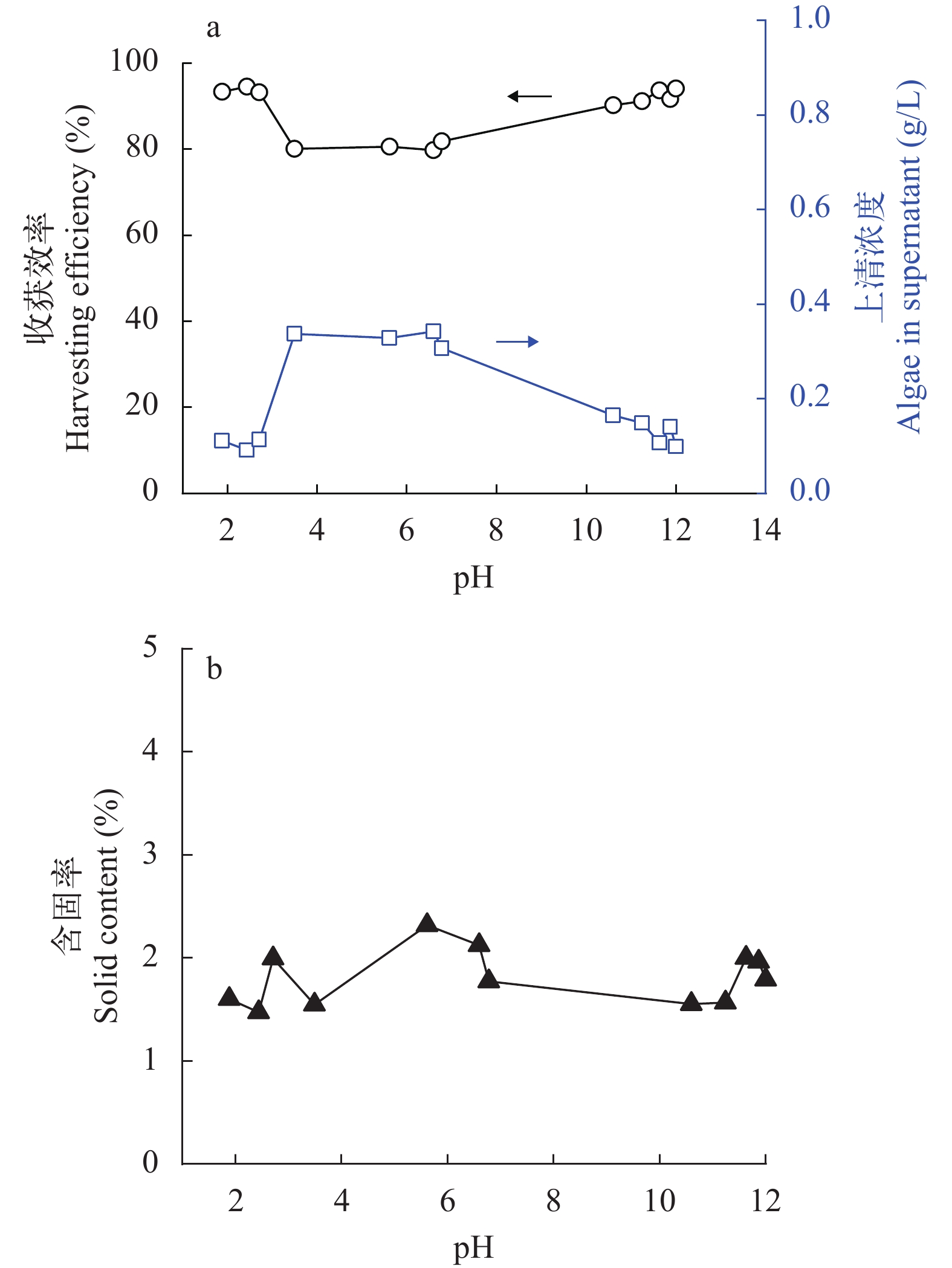
由图 2a可以看出, 在不调节pH (6.8)的情况下, 雨生红球藻自然沉降30 min后收获效率可达到80%。然而初始浓度1.7 g/L的藻细胞在自然沉降后上清液中仍然有0.3 g/L以上的藻细胞残留。通过调节pH对藻液进行预处理发现, 当pH在3.5—7时, 沉降收获效率与不调节pH时的变化不大, 仍然有20%左右的藻细胞残留在上清液中; 当pH低于2.7或者高于10.6时, 沉降收获效率显著增加到90%以上。同时, 上清液中残留的藻细胞明显降低到0.1 g/L左右。沉降收获后对底部堆积藻细胞的含固率分析如图 2b所示, 在不同pH条件下雨生红球藻细胞在沉降30min后含固率变化不大(1.47%—2.31%), 相对于收获前0.17%的含固率, 通过自然沉降或pH诱导沉降可使雨生红球浓缩8.6—13.6倍。
2.3 pH对气浮收获效率与含固率的影响
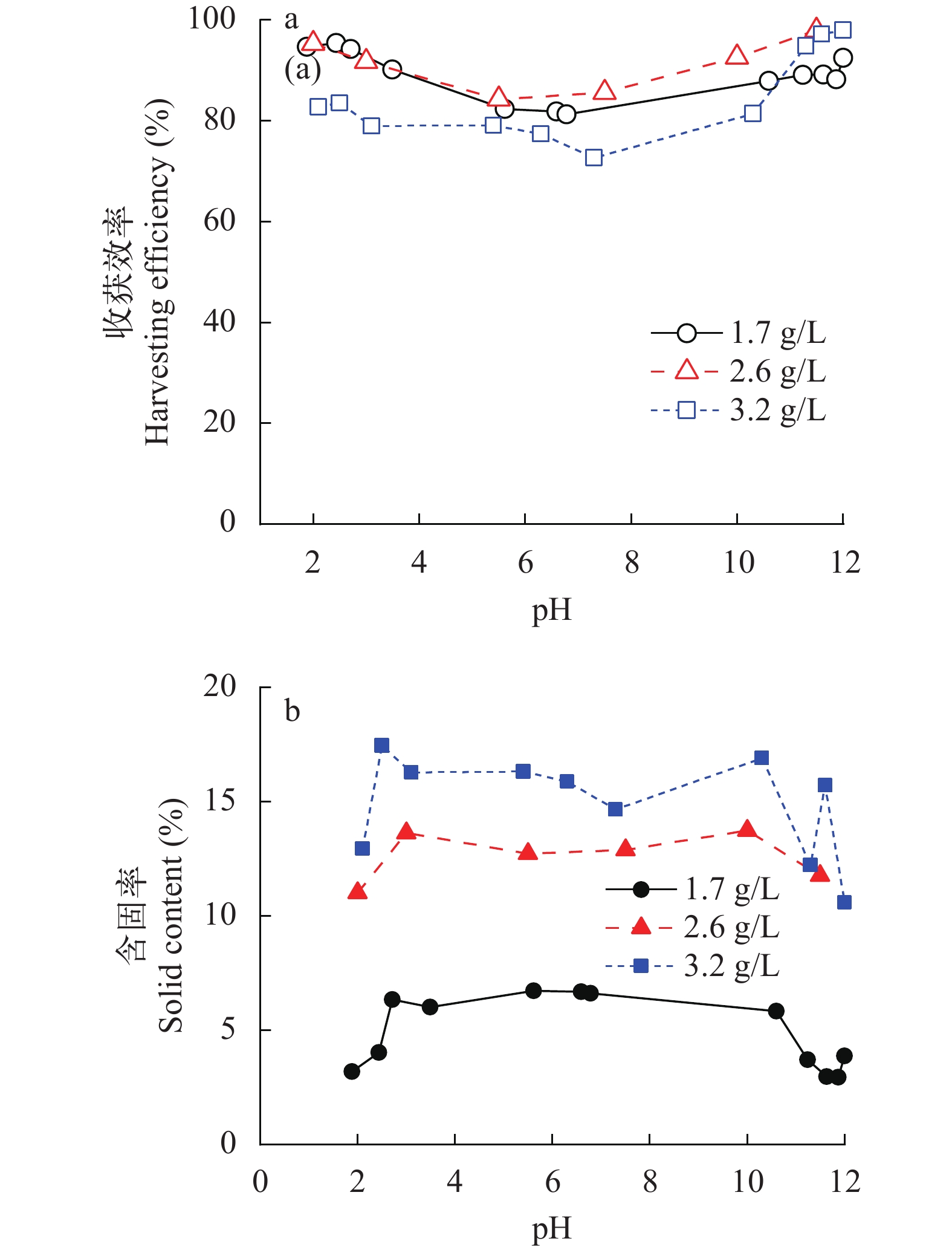
如图 3a所示, 当藻细胞初始浓度同样为1.7 g/L时, 在不调节pH条件下, 直接通入溶气水, 雨生红球藻的收获效率可以达到80%; 当低pH (3.5)和高pH (10)时, 气浮收获效率提高到90%。当藻细胞初始浓度增加到2.6 g/L时, 低pH (2.4)和高pH (11.3)诱导下的气浮收效率可达到95%以上。当初始浓度进一步增加到3.2 g/L时, 在pH 3—10时, 收获效率为77%—84%; 当pH高于11.3时, 气浮收效率同样可达到95%以上时。
由图 3b可知, pH诱导雨生红球藻气浮收获生物质的含固率要显著高于沉降收获。当初始浓度为1.7 g/L时, pH在2.7—10.6时, 气浮收获后的生物质含固率可以达到6%, 即气浮收获的浓缩倍数可达35倍; 但是继续增加或降低pH都会减少含固率。与气浮收获效率趋势不同的是, 当初始浓度增加到2.6和3.2 g/L时, 气浮收获后的含固率最大可以分别增加到13.7% (pH 10)和17.5% (pH 2.5), 即最大浓缩倍数可以达到53和55倍。在pH 3—10内, 气浮收获生物质的含固率最高。
2.4 pH对收获效率与含固率的动力学影响
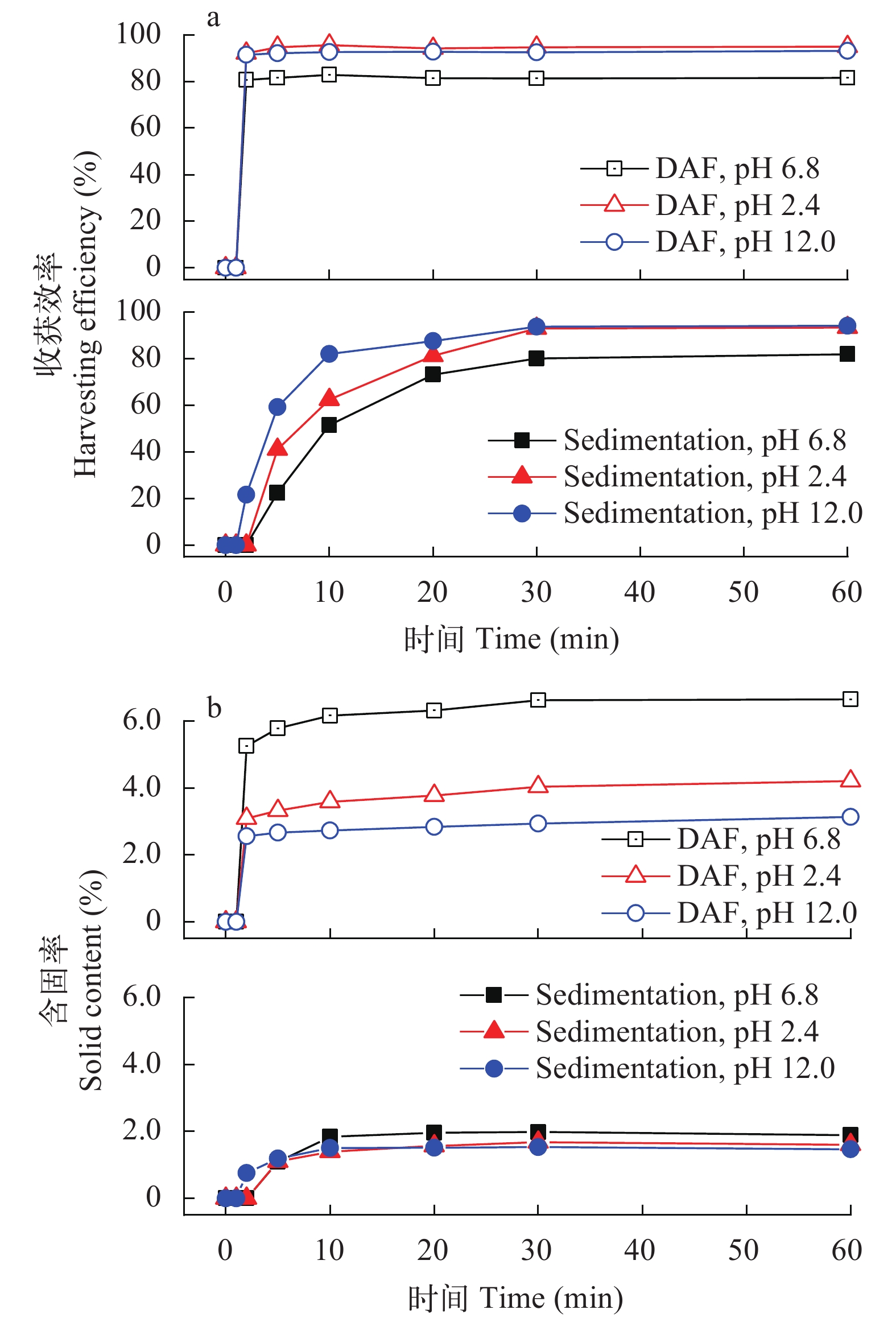
如图 4所示, 在不调节pH (6.8)的情况下, 通入气泡2min后, 收获效率可以达到80.6%; 当调低pH (2.4)或调高pH (12.0)时, 气浮2min后的收获效率可达到92%; 继续延长气浮时间, 收获效率并没有显著变化。然而, 对于沉降收获雨生红球藻时, 无论是低、中、高pH, 都需要30min才能达到最大的收获效率。气浮或沉降收获后的含固率的动力学曲线与收获效率的却不完全相似, 气浮2min后, 对不同pH条件下的气浮对雨生红球藻可以快速实现相对大的浓缩, 含固率分别可以达到3.1%、5.3%和2.6%。随着气浮时间的增加, 含固率也逐渐增加, 只有在气浮60min后, 含固率分别达到最大值4.2%、6.7%和3.1%。对于沉降收获, 沉降10min后, 低中高pH条件对应的含固率可达到近似的稳定, 分别为1.4%、1.8%和1.5%, 继续增加沉降时间, 含固率有略微增加, 但不明显。
2.5 pH诱导絮凝与药剂混凝气浮获效率与收获生物质含固率的比较
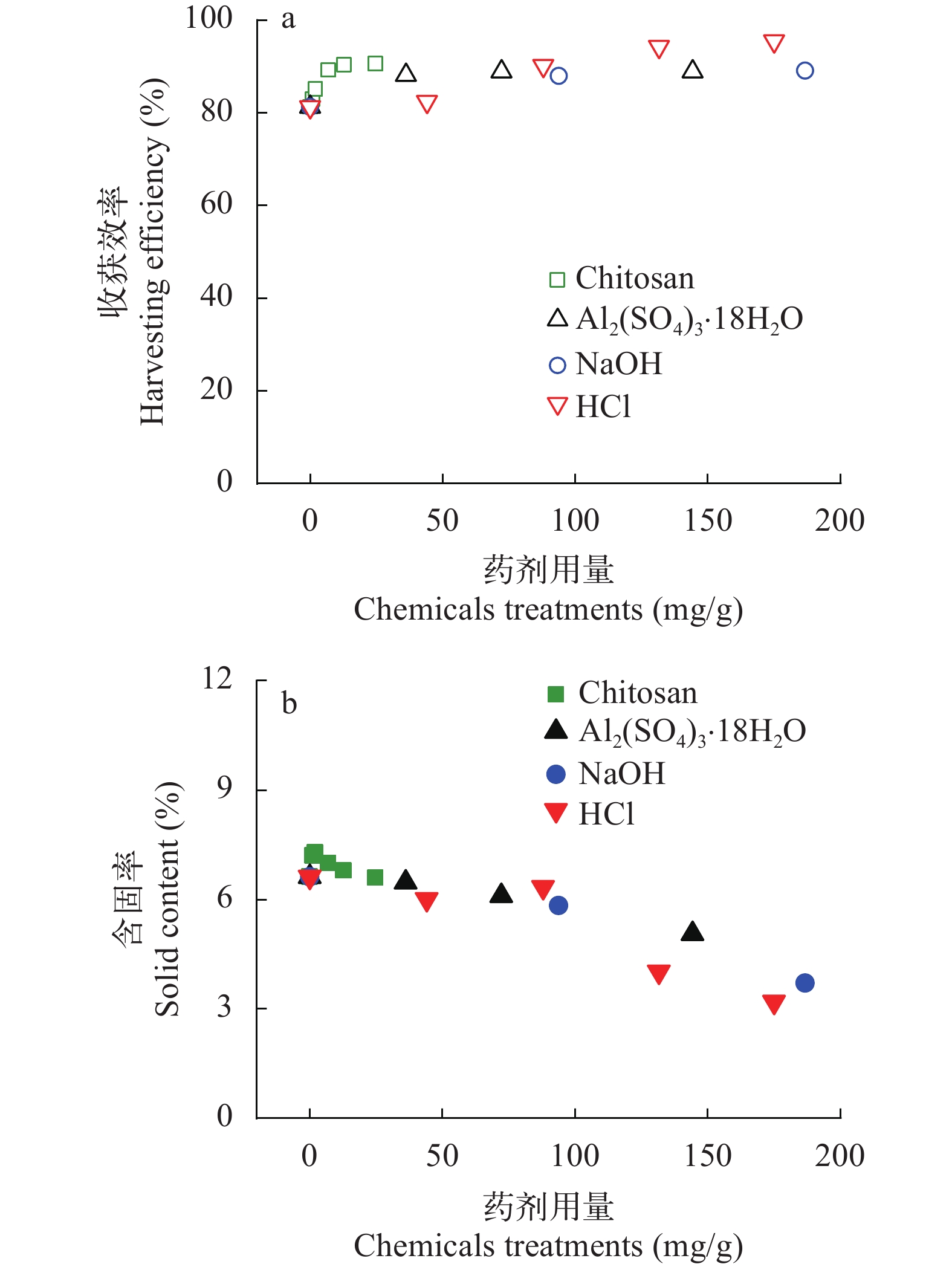
利用化学混凝剂(硫酸铝)和生物混凝剂(壳聚糖)以及pH诱导(NaOH或HCl)分别对雨生红球藻细胞进行预处理, 其气浮收获效率和含固率如图 5a所示。随着药剂用量的增加, 气浮收获效率从80%增加到90%以上。在达到最大收获效率时, 壳聚糖、硫酸铝、NaOH和HCl的用量分别为12.8、36.1、93.7和131.6 mg/g。另外, 通过HCl酸化预处理雨生红球藻的气浮收获效率可以达到95%以上, 而混凝剂(硫酸铝和壳聚糖)和NaOH预处理的气浮收获效率只能达到90%。由图 5b可知, 添加1.9 mg/g壳聚糖预处理时, 含固率从6.62%增加到7.3%, 进一步增加壳聚糖时, 含固率反而降低; 其他3种预处理方式均随着用量的增加, 含固率显著降低。在实验对应的最大用量时, 壳聚糖(24.7 mg/g)、硫酸铝(144.3 mg/g)、NaOH (186.7 mg/g)和HCl (175.1 mg/g)所获得的生物质的含固率分别为6.6%、5.1%、3.7%和3.2%。
3. 讨论
3.1 pH诱导雨生红球藻细胞絮凝分析
在不调节pH和不添加混凝剂的情况下, 雨生红球藻在自然沉降30min后, 收获效率可以达到80%, 说明雨生红球藻细胞具有较好的自沉降性能。雨生红球藻细胞表现出较好的自沉降性能可能与其自身的细胞尺寸分布特性有关。自然状态下其粒径主要分布在10—100 μm, D50为54.44 μm, 明显大于小球藻(Chlorella sorokiniana; 3—8 μm)和栅藻(Scenedesmus dimorphus; 5—30 μm)等藻细胞[20, 21]。因此, 在没有任何处理的自然沉降条件下雨生红球藻细胞就具有较好的沉降性能, 而其他粒径更小的藻细胞自然沉降较慢, 能较长时间稳定悬浮在培养液中。如Tan等[12]研究发现, 栅藻在沉降15min后, 沉降效率只有40%, 且沉降效率已明显趋于平缓, 说明其自然沉降效率难以随时间的增加而进一步显著增加。
随着生长时期的延长, 环境pH或藻细胞表面性质的改变, 部分藻细胞会发生团聚, 形成少量小的团聚体。研究表明, 当pH降低时, 藻细胞表面的羧基、磷酸根等基团由于质子化作用, 使得其表面的负电荷减少, 从而减少了藻细胞间的静电排斥作用, 打破了原有藻细胞稳定分散的平衡而相互聚集, 形成絮体[22, 23], 尤其是在接近其等电点附近时, 藻细胞表面电荷接近零, 藻细胞会发生明显团聚[24, 25]。当调高pH至碱性时, 会使得培养液中残留的Ca2+和Mg2+离子等形成荷正电沉淀物, 这些沉淀物可以通过类似混凝剂的网捕或卷扫等作用使藻细胞絮凝[25, 26]。
基于以上原因, 从而实现在不添加混凝剂的情况, 通过调低或调高pH诱导雨生红球藻细胞发生絮凝的现象。
3.2 pH诱导对雨生红球藻絮凝-沉降/气浮收获的影响分析
相比自然沉降, 调低或调高pH诱导雨生红球藻细胞絮凝生成团聚体, 可以明显提升其沉降效率, 这主要由于在pH诱导下, 藻细胞相互聚集, 形成数量更多、直径更大的絮体, 显著提高雨生红球藻的沉降性能[12]。同时, 由粒径分布对比图 1b可知, pH诱导下以单细胞形式存在的雨生红球藻(≤30 μm)明显减少。研究表明, 水体中的微细颗粒由于其粒径较小, 且表面荷负电, 能稳定悬浮在水溶液中[25]。因此, pH诱导雨生红球藻絮凝, 不仅增加了其粒径分布, 同时减少其能稳定悬浮的单细胞形态的细胞数量, 从而整体显著提升沉降收获效率, 使得收获效率可以增加到90%以上。
在气浮过程中, 与单细胞雨生红球藻相比, pH降低或升高时产生了粒径较大的藻细胞团聚体, 其与气泡之间的碰撞效率明显提高[27]。另外, 气泡表面荷负电, 当pH降低时, 絮体表面的电负性变弱, 容易黏附于气泡; 当pH增加到10以上时, 溶液中部分Ca2+和Mg2+离子形成荷正电胶体附着于团聚体上, 同样有利于与气泡的黏附, 提高气浮的效率[14]。因此在pH预处理后, 气浮收获效率可从80%增加到95%以上。
同时, 由沉降/气浮动力学曲线可以看出, pH诱导雨生红球藻细胞絮凝, 可以显著加快藻细胞的沉降或浮升性能, 即在相同的时间, 酸性或碱性处理的藻细胞比自然状态下的藻细胞的收获效率更高。根据Stokes沉降速度公式可知, 颗粒的沉降速度与细胞有效直径成正比[28], 因此pH诱导絮凝后, 增加了藻细胞团聚体的沉降速度, 进而使得pH调节后藻细胞的沉降效率高于自然状态的藻细胞。尤其当pH调节到12时, 由于可以形成粒径更大的絮体(D50为172.34 μm), 其沉降性能更高。对于气浮而言, 增加粒径可以提高絮体对气泡黏附概率, 增加絮体上气泡的黏附数量, 降低带气絮体的密度, 从而提高絮体的上浮速度[14], 研究表明, 微藻絮体(不带气泡)的沉降速度只有5 m/h[29], 而带有气泡的微藻絮体的上浮速度可以达到100 m/h[30], 比沉降的速度提高了近20倍, 因此, pH处理后的雨生红球藻细胞的气浮动力学更快, 实现了雨生红球藻的快速收获。
沉降收获后的含固率为2%左右, 不能直接用于干燥, 通常还需要进一步脱水处理, 以提高收获后的浓缩倍数。而气浮收获后的含固率可以达到5%, 甚至10%以上, 要明显高于沉降收获后的含固率, 可以基本满足喷雾干燥的入料要求[9]。这主要由于气浮过程中, 在气泡浮力的推动下, 使表层的藻细胞堆积层压缩, 形成较紧实的生物质浮渣层, 从而使得气浮收获的含固率要高于沉降收获, 尤其是当初始浓度高时, 气浮层的含固率更高。另外, 当pH≤3或≥10时诱导雨生红球藻絮凝, 无论是沉降还是气浮, 其收获后生物质的含固率均略低于自然状态下的藻细胞, 尤其当pH为12时形成的大絮体更为明显。研究表明, 在混凝过程中, 随着絮体尺寸的不断增加, 絮体的分支和孔隙也会增加, 从而降低了絮体的紧实度, 形成更加松散的絮体[31]。由图 1a中絮体形貌也可以看出, pH 12时的絮体明显更松散, 因而在沉降或气浮后, 其收获后的生物质含固率更低。
整体而言, pH诱导絮凝-气浮较絮凝-沉降收获雨生红球藻不仅效率更高, 对收获后的生物质也具有更好的浓缩效果。
3.3 pH诱导絮凝-气浮收获雨生红球藻细胞的优势分析
由pH诱导后的沉降和气浮收获效率的动力学曲线可知, 沉降需要30min才能达到90%以上的收获效率, 而气浮仅需要2min即可达到90%以上的收获效率, 对比沉降收获, 气浮收获雨生红球藻时在处理时效上更具有优势。同时, 气浮收获雨生红球藻具有较高的含固率, 最高可达17%, 可以省去进一步的离心、压滤等机械脱水过程, 直接进行干燥处理或虾青素提取, 可大幅度降低下游处理成本。
与化学混凝剂(硫酸铝)和生物混凝剂(壳聚糖)的混凝-气浮相比可以发现, 在不添加混凝剂的条件下, 通过pH诱导絮凝-气浮同样可以实现95%左右的收获效率。如图 6所示, 化学混凝剂会显著富集到收获的藻类生物质中, 生物质中的Al3+含量显著高于离心或自然状态下的生物质, 造成对生物质的污染, 从而影响生物质的进一步利用。虽然生物混凝剂一般来说对生物质没有污染, 但其价格较高, 如壳聚糖的价格在15万/吨, 使得收获成本较高。而pH诱导下的絮凝-气浮收获的雨生红球藻生物质中的金属元素含量与离心和生物混凝剂收获的相当, 甚至更低(pH 2.4)。因此, pH诱导絮凝-气浮不仅可以达到化学混凝-气浮的收获的高效率, 还可以有效避免化学混凝剂对生物质的污染。
另外, 收获过程是否会对微藻生物质中营养成分的含量与提取产生影响也是必须考虑的, 一种好的收获方式不仅应具有高效率、低成本, 还不能对生物质产生污染, 以及不能对生物质中的营养成分产生影响[16], 本研究以虾青素含量为分析指标[32, 33], 通过对比离心和pH诱导絮凝-气浮收获后的雨生红球藻生物质中的虾青素含量可以看出(表 1), 通过HCl或NaOH调节pH对雨生红球藻的虾青素含量并没有明显的影响, 其含量与离心和自然沉降的相当(2.3%—2.5%), 这主要由于本文中的pH预处理比传统雨生红球藻酸碱破壁提取虾青素的条件更加温和[34]。另外, 虾青素的活性通常是由物质和成分决定的, 从短时间pH预处理过的雨生红球藻提取的虾青素, 与通过酸碱破壁法提取虾青素过程相似, 因此可以推断pH诱导气浮收获雨生红球藻对其提取的虾青素的活性不会产生影响。综上所述, pH诱导絮凝-气浮可以实现雨生红球藻的高效率、高浓缩倍率、低成本和快速的收获, 同时也可以避免传统化学混凝剂对生物质的污染, 且不会对虾青素的提取产生影响; 为雨生红球藻的收获提供新的解决方案, 有望推广应用于雨生红球藻的大规模生产。
表 1 不同pH诱导气浮收获的雨生红球藻生物量中虾青素含量Table 1. Astaxanthin contents in the harvested H. pluvialis biomass with different pH treatments处理方式
Treatment虾青素含量
Astaxanthin contents (%)pH 2.4 2.30±0.06 pH 7.3 2.33±0.02 pH 12.0 2.36±0.03 离心Centrifuge 2.42±0.05 4. 结论
本文提出一种pH诱导絮凝-气浮的雨生红球藻收获方法, 实验研究表明, 无需添加任何混凝剂, 通过降低或提高藻液的pH就可以诱导藻细胞自发絮凝, 从而显著提高其收获效率从80%提高到95%。絮凝-气浮可在2min中实现95%左右的收获效率, 而絮凝-沉降则需要30min, 并且气浮收获后的含固率(最高17%)要显著高于沉降收获的(2%)。与传统混凝剂(硫酸铝和壳聚糖)絮凝-气浮对比发现, pH诱导絮凝-气浮不仅可以实现同样高的收获效率和含固率, 也不会造成生物质中金属离子增加, 且与生物混凝剂相比具有明显成本优势; 另外, 不同pH处理对虾青素的含量不会产生影响。因此, pH诱导絮凝-气浮有望实现雨生红球藻的快速、高效和无污染收获, 为雨生红球藻的大规模收获提供新的思路。
-
表 1 不同pH诱导气浮收获的雨生红球藻生物量中虾青素含量
Table 1 Astaxanthin contents in the harvested H. pluvialis biomass with different pH treatments
处理方式
Treatment虾青素含量
Astaxanthin contents (%)pH 2.4 2.30±0.06 pH 7.3 2.33±0.02 pH 12.0 2.36±0.03 离心Centrifuge 2.42±0.05 -
[1] 胡红伟, 闫凌鹏, 麻啸涛, 等. 虾青素在水产养殖中的应用研究进展 [J]. 饲料博览, 2021(7): 10-18. doi: 10.3969/j.issn.1001-0084.2021.07.003 Hu H W, Yan L P, Ma X T, et al. Application research progress on astaxanthin in aquaculture [J]. Feed Review, 2021(7): 10-18. doi: 10.3969/j.issn.1001-0084.2021.07.003
[2] 樊生华. 超级维生素E-虾青素 [J]. 中国科技信息, 2005(21): 52. Fan S H. Super vitamin E-astaxanthin [J]. China Science and Technology Information, 2005(21): 52.
[3] Yuan J P, Peng J, Yin K, et al. Potential health-promoting effects of astaxanthin: a high-value carotenoid mostly from microalgae [J]. Molecular Nutrition & Food Research, 2011, 55(1): 150-165.
[4] Koller M, Muhr A, Braunegg G. Microalgae as versatile cellular factories for valued products [J]. Algal Research, 2014(6): 52-63. doi: 10.1016/j.algal.2014.09.002
[5] Nogueira N, Canada P, Caboz J, et al. Effect of different levels of synthetic astaxanthin on growth, skin color and lipid metabolism of commercial sized red porgy (Pagrus pagrus) [J]. Animal Feed Science and Technology, 2021(276): 114916. doi: 10.1016/j.anifeedsci.2021.114916
[6] Khoo K S, Lee S Y, Ooi C W, et al. Recent advances in biorefinery of astaxanthin from Haematococcus pluvialis [J]. Bioresource Technology, 2019(288): 121606. doi: 10.1016/j.biortech.2019.121606
[7] 王潮岗, 韩燊, 陈甄倩, 等. 雨生红球藻抗氧化系统对活性氧的清除机制 [J]. 水生生物学报, 2012, 36(4): 804-808. Wang C G, Han S, Chen Z Q, et al. The scavenging of reactive oxygen species with antioxidant systems in Haematococcus pluvialis [J]. Acta Hydrobiologica Sinica, 2012, 36(4): 804-808.
[8] Şirin S, Trobajo R, Ibanez C, et al. Harvesting the microalgae Phaeodactylum tricornutum with polyaluminum chloride, aluminium sulphate, chitosan and alkalinity-induced flocculation [J]. Journal of Applied Phycology, 2012, 24(5): 1067-1080. doi: 10.1007/s10811-011-9736-6
[9] Zhang H, Gong T, Li J, et al. Study on the effect of spray drying process on the quality of microalgal biomass: a comprehensive biocomposition analysis of spray-dried S. acuminatus biomass [J]. BioEnergy Research, 2022, 15(1): 320-333. doi: 10.1007/s12155-021-10343-8
[10] Vandamme D, Foubert I, Meesschaert B, et al. Flocculation of microalgae using cationic starch [J]. Journal of Applied Phycology, 2010, 22(4): 525-530. doi: 10.1007/s10811-009-9488-8
[11] Barros A I, Gonçalves A L, Simões M, et al. Harvesting techniques applied to microalgae: a review [J]. Renewable and Sustainable Energy Reviews, 2015(41): 1489-1500. doi: 10.1016/j.rser.2014.09.037
[12] Tan D, Zhang H, Sun S, et al. Rapid flocculation-sedimentation of microalgae with organosilane-functionalized halloysite [J]. Applied Clay Science, 2019(177): 37-42. doi: 10.1016/j.clay.2019.05.005
[13] Chatsungnoen T, Chisti Y. Harvesting microalgae by flocculation-sedimentation [J]. Algal Research, 2016(13): 271-283. doi: 10.1016/j.algal.2015.12.009
[14] Zhang H, Zhang X. Microalgal harvesting using foam flotation: A critical review [J]. Biomass and Bioenergy, 2019(120): 176-188. doi: 10.1016/j.biombioe.2018.11.018
[15] Yang L, Wang L, Zhang H, et al. A novel low cost microalgal harvesting technique with coagulant recovery and recycling [J]. Bioresource Technology, 2018(266): 343-348. doi: 10.1016/j.biortech.2018.06.105
[16] 张宝玉, 李夜光, 耿亚红, 等. 适合大量培养的红球藻藻种的筛选 [J]. 水生生物学报, 2004, 28(3): 289-293. doi: 10.3321/j.issn:1000-3207.2004.03.011 Zhang B Y, Li Y G, Geng Y H, et al. Selection of Haematococcus strains suitable for mass culture [J]. Acta Hydrobiologica Sinica, 2004, 28(3): 289-293. doi: 10.3321/j.issn:1000-3207.2004.03.011
[17] Zhang H, Yang L, Zang X, et al. Effect of shear rate on floc characteristics and concentration factors for the harvesting of Chlorella vulgaris using coagulation-flocculation-sedimentation [J]. Science of the Total Environment, 2019(688): 811-817. doi: 10.1016/j.scitotenv.2019.06.321
[18] Teixeira M R, Rosa M J. Comparing dissolved air flotation and conventional sedimentation to remove cyanobacterial cells of Microcystis aeruginosa part I: the key operating conditions [J]. Separation and Purification Technology, 2006, 52(1): 84-94. doi: 10.1016/j.seppur.2006.03.017
[19] Kandasamy G, Shaleh S R M. Flotation removal of the microalga Nannochloropsis sp. using Moringa protein-oil emulsion: a novel green approach [J]. Bioresource Technology, 2018(247): 327-331. doi: 10.1016/j.biortech.2017.08.187
[20] 高正, 杨钰娟, 薛春叶, 等. 三氯化铁絮凝小球藻的采收工艺 [J]. 广东海洋大学学报, 2021, 41(2): 41-46. doi: 10.3969/j.issn.1673-9159.2021.02.006 Gao Z, Yang Y J, Xue C Y, et al. Harvesting technology of Chlorella sorokiniana using FeCl3 as a flocculant [J]. Journal of Guangdong Ocean University, 2021, 41(2): 41-46. doi: 10.3969/j.issn.1673-9159.2021.02.006
[21] Ye J, Sha J, Liu Q, et al. Influence of growth phase on the harvesting of Scenedesmus acuminatus using ultrafiltration [J]. Science of the Total Environment, 2019(660): 25-31. doi: 10.1016/j.scitotenv.2019.01.020
[22] Liu J, Zhu Y, Tao Y, et al. Freshwater microalgae harvested via flocculation induced by pH decrease [J]. Biotechnology for Biofuels, 2013, 6(1): 98. doi: 10.1186/1754-6834-6-98
[23] Zang X, Zhang H, Liu Q, et al. Harvesting of microcystis flos-aquae using chitosan coagulation: influence of proton-active functional groups originating from extracellular and intracellular organic matter [J]. Water Research, 2020(185): 116272. doi: 10.1016/j.watres.2020.116272
[24] 张晋阳, 王慧岭, 滕杰, 等. 微藻自絮凝采收工艺研究 [J]. 安徽农业科学, 2018, 46(18): 57-58. doi: 10.3969/j.issn.0517-6611.2018.18.018 Zhang J Y, Wang H L, Teng J, et al. Study on self-flocculation harvesting technology of microalgae [J]. Journal of Anhui Agricultural Sciences, 2018, 46(18): 57-58. doi: 10.3969/j.issn.0517-6611.2018.18.018
[25] Vandamme D, Foubert I, Muylaert K. Flocculation as a low-cost method for harvesting microalgae for bulk biomass production [J]. Trends in Biotechnology, 2013, 31(4): 233-239. doi: 10.1016/j.tibtech.2012.12.005
[26] Zhang X, Wang L, Sommerfeld M, et al. Harvesting microalgal biomass using magnesium coagulation-dissolved air flotation [J]. Biomass and Bioenergy, 2016(93): 43-49. doi: 10.1016/j.biombioe.2016.06.024
[27] Zhang X, Hewson J C, Amendola P, et al. Critical evaluation and modeling of algal harvesting using dissolved air flotation [J]. Biotechnology and Bioengineering, 2014, 111(12): 2477-2485. doi: 10.1002/bit.25300
[28] 常青. 水处理絮凝学 第二版 [M]. 北京: 化学工业出版社, 2011: 1-2. Chang Q. Flocculation in Water Treatment [M]. Beijing: Chemical Industry Press, 2011: 1-2.
[29] Zhang H, Liu C, Ou Y, et al. Development of a helical coagulation reactor for harvesting microalgae [J]. Journal of Bioscience and Bioengineering, 2019, 127(4): 447-450. doi: 10.1016/j.jbiosc.2018.09.012
[30] Zhang H, Lin Z, Tan D, et al. A novel method to harvest Chlorella sp. by co-flocculation/air flotation [J]. Biotechnology Letters, 2017, 39(1): 79-84. doi: 10.1007/s10529-016-2219-8
[31] Carissimi E, Rubio J. The flocs generator reactor-FGR: a new basis for flocculation and solid-liquid separation [J]. International Journal of Mineral Processing, 2005, 75(3/4): 237-247.
[32] 许文鑫, 朱琴, 朱梅, 等. UV-B对雨生红球藻生长及虾青素积累的影响 [J]. 水生生物学报, 2021, 45(6): 1281-1290. Xu W X, Zhu Q, Zhu M, et al. Ultraviolet-b radiation enhances the growth and astaxanthin production in Haematococcus pluvialis [J]. Acta Hydrobiologica Sinica, 2021, 45(6): 1281-1290.
[33] 孙双, 张婷, 方琰, 等. 雨生红球藻高产虾青素的培养条件优化 [J]. 现代食品科技, 2021, 37(6): 98-107. Sun S, Zhang T, Fang Y, et al. Optimization of culture medium for high-yield astaxanthin in Haematococcus pluvialis [J]. Modern Food Science and Technology, 2021, 37(6): 98-107.
[34] 任晓丽, 陈林, 刘天中, 等. 破壁方法对雨生红球藻湿藻生物质中虾青素提取的影响 [J]. 中国食品学报, 2018, 18(12): 110-117. Ren X L, Chen L, Liu T Z, et al. The effect of cell-wall disruption methods on astaxanthin extraction from wet algal biomass of Haematococcus pluvialis [J]. Journal of Chinese Institute of Food Science and Technology, 2018, 18(12): 110-117.



 下载:
下载: