SUSTAINED SWIMMING ON THE ENDURANCE TIME AND PHYSIOLOGICAL METABOLISM OF ACANTHOPAGRUS SCHLEGELI AND SCIAENOPS OCELLATUS
-
摘要: 为了确保黑鲷(Acanthopagrus schlegeli)和美国红鱼(Sciaenops ocellatus)在开放海域的养殖产量和鱼类养殖福利, 在20℃下, 对体长差异性不显著(P>0.05)的两种鱼进行续航游泳能力测试。首先, 确定不同流速下的耐力游泳时间, 然后选择耐力游泳时间为150min时的速度进行续航游泳实验。其中黑鲷和美国红鱼分别被迫以3.15和4.32 BL/s的恒定游泳速度, 进行0、30min、60min、90min、120min和150min的测试, 解剖鱼获得肌肉、血液和肝脏, 测定样品在6个时间点的代谢物浓度, 每个时间点保证3组有效数据。对0和150min的实验组对比, 结果显示, 两种鱼肝糖原、背肌乳酸和血糖浓度差异显著(P<0.05), 肌肉糖原浓度差异不显著(P>0.05)。双变量相关分析显示, 随着疲劳程度增加, 肝糖原浓度下降, 背肌乳酸和血糖上升。灰度关联分析和主成分分析显示, 血糖和肝糖原浓度是影响疲劳的主要因素, 但黑鲷相比美国红鱼, 其浓度变化范围更大。综上: (1)美国红鱼比黑鲷拥有更强的游泳能力, 而且黑鲷和美国红鱼不适合养殖在流速超过3.15和4.32 BL/s的环境中; (2)肝糖原浓度是限制两种鱼续航游泳能力的关键因素, 实验结果为其他鱼类游泳和代谢的研究提供参考。Abstract: It has become possible to set up deep-water cages in the open ocean in response to the further development of the marine aquaculture industry. In these conditions, fish encounter strong currents and waves, and ensuring their wellness becomes a crucial part of the farming process, so studying the endurance of farmed fish species is necessary. However, there are few studies on the ability of fish to swim continuously in constant current mode. Breeding of black snapper and American redfish is currently expanding into more open waters, so its endurance swimming ability needs to be assessed to ensure farmed yields and fish farming welfare. At 20℃, we tested the endurance swimming ability of two fish with no significant differences in body length (P>0.05). First, determine the endurance swimming time at different flow rates, and then choose the speed when the endurance swimming time is 150min to carry out the endurance swimming experiment. Black snapper and American redfish were tested for 0, 30min, 60min, 90min, 120min and 150min at constant swimming speeds of 3.15 and 4.32 BL/s, respectively. Measure the concentrations of metabolites in the muscle, blood, and liver of the fish at six-time points, ensuring that each time point produces three sets of valid data. At 0 and 150min, the concentrations of fish liver glycogen, back muscle lactic acid, and blood glucose were significantly different between the experimental groups (P<0.05), but the concentrations of muscle glycogen was not (P>0.05). A bivariate correlation analysis revealed that liver glycogen concentration decreased and dorsal muscle lactate and blood glucose increased with increasing fatigue. Gray-scale correlation analysis and principal component analysis showed that blood glucose and liver glycogen concentrations were the main factors affecting fatigue. However, the concentration range of black sea bream was larger than that of American redfish. Our experimental results concluded that: (1) American redfish have stronger swimming abilities than black snapper, and black snapper and American redfish are unsuitable for culture at flow rates exceeding 3.15 and 4.32 BL/s, respectively. (2) Liver glycogen concentration limits the endurance swimming ability of both fishes, and the results also provide a reference for the study on swimming and metabolism in other fishes.
-
水产养殖业(淡水和海洋)有着巨大的发展前景。预计到21世纪中叶, 全球水产养殖产量相比2014年的7380万吨将至少增长一倍[1, 2]。在粮食安全方面, 海洋水产养殖业的繁荣为持续增加的人口提供了重要保障[3, 4]。然而, 在开放海域养殖面临着一些关键问题。例如, 强大而持续的洋流将考验鱼类的持续游泳能力。尽管有许多关于鱼类游泳能力的详细记录[5], 考虑到海洋经济鱼类品种的多样化, 分别对每种鱼类进行研究, 不仅繁琐, 而且难以模拟真实的养殖环境。远海网箱技术的进步, 也对鱼类游泳能力的研究和养殖鱼种的选择提出了新的要求。
美国红鱼(Sciaenops ocellatus)起源于大西洋的东部和南部, 属于石首鱼科(Sciaenidae)[6]。黑鲷(Acanthopagrus schlegeli)属于鲷科(Sparidae), 在中国东南沿海大量养殖[7]。两种鱼同属鲈形目(Perciformes)。已成为我国海水养殖的主要经济鱼类[8]。随着技术和管理能力的进步, 我国水产养殖业目前正在寻求在远海建造深水网箱。但是极端天气造成的高强度洋流对养殖鱼类产生了不利影响, 必须了解影响物种游泳能力更深层次的因素。因种类而异, 鱼类持续游泳能力即有氧游泳能力的限制因素可能为心鳃系统对氧的摄取、运输, 代谢底物的储存、动员、活化, 代谢底物(如乳酸等)的清除和耐受能力。另外, 持续游泳也会涉及一些无氧成分。研究从两种鱼的相关代谢产物和代谢底物的浓度变化获得限制其持续游泳能力的因素。作为对水流的一种适应性反应, 许多鱼类进化出了增加新陈代谢或减少能量消耗的能力。代谢能力的增加是对强水流的常见即时反应, 这可能伴随着大量氧气的摄入和体内更快的物质交换速率。监测与游泳性能相关的代谢物浓度(能量底物及其代谢产物)变化能够很好地描述水流对鱼类游泳能力影响。在强水流的作用下, 硬骨鱼类通过加强有氧呼吸支持脂类代谢和糖代谢并产生大量ATP, 为游泳提供能量, 但整个过程还伴随无氧糖酵解, 产生乳酸和ATP。然而, 机体相关的代谢过程存在物种间的特异性差异, 也随鱼类的大小和年龄而变化, 这些差异显示它们对当前条件的耐受性。
研究通过测量美国红鱼和黑鲷的续航游泳速度(Sustained swimming speed)、生理代谢范围和血液生化参数, 研究水流速度对其游泳能力的影响。这项研究的结果将为鱼类对水流的适应性反应提供新的见解, 并用于制定这两种鱼类的养殖策略和养殖网箱的选址。
1. 材料与方法
1.1 实验材料
本实验选取美国红鱼和黑鲷作为实验对象(表 1)。实验鱼从浙江舟山的岱山养殖基地获得(30°02′ N, 122°13′ E)。采用鱼类活体运输车运回实验室, 分开暂养于半径为1.5 m、高1 m的4个圆形海水养殖池内14d, 两种鱼各100尾。暂养期间, 室内为自然光照条件, 使用舟山海域的自然海水, 通过加热器调整水体温度, 水温保持在20℃, 充氧泵曝气, 保持水体内溶氧>6.5 mg/L, 海水盐度为28—29。每日于 07:00 和 18:00 饱食投喂天邦牌浮性颗粒饲料(水分10.5%、脂肪7.5%、粗蛋白44.2%和灰分12%), 1h 后使用虹吸管吸出池内残留的饲料和粪便, 每日的投喂量约为鱼总重的3%。每天更换养殖池内25%的海水, 消除氨氮的累积。试验前 24h 停止投喂。实验室在暂养期间保持半封闭状态, 在自然光周期下运行(大约12h﹕12h, 昼﹕夜)。避免声音等外界环境对实验影响。
表 1 两种鱼的体长、体重和肥满度Table 1. Body length, weight and plumpness of two species of fish (n=5; mean±SE)指标Index 黑鲷
Acanthopagrus schlegeli美国红鱼
Sciaenops ocellatusF P 体长Body length (cm) 19.37±1.88 19.2±1.05 0.063 0.85 体重Weight (g) 203.77±5.13a 197.04±5.54b 7.932 0.011 肥满度Plumpness (%) 2.95±0.85 2.82±0.42 0.169 0.686 注: 同一行内上标不同字母表示差异显著(P<0.05); 平均数±标准误; 下同Note: In the same row, values with different superscript letters indicate significant differences (P<0.05); mean±SE; The same applies below 1.2 实验装备
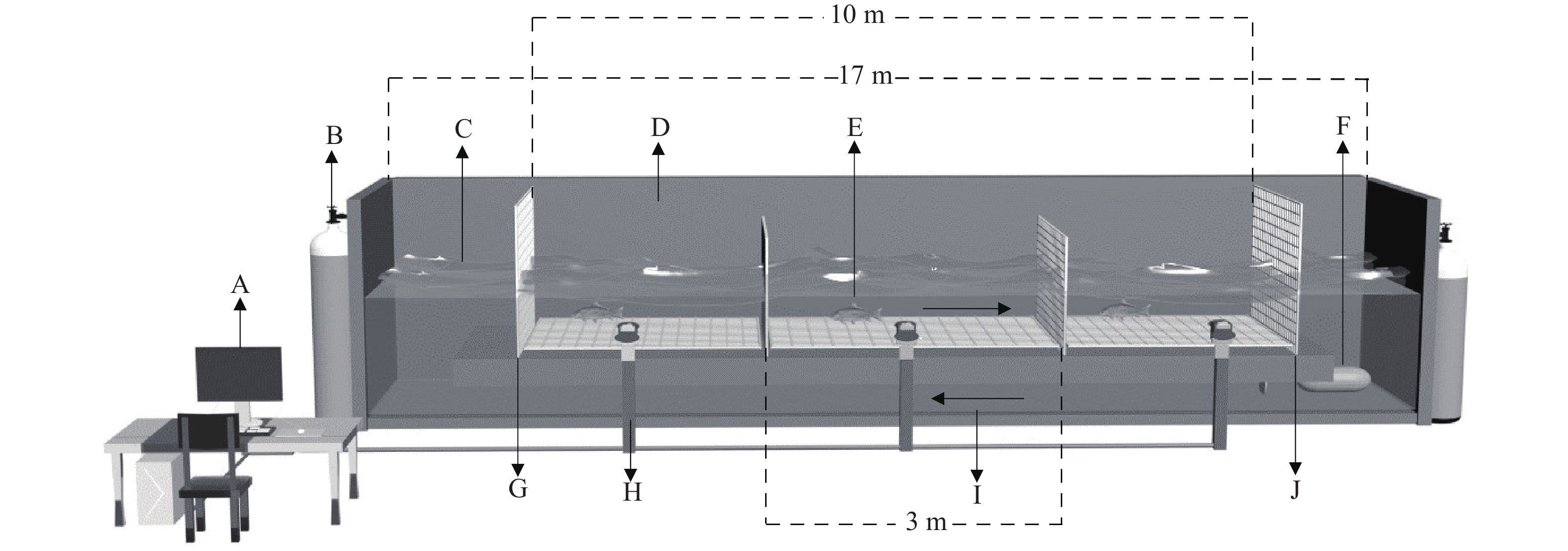
实验在浙江海洋大学科研中心水动力实验室的多功能水槽中进行(图 1, 3DMAX 2022绘制)。水槽外侧由透明玻璃制成, 全长17 m, 实验段长10 m, 宽0.5 m, 深0.8 m。通过调整电动机转速控制水流速度, 流速由小威龙流速仪标定(最大造流速度: 1.5 m/s)。水槽外接气泵, 实验全程泵氧, 保证氧气充足。水槽外架设摄像机, 全程观察记录两种鱼的游泳行为。设置整流装置(网目: 2 cm×2 cm), 用栅格网将试验段平均分成 3 段, 用来开展平行试验, 实验水深40 cm, 使用加热棒控制水温在20℃, 保证水槽内环境与暂养期间养殖池内环境一致。
1.3 鱼类耐力游泳测试
实验开始前1天停止喂食。在正式实验时, 先将单尾鱼在水深0.4 m的低流速(v<0.03 m/s)水槽中适应1h以上, 再将流速在1min内调整至设定流速。耐力游泳实验的初始速度统一设置为平均体长的2倍[9](V黑鲷和V美国红鱼=40 cm/s), 游泳速度定义为鱼逆流游泳时水流的速度。若黑鲷(美国红鱼)的续航游泳时间远大于(小于)200min, 上调(下调)流速。最终确定四组流速, 黑鲷是2.6、2.9、3.1和3.6 BL/s, 美国红鱼是3.6、3.9、4.1和4.6 BL/s, 每组流速设置10尾, 共计40尾鱼。在实验时, 逐尾进行, 并且每尾鱼只进行一次流速实验, 鱼类疲劳标志实验结束(游泳疲劳的判断标准定为实验鱼类停止游泳并触网持续20s以上), 将鱼迅速捞出, 记录其游泳时间、体长和体重后单独放置, 随机选择新的实验鱼以实施下一次测试。记录实验结果, 得到两种鱼在不同流速下的耐力游泳时间, 为后续实验提供依据。实验全程封闭, 避免环境对结果造成影响, 通过摄像机观察鱼类行为, 并对实验过程记录。详细实验可参考王萍等[10]。
1.4 鱼类续航游泳能力测试
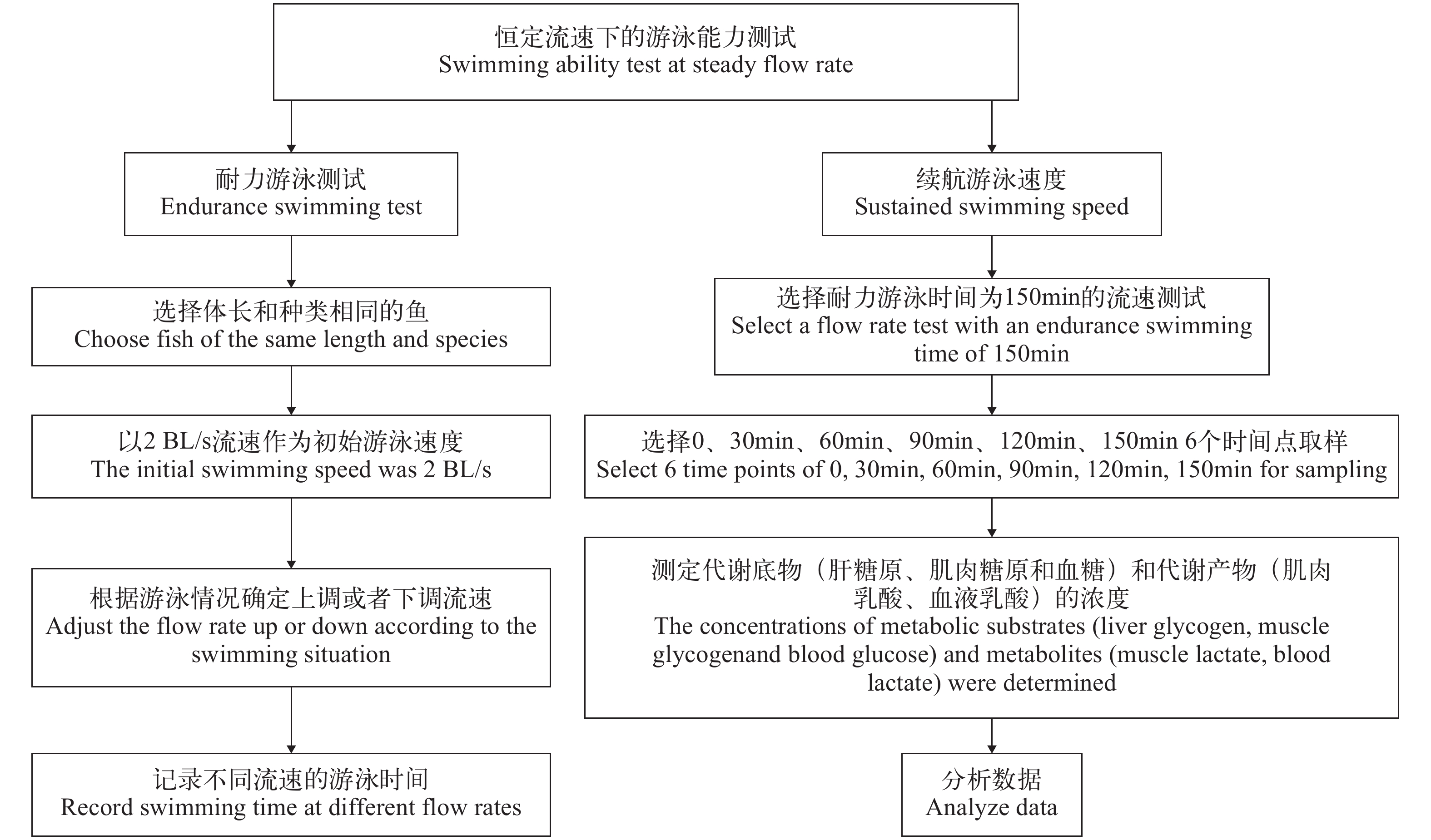
选取耐力游泳时间为150min时的水流速度, 对两种鱼进行续航游泳实验。两种鱼的体长无显著差异[P>0.05; 体长: 黑鲷=(19.37±0.59) cm; 美国红鱼=(19.20±0.33) cm], 每种鱼作为1个实验组, 分为0、30min、60min、90min、120min和150min六个时间点, 逐尾进行续航游泳实验。每个时间点的样本量5尾, 每种鱼的总量是30尾。到达设置时间点, 迅速取出实验鱼, 在丁香酚水溶液(60 mg/L)中麻醉30s后取出, 称重测量体长并记录, 使用1 mL无菌注射器从尾静脉取血, 抽取血液0.5 mL(鱼已经死亡), 4℃保存。解剖鱼体获得肝脏和肌肉(红肌), –80℃保存。所取样品用于血糖、血液乳酸、肝糖原、肌肉糖原和肌肉乳酸5种代谢物浓度测定。血糖(试剂盒序号: F006-1-1)浓度的测量采用葡萄糖氧化酶法, 肝糖原(试剂盒序号: A043-1-1)、肌糖原(试剂盒序号: A043-1-1)、肌肉乳酸(试剂盒序号: A019-2-1)和血液乳酸(试剂盒序号: A019-2-1)浓度的测试采用比色法。所有试剂盒购自南京建成生物工程研究所并按照说明书进行操作。图 2显示了两种游泳实验的具体流程, 详细实验可参考桂福坤等[11]。本研究严格遵循实验动物管理条例[12]。
1.5 数据分析
体重、体长、游泳时间、血糖、肝糖原、肌糖原、肌乳酸和血乳酸均以平均值±标准误表示。在分析之前, 对数据进行正态性检验和参数检验。相同代谢物浓度的实验数据采用齐性检验和单因素方差分析(ANOVA)。如果方差分析结果显示出显著差异(P<0.05), 则使用Duncan多重比较进一步比较数据差异。采用幂函数拟合模型计算游泳速度与耐力游泳时间的关系。所有数据采用Excel 2019和SPSS 26.0统计软件进行处理, 图像使用origin 2021绘制。
2. 结果
2.1 黑鲷和美国红鱼耐力游泳能力
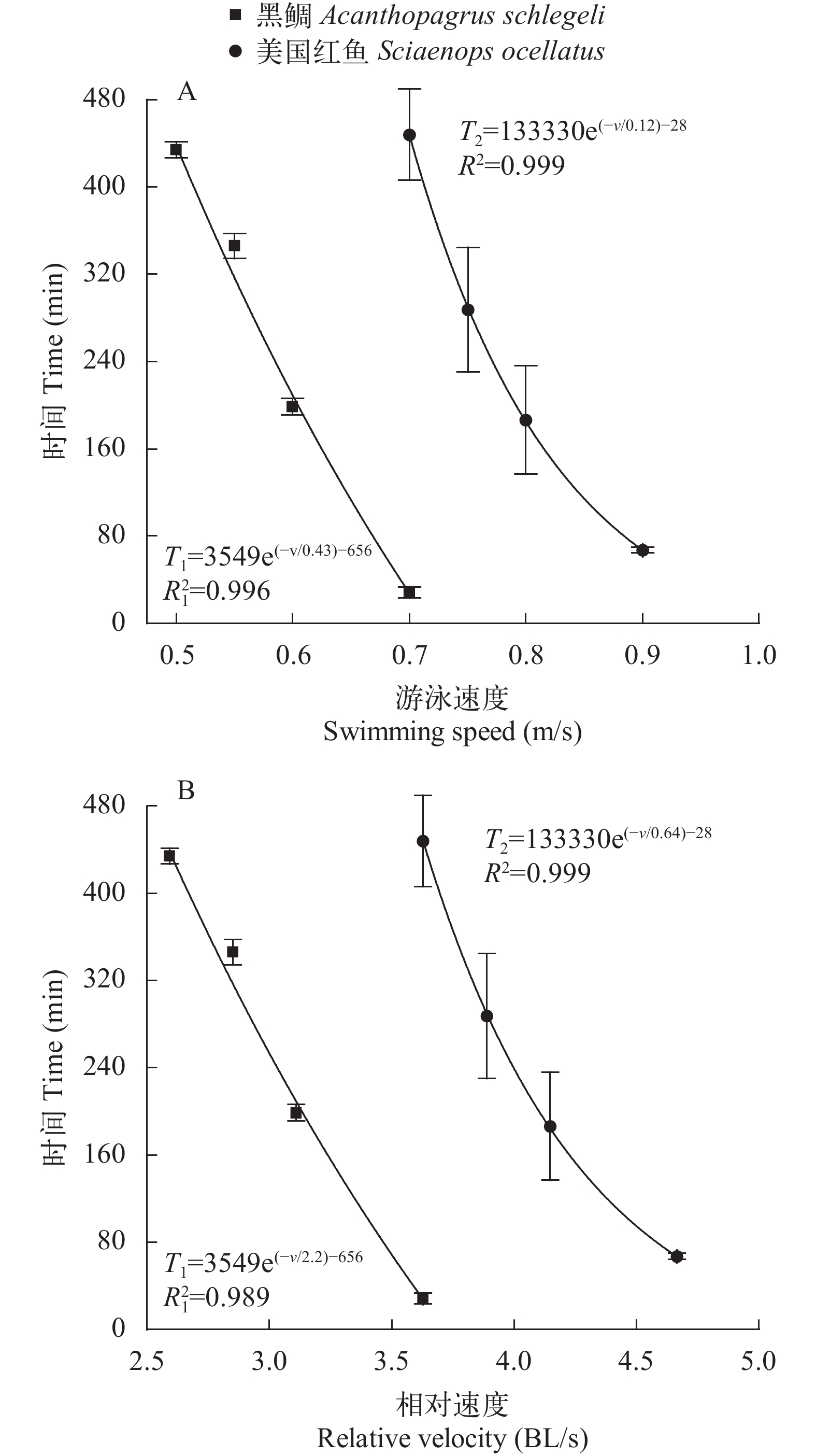
两种鱼的游泳能力呈显著差异(P<0.05), 图 3反映了幂函数拟合结果。相同规格的美国红鱼游泳能力强于黑鲷。在持续游泳时间约为440min的条件下, 美国红鱼的游泳速度为0.70 m/s显著大于黑鲷的0.50 m/s, 相同的结果还出现在持续游泳时间约为190min时, 美国红鱼的游泳速度为0.80 m/s显著大于黑鲷的0.60 m/s。图 3B描述了两种鱼相对游泳速度与时间的关系, 美国红鱼以3.6、3.9、4.15和4.67 BL/s的速度分别持续游泳约440min、288min、186min和67min, 而黑鲷以2.6、2.85、3.1和3.6 BL/s四个速度分别持续游泳约440min、346min、199min和28min。相同游泳时间, 相对速度比较显示, 美国红鱼的游泳能力显著强于黑鲷。
2.2 黑鲷和美国红鱼续航游泳的生理特性
在续航游泳实验过程中, 6种游泳时间下代谢底物(肝糖原、肌糖原和血糖)和产物(肌肉乳酸和血液乳酸)浓度的变化数据如表 2 所示。在所有2个实验组中, 续航游泳显著影响肝糖原水平(黑鲷: F=960.3, P<0.001; 美国红鱼: F=220.1, P<0.001), 两个实验组肝糖原浓度与游泳时间的双变量相关分析表明, 两者呈负相关关系。对黑鲷肝糖原浓度的进一步分析显示, 相邻时间组之间存在显著差异(P<0.05)。美国红鱼实验组的结果与黑鲷结果一致, 除去初始阶段(0和30min实验组)两组肝糖原浓度无显著差异。
表 2 两种鱼在不同游泳时间的代谢底物和产物浓度Table 2. Concentrations of metabolic substrates and products in two species at different swimming times (n=5; mean±SE)时间
Time
(min)代谢物 Metabolites 肝糖原
Hepatic glycogen (mg/g)肌肉糖原
Muscle glycogen (mg/g)背肌乳酸
Muscle lactic (mmol/g)血液乳酸
Blood lactic (mmol/L)血糖
Blood sugar (mg/mL)黑鲷
A. schlegeli美国红鱼
S. ocellatus黑鲷
A. schlegeli美国红鱼
S. ocellatus黑鲷
A. schlegeli美国红鱼
S. ocellatus黑鲷
A. schlegeli美国红鱼
S. ocellatus黑鲷
A. schlegeli美国红鱼
S. ocellatus0 5.13±0.05a 4.65±0.09a 7.96±0.55 6.43±0.67 17.24±0.31a 26.97±1.48c 4.55±0.2a 6.3±0.29 0.84±0.03a 0.34±0.03a 30 3.99±0.04b 4.26±0.58a 7.71±0.52 6.22±0.65 21.78±0.68b 30.34±2.14bc 5.64±0.14b 6.62±0.27 1.23±0.02b 0.47±0.02a 60 2.87±0.07c 3.25±0.48b 8.65±0.47 5.76±0.62 26.07±1.22c 35.9±3.15ab 6.4±0.14c 7.23±0.18 1.33±0.04c 0.73±0.03b 90 1.73±0.11d 2.4±0.39c 6.45±0.31 4.54±1.1 35.29±1.06d 37.25±2.22ab 8.69±0.2d 7.04±0.25 1.41±0.02c 1.52±0.06c 120 0.67±0.03e 1.22±0.22d 6.94±0.32 4.25±1.28 40.97±0.25e 41.71±2.09a 10.38±0.21e 7.33±0.07 1.36±0.03c 1.77±0.09d 150 0.44±0.02f 0.34±0.04e 7.36±0.72 5.87±1.02 50.54±1.12f 43.23±3.1a 11.49±0.09f 7.27±0.64 1.67±0.01d 1.96±0.09e F 960.3 220.1 2.4 1.0 211.5 6.8 261.3 1.5 97 135.221 Sig. <0.001 <0.001 0.069 0.467 <0.001 <0.001 <0.001 0.216 <0.001 <0.001 两种鱼的背部肌肉糖原浓度变化结果显示, 在不同游泳时间, 浓度差异不显著(P>0.05)。具体来说, 肌糖原浓度在黑鲷和美国红鱼显示出与游泳时间关系不大的波动状态, 黑鲷的背肌糖原浓度为6.45—8.65 mg/g, 美国红鱼为4.25—6.43 mg/g。
不同游泳时间背部肌肉和血液乳酸浓度的变化, 结果呈现显著差异。两种鱼的肌肉乳酸浓度在0和150min的实验组差异显著(P<0.05)。在不同的游泳时间, 相邻实验组的黑鲷肌肉乳酸和血液乳酸浓度差异均显著(P<0.05)。但是美国红鱼肌肉乳酸浓度变化呈现波动上升趋势, 其中0和150min的实验组差异极显著(P<0.01)。血液乳酸浓度差异不显著(P>0.05), 其浓度为6.30—7.33 mg/g。
在所有实验组中, 续航游泳的不同游泳时间显著影响血糖浓度(黑鲷: F=97, P<0.001; 美国红鱼: F=135.221, P<0.001), 两个实验组血糖浓度与游泳时间的双变量相关分析表明, 两者呈正相关关系。对黑鲷肝糖原浓度的进一步分析显示, 血糖浓度从初始时到150min接近力竭时上升约1.99倍。美国红鱼血糖浓度从初始到150min时上升约5.76倍。
2.3 两种鱼力竭状态的代谢底物和产物差异
在图 4中, 分别对两种鱼的5种代谢物进行灰色关联分析, 统一采用均值化处理。灰色关联分析是衡量系统内部因素间关联程度的一种方法, 通过因素间发展趋势的相似或相异程度来计算, 结果用关联系数衡量, 系数越大关联程度越高。结果显示, 在6个不同游泳时间时, 黑鲷和美国红鱼的血糖和肝糖原浓度与时间的关联系数最大, 表示两种代谢物是主要影响因素, 但两者的关联系数存在差异, 具体数据见表 3。
表 3 五种代谢物与续航游泳时间的关联度结果和排名Table 3. Association results and ranking of 5 metabolites with sustained swimming time代谢物 Metabolite 黑鲷 A. schlegeli 美国红鱼 S. ocellatus 关联系数
Correlation coefficient排名
Rank关联系数
Correlation coefficient排名
Rank血糖
Blood sugar0.982 1 0.974 1 肝糖原
Hepatic glycogen0.943 2 0.946 2 肌肉糖原
Muscle glycogen0.839 3 0.789 3 血液乳酸
Blood lactic0.784 4 0.764 4 肌肉乳酸
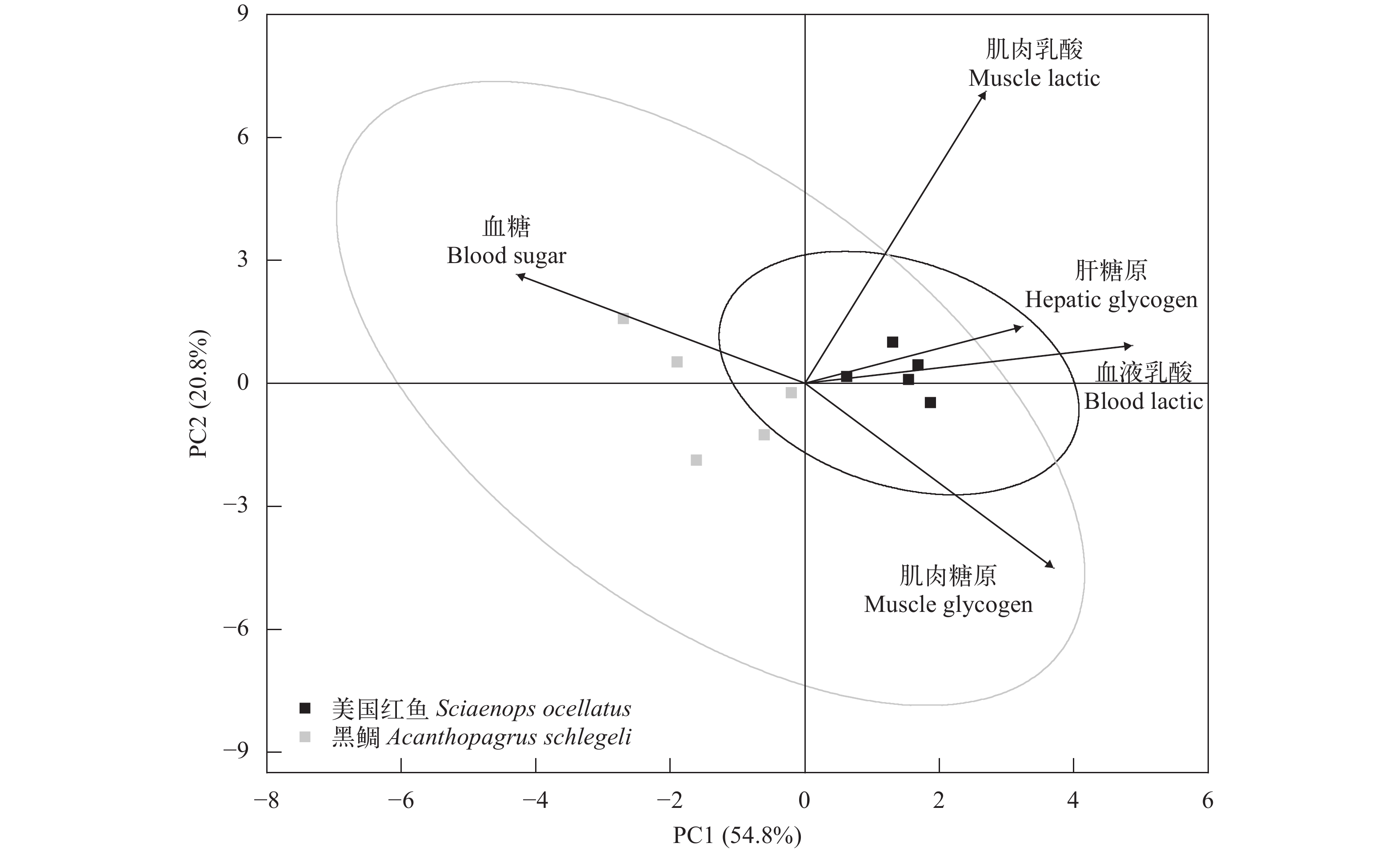
Muscle lactic0.372 5 0.434 5 虽然主要影响两种鱼游泳疲劳的代谢物相同, 即组内(相同种类鱼的五种代谢物与续航游泳时间)评价项排名相同, 但组间(两种鱼)差异不确定, 本研究使用主成分分析方法(Principal Component Analysis)比较。 PCA用于研究数据变化趋势和变量聚类[13]。它通常采用降维方法将每个数据点投影到前几个主成分上(坐标轴作为聚类参考, 本文无实际含义), 以获得低维数据, 同时尽可能地保留原始的数据变化。这些数据根据鱼的种类分为两组: 黑鲷和美国红鱼(图 5)。根据血糖、肝糖原和肌肉糖原浓度看出与置信椭圆形状密切相关, 也符合关联度排名结果。但黑鲷置信椭圆显著大于美国红鱼, 显示黑鲷数据方差更大, 即浓度变化范围更大。同时, 血糖浓度对黑鲷疲劳更显著。根据椭圆偏转角度差异, 显示美国红鱼相比黑鲷, 受肝糖原浓度影响更显著。
3. 讨论
3.1 两种鱼续航游泳能力研究
在实验室对相同规格的美国红鱼和黑鲷的续航游泳能力进行测试, 结果显示, 美国红鱼续航游泳能力更强。由于其强大的游泳能力, 美国红鱼能够应对高流速的海洋环境。据报道, 鳙(Aristichthys nobilis)在21℃持续游泳速度约为2.1 BL/s[14], 中华鲟(Acipenser sinensis)在19℃的持续游泳速度是2.5 BL/s[15], 大西洋鲑(Salmo salar)在13℃的持续游泳速度约为2.3 BL/s[16], 虽然温度能够显著影响鱼类游泳能力, 但从体形看, 中华鲟流线型的体型相比侧扁的鳙更适合游泳, 相同的结果还出现在美国红鱼和黑鲷的测试中。另据报道, 仅仅根据鱼的体型得出关于鱼的游泳能力的结论是不可靠的[17], 因为室内实验对不同鱼类造成的应激程度和方式不同, 但游泳能力的实质性差异反映了鱼类之间更深层次的区别。
鱼类的游泳能力也与其他形态特征密切相关, 包括胸鳍、尾鳍和背鳍的形状和长度。传统上认为, 游泳能力强的鱼胸鳍较长[18]。然而, 也有一些值得注意的例外表明关于胸鳍长度和游泳速度之间关系的问题。墨西哥四头鲸(Astyanax mexicanus)的胸鳍相对较短, 但其游泳速度非常快。美国红鱼相比黑鲷, 其背鳍、胸鳍和尾鳍比黑鲷更为宽大, 在强水流中能更好适应。对鱼类游动能力的研究有助于推断鱼类的近似生存条件, 构建更为适宜的养殖环境。
3.2 代谢底物和产物浓度变化
在网箱中的鱼, 总是顶流游泳, 它们通过有氧运动消耗大部分能量。这些能量主要来源于代谢底物中的脂质[19, 20]、蛋白质[20, 21]和碳水化合物[22, 23]。消耗脂肪和蛋白质的唯一方法是长时间低强度运动。在200min内, 耐力游泳主要消耗储存在白肌中的3种内源性燃料: 磷酸肌酸、ATP和糖原。鱼类在休息时储存糖原, 糖原的数量因鱼的种类而异[24]。运动后糖原作为代谢底物损失的程度因活动的类型、强度和持续时间而异。肌肉糖原的减少可能会减缓金鱼(Carassius auratus)的暴发游泳速度[25]。相比之下, 在相同的规格下, 美国红鱼和黑鲷的肌糖原浓度没有显著差异, 乌贼(Sepia officinalis)在低速游泳时肌糖原浓度的变化呈现了相同的结果[26]。推测肌肉糖原浓度与鱼类的耐力游泳能力没有直接关系。
传统上认为, 乳酸作为运动后肌肉产生的代谢产物, 大部分通过肌肉释放到血淋巴和血液中, 被其他组织(例如鸡胸)吸收和利用[27]。尽管有些仍然留在肌肉中, 并在原位代谢[28]。但在鱼类中, 有大量证据表明Cori循环在处理运动后乳酸方面不起重要作用[29, 30]。鲑和其他一些物种的肌肉只释放极少量的乳酸[31, 32]。底栖物种几乎不释放乳酸, 血液乳酸水平保持极低。在鱼类中, 肌肉乳酸和血乳酸之间的关系仍然存在争议。本研究的两组肌肉乳酸浓度均显著升高, 但黑鲷的血液乳酸浓度在不同疲劳阶段呈显著差异, 美国红鱼差异不显著。结果表明, 两种鱼的疲劳程度与乳酸浓度呈正相关。然而, 肌肉乳酸的增加远远大于血乳酸的增加。相比乳酸在中国对虾(Fenneropenaeus chinensis)内更快的转运速率[33], 这可能表明美国红鱼和黑鲷有Cori循环, 但血乳酸对疲劳的影响较小。
血液中的葡萄糖是代谢底物, 主要来自消化道和肝脏, 随着血液循环输送到各种组织和器官, 以支持身体的生命活动。过去, 人们认为鱼的血糖水平受压力[34]和环境温度[35]的影响, 而不是游泳。根据Kiermir[36]的研究, 鱼类运动不会显著增加血糖水平。在25℃游泳前后, 花鲈(Lateolabrax maculatus)和许氏平鲉(Sebastes schlegeli)的血糖水平都有相同的显著升高[37]。在本研究中, 在不同疲劳水平下测量了美国红鱼和黑鲷的血糖浓度, 结果表明, 随着疲劳水平的增加, 血糖浓度显著增加。目前, 强迫游泳对鱼类应激的影响仍有待研究。鱼类游泳时血糖浓度升高的一个可能解释是肾上腺素激活cAMP-PKA信号通路, 从而增加血糖浓度并为各种器官提供能量。
3.3 开放海域水产养殖的策略
研究显示, 养殖的黑鲷和美国红鱼分别能够维持2.8和3.7 BL/s的游泳速度至少游泳5h。然而就生产而言, 长期被迫生活在接近极限续航游泳速度的环境并不是最佳的选择, 因为持续的高强度有氧游泳可能会抑制鱼类的消化和生长[38]。例如, 大西洋鲑在1.5 BL/s的流速环境被迫生长6周对生长有明显的负面影响[39]。
此外, 还要考虑温度对鱼类游泳能力的影响, 因为冬季可能面临更多的短时强流。对鲤(Cyprinus carpio)的研究显示, 与有氧活动密切相关的白肌在低温下活力不足, 这可能降低其最大续航游泳速度[40]。鲑(Oncorhynchus keta)在温度对续航游泳能力影响的研究中也显示了相似的结果[16]。由于实验在20℃进行, 得到的最大续航游泳能力并不代表在较低温度的结果。
美国红鱼是一种具有高持续游泳能力的品种, 在游泳过程中还表现出高灵活性, 能够很好地应对不同的环境条件, 基于对生长中期的美国红鱼持续游泳能力的研究, 并结合对实际养殖场所的调查, 美国红鱼能够养殖在更多的开放海域。然而黑鲷无法达到与美国红鱼的相似的续航游泳速度, 因此不建议将黑鲷养殖在偶尔会发生高流速的海域。同时, 肝糖原和血糖浓度对两种鱼续航游泳能力的影响明显, 有必要对肝脏糖原与运动疲劳进行更深入的研究, 其中对肝脏进行转录组分析将会带来更多的发现, 这也成为实验下一阶段的方向。随着技术创新和先进养殖理念的引入, 未来我国海水养殖的发展潜力巨大。但更重要的是围绕养殖物种的生物学特性研究成为决策的核心, 其中了解鱼类的生理极限将至关重要。
-
表 1 两种鱼的体长、体重和肥满度
Table 1 Body length, weight and plumpness of two species of fish (n=5; mean±SE)
指标Index 黑鲷
Acanthopagrus schlegeli美国红鱼
Sciaenops ocellatusF P 体长Body length (cm) 19.37±1.88 19.2±1.05 0.063 0.85 体重Weight (g) 203.77±5.13a 197.04±5.54b 7.932 0.011 肥满度Plumpness (%) 2.95±0.85 2.82±0.42 0.169 0.686 注: 同一行内上标不同字母表示差异显著(P<0.05); 平均数±标准误; 下同Note: In the same row, values with different superscript letters indicate significant differences (P<0.05); mean±SE; The same applies below 表 2 两种鱼在不同游泳时间的代谢底物和产物浓度
Table 2 Concentrations of metabolic substrates and products in two species at different swimming times (n=5; mean±SE)
时间
Time
(min)代谢物 Metabolites 肝糖原
Hepatic glycogen (mg/g)肌肉糖原
Muscle glycogen (mg/g)背肌乳酸
Muscle lactic (mmol/g)血液乳酸
Blood lactic (mmol/L)血糖
Blood sugar (mg/mL)黑鲷
A. schlegeli美国红鱼
S. ocellatus黑鲷
A. schlegeli美国红鱼
S. ocellatus黑鲷
A. schlegeli美国红鱼
S. ocellatus黑鲷
A. schlegeli美国红鱼
S. ocellatus黑鲷
A. schlegeli美国红鱼
S. ocellatus0 5.13±0.05a 4.65±0.09a 7.96±0.55 6.43±0.67 17.24±0.31a 26.97±1.48c 4.55±0.2a 6.3±0.29 0.84±0.03a 0.34±0.03a 30 3.99±0.04b 4.26±0.58a 7.71±0.52 6.22±0.65 21.78±0.68b 30.34±2.14bc 5.64±0.14b 6.62±0.27 1.23±0.02b 0.47±0.02a 60 2.87±0.07c 3.25±0.48b 8.65±0.47 5.76±0.62 26.07±1.22c 35.9±3.15ab 6.4±0.14c 7.23±0.18 1.33±0.04c 0.73±0.03b 90 1.73±0.11d 2.4±0.39c 6.45±0.31 4.54±1.1 35.29±1.06d 37.25±2.22ab 8.69±0.2d 7.04±0.25 1.41±0.02c 1.52±0.06c 120 0.67±0.03e 1.22±0.22d 6.94±0.32 4.25±1.28 40.97±0.25e 41.71±2.09a 10.38±0.21e 7.33±0.07 1.36±0.03c 1.77±0.09d 150 0.44±0.02f 0.34±0.04e 7.36±0.72 5.87±1.02 50.54±1.12f 43.23±3.1a 11.49±0.09f 7.27±0.64 1.67±0.01d 1.96±0.09e F 960.3 220.1 2.4 1.0 211.5 6.8 261.3 1.5 97 135.221 Sig. <0.001 <0.001 0.069 0.467 <0.001 <0.001 <0.001 0.216 <0.001 <0.001 表 3 五种代谢物与续航游泳时间的关联度结果和排名
Table 3 Association results and ranking of 5 metabolites with sustained swimming time
代谢物 Metabolite 黑鲷 A. schlegeli 美国红鱼 S. ocellatus 关联系数
Correlation coefficient排名
Rank关联系数
Correlation coefficient排名
Rank血糖
Blood sugar0.982 1 0.974 1 肝糖原
Hepatic glycogen0.943 2 0.946 2 肌肉糖原
Muscle glycogen0.839 3 0.789 3 血液乳酸
Blood lactic0.784 4 0.764 4 肌肉乳酸
Muscle lactic0.372 5 0.434 5 -
[1] Waite R, Beveridge M, Brummett R, et al. Improving Productivity and Environmental Performance of Aquaculture [M]. WorldFish, 2014: 10-15
[2] Pauly D, Zeller D. Comments on FAOs state of world fisheries and aquaculture (SOFIA 2016) [J]. Marine Policy, 2017(77): 176-181.
[3] Gentry R R, Froehlich H E, Grimm D, et al. Mapping the global potential for marine aquaculture [J]. Nature Ecology & Evolution, 2017, 1(9): 1317-1324.
[4] Hambrey J. The 2030 Agenda and the sustainable development goals: the challenge for aquaculture development and management [J]. FAO Fisheries and Aquaculture Circular, 2017(1141): 26-33.
[5] Leavy T R, Bonner T H. Relationships among swimming ability, current velocity association, and morphology for freshwater lotic fishes [J]. North American Journal of Fisheries Management, 2009, 29(1): 72-83. doi: 10.1577/M07-040.1
[6] Katalinas C J, Brenkert K, Darden T, et al. A genetic assessment of a red drum, Sciaenops ocellatus, stock enhancement program [J]. Journal of the World Aquaculture Society, 2018, 49(3): 523-539. doi: 10.1111/jwas.12442
[7] Hu J, Liu Y, Yu G, et al. Osteological development of the vertebral column and caudal complex in larval and juvenile blackhead seabream, Acanthopagrus schlegelii (Perciformes, Sparidae) [J]. Pakistan Journal of Zoology, 2019, 51(5): 1859.
[8] Yearbook C F S. China Fishery Statistical Yearbook [M]. Beijing: China Agriculture Press, 2020: 24-34.
[9] 王萍, 桂福坤, 吴常文. 鱼类游泳速度分类方法的探讨 [J]. 中国水产科学, 2010, 17(5): 1137-1146. Wang P, Gui F K, Wu C W. Classification of fish swimming speed [J]. Journal of Fishery Sciences of China, 2010, 17(5): 1137-1146.
[10] 王萍, 桂福坤, 吴常文. 美国红鱼(Sciaenops ocellatus), 鲈鱼(Lateolabrax maculatus), 斜带髭鲷(Hapalogenys nitens)耐流性试验研究 [J]. 海洋与湖沼, 2010, 41(6): 923-929. doi: 10.11693/hyhz201006019019 Wang P, Gui F K, Wu C W. Swimming ability of Sciaenops ocellatus, Lateolabrax maculatus and Hapalogenys nitens [J]. Oceanologia et Limnologia Sinica, 2010, 41(6): 923-929. doi: 10.11693/hyhz201006019019
[11] 桂福坤, 王萍, 吴常文. 适应条件对鱼类续航游泳能力的影响 [J]. 水产学报, 2010, 34(8): 1227-1235. Gui F K, Wang P, Wu C W. Influence of acclimation conditions on fish’s sustainable swimming performance [J]. Journal of Fisheries of China, 2010, 34(8): 1227-1235.
[12] 实验动物管理条例 [J]. 实用器官移植电子杂志, 2016, 4(2): 66-67. Laboratory Animal Management Regulations [J]. Practical Journal of Organ Transplantation (Electronic Version), 2016, 4(2): 66-67.
[13] Jolliffe I T, Cadima J. Principal component analysis: a review and recent developments [J]. Philosophical Transactions of the Royal Society A: Mathematical, Physical and Engineering Sciences, 2016, 374(2065): 20150202. doi: 10.1098/rsta.2015.0202
[14] 侯轶群, Lynda Newbold, 蔡露, 等. 基于固定流速法的鳙(Aristichthys nobilis)幼鱼游泳能力 [J]. 生态学杂志, 2016, 35(6): 1583-1588. Hou Y Q, Lynda N, Cai L, et al. Swimming performance of juvenile Aristichthys nobilis under fixed velocity swimming tests [J]. Acta Hydrobiologica Sinica, 2016, 35(6): 1583-1588.
[15] Fang M, Cai L, Gao Y, et al. Swimming and recovery abilities of juvenile Chinese sturgeon Acipenser sinensis [J]. Transactions of the American Fisheries Society, 2017, 146(6): 1186-1192. doi: 10.1080/00028487.2017.1362469
[16] Hvas M, Oppedal F. Sustained swimming capacity of Atlantic salmon [J]. Aquaculture Environment Interactions, 2017(9): 361-369.
[17] Downie A T, Leis J M, Cowman P F, et al. The influence of habitat association on swimming performance in marine teleost fish larvae [J]. Fish and Fisheries, 2021, 22(6): 1187-1212. doi: 10.1111/faf.12580
[18] Aguilar-Medrano R, Frédérich B, Balart E F, et al. Diversification of the pectoral fin shape in damselfishes (Perciformes, Pomacentridae) of the Eastern Pacific [J]. Zoomorphology, 2013, 132(2): 197-213. doi: 10.1007/s00435-012-0178-8
[19] Rosewarne P J, Wilson J M, Svendsen J C. Measuring maximum and standard metabolic rates using intermittent-flow respirometry: a student laboratory investigation of aerobic metabolic scope and environmental hypoxia in aquatic breathers [J]. Journal of Fish Biology, 2016, 88(1): 265-283. doi: 10.1111/jfb.12795
[20] Weber J M, Haman F O. Pathways for metabolic fuels and oxygen in high performance fish [J]. Comparative Biochemistry and Physiology Part A Physiology, 1996, 113(1): 33-38. doi: 10.1016/0300-9629(95)02063-2
[21] Moon T W, Johnston I A. Starvation and the activities of glycolytic and gluconeogenic enzymes in skeletal muscles and liver of the plaice, Pleuronectes platessa [J]. Journal of Comparative Physiology, 1980, 136(1): 31-38. doi: 10.1007/BF00688619
[22] Sanz-Ronda F J, Ruiz-Legazpi J, Bravo-Córdoba F J, et al. Sprinting performance of two Iberian fish: Luciobarbus bocagei and Pseudochondrostoma duriense in an open channel flume [J]. Ecological Engineering, 2015(83): 61-70.
[23] Richards J G, Mercado A J, Clayton C A, et al. Substrate utilization during graded aerobic exercise in rainbow trout [J]. The Journal of Experimental Biology, 2002, 205(14): 2067-2077. doi: 10.1242/jeb.205.14.2067
[24] Kolarevic J, Aas H, Espmark A, et al. The use of acoustic acceleration transmitter tags for monitoring of Atlantic salmon swimming activity in recirculating aquaculture systems (RAS) [J]. Aquacultural Engineering, 2016(72): 30-39.
[25] Sinha A K, Liew H J, Diricx M, et al. The interactive effects of ammonia exposure, nutritional status and exercise on metabolic and physiological responses in gold fish (Carassius auratus L.) [J]. Aquatic Toxicology, 2012(109): 33-46.
[26] Ahmmed M K, Ahmmed F, Kabir K A, et al. Biochemical impacts of salinity on the catfish, Heteropneustes fossilis (Bloch, 1794), and possibility of their farming at low saline water [J]. Aquaculture research, 2017, 48(8): 4251-4261. doi: 10.1111/are.13246
[27] Robles-Romo A, Zenteno-Savín T, Racotta I S. Bioenergetic status and oxidative stress during escape response until exhaustion in whiteleg shrimp Litopenaeus vannamei [J]. Journal of Experimental Marine Biology and Ecology, 2016(478): 16-23.
[28] Roques S, Deborde C, Richard N, et al. Metabolomics and fish nutrition: a review in the context of sustainable feed development [J]. Reviews in Aquaculture, 2020, 12(1): 261-282. doi: 10.1111/raq.12316
[29] Paoli A, Moro T, Marcolin G, et al. High-Intensity Interval Resistance Training (HIRT) influences resting energy expenditure and respiratory ratio in non-dieting individuals [J]. Journal of Translational Medicine, 2012, 10(1): 1-8. doi: 10.1186/1479-5876-10-1
[30] Kwong R W M, Kumai Y, Perry S F. Neuroendocrine control of ionic balance in zebrafish [J]. General and Comparative Endocrinology, 2016(234): 40-46.
[31] Owen S F, Giltrow E, Huggett D B, et al. Comparative physiology, pharmacology and toxicology of β-blockers: mammals versus fish [J]. Aquatic Toxicology, 2007, 82(3): 145-162. doi: 10.1016/j.aquatox.2007.02.007
[32] Kennedy K M, Dewhirst M W. Tumor metabolism of lactate: the influence and therapeutic potential for MCT and CD147 regulation [J]. Future Oncology, 2010, 6(1): 127-148. doi: 10.2217/fon.09.145
[33] Li J, Li W, Zhang X. Lower-intensity net-chasing training facilitates the survival and growth of the Chinese shrimp Fenneropenaeus chinensis reared at high stocking densities [J]. Aquaculture, 2019(508): 36-45.
[34] Lennox R J, Mayer I, Havn T B, et al. Effects of recreational angling and air exposure on the physiological status and reflex impairment of European grayling (Thymallus thymallus) [J]. Boreal Environment Research, 2016(21): 461-470.
[35] Abdelkhalek N K M, Eissa I A M, Ahmed E, et al. Protective role of dietary Spirulina platensis against diazinon-induced oxidative damage in Nile tilapia; Oreochromis niloticus [J]. Environmental Toxicology and Pharmacology, 2017(54): 99-104.
[36] Kuz’Mina V V. Hormonal regulation of metabolism and processes of exotrophy in fish. polyfunctionality and polypotentiality [J]. Journal of Evolutionary Biochemistry and Physiology, 2000, 36(6): 670-684. doi: 10.1023/A:1017518603599
[37] 井爱国. 花鲈、许氏平鲉运动生理学的初步研究 [D]. 青岛: 中国海洋大学, 2005: 36-41. Jing A G. Sustained swimming performance and physiology of Lateolabrax maculatus and Sebastes schlegeli [D]. Qingdao: Ocean University of China, 2005: 36-41.
[38] Farrell A P, Thorarensen H, Axelsson M, et al. Gut blood flow in fish during exercise and severe hypercapnia [J]. Comparative Biochemistry and Physiology Part A: Molecular & Integrative Physiology, 2001, 128(3): 549-561.
[39] Solstorm F, Solstorm D, Oppedal F, et al. Fast water currents reduce production performance of post-smolt Atlantic salmon Salmo salar [J]. Aquaculture Environment Interactions, 2015, 7(2): 125-134. doi: 10.3354/aei00143
[40] Gleiss A C, Wilson R P, Shepard E L C. Making overall dynamic body acceleration work: on the theory of acceleration as a proxy for energy expenditure [J]. Methods in Ecology and Evolution, 2011, 2(1): 23-33. doi: 10.1111/j.2041-210X.2010.00057.x
-
期刊类型引用(5)
1. 朱庭耀,李冬春,向坤,梁超,朋泽群,赵建,郭建林,叶章颖. 流速对鱼类的影响及其在循环水养殖中的应用. 水生生物学报. 2025(01): 211-221 .  本站查看
本站查看
2. 高阳阳,陈卓,刘科,汪杰,盛城,张心怡,昌子多,冯镜洁. 基于鱼类感应流速的水库放流位置选择研究. 人民珠江. 2025(02): 83-90 .  百度学术
百度学术
3. 张静,胡长圣,刘前,戴佳玥,王学锋,汤保贵. 流速对卵形鲳鲹游泳行为及运动生理的影响. 中国水产科学. 2024(04): 381-390 .  百度学术
百度学术
4. 汤保贵,陈秀灿,胡长圣,戴佳玥,王学锋,张静. 流速对黑鲷幼鱼游泳行为及运动生理的影响. 水生生物学报. 2023(12): 1993-2002 .  本站查看
本站查看
5. 张静静,王亚冰,王倩,韩多彩,彭士明. 不同抗流能力大黄鱼(Larimichthys crocea)肌肉转录组学差异分析. 海洋与湖沼. 2023(05): 1507-1516 .  百度学术
百度学术
其他类型引用(5)



 下载:
下载: