A REVIEW ON ANTIALGAL EFFECTIVENESS AMONG DISTINCT ALLELOCHEMICALS AND JOINT INHIBITORY EFFECTS ON CYANOBACTERIAL GROWTH
-
摘要: 世界范围内的蓝藻水华持续威胁着水生生态系统功能和人类健康, 化感物质凭借其环境安全和对微藻有特异毒性等特征可以短期抑制蓝藻水华的暴发和生长。文章分别概括了酚类化合物、含氮化合物、脂肪酸/酯类、萜类化合物四类化感物质及其衍生物对蓝藻的杀藻效果、潜在机制及特异作用靶点, 并依据高效抑藻化感物质(EC50<10 mg/L)的经济成本进一步预估其实际应用潜能。结果表明, 单独胁迫下的各类化感物质具不同抑藻特性: 脂肪酸/酯类的性价比最优, 能以较少剂量对蓝藻产生极强毒性, 对蓝藻多样的作用靶点是其具有极强抑制效果的关键, 可在0.015—52.95 mg/L浓度范围内将目标蓝藻抑制50%; 酚类化合物总数最多、活性普遍较高, 半数效应浓度(EC50)为0.05—162.53 mg/L, 可通过抑制光合作用、破坏细胞氧化应激平衡和损害细胞壁/膜结构等多种机制抑制蓝藻生长, 但高效杀藻酚类化合物的理论成本差异较大, 性价比次于脂肪酸位于第二位; 含氮化合物对蓝藻生长存在特异性和均匀高效的杀藻作用, EC50集中于0.3—8.14 mg/L, 主要通过破坏蓝藻的光合作用、阻断电子传递和破坏细胞结构(包括超微结构)而对蓝藻造成不可逆转的严重损伤, 但成本较高、性价比最低而难以广泛实际应用; 萜类化合物杀藻作用弱于其他三个类别的化感物质, 主要集中于多途径破坏蓝藻细胞的光合功能, 但 EC50高达25.3—228 mg/L,实际应用也受限。为减少各种化感物质用量、降低经济成本并实现更高效的杀藻效果, 文章总结归纳相同和不同类型化感物质联合作用方式和特点, 指出化感物质所产生的联合作用效果取决于混合化感物质的数量、作用靶点、混合比例和混合物含量四个因素。综述还提出抑藻靶点多样且互补的化感物质混合(“多靶点组合”)可产生协同杀藻作用, 且在混合物中应增加具有高杀藻活性化感物质的比例(“新木桶效应”协同效应)。同时指出依据植物实际分泌物的种类、含量及比例进行多元混合抑藻更易出现协同杀藻作用, 为科学、综合、合理地选择和应用化感物质并优化其配比以控制蓝藻水华提供新见解。Abstract: Cyanobacterial blooms worldwide pose severe threat to aquatic ecosystem functions and even human health. Due to environmental-friendliness and high selectivity, allelochemicals have put forward a promising option for inhibiting cyanobacterial overgrowth and therefore mitigating blooms in a short term. This study overviewed the algicidal effects of four types of allelochemicals, i.e., polyphenolics, nitrogen-containing compounds, fatty acids/esters and terpenoids, as well as underlying mechanisms and specific target sites against cyanobacteria, and further evaluated the application potential based on economic costs of highly effective cyanobacterium-inhibiting allelochemicals. The results demonstrated distinctive algicidal characteristics among each type of allelochemicals: Fatty acids/esters were the most cost-effective in algicidal activity, which induced extremely strong toxicity to cyanobacteria at low doses due to various action targets and suppressed target cyanobacterial growth by 50% in concentration range of 0.015—52.95 mg/L; Polyphenolics as the most abundant allelochemicals generally exhibited high algicidal activity with median effect concentration (EC50) ranging from 0.05 to 162.53 mg/L, and could restrain cyanobacterial growth by multiple mechanisms such as inhibiting photosynthesis, disrupting cellular oxidative stress balance and damaging cell wall/membrane structure. However, the theoretical costs vastly differed among highly effective algicidal polyphenolics, whose cost-efficiencies were inferior to fatty acids and thus ranked as 2nd place following fatty acids; N-containing compounds generally exhibited specific and evenly effective algicidal effect against cyanobacterial growth, with EC50 varying from 0.3 to 8.14 mg/L, and induced irreversible cell damage by mainly disrupting cyanobacterial photosynthesis, blocking electron transfer, and destroying cellular structures (including ultrastructure). However, N-containing compounds involved high costs and lowest effectiveness that hindered their wide application. Terpenoids exhibited relatively weak algicidal effect as compared to other three types of allelochemicals, which exerted algicidal effect through multi-routes to mainly disrupt photosynthetic function of cyanobacterial cells, with higher EC50 reaching up to 25.3—228 mg/L that limited their actual application. Consequently, this review summarized joint action effect modes and characteristics of same type and different types of allelochemicals on cyanobacterial (mainly Microcystis aeruginosa) growth to decrease applying dosages of allelochemicals, diminish economic costs and achieve more efficient algicidal effects, and pointed out that allelochemicals number in mixture, action target sites, each allelochemical proportion in mixture and mixture dosage were key factors to determine joint action effect of mixed allelochemicals. This review also proposed that different allelochemicals with diverse and complementary action target sites (referred as ‘multi-target mixture’) could exert synergistic effects, and that proportions of allelochemicals with high algicidal activity should be increased in mixture (referred as ‘new-barrel effect’ synergistic effect). Moreover, this review also proposed that multiple allelochemicals were more likely to arouse synergistic algicidal effects when they were mixed based on their inherent types, contents and proportions actually excreted by plants, which provided novel insights for scientific, comprehensive and reasonable choice, application and optimally mixing of allelochemicals, in controlling cyanobacterial blooms.
-
水体富营养化和气候变暖持续促进蓝藻水华的全球性扩张[1], 以微囊藻(Microcystis)为优势种的水华蓝藻过度消耗水体溶解氧并释放微囊藻毒素严重威胁生态健康。目前, 控制蓝藻生长(尤其是微囊藻)及抑制微囊藻毒素的产生与释放已成为全球关注热点。物理分离、沉降、充氧、暴气和超声降解等方法低效率高能耗[2], 明矾、镧膨润土及应用基于铜、钙、铁的化学抑藻剂可快速杀藻但易形成二次污染[3], 植物源化感物质具特异毒性、环境安全和易降解等特性, 或为抑制蓝藻水华至关重要的生态可持续策略。
近年来, 大量研究证实水生、陆生植物分泌的化感物质均可对蓝藻产生抑制效应, 其中针对微囊藻的研究较多, 现已提取并鉴定90余种抑藻化感物质, 可划分为酚类化合物、脂肪酸/酯类、萜类和含氮化合物等常见类型[4]。然而, 化感物质在水体中的实际应用仍有待探究, 例如香草酸与没食子酸、月桂酸与亚油酸分别属于相同类型化感物但抑藻活性差异较大, 影响同类物质抑藻差异的因素不够清晰; 以青蒿素为代表的化感物质损伤藻细胞结构的同时致使细胞破裂和大量藻毒素释放, 带来的二次污染风险更为严重与棘手[5]; β-环柠檬醛等因环境含量少和抑藻活性低等问题直接影响抑藻效益[6]。因此对不同化感物质的抑藻能力、作用机制和应用成本的全面剖析势在必行。
此外, 多种植物产生和释放的化感物质通常共存于水体环境中, 可产生协同、加和、拮抗和独立等联合效应, 但同一、不同类型化感物质的联合作用规律和影响因素仍不清晰。本文通过概述化感物质的抑藻活性、对藻细胞的损伤机制及抑藻成本, 并在总结化学结构异同的化感物质联合抑藻效应特性基础上摸索结果-效应规律, 旨在为控制蓝藻水华、提高抑藻效率及抑藻化感物选择提供依据与参考。
1. 抑藻化感物质分类及损伤机制
化感作用自1937年Molish[7]首次提出后被广泛应用于农林生产和环境保护等领域, 也为蓝藻水华的预防、控制和治理提供新的思路和方法。原位生长的水生植物能通过根、茎和叶直接释放化感物质至水环境, 对藻类产生极大影响, 沉水植物苦草(Vallisneria natans)[8]和穗花狐尾藻(Myriophyllum spicatum)[9]、挺水植物菖蒲(Acorus calamus)[10]和梭鱼草(Pontederia cordata)[11]、浮水植物萍蓬草(Nuphar pumilum)[12]等浸提液对藻类的有效抑制率可达52.9%—94.6%。同时, 异位陆生植物的化感物质亦可通过凋落物降解、土壤冲洗、雨雾淋溶及人工投放等途径进入水体, 也发挥着显著效用, 甚至被认为比原位水生植物对抑藻的贡献更大[13], 如菊科/罂粟科、百合科和禾本科等陆生草本植物种植水及浸提液能对铜绿微囊藻(Microcystis aeruginosa)的生长表现出不同程度抑制, 同时降低叶绿素含量[14]; 木本植物的壳斗科栎属17种植物的树皮浸提液对铜绿微囊藻的生长抑制率均超过50%[15]。对40种常见中药材抽提液的抑藻效应研究发现, 0.1%(w/v)的黄连(Coptis chinensis Franch.)96h内对铜绿微囊藻生长抑制率可达90.75%, 还有6种中药材也表现出明显的抑藻效果[16]。将这些有抑藻效应的植物提取物进一步鉴定和提纯, 可筛选出能有效抑制有害蓝藻水华的化感物质(表 1)。
表 1 按化学结构对抑藻化感物质分类[4]Table 1. The classification of allelochemicals in terms of their chemical structure[4]化学结构分类
Chemical structure classification化感物质Allelochemical 酚类化合物及其衍生物
Polyphenolics and deribvatives简单酚 Simple phenols 苯甲酸及其衍生物 Benzoic acid and deribvatives 肉桂酸及其衍生物 Cinnamic acid and derivatives 黄酮类 Flavonoids 单宁 Tannin 香豆素类 Coumarins 醌类Quinones 含氮化合物
N-containing compounds and deribvatives生物碱Alkaloid 苯胺、萘胺Anilines and Naphthylamine 氨基酸Amino acids 脂肪酸及酯类
Aliphatic compounds脂肪酸Fatty acid 酯类Esters 萜类及其衍生物Terpenoids and their derivatives 1.1 酚类化合物及其衍生物
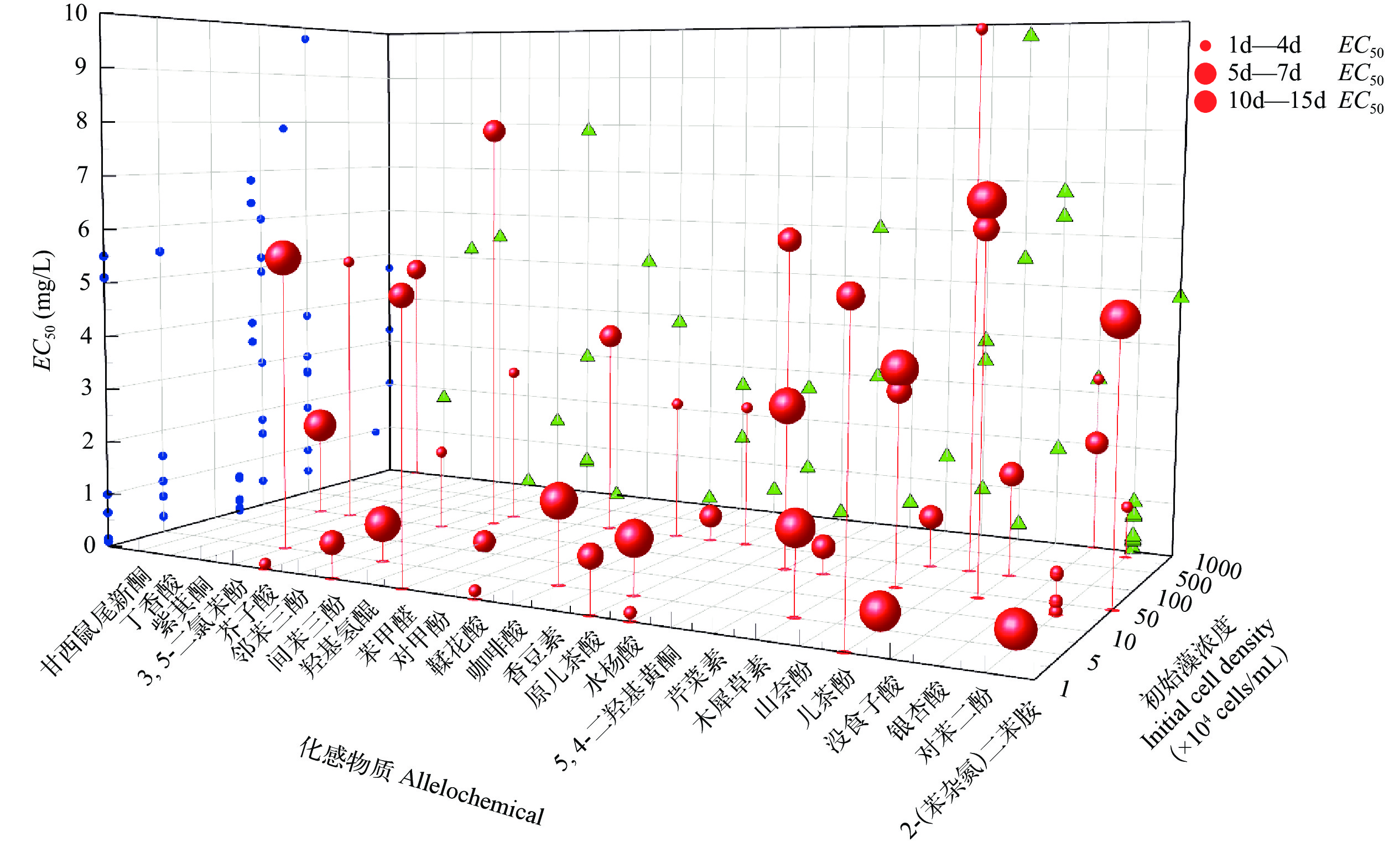
酚类化合物是自然界中种类最多、存在最广泛的一类化感物质, 分为植物分泌的内源性酚和人工合成的外源性酚, 包含其衍生物在内现已鉴定超过8000种[17], 其中具有一定水溶性和较高生物活性的酚类可表现出优良的化感抑藻效应[18, 19], 如含有多种酚类的菖蒲根部提取物可使微囊藻主导的水华蓝藻总生物量下降90%以上长达7d[10]。酚类化合物及其衍生物含量丰富, 抑藻活性强, 现已成为研究最多的化感物类群。图 1采用Origin 2022作为可视化工具绘制了不同初始藻浓度下, 各酚类化合物在不同胁迫时间内对蓝藻半数效应浓度(Median effect concentration, EC50)的三维散点图。
![]() 图 1 初始藻浓度-酚类化合物-EC50相互关系的三维散点图(展示EC50小于10 mg/L的化感物质)YZ投影面的圆点表示忽视初始浓度和处理时间时, 不同化合物对应的EC50值; XZ投影面的三角形表示不同初始浓度下EC50值分布状况; 下同Figure 1. Three-dimensional scatter plot of the relationship between polyphenolics, initial cell density and EC50 (EC50 less than 10 mg/L are illustrated)The dots in YZ projection indicates EC50 corresponding to polyphenolics when the initial cell density and time are ignored. The triangle in XZ projection indicates the distribution of EC50 under different initial cell densities; the same applies below
图 1 初始藻浓度-酚类化合物-EC50相互关系的三维散点图(展示EC50小于10 mg/L的化感物质)YZ投影面的圆点表示忽视初始浓度和处理时间时, 不同化合物对应的EC50值; XZ投影面的三角形表示不同初始浓度下EC50值分布状况; 下同Figure 1. Three-dimensional scatter plot of the relationship between polyphenolics, initial cell density and EC50 (EC50 less than 10 mg/L are illustrated)The dots in YZ projection indicates EC50 corresponding to polyphenolics when the initial cell density and time are ignored. The triangle in XZ projection indicates the distribution of EC50 under different initial cell densities; the same applies below然而, 不同酚类化合物的抑藻活性存在明显差异, 杨柳科的水杨酸[20]和芸香科的香豆素[21]对铜绿微囊藻的影响最为显著, 半数效应浓度低至0.01和0.5 mg/L; 而香草酸和阿魏酸在相似初始藻浓度和处理时间下, EC50却高达106[22]和302.94 mg/L[23]。这种抑藻能力的悬殊与酚类苯环上的取代基类型相关[24], 即香草酸、阿魏酸苯环上的甲氧基直接降低二者抑藻活性[8, 25]。此外, 酚类苯环上羟基的数量和位置也会直接影响到酚类的抑藻活性。Huang等[26]证明具有较多羟基取代基的山奈酚和木犀草素, 抑藻能力显著强于较少羟基取代基的7-羟基黄酮和6-羟基黄酮。当羟基个数相同时, 酚类的抑藻活性取决于羟基位置, Nakai等[8]将邻苯二酚、邻苯三酚和它们的同分异构体相互比较, 结果清晰显示羟基位于对位和邻位的酚类比位于间位的酚类对铜绿微囊藻的抑制作用更强。此外, 酚被氧化成醌类物质后对藻类的抑制作用可增强近百倍[27], 例如2 mg/L的1-萘酚可抑制细长聚球藻(Synechococcus elongatus)细胞生物量的35.54%[28], 氧化为1, 2-萘醌后仅0.04 mg/L即可将铜绿微囊藻抑制50%[27]。
This page contains the following errors:
error on line 1 at column 1: Start tag expected, '<' not foundBelow is a rendering of the page up to the first error.
1.2 含氮化合物
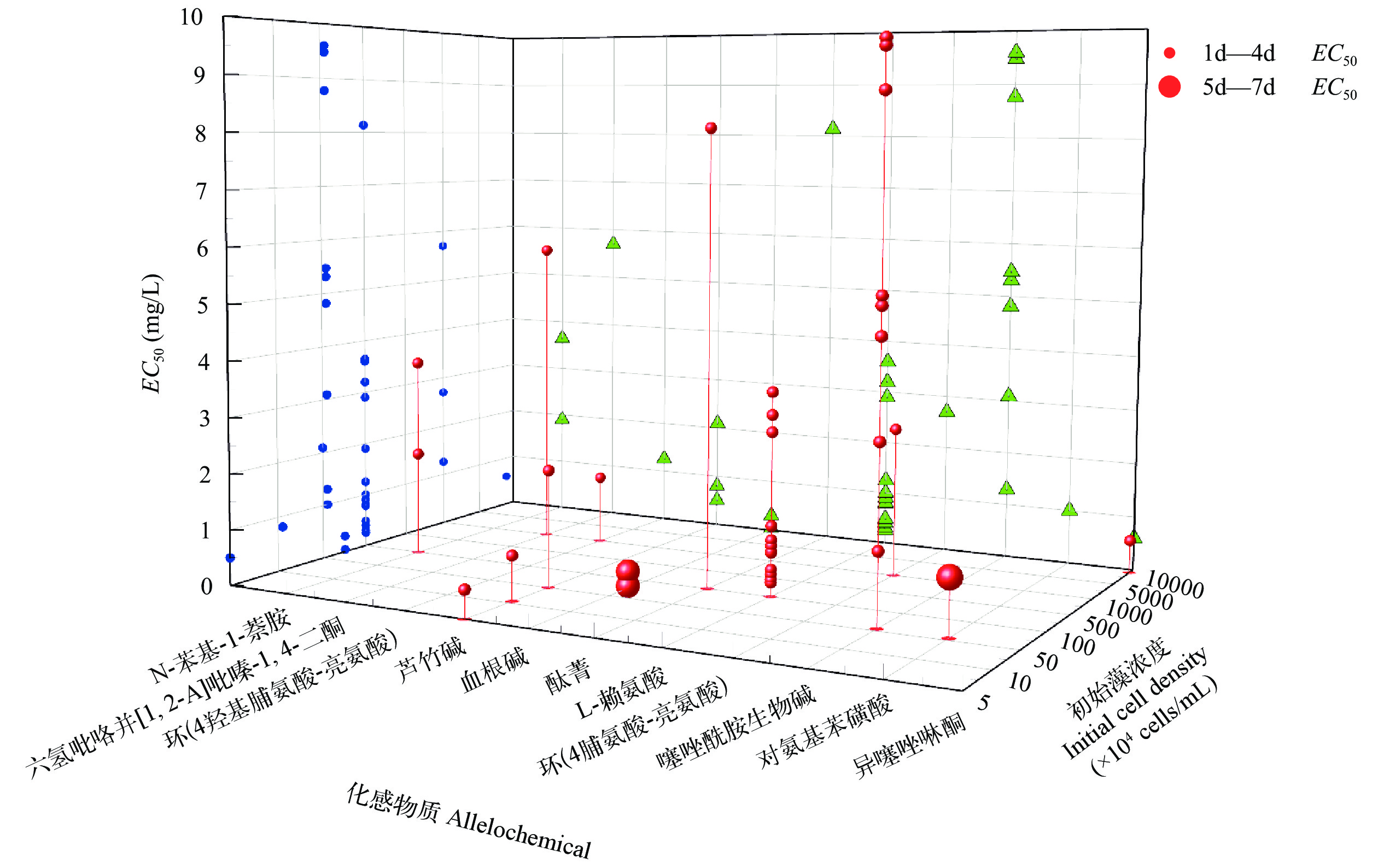
生物碱、氨基酸、苯胺及其衍生物是抑藻效用明显的常见含氮化合物(图 2)。含氮化合物在自然界中含量较少、分布不均匀, 但功能多样、具有显著的生物活性, 对蓝藻存在广谱抑制作用且整体抑藻能力差别较小, 10 mg/L以内剂量均可将蓝藻生长抑制50%。
![]() 图 2 初始藻浓度-含氮化合物-EC50相互关系的三维散点图(展示EC50小于10 mg/L的化感物质)YZ投影面的圆点表示忽视初始浓度和处理时间时, 不同化合物对应的EC50值; XZ投影面的三角形表示不同初始浓度下EC50值分布状况; 下同Figure 2. Three-dimensional scatter plot of the relationship between N-containing allelochemicals, initial cell density and EC50 (EC50 less than 10 mg/L are illustrated)The dots in YZ projection indicates EC50 corresponding to polyphenolics when the initial cell density and time are ignored. The triangle in XZ projection indicates the distribution of EC50 under different initial cell densities; the same applies below
图 2 初始藻浓度-含氮化合物-EC50相互关系的三维散点图(展示EC50小于10 mg/L的化感物质)YZ投影面的圆点表示忽视初始浓度和处理时间时, 不同化合物对应的EC50值; XZ投影面的三角形表示不同初始浓度下EC50值分布状况; 下同Figure 2. Three-dimensional scatter plot of the relationship between N-containing allelochemicals, initial cell density and EC50 (EC50 less than 10 mg/L are illustrated)The dots in YZ projection indicates EC50 corresponding to polyphenolics when the initial cell density and time are ignored. The triangle in XZ projection indicates the distribution of EC50 under different initial cell densities; the same applies below生物碱凭借其抗菌、杀虫功效和抗癌潜能[36]等特性引起广泛关注, 目前异喹啉类生物碱和吲哚生物碱的强大抑藻能力已被证实。异喹啉类生物碱是种类最多、结构类型多样的生物碱类别, 其中苣叶秃疮花(Dicranostigma lactucoides)和血根草(Sanguinaria canadensis)等提取物可对蓝、绿藻产生极强毒性[37], 经鉴定和检测后发现抑藻有效成分主要为白屈菜红碱、血根碱、小檗碱和黄连碱, 进一步提纯检验表明这些生物碱在96h内对铜绿微囊藻和窗格隐杆藻(Aphanothece clathrata)等蓝藻的EC50仅为0.28—0.82 mg/L[38]; 而含有吲哚生物碱的侧生藻(Fischerella sp.)可在共培养期间抑制其他7株包括念珠藻(Nostoc sp.)和假鱼腥藻(Pseudanabaena sp.)等蓝藻的生长。
生物碱的抑藻活性与光照条件关系密切, 在光暗交替条件下, 小檗碱可显著降低铜绿微囊藻的叶绿素荧光参数和生长密度, 且这种抑制作用随光照强度的增加而增加, 而在恒定黑暗条件下却未观察到小檗碱诱导的显著变化[39]。Zhang等[40]认为这是由于黑暗中铜绿微囊藻无法进行光合作用, 小檗碱缺乏作用靶点因而细胞未受抑制。因而, 干扰光合作用过程可能是生物碱抑藻的主要机制之一, 并且这种干扰主要是通过阻断电子传递链, 影响碳同化和光呼吸碳氧化而造成的[41]。Shao等[42]发现PS Ⅱ反应中心电子供、受体侧都是血根碱对铜绿微囊藻的靶点, 白屈菜红碱也能显著抑制PS Ⅱ供体侧电子传递[43]; 小檗碱胁迫下的铜绿微囊藻光合色素减少[44], 光合作用相关基因psaB和psbD1表达受抑[41], 这些基因转录减少正是阻断了电子转运[45]。而隶属吲哚生物碱的芦竹碱可抑制藻胆色素和PS Ⅱ之间的能量转移而抑制鱼腥藻(Anabaena sp.)生长[46]。另外, 生物碱的抑藻机制还表现为蓝藻细胞壁/膜和超微结构损伤, Shao等[42]发现血根碱能降低细胞质的含量从而导致细胞透射率显著增加, 类囊体含量也降低; 在小檗碱胁迫下铜绿微囊藻细胞壁/膜及类囊体等超微结构被严重破坏[44]; 从侧生藻中提取出的 Hapalindole型生物碱导致小球藻(Chlorella sp.)和月牙藻(Selenastrum sp.)等6株绿藻超微结构的大面积损伤, 并对光合活性的抑制呈现时间和剂量依赖性[47]。与之类似, 另一种吲哚生物碱——色胺同样造成蓝藻类囊体空泡化等超微结构异常, 产生不可逆损伤[48]。
氨基酸对蓝藻(尤其是微囊藻)的特异性抑制作用(对硅藻和绿藻没有抑制作用[49])和机制也符合含氮化合物的抑藻机制特征, 这种作用也是通过使蓝藻细胞结构强烈破损实现的。Yamamoto等[50]通过扫描电镜观察到1.2—5 mg/L的L-赖氨酸可以对所有供试铜绿微囊藻细胞壁造成严重损伤并迅速裂解细胞, 惠氏微囊藻(Microcystis wesenbergii)对L-赖氨酸最为敏感, 0.6 mg/L处理24h后细胞便死亡。L-赖氨酸经过丙二酰化修饰后, 抑藻效应进一步增强, 0.6 mg/L足以完全裂解所有藻细胞[49]。L-缬氨酸的抑藻活性甚至更强于L-赖氨酸, 能以更快的速率影响微囊藻形态和完整性, 导致细胞穿孔和塌陷, 并伴随着氧化应激失衡而脂质过氧化[51]。
苯胺及其衍生物对多种蓝藻也表现出高毒性[52]。1—100 μg对甲苯胺即可抑制包括阿格门氏藻(Agmenellum quadruplicatum)在内的8种蓝藻正常生长[53]; 4-(3, 5-二甲氧基苯乙烯)苯胺的顺、反式异构体均对秋葵颤藻(Oscillatoria perornata)具有选择性杀藻活性[54]; 在重复投药方式下, 2.5 mg/L N-苯基-1-萘胺(每次0.05 mg/L)可彻底抑制铜绿微囊藻PS Ⅱ活性, 且对细胞膜损伤面积达到90%以上[55]; 酯酶常用作表征膜完整性的标志物[23], 即使是一次性投加4.39 mg/L N-苯基-1-萘胺也可降低其酯酶活性的22.2%[56]。由上可知, 含氮化合物主要通过干扰光合作用过程(尤其是阻断电子转运), 损伤细胞膜/壁结构, 甚至深入蓝藻细胞损伤超微结构而对藻细胞造成严重损伤。
1.3 脂肪酸/酯类
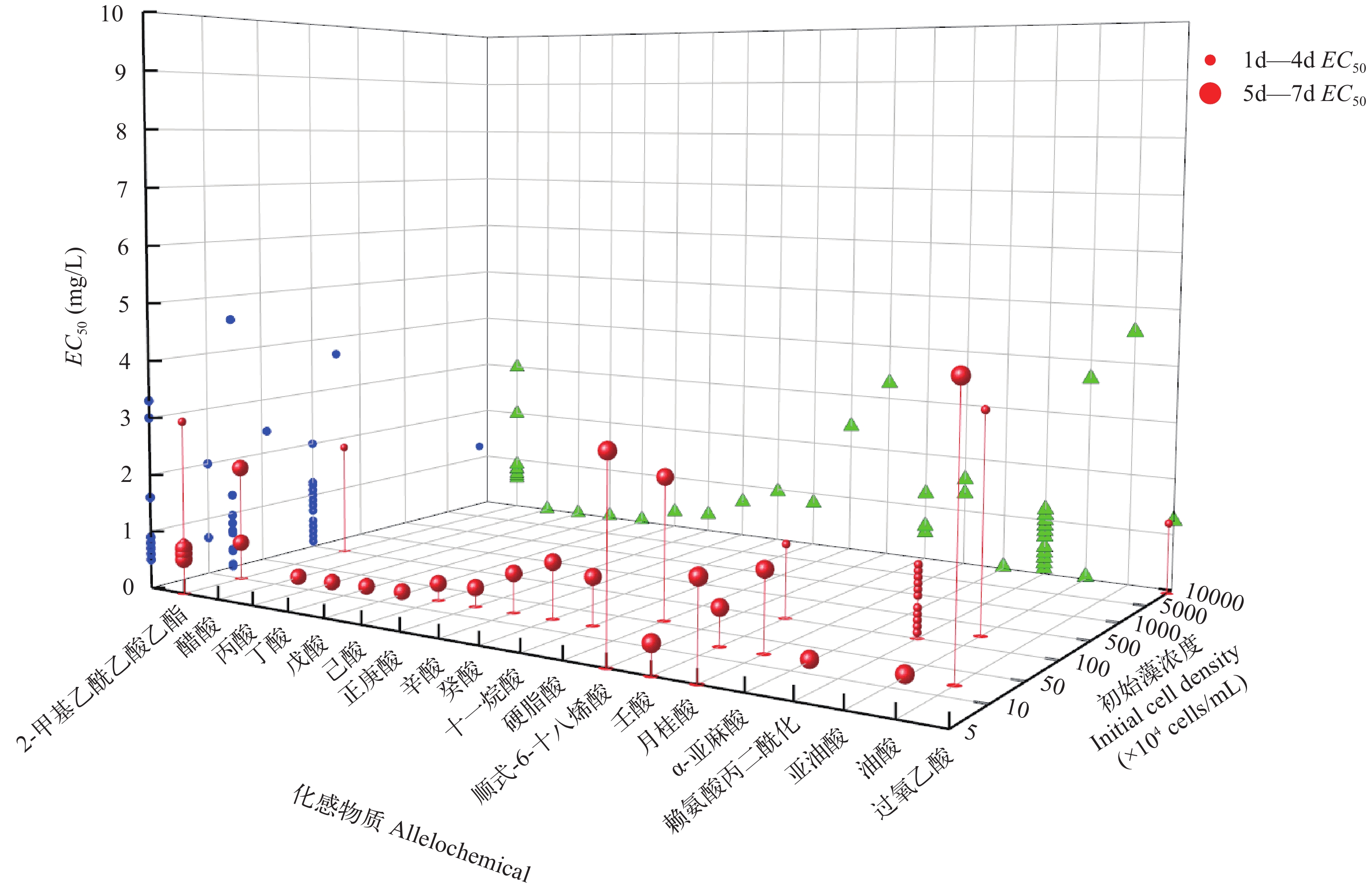
自然界约有40种脂肪酸, 少部分以游离形式存在, 通常以酯的形式存在于脂质成分中[17]。根据当前已统计的、对蓝藻有抑制效应并量化的有18种, 其中77%的脂肪酸或酯类能以较少剂量对蓝藻呈现极强毒性(EC50<1 mg/L; 图 3), 如亚油酸(EC50=0.047 mg/L)[57]、α-亚麻酸(EC50=0.036 mg/L)[57]和2-甲基乙酰乙酸乙酯(Ethyl 2-methylacetoacetate, EMA, EC50=0.65 mg/L)[58]等。
![]() 图 3 初始藻浓度-脂肪酸/酯类-EC50相互关系的三维散点图(展示EC50小于10 mg/L的化感物质)YZ投影面的圆点表示忽视初始浓度和处理时间时, 不同化合物对应的EC50值; XZ投影面的三角形表示不同初始浓度下EC50值分布状况; 下同Figure 3. Three-dimensional scatter plot of the relationship between fatty acids/esters, initial cell density and EC50 (EC50 less than 10 mg/L are illustrated)The dots in YZ projection indicates EC50 corresponding to polyphenolics when the initial cell density and time are ignored. The triangle in XZ projection indicates the distribution of EC50 under different initial cell densities; the same applies below
图 3 初始藻浓度-脂肪酸/酯类-EC50相互关系的三维散点图(展示EC50小于10 mg/L的化感物质)YZ投影面的圆点表示忽视初始浓度和处理时间时, 不同化合物对应的EC50值; XZ投影面的三角形表示不同初始浓度下EC50值分布状况; 下同Figure 3. Three-dimensional scatter plot of the relationship between fatty acids/esters, initial cell density and EC50 (EC50 less than 10 mg/L are illustrated)The dots in YZ projection indicates EC50 corresponding to polyphenolics when the initial cell density and time are ignored. The triangle in XZ projection indicates the distribution of EC50 under different initial cell densities; the same applies belowThis page contains the following errors:
error on line 1 at column 1: Start tag expected, '<' not foundBelow is a rendering of the page up to the first error.
1.4 萜类化合物及其衍生物
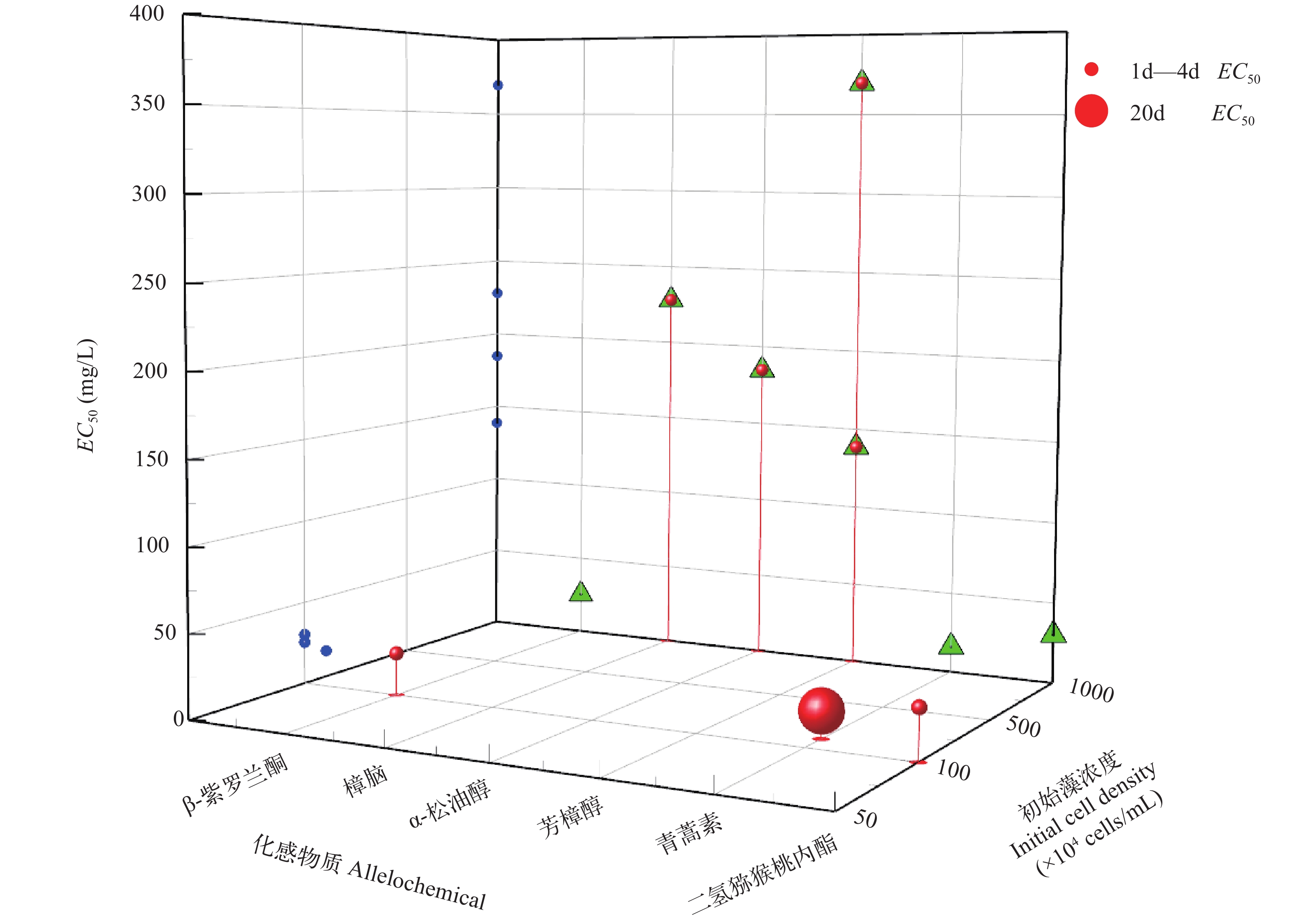
萜类化合物是具有异戊二烯[(C5H8)n]通式的碳氢化合物及其含氧衍生物(如醇、醛、酮、羧酸等)的总称[17], 多数具有较强的香气和生理活性, 不仅可对生物自身具有防护作用[64], 还可吸引其他生物, 具有趋避、抗菌、驱虫、杀虫和抑藻等功效[65](图 4), 但具有抑藻能力的萜类化合物数量及抑制效果均不及其他三个类别的化合物(EC50>10 mg/L; 图 5a), 挥发性较强和对蓝藻细胞作用靶点单一是其抑藻效果相对较弱的主要原因。
![]() 图 4 初始藻浓度-萜类化合物-EC50相互关系的三维散点图YZ投影面的圆点表示忽视初始浓度和处理时间时, 不同化合物对应的EC50值; XZ投影面的三角形表示不同初始浓度下EC50值分布状况Figure 4. Three-dimensional scatter plot of the relationship between terpenoids, initial cell density and EC50The dots in YZ projection indicates EC50 corresponding to polyphenolics when the initial cell density and time are ignored. The triangle in XZ projection indicates the distribution of EC50 under different initial cell densities
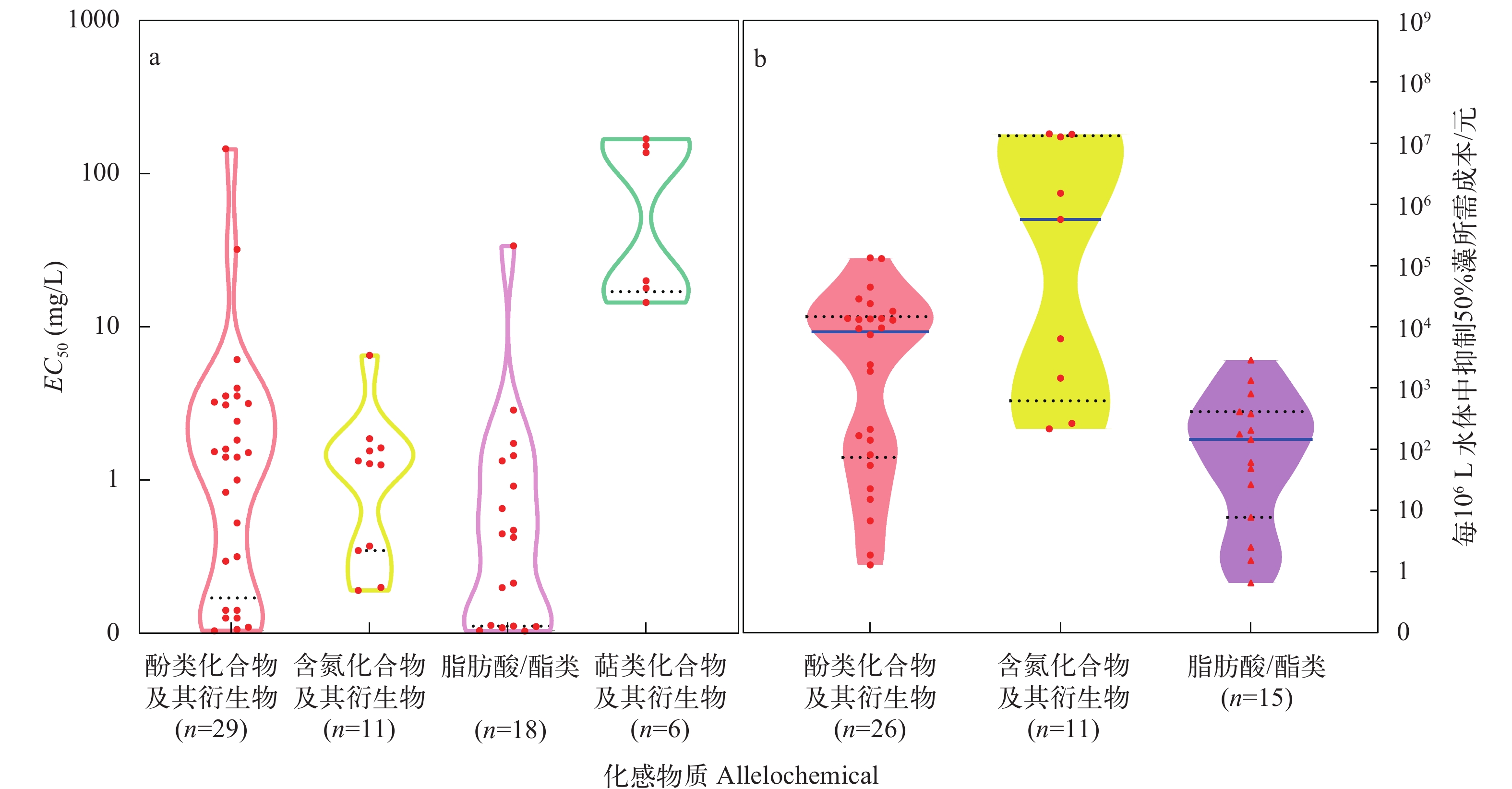
图 4 初始藻浓度-萜类化合物-EC50相互关系的三维散点图YZ投影面的圆点表示忽视初始浓度和处理时间时, 不同化合物对应的EC50值; XZ投影面的三角形表示不同初始浓度下EC50值分布状况Figure 4. Three-dimensional scatter plot of the relationship between terpenoids, initial cell density and EC50The dots in YZ projection indicates EC50 corresponding to polyphenolics when the initial cell density and time are ignored. The triangle in XZ projection indicates the distribution of EC50 under different initial cell densities![]() 图 5 四种化感物质抑藻活性的提琴图(a)及高效抑藻化感物质(EC50<10 mg/L)理论耗材成本的提琴图(b)以百万升密度为104—106的单一蓝藻水体达到50%抑制率时各化感物质所耗费的成本为例, 提琴图的宽度、高度分别表示数据的密集度和极差, 蓝线、黑虚线分别为中位数、四分位数所在值Figure 5. Violin plot of inhibiting capacities of allelochemicals from different categories (a) and Violin plot of the cost of theoretical consumables (b)A case study of “allelochemicals to inhibit the growth of 50% of cyanobacteria, with initial density is 104 to 106, in a million liters of water” The width and height of the violin plot indicate the density and difference of the data, respectively, of which the blue line and the black dotted line are the median and quartile values, respectively
图 5 四种化感物质抑藻活性的提琴图(a)及高效抑藻化感物质(EC50<10 mg/L)理论耗材成本的提琴图(b)以百万升密度为104—106的单一蓝藻水体达到50%抑制率时各化感物质所耗费的成本为例, 提琴图的宽度、高度分别表示数据的密集度和极差, 蓝线、黑虚线分别为中位数、四分位数所在值Figure 5. Violin plot of inhibiting capacities of allelochemicals from different categories (a) and Violin plot of the cost of theoretical consumables (b)A case study of “allelochemicals to inhibit the growth of 50% of cyanobacteria, with initial density is 104 to 106, in a million liters of water” The width and height of the violin plot indicate the density and difference of the data, respectively, of which the blue line and the black dotted line are the median and quartile values, respectively单萜(n=2)和倍半萜(n=3)化合物是挥发油的主要成分, 可从植物体缓慢释放, 具有相对活跃的化感抑藻活性[17]。紫罗兰酮作为单萜的丙酮加成物与其衍生物α-紫罗兰酮[66]、β-紫罗兰酮[67]、3-氧化-紫罗兰酮[66]和4-氧化-β-紫罗兰酮[68]等均对铜绿微囊藻产生一定抑制, 其中弱水溶性的3-氧化-紫罗兰酮对铜绿微囊藻的抑制更具有时间和剂量依赖性。水生植物小叶眼子菜(Potamogeton cristatus)和黄丝草(Potamogeton maackianus)等精油中分离出的二氢猕猴桃内酯属于倍半萜内酯, 也可抑制铜绿微囊藻, 但EC50值达到30.1 mg/L[67], 且有机合成或植物提取成本较高, 工业应用仍存在限制。
萜类化合物对于铜绿微囊藻的抑制机理主要集中于多途径干扰细胞的光合功能, 包括降低光合色素、降低最大光化学量子产率、升高非光化学猝灭及中断PS Ⅱ反应中心的电子传递等[5, 66, 69]。例如, 较高浓度的樟脑、α-松油醇和芳樟醇可以诱导铜绿微囊藻和莱茵衣藻(Chlamydomonas reinhardtii)中叶绿素a和叶黄素等光合色素降解, 降低PS Ⅱ效率[69]; 50 μg/L的3-氧化-紫罗兰酮可破坏铜绿微囊藻细胞类囊体膜, 中断PS Ⅱ反应中心的电子传递, 导致关键光合功能受阻而死亡[66]。Ni等证明约16 mg/L青蒿素可降低藻胆蛋白含量[5, 70], 改变光合系统的电子转移过程, 同时导致细胞肿胀变形、膜破裂导致藻凋亡。
2. 化感物质抑藻的效应-制造成本综合预估
提纯后化感物质的实际应用除需考虑化感物质本身的抑藻效应外, 所涉及的经济成本(尤其是制造成本)也是评价其实用性的重要因素, 制造成本主要取决于植物源化感物质的广泛性和提取合成的难易程度等, 朱小琴等[71]将13种植物化感物质在同一公司的分析纯制品的价格作为衡量标准以反映制造成本, 得出对羟基苯甲酸>小檗碱>芦竹碱>壬酸等的抑藻成本顺序。为此, 本综述选用国内三家化学试剂种类齐全、纯度符合要求的自主试剂品牌公司(麦克林, 上海麦克林生化科技有限公司; 安耐吉, 萨恩化学技术有限公司; 阿拉丁, 上海阿拉丁生化科技股份有限公司; 分析纯制品)的售卖价格取平均值, 以更准确反映国内化感物普遍生产成本。综合各类高效化感抑藻物质(以EC50低于10 mg/L为标准)的生产成本和抑藻活性, 计算并预估其用于抑藻时的理论耗材成本, 以5—7d内对百万升初始密度为105—106 cells/mL的单一蓝藻生长抑制50%时所需剂量的成本为例, 预估各类高效抑藻化感物的应用潜力(其中具有抑藻活性的萜类化合物个数较少且抑藻活性较低, EC50高达25.3—228 mg/L, 因而不参与成本评估)。
基于以上数据, 选取GraphPad Prism 8.0.2作为可视化工具, 结合提琴图展示四类化感物抑藻活性、高效抑藻化感物质的理论耗材成本的分布状态、统计数字特征及概率密度, 由图 5所示, 以醋酸、丁酸和己酸等为代表的脂肪酸/酯类的EC50为0.015—52.95 mg/L, 抑藻活性图宽度均匀、中位值最小, 整体化感高效(图 5a)。其高效抑藻脂肪酸的理论耗材成本图宽度也较为均衡, 极大值、极小值和中位值均最低, 且纵向跨度较小, 表明其性价比最优(图 5b)。47%和87%的脂肪酸/酯类可在100元、1000元以内将百万升初始浓度为105—106 cells/mL的单一蓝藻生长抑制50%, 极具微囊藻水华防治的应用潜能。
具有抑藻活性的酚类化合物总数最多, 抑藻活性的纵向跨度最大, EC50为0.05—162.53 mg/L。高效抑藻酚类的理论耗材成本也存在较大差异, 但数值分布更为集中, 中位数位列四类化合物的第二名。以水杨酸、蒽醌和苯甲醛等为代表的酚类化合物抑藻活性极强且成本较低, 10元以内即可达到目标抑藻效果。邻苯二酚和5, 4-二羟基黄酮虽抑藻活性强但剂量价格昂贵, 相同抑藻效果下所需剂量的成本是水杨酸、蒽醌和苯甲醛等的数万倍。对甲苯酚、香豆素、对苯二酚和没食子酸等均是性价比较高的抑藻化感物。
含氮化合物的抑藻活性整体对蓝藻有特异性、高抑制活性, 中位数与酚类化合物相当, EC50集中于0.3—8.14 mg/L。但其理论耗材成本的中位数却最大, 极大值、极小值及变化幅度也较大。其中对羟基苯磺酸、L-赖氨酸的抑藻成本最低, 均在1000元内; 与此差距较大的盐酸黄连碱、芦竹碱和白屈菜红碱虽具有极强的抑藻能力, 但由于其提纯或人工合成仍未具备大规模生产条件, 导致其作为抑藻剂的成本极高, 达到50%抑藻效果需耗费上千万元, 与酚类化合物中香豆素等抑藻能力相当的白屈菜红碱和黄连碱所需经济成本却超出香豆素的上万倍; 小檗碱和血根碱的经济成本分别是抑藻能力相当的正庚酸的194倍和45608倍, 极大限制了含氮化合物(尤其是生物碱)的实际应用。
具有抑藻活性的萜类化合物个数和抑藻活性均不如其他三类, EC50高达25.3—228 mg/L, 因此, 选取单一化感物质实际抑藻时, 酚类化合物和脂肪酸是优先考虑的物质类别。
3. 化感物质联合抑藻
在自然水体中, 单一化感物质含量远远达不到有效抑制藻类生长的EC50值, 如自然水体中酚类浓度仅为μg/L水平[72], 即使人工施入达到理想浓度也会给环境生态带来较多不确定性; 根据上述分析各类化感物质抑藻活性、作用机制和所需成本发现, 部分化感物质的抑藻活性强但所需成本高, 而有的成本较低但活性却较弱, 因此仅依靠某一种化感物质常常无法经济、有效地控制蓝藻水华。值得注意的, 植物或微生物产生、释放的化感物质本身共存于自然水体, 因此, 多种化感物联合抑藻(以下简称“联合抑藻”)是符合自然规律、更切合环境生态实际的抑藻思路, 并且多数研究发现联合抑藻下每一种化感物质用量减少、抑藻效率高且经济。为更好理解化感物质联合作用所产生的抑藻效应, 从上述四类物质抑藻活性、作用靶点出发并根据已有研究, 探讨同一(表 2)和不同类型(表 3)化感物质联合产生的抑藻效应与机理。
表 2 相同类型化感物质的联合作用Table 2. Joint effect of similar allelochemicals on Microcystis aeruginosa growth化感物质
Allelochemical混合模式
Mixing mode评价方式
Assessment method初始藻浓度
Initial cell density (cells/mL)时间
Time (d)联合作用
Joint effect参考文献Reference 1. 酚类+酚类 (1)邻苯三酚+邻苯二酚 等效浓度比 相加指数法
半致死剂量指数法2×106—
3×1063 协同作用 [79] (2)邻苯二酚+没食子酸 加和作用 (3)邻苯三酚+没食子酸 (4)邻苯三酚+没食子酸 (1﹕4); (2﹕3); (1﹕1);
(3﹕2); (4﹕1)
终浓度为2.5 mg/L毒性指数法
毒性单位法
等效线图法1×106 3 加和作用 [81] (5)邻苯三酚+没食子酸+邻苯二酚 (1﹕1﹕3); (1﹕2﹕2);
(3﹕1﹕1); (1﹕1﹕1);
(2﹕2﹕1); (1﹕3﹕1)1×106 3 加和作用 [81] (6)邻苯三酚+没食子酸+邻苯二酚+鞣花酸 穗状狐尾藻水培液
检测浓度实际测定的结果与
预测抑制结果对比104— 105 3 协同作用 [9] (7)香豆素+对羟基苯甲酸 80%﹕20% EC50
60%﹕40% EC50实际测定的结果与
预测抑制结果对比5.5×105 2、4、6、8、10 协同作用 [83] (8)香豆素+对羟基苯甲酸 20%﹕80% EC50
40%﹕60% EC50拮抗作用 (9)对香豆酸+水杨酸+
苯甲酸终浓度0.01 mg/L 对比生长抑制率 — 8 协同作用 [20] (10)香草酸+肉桂酸 等效浓度比 毒性单位法
相加指数法A650=0.15 — 协同作用 [22] (11)咖啡酸+原儿茶酸 等效浓度比 毒性指数法(TI) 1×106 3 拮抗作用 [87] (12)咖啡酸+原儿茶酸+香草酸 加和作用 (13)咖啡酸+原儿茶酸+香草酸+阿魏酸 (14)咖啡酸+原儿茶酸+香草酸+阿魏酸+苯甲酸+对羟基苯甲酸 2. 脂肪酸+脂肪酸 (1)亚油酸+α-亚麻酸+油酸 0.04 mg/L+0.03 mg/L +0.70 mg/L 实际测定的结果与预测抑制结果对比 (2)2×105 5 协同作用 [57] (2)亚油酸+油酸+辛酸 0.04 mg/L+0.70 mg/L +0.50 mg/L (3)棕榈酸+乳酸 等效浓度比 联合效应系数 105— 106 3 加和作用 [88] 3. 含氮化合物+含氮化合物 (1)环(4羟基脯氨酸-亮氨酸)+环(脯氨酸-亮氨酸) 0.4 mg/L和0.4 mg/L
(单独作用时为
弱杀藻作用)观察生长曲线和单独培养对比 1×107 2 协同作用 [86] (2)血根碱+白屈菜红碱 等效浓度比 毒性指数法 A680=0.09 6 协同作用 [85] 表 3 不同类型化感物质的联合作用Table 3. Joint effect of dissimilar allelochemicals on Microcystis aeruginosa growth化感物质
Allelochemical混合模式
Mixing mode评价方式
Assessment method初始藻浓度Initial cell density (cells/mL) 时间
Time (d)联合作用
Joint effect参考文献
Reference1. 酚类+脂肪酸 (1)邻苯二酚+亚油酸 等效浓度比 相加指数法
半致死剂量指数法2×106 — 3×106 3 协同作用 [79] (2)焦棓酸+亚油酸 加和作用 (3)没食子酸+亚油酸 协同、加和作用 (4)原儿茶酸+硬脂酸 20%﹕80% EC50
40%﹕60% EC50实际测定的结果与预测抑制结果对比 5.5×105 2、4、6、8、10 协同作用 [83] (5)原儿茶酸+硬脂酸 80%﹕20% EC50
50%﹕50% EC50
60%﹕40% EC50拮抗作用 (6)肉桂酸+丁二酸 等效浓度比 毒性单位法
相加指数法A650=0.15 — 协同作用 [22] (7)香草酸+丁二酸 (8)肉桂酸+香草酸+丁二酸 (9)苯甲酸+棕榈酸 等效浓度比 联合效应系数 105— 106 3 加和作用 [88] (10)咖啡酸+壬酸 相同浓度比 混合物EC50与个体EC50之和相比 (1)0×106 3 协同作用 [82] 等效浓度比 拮抗作用 2. 脂肪酸+含氮化合物 (1)过氧乙酸+异噻唑啉酮 等效浓度比 协同指数 9×107 4 协同作用 [91] (2)硬脂酸+对氨基苯磺酸 20%﹕80% EC50
40%﹕60% EC50实际测定的结果与预测抑制结果对比 5.5×105 2、4、6、8、10 协同作用 [83] 80%﹕20% EC50
50%﹕50% EC50
60%﹕40% EC50拮抗作用 3. 酚类+含氮化合物 (1)原儿茶酸+对氨基苯磺酸 80%﹕20% EC50
40%﹕60% EC50理论抑藻率与实际抑藻率相比 5.5×105 2、4、6、8、10 协同作用 [83] 50%﹕50% EC50 加和作用 20%﹕80% EC50
40%﹕60% EC50拮抗作用 (2)咖啡酸+ N-苯基-1-萘胺 相同浓度比 混合物EC50与个体EC50之和相比 (1)0×106 3 拮抗作用 [82] 等效浓度比 拮抗作用 4. 酚类+脂肪酸+含氮化合物 (1)原儿茶酸+硬脂酸+对氨基苯磺酸 25%﹕50%﹕25% EC50
20%﹕40%﹕40% EC50理论抑藻率与实际抑藻率相比 5.5×105 2、4、6、8、10 协同作用 [83] 50%﹕25%﹕25% EC50
25%﹕25%﹕50% EC50拮抗作用 33.3%﹕33.3%﹕33.3% EC50 加和作用 40%﹕20%﹕40% EC50
40%﹕40%﹕20% EC504天前拮抗作用, 4天后协同作用 (2)香豆素+对氨基苯甲酸+硬脂酸+对氨基苯磺酸 (80%+20%)﹕(80%+20%) EC50
(80%+20%)﹕(20%+80%) EC50
(50%+50%)﹕(50%+50%) EC50
(60%+40%)﹕(60%+40%) EC50
(60%+40%)﹕(40%+60%)
EC50拮抗作用 (3)香豆素+对氨基苯甲酸+邻苯二酚+硬脂酸+对氨基苯磺酸 (80%+20%)﹕(25%+50%+
25%)EC50
(80%+20%)﹕(20%+40%+
40%)EC50
(40%+60%)﹕(25%+50%+
25%)EC50
(40%+60%)﹕(20%+40%+
40%)EC50理论抑藻率与实际抑藻率相比 拮抗作用 (4)咖啡酸+壬酸+N-苯基-1-萘胺 相同浓度比
等效浓度比混合物EC50与个体EC50之和相比 (1)0×106 3 协同作用 [82] 3.1 同一类型的化感物质联合作用
化感物质联合作用是指两种及以上化感物质产生的生物学效应, 分为协同(Synergism)、加和(Additive effect)、拮抗(Antagonism)及独立作用(Independent action)[73]。协同、加和、拮抗作用指的是两种或两种以上物质对生物机体产生的生物学效应强度大于、等于、小于单一物质生物学效应的总和, 独立作用指各物质单独发挥作用而无交互作用[74, 75]。既往研究认为, 同一结构类型的化感物质不可能出现协同效应, 除非二者混合后反应生成新化合物[76], 且这种化合物的生物活性远大于反应前的两者。但经过后续研究验证, 同类化感物联合仍可出现协同作用, 但具体机理却不甚清晰, 因此本文针对同一类型化感物质混合产生的联合效应进行分类讨论, 并探讨产生这种联合效应的内在规律。
酚类+酚类 作为含量丰富、化感活性极强、作用靶点多样且成本可控的抑藻物质之一, 酚类化合物的联合成为抑藻研究重点, 尽管先前众多研究表明, 酚类化合物的联合作用多产生拮抗效应, 如对羟基苯甲酸、对香豆酸和阿魏酸共同作用于黑麦草(Loliumperenne L)根系, 这几种酚类物质会产生拮抗作用[76]; Lyu等[77]发现香草酸和对香豆酸共同施用时, 彼此会降低共施物的生物有效性, 但对于酚类化合物的联合抑藻机制仍需进一步考察。
祁茜等[78]认为化感物对受体细胞的作用靶点越多, 协同作用越强, 反之则具有拮抗作用。如邻苯三酚可对蓝藻光合作用、呼吸作用和氧化应激平衡等多个靶点造成损伤, 且自氧化速度极快(1h内)[62], 是最常见的用于混合抑藻的选择成分之一, 可分别与严重诱导细胞氧化损伤的邻苯二酚[79]、抑制光合色素含量的水杨酸[80]和破坏细胞膜结构的肉桂酸[22]二元混合, 达到互补增强的效果, 从而产生协同作用。而没食子酸和邻苯三酚无论以怎样配比, 都无法呈现协同作用[9, 79, 81], 根据已报道文献, 认为二者具有相似的抑藻机制, 即没食子酸可以显著减少铜绿微囊藻PS Ⅱ效率和整个电子传递链活动, 而这也正是邻苯三酚的作用靶点之一[9]。因此具有多样、互补的抑藻靶点增加了产生协同作用的可能性(以下称之为“多靶点效应”)。
具有相同作用靶点的酚类所产生的联合作用是加和还是拮抗, 取决于混合物的总浓度[76]。Inderjit等[76]以酚类对细胞的作用靶点之一细胞膜为例, 提出了化感物分子总数与膜靶点之间的相对关系影响联合作用类型的假设: 酚类结构各异, 对膜(作用靶点)亲和力和内在活性不同。若可供作用的膜靶点多于化感物质分子数时, 那化感物质产生的联合效应为加和, 但若分子总数多于作用靶点, 则活性更强、更具竞争力的化感物质将捕获更多靶点, 另一化感物质则捕获更少靶点, 由于这一化感物质并未完全发挥作用, 因而各成分间呈现出拮抗作用。
但多靶点组合并不是形成协同作用的唯一前提条件。例如, 香豆素、对羟基苯甲酸和阿魏酸三者同样以降低叶绿素a含量、诱导活性氧激增导致膜结构受损为主要抑藻机制, 但前两者与后两者的联合均呈现出协同作用, 这表明联合作用不仅仅与作用靶点有关, 还与其他因素有关。Gao等[82]认为化感物混合比例和组合成分的固有抑藻活性是影响化感物联合效应的两个因素。Zuo等[83]发现抑藻活性较强的香豆素与对羟基苯甲酸混合时占比超过50%时出现协同作用, 反之则出现拮抗作用。本文将这种规律概括为“新木桶效应”, 即联合抑藻效果与单一化感物质的化感活性有关, 增加化感活性强的物质比例会增强组合整体的化感作用, 反之则会降低联合作用。
四种、五种化合物的混合抑藻效应较为复杂。Nakai等[62]和Zhu等[9]先后将邻苯三酚、没食子酸、儿茶酚和鞣花酸按照自然条件下植物体内固有浓度比例混合, 作用于铜绿微囊藻及铜绿微囊藻与羊角月牙藻(Selenastrum capricornutum)的混合体系, 发现这四种化合物呈现协同效应, 然而将这四种化合物按照等效浓度比(各自单独胁迫时的EC50)混合, 却仅呈现出加和作用。这与Warne等[84]得出的漏斗假说相符合, 即以等效浓度混合的化合物随组分数量增加, 出现加和效应的可能性更大, 出现协同和拮抗的可能性减少。这表明四种化感物的组合及其在植物体内的固有比例可能是适应自然、长期进化而形成的, 各自过高的浓度引发成分间拮抗反而不利于它们的联合抑藻效应。水稻中提取的对香豆酸、水杨酸和苯甲酸按体内固有比例混合, 终浓度为0.01 mg/L同样产生了协同作用[20]。
含氮化合物+含氮化合物 与酚类“‘多靶点组合’易产生协同作用”相符合, 含氮化合物的联合应用也呈现出相似的规律。血根碱可使PSⅡ反应中心电子的供、受体侧均受损, 白屈菜红碱仅损伤PS Ⅱ供体侧, 但能显著抑制细胞外的多糖、蛋白质等多聚物(Extracellular polymeric substances, EPSs)和碱性磷酸酶含量, 两者在靶点层面上相互补充, 取长补短, 故而产生协同的抑藻效果[85]。“多靶点组合”抑藻还出现在太湖中分离的金黄杆菌属(Chryseobacterium sp.)产生的两种抑藻化合物混合体系中, Guo等[86]发现环(4羟基脯氨酸-亮氨酸)和环(脯氨酸-亮氨酸)可以分别对铜绿微囊藻细胞的PS Ⅱ和抗氧化酶活性造成干扰, 两者组合产生的协同作用加速了细胞氧化稳态的破坏和光合能力受损, 严重抑制细胞生长。
脂肪酸+脂肪酸 脂肪酸单个抑藻效应极强、作用靶点多样, 混合常产生协同或加和作用, 并且这种联合效应多取决于不饱和脂肪酸的个数, 个数越多, 协同抑藻效果越好[57, 59]。从马来眼子菜中提取出以硬脂酸和棕榈酸等为主要成分的9种脂肪酸, 不论是饱和脂肪酸之间、相同碳链不同饱和程度的脂肪酸之间以及所有脂肪酸联合, 抑藻均具有协同作用, 但发现不饱和脂肪酸越多协同作用强度越大[59]。这可能与不饱和脂肪酸的自氧化或光氧化有关, 氧化产生的羟基化合物发挥主要抑藻活性, 且双键数目越多, 生成的过氧化氢越多, 造成细胞脂质过氧化程度越高[79]。张庭廷等[57]也得出相似结论, 即三种不饱和脂肪酸组合(α-亚麻酸、亚油酸和油酸)在第5天对单独培养的铜绿微囊藻的协同抑制率高达94%—100%, 且协同抑藻作用大于两种不饱和脂肪酸与一种饱和脂肪酸组合(辛酸、亚油酸、油酸)。同时该种协同抑藻效应还具有对藻种的选择特异性, 也就是将这两种组合作用于铜绿微囊藻与斜生栅藻的共培养体系, 铜绿微囊藻表现出对脂肪酸的协同抑制更为敏感[57]。
萜类化合物+萜类化合物 当前针对于萜类化合物的混合抑藻试验研究较少, 樟脑、α-松油醇和芳樟醇按照樟树鲜叶中固有比例(1﹕3﹕6)混合作用于铜绿微囊藻呈现出协同效应, 抑制率可达96%[69]。
总的来说, 同一类型化感物的混合抑藻试验中, 酚类化合物的混合抑藻研究最为广泛, 可得出混合化感物各组分的作用靶点多样(多靶点组合)、抑藻活性相对高的化感物占比大于50%(符合“新木桶效应”)和生物以固有比例混合三种情况出现协同的可能性更大的结论; 含氮化合物混合也得出“多靶点组合”更易协同的相似结论。脂肪酸之间的联合作用还取决于不饱和脂肪酸的占比, 不饱和脂肪酸越多越容易产生协同作用。当前针对于萜类化合物的混合抑藻试验研究较少, 按照固有比例混合出现了协同作用。
3.2 不同类型化感物质联合作用
酚类+脂肪酸 酚类和脂肪酸类化合物是最常见的两类化感抑藻物质[79, 89], 在植物分泌的化感物质体系中常相伴存在, Gao和Huang等[26, 82]先后从伊乐藻(Elodea nuttallii)浸提液中提取出壬酸等脂肪酸与芹菜素、咖啡酸、木犀草素等酚类化合物, 都是抑制铜绿微囊藻的主要化感成分。穗状狐尾藻中5种酚类和3种脂肪酸产生的联合作用甚至可占穗状狐尾藻整体化感作用的53%[90]。这两类化感物质都具有多样的作用靶点, 其联合多表现出协同或加和作用。
邻苯二酚、邻苯三酚分别与亚油酸组成的二元混合物产生协同、加和作用, 三者单独作用时均可不同程度地抑制铜绿微囊藻的光合作用并引发细胞氧化损伤, 联合作用使得这种抑制与损伤更加严重和迅速[79]。倪利晓等[79]认为这是由于酚类和不饱和脂肪酸产生了连锁反应, 即酚类化合物的强自氧化性可释放自由基, 自由基进一步氧化不饱和脂肪酸, 不饱和脂肪酸的氧化产物具有较强的抑藻效果, 从而产生协同作用。
酚类化合物与饱和脂肪酸的联合效应符合“新木桶定律”。硬脂酸可降低铜绿微囊藻叶绿素a含量和藻胆蛋白含量, 原儿茶酸的作用靶点同样集中降低细胞光合效率, 可使PS Ⅱ电子的传递、转移受阻, 二者虽具有相似的作用靶点, 但试验证明当硬脂酸占比超过50%时可产生协同作用, 反之则产生拮抗作用[83]。同样的现象也出现在从梭鱼草中分离出的酚类(肉桂酸、香草酸)和脂肪酸(丁二酸)的二元、三元混合物, 虽然均对铜绿微囊藻的生长表现出协同抑制, 但协同抑制强度却有所差异, 在单独作用时, 肉桂酸的抑藻效果强于香草酸, 因而与丁二酸组成的二元混合物协同程度也较高, 总浓度100 mg/L处理7d时抑制率可达92.78%, 丁二酸与香草酸混合物仅为84.81%[22]。由此说明, 单一作用时抑藻效果较好的化感物质进行联合作用时抑藻效果也相对较好, 而抑藻能力较差的化感物质在联合作用时会削弱整体的抑藻效果。
酚类或脂肪酸+含氮化合物 含氮化合物主要干扰细胞光合作用(尤其是阻断电子传递)、破坏细胞壁/膜结构和超显微结构等, 而脂肪酸、酚酸作用集中于细胞内部损伤且损伤靶点多样, 因此认为这种组合方式符合“多靶点组合”标准, 理论上具有明显的配合互补, 产生协同作用的可能较大。经过试验验证与理论相符, 郑串[91]发现过氧乙酸与异噻唑啉酮的多种配比对铜绿微囊藻都产生显著的协同抑藻效果, 并推测二者的协同作用具体是通过异噻唑啉酮改变藻细胞壁、膜通透性, 有利于过氧乙酸进入细胞利用其酸性和强氧化性直接破坏细胞内的叶绿素和酶系统而实现的。“新木桶效应”同样存在于这类组合中, 具有较强抑藻活性的对氨基苯磺酸(EC50=1 mg/L)与相对较低抑藻活性的硬脂酸(EC50=2.4 mg/L)混合时, 占比50%以上才可出现协同作用, 否则为拮抗作用[83]。酚类或脂肪酸与含氮化合物的联合抑藻是有效且具前景的, 从细胞内、外作用靶点互补、成本-活性优势互补, 是日后化感抑藻发展的突破点。
酚类+脂肪酸+含氮化合物 随着混合物组合的种类数量增多、比例多样, 产生联合抑藻效应规律也逐渐复杂化。Zuo等[83]将香豆素、对羟基苯甲酸、原儿茶酸、硬脂酸和氨基苯磺酸五种化感物质按不同比例组成三元、四元和五元混合物, 结果表明只有原儿茶酸、硬脂酸和对氨基苯磺酸的三元混合物出现协同和加和作用, 而其他四元、五元混合物的各种比例均产生拮抗作用, 这种现象的出现可以用Inderjit等[76]的“化感物分子总数与膜靶点之间的相对关系影响联合作用类型的假设”解释, 四、五元混合物的化感物质总分子数多于可供作用的藻细胞靶点, 使得只有其中一些化感活性强的、有竞争力的化合物起化感作用, 其他活性较低的化合物未完全表达, 因而出现拮抗作用。同时, 多元混合也遵循“新木桶效应”, 抑藻活性较低的咖啡酸在壬酸与N-苯基- 1 -萘胺的混合物中占比的增加降低了混合物的联合毒性, 验证化感物比例与单一物质的抑藻活性均会影响最终的联合抑藻效果[82]。
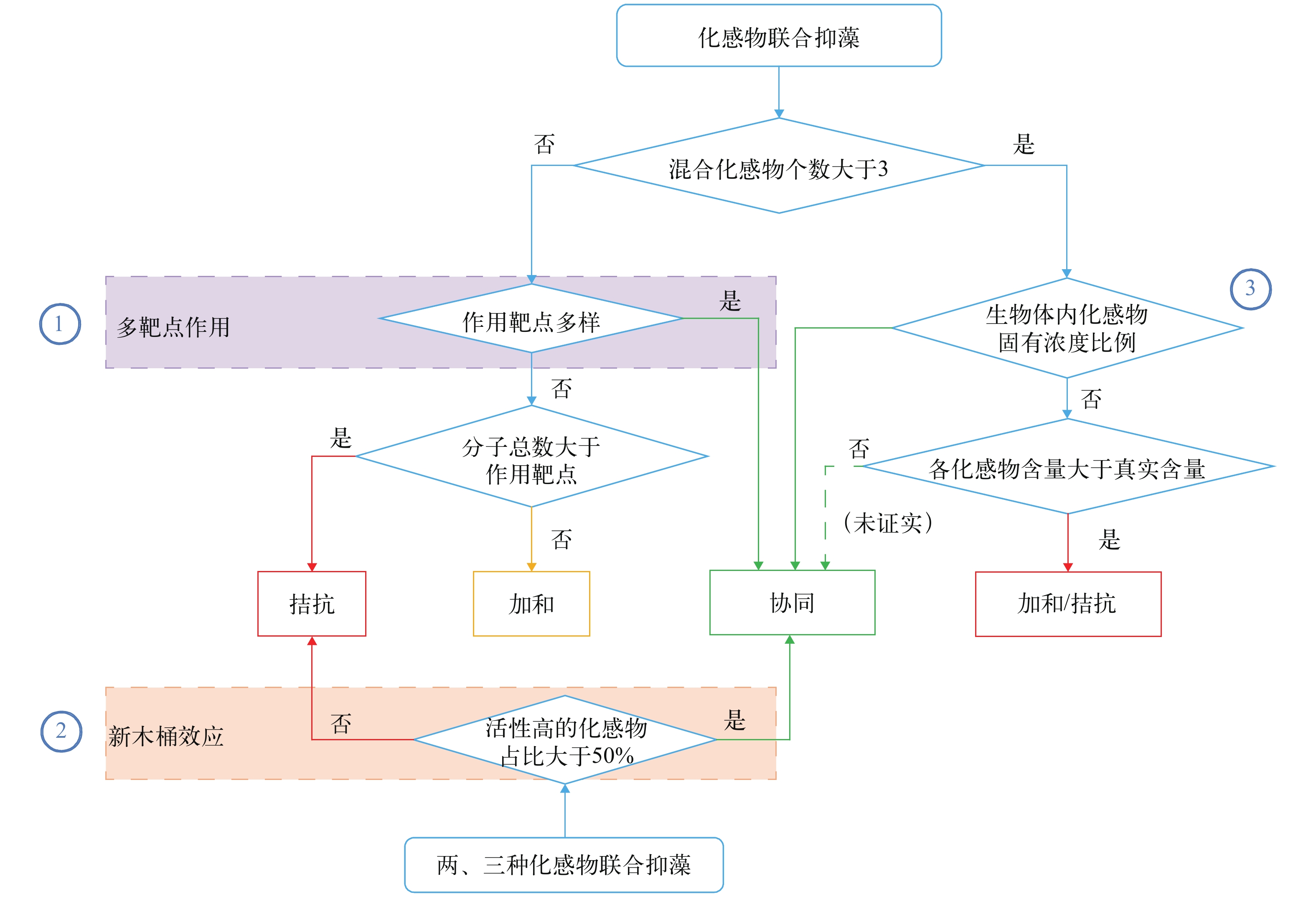
酚类和脂肪酸组合, 以及分别与含氮化合物组成的二、三元化合物较大程度上出现协同作用, “多靶点组合”和“新木桶效应”是产生该作用的主要因素(图 6)。而多元(指四元及以上)混合伴随着化合物含量多于细胞作用靶点的风险, 易出现拮抗作用, 多元混合的化合物种类和含量可参考实际植物分泌的种类与含量, 更易出现协同作用。
化感物质产生的联合作用复杂且繁琐, 受混合化感物质的数量、作用靶点、混合比例和混合物总含量四个因素的影响。不论化感物类型相同与否, 二、三元化合物遵循“多靶点组合”和“新木桶效应”可增加协同效应的可能性, 增强对细胞候选靶点破坏的速度与强度。另外, 混合化感物质的最终浓度也对联合抑藻效应有较大影响, 高的化感物质的终浓度会增加预期抑藻效应, 协同作用的可能性减少, 这与漏斗假说“测定终点为高毒性浓度的混合物比低毒性浓度的混合物的毒性偏离加和毒性的可能性更大”相吻合[84]。多元(指四元及以上)混合可依据植物分泌的化感物质固有种类、含量和比例, 相较于人为等效比例投加更易出现协同作用。
此外, 不同评价方法对联合作用类型的结果会产生一定影响。当前被广泛应用的联合作用评价方法有定性分析法, 如等效线图法[92]和毒性单位法(Toxic unit, TU)[93]等, 以及定量分析法包括相加指数法(Additive index, AI)[94]、半致死剂量指数法[79]、毒性指数法(Toxicity index, TI)[75]、联合效应系数(K)[88]、浓度加和模型(Concentration addition, CA)、独立作用模型(Independent action, IA)及通过实际抑藻效率与预测抑制效率相比较等方法, 在进行联合作用分析时, 采取多种模型分析得出最终联合作用方式更具说服力。
4. 结论
本文详细论述了酚类化合物、含氮化合物、脂肪酸/酯类、萜类化合物及其衍生物四类化感物质对蓝藻水华典型藻种的抑制效应及机制, 并综合经济成本预估其应用潜能。通过分析各类化合物的抑藻活性和机制, 总结同一、不同类型化感物质组合的联合作用规律。具体如下: (1)单一化感物质具有不同的抑藻活性和代表性胁迫作用靶点: 酚类化合物种类繁多、活性普遍较高但也存在差异(EC50为0.05—162.53 mg/L), 可通过抑制光合作用、破坏细胞氧化应激平衡和干扰细胞壁/膜结构等多重机制抑制蓝藻生长, 是当前研究最多的化感物类别。但其高效抑藻酚类的理论耗材成本差异较大, 性价比次于脂肪酸位于第二位; 含氮化合物对蓝藻存在特异性抑制作用且整体抑藻能力较均衡, EC50集中于0.3—8.14 mg/L, 主要通过干扰光合作用过程(尤其是阻断电子转运)、损伤细胞膜/壁结构, 甚至深入蓝藻细胞损伤超微结构而对藻细胞造成严重损伤。但由于自然中含量较少、提取成本较高, 理论耗材成本普遍较高且各化感物成本差异较大, 性价比最低, 难以广泛实际应用; 脂肪酸/酯类成本较低, 且能以较少剂量对蓝藻产生极强毒性, 对蓝藻多样的作用靶点是脂肪酸具有极强抑制效果的关键, 可在0.015—52.95 mg/L浓度范围内将目标蓝藻抑制50%, 性价比最优; 萜类化合物抑制效果弱于其他3个类别的化感物, 主要集中于多途径干扰蓝藻细胞的光合功能, 但EC50高达25.3—228 mg/L, 实际应用也受限。因此, 选取单一化感物质实际抑藻时, 酚类化合物和脂肪酸是优先考虑的物质类别。(2)化感物质组合产生的联合作用受组合中的化感物质的数量、作用靶点、混合比例和混合物总含量四个因素影响。不论化感物类型相同与否, 二、三元化合物遵循“多靶点组合”和“新木桶效应”可增加协同效应的可能性; 多元(指四元及以上)混合可依据植物分泌的化感物质固有种类、含量和比例, 相较于人为等效比例投加更易出现协同作用。
尽管当前化感物质研究进展较为迅速, 但仍存在一些问题亟待解决: (1)当前化感物质抑藻作用研究局限于短期内, 对短期抑藻后蓝藻的恢复情况、长期有效抑藻的研究仍很缺乏, 对化感物质抑藻机制的理解仍不全面不充分, 如何在整个水华暴发期持久稳定防治蓝藻水华并深入剖析其机理成为今后研究热点之一。(2)建立在已综述的化感物联合抑藻规律上, 寻找或合成高效特异性控制优势藻类水华、抑制藻毒素产生和释放的多功能化感物质, 并合理进行化感物组合配比具有重要意义。(3)以抑藻活性较强的化感物作为抑藻剂, 需开发更科学、合理的固定化制备工艺和包埋材料, 如生物炭基吸附剂等, 这有助于化感物释放的同时吸附水体中其他污染物, 实现较高的生态修复效益。(4)当前研究多集中于单一藻种, 而自然水体藻际群落内部各藻种互作可能会影响化感物的抑藻作用, 这要求选择多种典型藻种共培养抑制。抑藻化感物对蓝藻水华产生抑制作用的同时, 对其他水生生物个体和有益种群、群落结构的影响仍不可忽视, 因此直接在水华区域原位抑制或将水华水体取样至人工池等异位抑制实验是化感抑藻应用的关键发展方向。
-
图 1 初始藻浓度-酚类化合物-EC50相互关系的三维散点图(展示EC50小于10 mg/L的化感物质)
YZ投影面的圆点表示忽视初始浓度和处理时间时, 不同化合物对应的EC50值; XZ投影面的三角形表示不同初始浓度下EC50值分布状况; 下同
Figure 1. Three-dimensional scatter plot of the relationship between polyphenolics, initial cell density and EC50 (EC50 less than 10 mg/L are illustrated)
The dots in YZ projection indicates EC50 corresponding to polyphenolics when the initial cell density and time are ignored. The triangle in XZ projection indicates the distribution of EC50 under different initial cell densities; the same applies below
图 2 初始藻浓度-含氮化合物-EC50相互关系的三维散点图(展示EC50小于10 mg/L的化感物质)
YZ投影面的圆点表示忽视初始浓度和处理时间时, 不同化合物对应的EC50值; XZ投影面的三角形表示不同初始浓度下EC50值分布状况; 下同
Figure 2. Three-dimensional scatter plot of the relationship between N-containing allelochemicals, initial cell density and EC50 (EC50 less than 10 mg/L are illustrated)
The dots in YZ projection indicates EC50 corresponding to polyphenolics when the initial cell density and time are ignored. The triangle in XZ projection indicates the distribution of EC50 under different initial cell densities; the same applies below
图 3 初始藻浓度-脂肪酸/酯类-EC50相互关系的三维散点图(展示EC50小于10 mg/L的化感物质)
YZ投影面的圆点表示忽视初始浓度和处理时间时, 不同化合物对应的EC50值; XZ投影面的三角形表示不同初始浓度下EC50值分布状况; 下同
Figure 3. Three-dimensional scatter plot of the relationship between fatty acids/esters, initial cell density and EC50 (EC50 less than 10 mg/L are illustrated)
The dots in YZ projection indicates EC50 corresponding to polyphenolics when the initial cell density and time are ignored. The triangle in XZ projection indicates the distribution of EC50 under different initial cell densities; the same applies below
图 4 初始藻浓度-萜类化合物-EC50相互关系的三维散点图
YZ投影面的圆点表示忽视初始浓度和处理时间时, 不同化合物对应的EC50值; XZ投影面的三角形表示不同初始浓度下EC50值分布状况
Figure 4. Three-dimensional scatter plot of the relationship between terpenoids, initial cell density and EC50
The dots in YZ projection indicates EC50 corresponding to polyphenolics when the initial cell density and time are ignored. The triangle in XZ projection indicates the distribution of EC50 under different initial cell densities
图 5 四种化感物质抑藻活性的提琴图(a)及高效抑藻化感物质(EC50<10 mg/L)理论耗材成本的提琴图(b)
以百万升密度为104—106的单一蓝藻水体达到50%抑制率时各化感物质所耗费的成本为例, 提琴图的宽度、高度分别表示数据的密集度和极差, 蓝线、黑虚线分别为中位数、四分位数所在值
Figure 5. Violin plot of inhibiting capacities of allelochemicals from different categories (a) and Violin plot of the cost of theoretical consumables (b)
A case study of “allelochemicals to inhibit the growth of 50% of cyanobacteria, with initial density is 104 to 106, in a million liters of water” The width and height of the violin plot indicate the density and difference of the data, respectively, of which the blue line and the black dotted line are the median and quartile values, respectively
表 1 按化学结构对抑藻化感物质分类[4]
Table 1 The classification of allelochemicals in terms of their chemical structure[4]
化学结构分类
Chemical structure classification化感物质Allelochemical 酚类化合物及其衍生物
Polyphenolics and deribvatives简单酚 Simple phenols 苯甲酸及其衍生物 Benzoic acid and deribvatives 肉桂酸及其衍生物 Cinnamic acid and derivatives 黄酮类 Flavonoids 单宁 Tannin 香豆素类 Coumarins 醌类Quinones 含氮化合物
N-containing compounds and deribvatives生物碱Alkaloid 苯胺、萘胺Anilines and Naphthylamine 氨基酸Amino acids 脂肪酸及酯类
Aliphatic compounds脂肪酸Fatty acid 酯类Esters 萜类及其衍生物Terpenoids and their derivatives 表 2 相同类型化感物质的联合作用
Table 2 Joint effect of similar allelochemicals on Microcystis aeruginosa growth
化感物质
Allelochemical混合模式
Mixing mode评价方式
Assessment method初始藻浓度
Initial cell density (cells/mL)时间
Time (d)联合作用
Joint effect参考文献Reference 1. 酚类+酚类 (1)邻苯三酚+邻苯二酚 等效浓度比 相加指数法
半致死剂量指数法2×106—
3×1063 协同作用 [79] (2)邻苯二酚+没食子酸 加和作用 (3)邻苯三酚+没食子酸 (4)邻苯三酚+没食子酸 (1﹕4); (2﹕3); (1﹕1);
(3﹕2); (4﹕1)
终浓度为2.5 mg/L毒性指数法
毒性单位法
等效线图法1×106 3 加和作用 [81] (5)邻苯三酚+没食子酸+邻苯二酚 (1﹕1﹕3); (1﹕2﹕2);
(3﹕1﹕1); (1﹕1﹕1);
(2﹕2﹕1); (1﹕3﹕1)1×106 3 加和作用 [81] (6)邻苯三酚+没食子酸+邻苯二酚+鞣花酸 穗状狐尾藻水培液
检测浓度实际测定的结果与
预测抑制结果对比104— 105 3 协同作用 [9] (7)香豆素+对羟基苯甲酸 80%﹕20% EC50
60%﹕40% EC50实际测定的结果与
预测抑制结果对比5.5×105 2、4、6、8、10 协同作用 [83] (8)香豆素+对羟基苯甲酸 20%﹕80% EC50
40%﹕60% EC50拮抗作用 (9)对香豆酸+水杨酸+
苯甲酸终浓度0.01 mg/L 对比生长抑制率 — 8 协同作用 [20] (10)香草酸+肉桂酸 等效浓度比 毒性单位法
相加指数法A650=0.15 — 协同作用 [22] (11)咖啡酸+原儿茶酸 等效浓度比 毒性指数法(TI) 1×106 3 拮抗作用 [87] (12)咖啡酸+原儿茶酸+香草酸 加和作用 (13)咖啡酸+原儿茶酸+香草酸+阿魏酸 (14)咖啡酸+原儿茶酸+香草酸+阿魏酸+苯甲酸+对羟基苯甲酸 2. 脂肪酸+脂肪酸 (1)亚油酸+α-亚麻酸+油酸 0.04 mg/L+0.03 mg/L +0.70 mg/L 实际测定的结果与预测抑制结果对比 (2)2×105 5 协同作用 [57] (2)亚油酸+油酸+辛酸 0.04 mg/L+0.70 mg/L +0.50 mg/L (3)棕榈酸+乳酸 等效浓度比 联合效应系数 105— 106 3 加和作用 [88] 3. 含氮化合物+含氮化合物 (1)环(4羟基脯氨酸-亮氨酸)+环(脯氨酸-亮氨酸) 0.4 mg/L和0.4 mg/L
(单独作用时为
弱杀藻作用)观察生长曲线和单独培养对比 1×107 2 协同作用 [86] (2)血根碱+白屈菜红碱 等效浓度比 毒性指数法 A680=0.09 6 协同作用 [85] 表 3 不同类型化感物质的联合作用
Table 3 Joint effect of dissimilar allelochemicals on Microcystis aeruginosa growth
化感物质
Allelochemical混合模式
Mixing mode评价方式
Assessment method初始藻浓度Initial cell density (cells/mL) 时间
Time (d)联合作用
Joint effect参考文献
Reference1. 酚类+脂肪酸 (1)邻苯二酚+亚油酸 等效浓度比 相加指数法
半致死剂量指数法2×106 — 3×106 3 协同作用 [79] (2)焦棓酸+亚油酸 加和作用 (3)没食子酸+亚油酸 协同、加和作用 (4)原儿茶酸+硬脂酸 20%﹕80% EC50
40%﹕60% EC50实际测定的结果与预测抑制结果对比 5.5×105 2、4、6、8、10 协同作用 [83] (5)原儿茶酸+硬脂酸 80%﹕20% EC50
50%﹕50% EC50
60%﹕40% EC50拮抗作用 (6)肉桂酸+丁二酸 等效浓度比 毒性单位法
相加指数法A650=0.15 — 协同作用 [22] (7)香草酸+丁二酸 (8)肉桂酸+香草酸+丁二酸 (9)苯甲酸+棕榈酸 等效浓度比 联合效应系数 105— 106 3 加和作用 [88] (10)咖啡酸+壬酸 相同浓度比 混合物EC50与个体EC50之和相比 (1)0×106 3 协同作用 [82] 等效浓度比 拮抗作用 2. 脂肪酸+含氮化合物 (1)过氧乙酸+异噻唑啉酮 等效浓度比 协同指数 9×107 4 协同作用 [91] (2)硬脂酸+对氨基苯磺酸 20%﹕80% EC50
40%﹕60% EC50实际测定的结果与预测抑制结果对比 5.5×105 2、4、6、8、10 协同作用 [83] 80%﹕20% EC50
50%﹕50% EC50
60%﹕40% EC50拮抗作用 3. 酚类+含氮化合物 (1)原儿茶酸+对氨基苯磺酸 80%﹕20% EC50
40%﹕60% EC50理论抑藻率与实际抑藻率相比 5.5×105 2、4、6、8、10 协同作用 [83] 50%﹕50% EC50 加和作用 20%﹕80% EC50
40%﹕60% EC50拮抗作用 (2)咖啡酸+ N-苯基-1-萘胺 相同浓度比 混合物EC50与个体EC50之和相比 (1)0×106 3 拮抗作用 [82] 等效浓度比 拮抗作用 4. 酚类+脂肪酸+含氮化合物 (1)原儿茶酸+硬脂酸+对氨基苯磺酸 25%﹕50%﹕25% EC50
20%﹕40%﹕40% EC50理论抑藻率与实际抑藻率相比 5.5×105 2、4、6、8、10 协同作用 [83] 50%﹕25%﹕25% EC50
25%﹕25%﹕50% EC50拮抗作用 33.3%﹕33.3%﹕33.3% EC50 加和作用 40%﹕20%﹕40% EC50
40%﹕40%﹕20% EC504天前拮抗作用, 4天后协同作用 (2)香豆素+对氨基苯甲酸+硬脂酸+对氨基苯磺酸 (80%+20%)﹕(80%+20%) EC50
(80%+20%)﹕(20%+80%) EC50
(50%+50%)﹕(50%+50%) EC50
(60%+40%)﹕(60%+40%) EC50
(60%+40%)﹕(40%+60%)
EC50拮抗作用 (3)香豆素+对氨基苯甲酸+邻苯二酚+硬脂酸+对氨基苯磺酸 (80%+20%)﹕(25%+50%+
25%)EC50
(80%+20%)﹕(20%+40%+
40%)EC50
(40%+60%)﹕(25%+50%+
25%)EC50
(40%+60%)﹕(20%+40%+
40%)EC50理论抑藻率与实际抑藻率相比 拮抗作用 (4)咖啡酸+壬酸+N-苯基-1-萘胺 相同浓度比
等效浓度比混合物EC50与个体EC50之和相比 (1)0×106 3 协同作用 [82] -
[1] Huisman J, Codd G A, Paerl H W, et al. Cyanobacterial blooms [J]. Nature Reviews Microbiology, 2018, 16(8): 471-483. doi: 10.1038/s41579-018-0040-1
[2] Kibuye F A, Zamyadi A, Wert E C. A critical review on operation and performance of source water control strategies for cyanobacterial blooms: part Ⅱ-mechanical and biological control methods [J]. Harmful Algae, 2021(109): 102119.
[3] Kibuye F A, Zamyadi A, Wert E C. A critical review on operation and performance of source water control strategies for cyanobacterial blooms: part I-chemical control methods [J]. Harmful Algae, 2021(109): 102099.
[4] Zhu X Q, Dao G H, Tao Y, et al. A review on control of harmful algal blooms by plant-derived allelochemicals [J]. Journal of Hazardous Materials, 2021(401): 123403.
[5] Ni L X, Wu H Q, Du C H, et al. Effects of allelochemical artemisinin in Artemisia annua on Microcystis aeruginosa: growth, death mode, and microcystin-LR changes [J]. Environmental Science and Pollution Research, 2021, 28(33): 45253-45265. doi: 10.1007/s11356-021-13793-x
[6] Ozaki K, Ohta A, Iwata C, et al. Lysis of cyanobacteria with volatile organic compounds [J]. Chemosphere, 2008, 71(8): 1531-1538. doi: 10.1016/j.chemosphere.2007.11.052
[7] Molisch H. Der einfluss einer pflanze auf die andere, allelopathie [J]. Nature, 1938, 141(3568): 493. doi: 10.1038/141493a0
[8] Nakai S, Inoue Y, Hosomi M. Algal growth inhibition effects and inducement modes by plant-producing phenols [J]. Water Research, 2001, 35(7): 1855-1859. doi: 10.1016/S0043-1354(00)00444-9
[9] Zhu J Y, Liu B Y, Wang J, et al. Study on the mechanism of allelopathic influence on cyanobacteria and chlorophytes by submerged macrophyte (Myriophyllum spicatum) and its secretion [J]. Aquatic Toxicology, 2010, 98(2): 196-203. doi: 10.1016/j.aquatox.2010.02.011
[10] Zhang S H, Zhang S Y, Li G. Acorus calamus root extracts to control harmful cyanobacteria blooms [J]. Ecological Engineering, 2016(94): 95-101.
[11] Qian Y P, Xu N, Liu J, et al. Inhibitory effects of Pontederia cordata on the growth of Microcystis aeruginosa [J]. Water Science and Technology, 2017(1): 99-107.
[12] Sütfeld R, Petereit F, Nahrstedt A. Resorcinol in exudates of Nuphar lutea [J]. Journal of Chemical Ecology, 1996, 22(12): 2221-2231. doi: 10.1007/BF02029542
[13] 倪利晓, 陈世金, 任高翔, 等. 陆生植物化感作用的抑藻研究进展 [J]. 生态环境学报, 2011, 20(Z1): 1176-1182. doi: 10.3969/j.issn.1674-5906.2011.06.033 Ni L X, Chen S J, Ren G X, et al. Advance research on the allelopathy of terrestrial plants in inhibition of algae [J]. Ecology and Environmental Sciences, 2011, 20(Z1): 1176-1182. doi: 10.3969/j.issn.1674-5906.2011.06.033
[14] 周丽, 付子轼, 陈桂发, 等. 陆生植物化感抑制铜绿微囊藻作用效应及机制研究进展 [J]. 应用生态学报, 2018, 29(5): 1715-1724. Zhou L, Fu Z S, Chen G F, et al. Research advance in allelopathy effect and mechanism of terrestrial plants in inhibition of Microcystis aeruginosa [J]. Chinese Journal of Applied Ecology, 2018, 29(5): 1715-1724.
[15] Park M H, Hwang S J, Ahn C Y, et al. Screening of seventeen oak extracts for the growth inhibition of the cyanobacterium Microcystis aeruginosa Kütz em. Elenkin [J]. Bulletin of Environmental Contamination and Toxicology, 2006, 77(1): 9-14. doi: 10.1007/s00128-006-1025-8
[16] 张树林. 中草药对铜绿微囊藻的抑制作用及机理研究 [D]. 青岛: 中国海洋大学, 2011: 28-29. Zhang S L. Inhibitory effect of Chinese herb on Microcystic aeruginosa and its mechanism [D]. Qingdao: Ocean University of China, 2011: 28-29.
[17] Li B H, Yin Y J, Kang L F, et al. A review: application of allelochemicals in water ecological restoration-algal inhibition [J]. Chemosphere, 2021(267): 128869.
[18] Weidenhamer J D, Macias F A, Fischer N H, et al. Just how insoluble are monoterpenes [J]? Journal of Chemical Ecology, 1993, 19(8): 1799-1807. doi: 10.1007/BF00982309
[19] 张学文, 刘亦学, 刘万学, 等. 植物化感物质及其释放途径 [J]. 中国农学通报, 2007, 23(7): 295-297. doi: 10.3969/j.issn.1000-6850.2007.07.068 Zhang X W, Liu Y X, Liu W X, et al. Allelochemicals and its releasing modes [J]. Chinese Agricultural Science Bulletin, 2007, 23(7): 295-297. doi: 10.3969/j.issn.1000-6850.2007.07.068
[20] Park M H, Han M S, Ahn C Y, et al. Growth inhibition of bloom-forming cyanobacterium Microcystis aeruginosa by rice straw extract [J]. Letters in Applied Microbiology, 2006, 43(3): 307-312. doi: 10.1111/j.1472-765X.2006.01951.x
[21] 郭亚丽, 傅海燕, 黄国和, 等. 阿魏酸和香豆素对铜绿微囊藻的化感作用 [J]. 环境科学, 2013, 34(4): 1492-1497. Guo Y L, Fu H Y, Huang G H, et al. Allelopathy effects of ferulic acid and coumarin on Microcystis aeruginosa [J]. Environmental Science, 2013, 34(4): 1492-1497.
[22] 赵楚, 钱燕萍, 田如男. 梭鱼草化感物质丁二酸、肉桂酸及香草酸对铜绿微囊藻生长的抑制效应 [J]. 浙江农林大学学报, 2020, 37(6): 1105-1111. doi: 10.11833/j.issn.2095-0756.20190722 Zhao C, Qian Y P, Tian R N. Inhibitory effect of succinic acid, cinnamic acid and vanillic acid from Pontederia cordata on Microcystis aeruginosa [J]. Journal of Zhejiang A & F University, 2020, 37(6): 1105-1111. doi: 10.11833/j.issn.2095-0756.20190722
[23] Wang R, Hua M, Yu Y, et al. Evaluating the effects of allelochemical ferulic acid on Microcystis aeruginosa by pulse-amplitude-modulated (PAM) fluorometry and flow cytometry [J]. Chemosphere, 2016(147): 264-271.
[24] Wang H Q, Wu Z B, Zhang S H, et al. Relationship between the allelopathic activity and molecular structure of hydroxyl derivatives of benzoic acid and their effects on cyanobacterium Microcystis aeruginosa [J]. Allelopathy Journal, 2008, 22(1): 205-211.
[25] Gao Y N, Fu Q, Lu J, et al. Enhanced pyrogallol toxicity to cyanobacterium Microcystis aeruginosa with increasing alkalinity [J]. Journal of Applied Phycology, 2020, 32(3): 1827-1835. doi: 10.1007/s10811-020-02096-2
[26] Huang H M, Xiao X, Ghadouani A, et al. Effects of natural flavonoids on photosynthetic activity and cell integrity in Microcystis aeruginosa [J]. Toxins, 2015, 7(1): 66-80. doi: 10.3390/toxins7010066
[27] Pillinger J M, Cooper J A, Ridge I. Role of phenolic compounds in the antialgal activity of barley straw [J]. Journal of Chemical Ecology, 1994, 20(7): 1557-1569. doi: 10.1007/BF02059880
[28] Megharaj M, Venkateswarlu K, Naidu R. Effects of carbaryl and 1-naphthol on soil population of cyanobacteria and microalgae and select cultures of diazotrophic cyanobacteria [J]. Bulletin of Environmental Contamination and Toxicology, 2011, 87(3): 324-329. doi: 10.1007/s00128-011-0347-3
[29] Dziga D, Suda M, Bialczyk J, et al. The alteration of Microcystis aeruginosa biomass and dissolved-microcystin-LR concentration following exposure to plant-producing phenols [J]. Environmental Toxicology, 2007, 22(4): 341-346. doi: 10.1002/tox.20276
[30] Ni L X, Acharya K, Hao X Y, et al. Antioxidant and metabolism responses to polyphenol stress in cyanobacterium Microcystis aeruginosa [J]. Journal of Environmental Science and Health Part B, Pesticides, Food Contaminants, and Agricultural Wastes, 2013, 48(2): 153-161.
[31] Wang J, Liu Q, Feng J, et al. Photosynthesis inhibition of pyrogallol against the bloom-forming cyanobacterium Microcystis aeruginosa TY001 [J]. Polish Journal of Environmental Studies, 2016, 25(6): 2601-2608. doi: 10.15244/pjoes/63412
[32] 田敏, 饶龙兵, 李纪元. 植物细胞中的活性氧及其生理作用 [J]. 植物生理学通讯, 2005, 41(2): 235-241. Tian M, Rao L B, Li J Y. Reactive oxygen species (ROS) and its physiological functions in plant cells [J]. Plant Physiology Communications, 2005, 41(2): 235-241.
[33] Li J M, Cao L R, Guo Z H, et al. Time- and dose-dependent allelopathic effects and mechanisms of kaempferol on toxigenic Microcystis growth [J]. Ecotoxicology and Environmental Safety, 2021(222): 112508.
[34] Li J M, Hu J Q, Cao L R, et al. Growth, physiological responses and microcystin-production/-release dynamics of Microcystis aeruginosa exposed to various luteolin doses [J]. Ecotoxicology and Environmental Safety, 2020(196): 110540.
[35] Żyszka B, Anioł M, Lipok J. Modulation of the growth and metabolic response of cyanobacteria by the multifaceted activity of naringenin [J]. PLoS One, 2017, 12(5): e0177631. doi: 10.1371/journal.pone.0177631
[36] Tohme R, Darwiche N, Gali-Muhtasib H. A journey under the sea: the quest for marine anti-cancer alkaloids [J]. Molecules (Basel, Switzerland)
, 2011, 16(11): 9665-9696. doi: 10.3390/molecules16119665 [37] Jančula D, Suchomelová J, Gregor J, et al. Effects of aqueous extracts from five species of the family Papaveraceae on selected aquatic organisms [J]. Environmental Toxicology, 2007, 22(5): 480-486. doi: 10.1002/tox.20290
[38] Jančula D, GregorováJ, Marsalek Maršálek B. Algicidal and cyanocidal effects of selected isoquinoline alkaloids [J]. Aquaculture Research, 2010, 41(4): 598-601. doi: 10.1111/j.1365-2109.2009.02342.x
[39] Liu L, Zhang S L, Dai W, et al. Comparing effects of berberine on the growth and photosynthetic activities of Microcystis aeruginosa and Chlorella pyrenoidosa [J]. Water Science and Technology, 2019, 80(6): 1155-1162. doi: 10.2166/wst.2019.357
[40] Zhang S L, Dai W, Bi X D, et al. Effect of environmental factors on allelopathic inhibition of Microcystis aeruginosa by berberine [J]. Water Science and Technology, 2013, 68(2): 419-424. doi: 10.2166/wst.2013.243
[41] Bi X D, Dai W, Zhang S L et al. Inhibition of photosynthesis-related gene expression by berberine in Microcystis aeruginosa [J]. Allelopathy Journal, 2014, 34(2): 335-343.
[42] Shao J H, Liu D M, Gong D X, et al. Inhibitory effects of sanguinarine against the cyanobacterium Microcystis aeruginosa NIES-843 and possible mechanisms of action [J]. Aquatic Toxicology, 2013(142/143): 257-263.
[43] 刘彦彦, 邵继海, 刘德明, 等. 白屈菜红碱对铜绿微囊藻生长和光合系统的影响 [J]. 水生生物学报, 2015, 39(1): 149-154. doi: 10.7541/2015.19 Liu Y Y, Shao J H, Liu D M, et al. Effect of chelerythrine on the growth and photosynthetic system of Microcystis aeruginosa [J]. Acta Hydrobiologica Sinica, 2015, 39(1): 149-154. doi: 10.7541/2015.19
[44] Bi X D, Zhang S L, Zhang B, et al. Effects of berberine on the photosynthetic pigments compositions and ultrastructure of cyanobacterium Microcystis aeruginosa [J]. Advanced Materials Research, 2011(343/344): 1117-1125.
[45] Qian H F, Li J J, Pan X J, et al. Effects of streptomycin on growth of algae Chlorella vulgaris and Microcystis aeruginosa [J]. Environmental Toxicology, 2012, 27(4): 229-237. doi: 10.1002/tox.20636
[46] Foguel D, Chaloub R M. Effects of the alkaloid gramine on the light-harvesting, energy-transfer, and growth of Anabaena sp. (PCC-7119) [J]. Plant Physiology, 1993, 101(2): 633-639. doi: 10.1104/pp.101.2.633
[47] Gantar M, Berry J P, Thomas S, et al. Allelopathic activity among cyanobacteria and microalgae isolated from Florida freshwater habitats [J]. FEMS Microbiology Ecology, 2008, 64(1): 55-64. doi: 10.1111/j.1574-6941.2008.00439.x
[48] Churro C, Fernandes A S, Alverca E, et al. Effects of tryptamine on growth, ultrastructure, and oxidetive stress of cyanobacteria and microalgae cultures [J]. Hydrobiologia, 2010, 649(1): 195-206. doi: 10.1007/s10750-010-0245-4
[49] Hehmann A, Kaya K, Watanabe M M. Selective control of Microcystis using an amino acid - A laboratory assay [J]. Journal of Applied Phycology, 2002, 14(2): 85-89. doi: 10.1023/A:1019546829940
[50] Yamamoto Y, Kouchiwa T, Hodoki Y, et al. Distribution and identification of actinomycetes lysing cyanobacteria in a eutrophic lake [J]. Journal of Applied Phycology, 1998, 10(4): 391-397. doi: 10.1023/A:1008077414808
[51] Zhang B H, Chen W, Li H Q, et al. L-valine, an antialgal amino acid from Streptomyces jiujiangensis JXJ 0074T [J]. Applied Microbiology and Biotechnology, 2016, 100(10): 4627-4636. doi: 10.1007/s00253-015-7150-8
[52] Cerniglia C E, Freeman J P, Van Baalen C. Biotransformation and toxicity of aniline and aniline derivatives in cyanobacteria [J]. Archives of Microbiology, 1981, 130(4): 272-275. doi: 10.1007/BF00425939
[53] Batterton J, Winters K, Van Baalen C. Anilines: selective toxicity to blue-green algae [J]. Science, 1978, 199(4333): 1068-1070. doi: 10.1126/science.415361
[54] Mizuno C S, Schrader K K, Rimando A M. Algicidal activity of stilbene analogues [J]. Journal of Agricultural and Food Chemistry, 2008, 56(19): 9140-9145. doi: 10.1021/jf801988p
[55] Gao Y N, Ge F J, Zhang L P, et al. Enhanced toxicity to the cyanobacterium Microcystis aeruginosa by low-dosage repeated exposure to the allelochemical N-phenyl-1-naphthylamine [J]. Chemosphere, 2017(174): 732-738.
[56] Cheng L, He Y, Tian Y, et al. Comparative biotoxicity of N-phenyl-1-naphthylamine and N-phenyl-2-naphthylamine on cyanobacteria Microcystis aeruginosa [J]. Chemosphere, 2017(176): 183-191.
[57] 张庭廷, 郑春艳, 何梅, 等. 脂肪酸类物质的抑藻效应及其构效关系 [J]. 中国环境科学, 2009, 29(3): 274-279. doi: 10.3321/j.issn:1000-6923.2009.03.009 Zhang T T, Zheng C Y, He M, et al. Inhibition on algae of fatty acids and the structure-effect relationship [J]. China Environmental Science, 2009, 29(3): 274-279. doi: 10.3321/j.issn:1000-6923.2009.03.009
[58] Li F M, Hu H Y. Isolation and characterization of a novel antialgal allelochemical from Phragmites communis [J]. Applied and Environmental Microbiology, 2005, 71(11): 6545-6553. doi: 10.1128/AEM.71.11.6545-6553.2005
[59] 胡陈艳, 葛芳杰, 张胜花, 等. 马来眼子菜体内抑藻物质分离及常见脂肪酸抑藻效应 [J]. 湖泊科学, 2010, 22(4): 569-576. Hu C Y, Ge F J, Zhang S H, et al. Isolation of antialgal compounds from Potamogeton malaianus and algal inhibitory effects of common fatty acids [J]. Journal of Lake Sciences, 2010, 22(4): 569-576.
[60] Huang H M, Xiao X, Shi J Y, et al. Structure-activity analysis of harmful algae inhibition by congeneric compounds: case studies of fatty acids and thiazolidinediones [J]. Environmental Science and Pollution Research, 2014, 21(11): 7154-7164. doi: 10.1007/s11356-014-2626-0
[61] Shao J H, Wu X Q, Li R H, et al. Physiological responses of Microcystis aeruginosa PCC7806 to nonanoic acid stress [J]. Environmental Toxicology, 2009, 24(6): 610-617. doi: 10.1002/tox.20462
[62] Nakai S, Inoue Y, Hosomi M, et al. Myriophyllum spicatum-released allelopathic polyphenols inhibiting growth of blue-green algae Microcystis aeruginosa [J]. Water Research, 2000, 34(11): 3026-3032. doi: 10.1016/S0043-1354(00)00039-7
[63] Ni L X, Rong S Y, Gu G X, et al. Inhibitory effect and mechanism of linoleic acid sustained-release microspheres on Microcystis aeruginosa at different growth phases [J]. Chemosphere, 2018(212): 654-661.
[64] Pichersky E, Raguso R A. Why do plants produce so many terpenoid compounds [J]? New Phytologist, 2018, 220(3): 692-702. doi: 10.1111/nph.14178
[65] 徐士超, 董欢欢, 曾小静, 等. 萜类植物源农药的筛选及活性研究进展 [J]. 林产化学与工业, 2019, 39(1): 1-12. doi: 10.3969/j.issn.0253-2417.2019.01.001 Xu S C, Dong H H, Zeng X J, et al. Research progress in screening and bioactivity of terpenoid botanical pesticides [J]. Chemistry and Industry of Forest Products, 2019, 39(1): 1-12. doi: 10.3969/j.issn.0253-2417.2019.01.001
[66] Wu Y H, Liu J T, Yang L Z, et al. Allelopathic control of cyanobacterial blooms by periphyton biofilms [J]. Environmental Microbiology, 2011, 13(3): 604-615. doi: 10.1111/j.1462-2920.2010.02363.x
[67] Wang H Q, Zhu H J, Zhang L Y, et al. Identification of antialgal compounds from the aquatic plant Elodea nuttallii [J]. Allelopathy Journal, 2014, 34(2): 207-213.
[68] Xian Q M, Chen H D, Liu H L, et al. Isolation and identification of antialgal compounds from the leaves of Vallisneria spiralis L. by activity-guided fractionation [J]. Environmental Science and Pollution Research International, 2006, 13(4): 233-237. doi: 10.1065/espr2006.06.314
[69] Chen S L, Zheng T F, Ye C L, et al. Algicidal properties of extracts from Cinnamomum camphora fresh leaves and their main compounds [J]. Ecotoxicology and Environmental Safety, 2018, 163(15): 594-603.
[70] Ni L X, Acharya K, Hao X Y, et al. Effects of artemisinin on photosystem Ⅱ performance of Microcystis aeruginosa by in vivo chlorophyll fluorescence [J]. Bulletin of Environmental Contamination and Toxicology, 2012, 89(6): 1165-1169. doi: 10.1007/s00128-012-0843-0
[71] 朱小琴, 刀国华, 陶益, 等. 典型植物化感物质对铜绿微囊藻生长的抑制效果评价 [J]. 中国环境科学, 2020, 40(5): 2230-2237. doi: 10.3969/j.issn.1000-6923.2020.05.045 Zhu X Q, Dao G H, Tao Y, et al. Evaluation of growth inhibition of typical plant-derived allelochemicals on Microcystis aeruginosa [J]. China Environmental Science, 2020, 40(5): 2230-2237. doi: 10.3969/j.issn.1000-6923.2020.05.045
[72] Hilt (nee Körner) S, Ghobrial M G N, Gross E M. In situ allelopathic potential of Myriophyllum verticillatum (Haloragaceae) against selected phytoplankton species [J]. Journal of Phycology, 2006, 42(6): 1189-1198. doi: 10.1111/j.1529-8817.2006.00286.x
[73] 高云霓, 董静, 何燕, 等. 基于化感物质释放特性的沉水植物抑藻作用模式研究进展 [J]. 水生生物学报, 2016, 40(6): 1287-1294. doi: 10.7541/2016.167 Gao Y N, Dong J, Yan H E, et al. Research advances on the modes of action for allelopathic algal inhibition by submerged macrophytes based on the release characteristics of allelochemicals [J]. Acta Hydrobiologica Sinica, 2016, 40(6): 1287-1294. doi: 10.7541/2016.167
[74] 蔡宏道. 中国医学百科全书 (环境卫生学) [M]. 上海: 上海科学技术出版社, 1987. Cai H D. Encyclopedia of Chinese Medicine (Environmental Hygiene) [M]. Shanghai: Shanghai Scientific & Technical Publishers, 1987.
[75] 庄路儿. 含氮化合物联合胁迫下对球形棕囊藻抑藻机制的初探 [D]. 广州: 暨南大学, 2018: 8-37. Zhuang L E. A preliminary study of algal inhibition mechannism on Phaeocystis globosa under combined nitrogen-containing compounds [D]. Guangzhou: Jinan University, 2018: 8-37.
[76] Inderjit, Streibig J C, Olofsdotter M, et al. Joint action of phenolic acid mixtures and its significance in allelopathy research [J]. Physiologia Plantarum, 2002, 114(3): 422-428. doi: 10.1034/j.1399-3054.2002.1140312.x
[77] Lyu S W, Blum U, Gerig T M, et al. Effects of mixtures of phenolic acids on phosphorus uptake by cucumber seedlings [J]. Journal of Chemical Ecology, 1990, 16(8): 2559-2567. doi: 10.1007/BF01017478
[78] 祁茜, 辛建攀, 李文明, 等. 化感效应及其对藻类光合作用影响的研究进展 [J]. 环境科学与技术, 2019, 42(4): 43-52. Qi X, Xin J P, Li W M, et al. Research advance on allelopathy and its inhibitory effects of algae photosynthetics [J]. Environmental Science & Technology, 2019, 42(4): 43-52.
[79] 倪利晓, 任高翔, 陈世金, 等. 酚酸和不饱和脂肪酸对铜绿微囊藻的联合作用 [J]. 环境化学, 2011, 30(8): 1428-1432. Ni L X, Ren G X, Chen S J, et al. Study on joint action of phenolic acids and unsaturated fatty acids to Microcystis aeruginosa [J]. Environmental Chemistry, 2011, 30(8): 1428-1432.
[80] 胡利静, 童桂香, 黄光华, 等. 水杨酸对铜绿微囊藻的化感抑制作用 [J]. 南方农业学报, 2017, 48(1): 169-173. doi: 10.3969/j:issn.2095-1191.2017.01.169 Hu L J, Tong G X, Huang G H, et al. Allelopathy inhibition of salicylic acid on Microcystis aeruginosa [J]. Journal of Southern Agriculture, 2017, 48(1): 169-173. doi: 10.3969/j:issn.2095-1191.2017.01.169
[81] Huang S Z, Zhu J Y, Zhang L, et al. Combined effects of allelopathic polyphenols on Microcystis aeruginosa and response of different chlorophyll fluorescence parameters [J]. Frontiers in Microbiology, 2020(11): 614570.
[82] Gao Y N, Liu B Y, Ge F J, et al. Joint effects of allelochemical nonanoic acid, N-phenyl-1-naphtylamine and caffeic acid on the growth of Microcystis aeruginosa [J]. Allelopathy Journal, 2015, 35(2): 249-257.
[83] Zuo S P, Zhou S B, Ye L T, et al. Synergistic and antagonistic interactions among five allelochemicals with antialgal effects on bloom-forming Microcystis aeruginosa [J]. Ecological Engineering, 2016(97): 486-492.
[84] Warne M S J, Hawker D W. The number of components in a mixture determines whether synergistic and antagonistic or additive toxicity predominate: the funnel hypothesis [J]. Ecotoxicology and Environmental Safety, 1995, 31(1): 23-28. doi: 10.1006/eesa.1995.1039
[85] 刘彦彦. 两种异喹啉类生物碱对铜绿微囊藻和蛋白核小球藻生长抑制效应及抑藻机理探究 [D]. 长沙: 湖南农业大学, 2015: 52-62. Liu Y Y. The growth inhibitory effect and algicidal mechanism research of two isoquinoline alkaloids on Microcystis aeruginosa and Chlorella pyrenoidosa [D]. Changsha: Hunan Agricultural University, 2015: 52-62.
[86] Guo X L, Liu X L, Pan J L, et al. Synergistic algicidal effect and mechanism of two diketopiperazines produced by Chryseobacterium sp. strain GLY-1106 on the harmful bloom-forming Microcystis aeruginosa [J]. Scientific Reports, 2015(5): 14720.
[87] 高云霓, 刘碧云, 王静, 等. 苦草(Vallisneria spiralis)释放的酚酸类物质对铜绿微囊藻(Microcystis aeruginosa)的化感作用 [J]. 湖泊科学, 2011, 23(5): 761-766. doi: 10.18307/2011.0514 Gao Y N, Liu B Y, Wang J, et al. Allelopathic effects of phenolic compounds released by Vallisneria spiralis on Microcystis aeruginosa [J]. Journal of Lake Sciences, 2011, 23(5): 761-766. doi: 10.18307/2011.0514
[88] Wang H Q, Cheng S P, Zhang S H, et al. Chemical composition in aqueous extracts of Potamogeton malaianus and Potamogeton maackianus and their allelopathic effects on Microcystis aeruginosa [J]. Polish Journal of Environmental Studies, 2010, 19(1): 213-218.
[89] Macías F A, Galindo J L G, García-Díaz M D, et al. Allelopathic agents from aquatic ecosystems: potential biopesticides models [J]. Phytochemistry Reviews, 2008, 7(1): 155-178.
[90] Nakai S, Zou G, Okuda T, et al. Polyphenols and fatty acids responsible for anti-cyanobacterial allelopathic effects of submerged macrophyte Myriophyllum spicatum [J]. Water Science and Technology, 2012, 66(5): 993-999. doi: 10.2166/wst.2012.272
[91] 郑串. 过氧乙酸和异噻唑啉酮对养殖水体有害藻华的联合抑制效果及应用研究 [D]. 上海: 上海海洋大学, 2018: 20-30. Zheng C. Study on the combined inhibition effects and application of peracetic acid and isothiazolone on harmful algal bloom in aquaculture water [D]. Shanghai: Shanghai Ocean University, 2018: 20-30.
[92] Boillot C, Perrodin Y. Joint-action ecotoxicity of binary mixtures of glutaraldehyde and surfactants used in hospitals: use of the Toxicity Index model and isoblogram representation [J]. Ecotoxicology and Environmental Safety, 2008, 71(1): 252-259. doi: 10.1016/j.ecoenv.2007.08.010
[93] Sprague J B. Measurement of pollutant toxicity to fish. Ⅱ. Utilizing and applying bioassay results [J]. Water Research, 1970, 4(1): 3-32. doi: 10.1016/0043-1354(70)90018-7
[94] 张朝, 竺乃恺, 夏希娟, 等. 1-硝基芘与苯衍生物共存对斜生栅藻的联合毒性 [J]. 环境化学, 1999, 18(1): 87-91. Zhang Z, Zhu N K, Xia X J, et al. Associated effects of 1-nitropyrene and concomitant benzene derviatives on Scenedesmus oblipuus Kütz [J]. Environmental Chemistry, 1999, 18(1): 87-91.
-
期刊类型引用(5)
1. 张梅,牛敏敏,杨兴丽,江润海,温绍福,朱城强,靳松,侯秀丽,常学秀. 不同种植密度苦草与铜绿微囊藻的交互作用. 环境科学与技术. 2024(01): 22-34 .  百度学术
百度学术
2. 陈锋,陈俊鹏,黄小威. 控藻剂与小球藻联合控制蓝藻水华效果研究. 环境科技. 2024(03): 30-34 .  百度学术
百度学术
3. 朱玲,魏天兴,于欢,王仙,范德卉,赵雨琪. 刺槐根系和根际土对7种乔灌草植物的化感潜力. 生态环境学报. 2024(09): 1406-1415 .  百度学术
百度学术
4. 江雨萌,张稳乐,罗朝晖,李辉信,陈丹. 萜类物质抑藻效应及富萜植物共培养抑藻研究. 中国环境科学. 2024(10): 5788-5800 .  百度学术
百度学术
5. 邢春玉,李世栋,谯旭. 化感物质联合作用对铜绿微囊藻的抑制研究. 环境科学与技术. 2024(S2): 139-146 .  百度学术
百度学术
其他类型引用(4)



 下载:
下载: