COMPARATIVE OF PHOTOSYNTHESIS OF DIFFERENT CHLAMYDOMONAS REINHARDTII IN RESPONSE TO MERCURY STRESS
-
摘要:
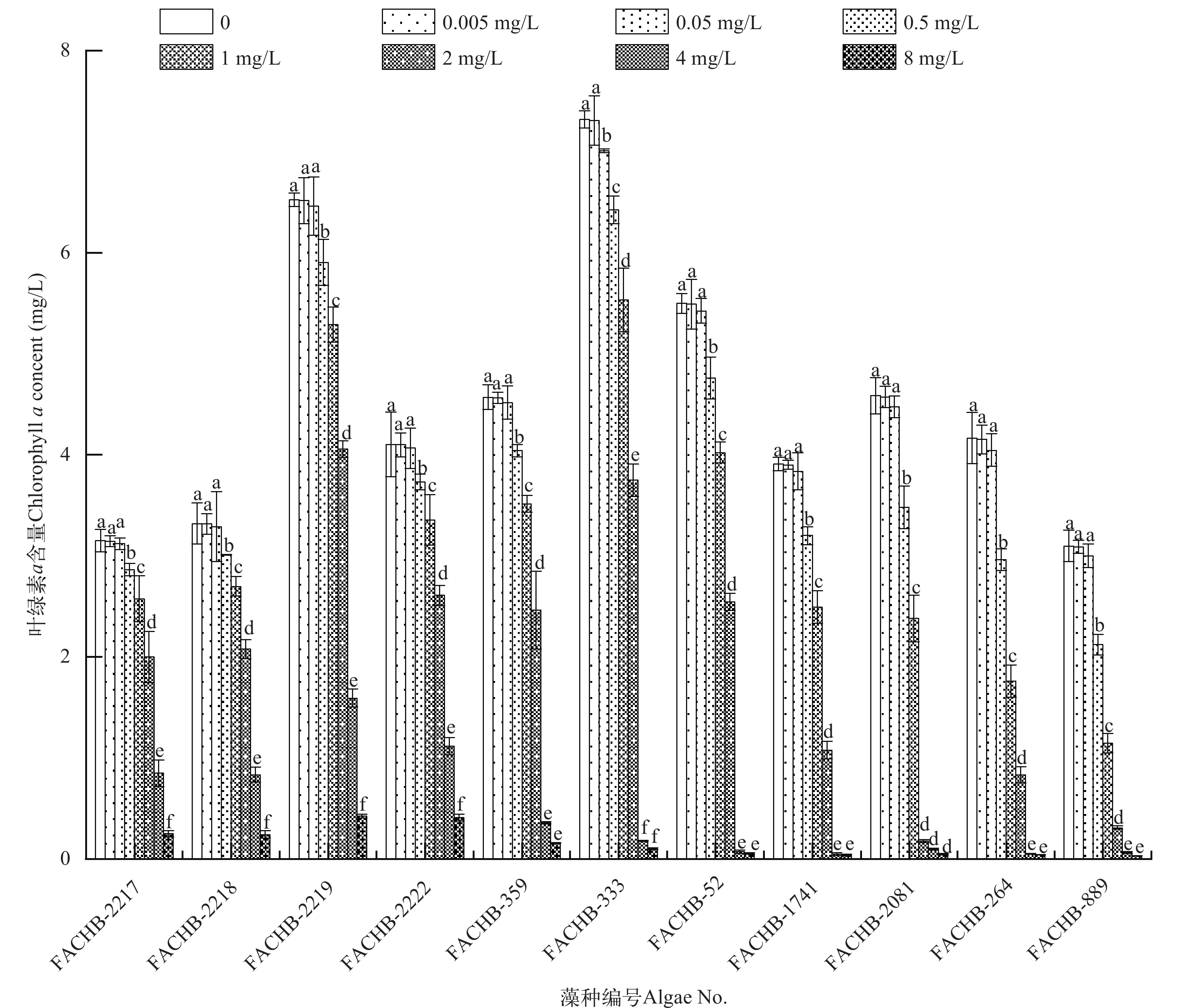
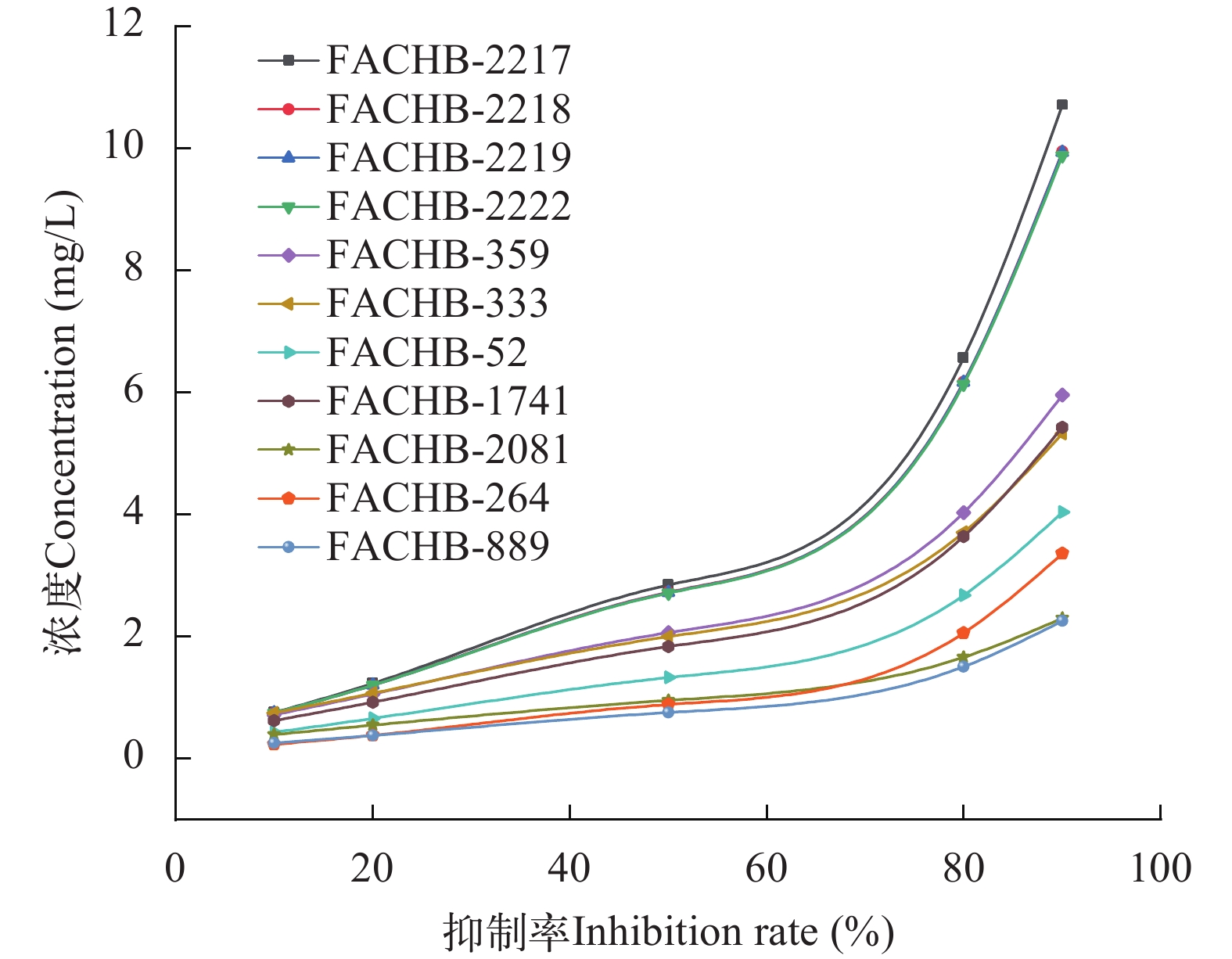
为筛选耐受汞胁迫的衣藻(Chlamydomonas reinhardtii)藻株, 研究不同衣藻光合作用过程响应汞胁迫的差异, 比较了不同汞浓度下11株衣藻的生长、叶绿素a含量及叶绿素荧光活性。结果表明, 随着汞离子浓度升高, 叶绿素a含量显著下降且生长受抑制, 叶绿素荧光活性参数Wk、Vj和Mo快速增加, ψo和φEo快速下降, 表明光合系统Ⅱ (PSⅡ)反应中心的供体侧和受体侧的电子传递受阻, 光合活性被抑制。在11株衣藻中, 衣藻FACHB-889 (EC50为0.762 mg/L)对汞耐受能力最弱, 衣藻FACHB-2217对汞耐受能力最强(EC50为2.848 mg/L)。与对照相比, 在低浓度汞(<0.5 mg/L)胁迫下, 衣藻FACHB-889 PSⅡ活性显著降低(P<0.05), 衣藻FACHB-2217光合系统Ⅱ (PSⅡ)活性无显著差异。在高浓度汞(>1.0 mg/L)胁迫下, 衣藻FACHB-889光合活性受抑制, 单位面积活性反应中心数量(RC/CSo)显著下降(P<0.05), 单位活性反应中心吸收的能量(ABS/RC)持续增加, 单位反应中心耗散的能量(DIo/RC)和单位反应中心捕获的用于电子传递的能量(ETo/RC)呈下降趋势, 表明吸收的能量不能被光合作用有效利用, 且无法通过热耗散释放, 导致能量的非正常积累, 使细胞失活甚至死亡; 衣藻FACHB-2217单位活性反应中心吸收的能量(ABS/RC)、用于还原QA的能量 (TRo/RC)及用于电子传递的能量(ETo/RC)均显著升高, 细胞通过有活性的单位反应中心光合能力的增强, 有效转化吸收的能量, 消除部分反应中心失活的负面影响。研究表明, 光合活性及其能量分配的差异是衣藻对汞敏感/耐受的重要原因。
Abstract:Algal growth and photosynthesis are susceptible to Hg stress. To screen for Hg-tolerant Chlamydomonas reinhardtii strains, the growth, chlorophyll a content, and chlorophyll fluorescence activity of 11 Chlamydomonas reinhardtii strains were compared at different Hg concentrations. The results showed a significant decrease in chlorophyll a content d and inhibited growth as mercury ion concentration increased. Parameters such as Vj and Mo increased rapidly, while ψo and φEo decreased rapidly. It indicated a disruption in the electron transfer between the donor and acceptor side of the photosynthesis system Ⅱ (PSⅡ) reaction center, leading to inhibition of photosynthetic activity. Among the 11 Chlamydomonas reinhardtii strains, Chlamydomonas reinhardtii FACHB-889 displayed the lowest tolerance to Hg (EC50 of 0.762 mg/L), whereas Chlamydomonas reinhardtii FACHB-2217 demonstrated the highest tolerant (EC50 of 2.848 mg/L). Under low mercury concentration stress (<0.5 mg/L), PSⅡ activity of Chlamydomonas reinhardtii FACHB-889 was significantly reduced compared to the control ( P <0.05), and there was no significant difference in the activity of photosynthetic system Ⅱ (PSⅡ) of Chlamydomonas reinhardtii FACHB-2217. Under high mercury concentration stress (>1.0 mg/L), Chlamydomonas reinhardtii FACHB-889 inhibited photosynthetic activity, with a notable decrease in the number of active reaction centers per unit area (P<0.05). This resulted in the inefficient utilization of absorbed energy by photosynthesis, leading to abnormal energy accumulation and cell inactivation or death. In contrast, Chlamydomonas reinhardtii FACHB-2217 showed a significant increase in energy absorbed (ABS/RC), energy used for QA reduction (TRo/RC), and energy used for electron transfer (ETo/RC) in the active unit reaction centers (URCs), and the cells were able to efficiently convert the absorbed energy through the increased photosynthetic capacity of active URCs. energy and eliminating the negative effects of partial reaction center inactivation. The study suggests that differences in photosynthetic activity and energy partitioning are important factors in the sensitivity/tolerance of Chlamydomonas reinhardtii to Hg.
-
Keywords:
- Mercury /
- Photosystem Ⅱ /
- Toxic effects /
- Chlamydomonas reinhardtii
-
蛋白源是水产动物配合饲料的主要成分。鱼粉因高消化率、适宜的氨基酸和脂肪酸组成, 成为水产动物饲料中最常用且最重要的蛋白源。随着水产养殖业的发展, 鱼粉的需求量不断增加, 但是随着气候环境的变化, 海洋渔业资源不断衰退, 鱼粉的供需矛盾变得极为紧张。价格低廉且来源广泛的以豆粕、棉粕、菜粕为主的植物蛋白被大量应用于水产饲料, 但这些植物蛋白中存在抗营养因子、缺乏如赖氨酸和蛋氨酸等必需氨基酸, 无法完全替代鱼粉, 使用具有一定的局限性。近年来, 以菌体和藻类为主的单细胞蛋白在水产饲料中的应用也逐步深入。
乙醇梭菌蛋白(Clostridium autoethanogenum protein, CAP)是一种价廉质优的单细胞蛋白, 其蛋白含量, 氨基酸组成相对平衡。同时, CAP是乙醇工业化生产中得到的副产品, 产量巨大, 产能稳定, 因此CAP的生产不会消耗额外的其他资源, 是一种可靠的新型饲料蛋白源[1]。研究表明, CAP可在建鲤(Cyprinus carpiovar Jian)的配合饲料中替代植物蛋白[1], 在大口黑鲈(Micropterus salmoides)饲料中替代鱼粉[2, 3], 吉富罗非鱼(Oreochromis niloticus)配合饲料中替代豆粕[4]。此外, 在甲壳类动物中, CAP也可以替代鱼粉用于凡纳滨对虾(Litopenaeus vannamei)[5]和克氏原螯虾(Procambarus clarkii)[6]的配合饲料。
日本沼虾(Macrobrachium nipponense)俗称河虾、青虾, 是我国国内广泛存在的本土淡水虾品种。因其生长快、品质高、抗病性强、经济价值高而开始被大面积养殖。2023年, 日本沼虾全国年产量已超22.6万吨, 主要产区位于江苏省。2023年江苏省日本沼虾养殖产量已经超过10万吨, 接近全国产量的一半[7]。研究表明日本沼虾的配合饲料中需要约25%的鱼粉[8]。在鱼粉使用成本过高、用量有限的当下, 若能使用CAP替代鱼粉, 则能够节省更多的成本, 让日本沼虾的养殖具有更高的经济效益。本试验以CAP替代日本沼虾配合饲料中不同的鱼粉水平, 评估CAP替代鱼粉对日本沼虾生长、蛋白质和脂肪代谢的影响, 以探讨在日本沼虾配合饲料中CAP替代鱼粉的可行性以及最适宜添加量, 为新型单细胞蛋白源CAP在水产饲料中的应用提供数据支撑。
1. 材料与方法
1.1 试验动物
日本沼虾幼虾[平均初始体重(0.102±0.001) g, 初始体长约15 mm]来自淡水渔业研究中心宜兴大浦基地养殖场(江苏无锡)。在饲养试验前, 用青虾“太湖2号”专用商品料(江苏冠乾特种水产饲料有限公司, 常州溧阳)饲喂幼虾2周, 以适应养殖环境。禁食24h后, 将日本沼虾(n=1200)随机分配到24个养殖桶, 每个桶50尾虾。
1.2 饲料制备
乙醇梭菌蛋白(CAP)由北京首朗生物科技有限公司(中国河北)提供, 干物质含量92.83%、粗蛋白含量为89.25%、粗脂肪含量为2.30%, 其中必需氨基酸赖氨酸含量为8.59%、蛋氨酸含量为3.54%。利用CAP替代不同水平鱼粉, 配制6组等氮等脂(粗蛋白37.25%, 粗脂肪7.70%)的试验饲料(表 1)。对照组D1饲料中含25%鱼粉, D2组饲料中CAP替代10%鱼粉、D3组饲料CAP替代20%鱼粉、D4组饲料CAP替代30%鱼粉、D5组饲料CAP替代40%鱼粉和D6组饲料CAP替代50%鱼粉。在各组饲料中添加L-赖氨酸和D、L-蛋氨酸以保证各组饲料中赖氨酸和蛋氨酸平衡。根据试验饲料配方表, 将所有原料粉碎过60目筛, 随后采用逐级混合扩大法将所有原料混合均匀。采用双螺杆挤条机(F-26, 广州华中光电科技有限公司, 广州, 中国)挤压混合原料, 制备直径为1.0 mm的日本沼虾饲料。饲料在室温晾干后, –20℃保存备用。
表 1 试验饲料配方和营养成分Table 1. Experimental diets formulation and proximate composition原料Ingredient 鱼粉替代水平 Fishmeal replacement (%) D1 (0) D2 (10%) D3 (20%) D4 (30%) D5 (40%) D6 (50%) 鱼粉Fish meal 25.00 22.50 20.00 17.50 15.00 12.50 乙醇梭菌蛋白CAP 0.00 1.86 3.70 5.57 7.42 9.30 豆粕Soybean meal 20.00 20.00 20.00 20.00 20.00 20.00 菜粕Canola meal 10.00 10.00 10.00 10.00 10.00 10.00 虾粉Shrimp powder 5.00 5.00 5.00 5.00 5.00 5.00 花生粕Peanut meal 8.00 8.00 8.00 8.00 8.00 8.00 乌贼膏Squid 2.00 2.00 2.00 2.00 2.00 2.00 α-淀粉α-starch 17.16 17.66 18.15 18.63 19.12 19.59 米糠Rice bran 5.00 5.00 5.00 5.00 5.00 5.00 鱼油Fish oil 1.50 1.50 1.50 1.50 1.50 1.50 豆油Soybean oil 1.20 1.39 1.59 1.79 1.99 2.19 大豆磷脂Soy lecithin 0.50 0.50 0.50 0.50 0.50 0.50 胆固醇Cholesterol 0.50 0.50 0.50 0.50 0.50 0.50 磷酸二氢钙Ca (H2PO4)2 2.00 2.00 2.00 2.00 2.00 2.00 多维多矿预混Vitamin & Mineral premix1 1.00 1.00 1.00 1.00 1.00 1.00 维生C Vitamin C 0.50 0.50 0.50 0.50 0.50 0.50 氯化胆碱Chlorine chloride 0.25 0.25 0.25 0.25 0.25 0.25 赖氨酸Lysine 0.26 0.23 0.21 0.18 0.15 0.12 蛋氨酸Met 0.13 0.11 0.10 0.08 0.07 0.05 营养成分(%干物质) Proximate Composition (% of dry matter) 粗蛋白Crude protein 37.38 37.22 37.27 37.28 37.21 37.25 粗脂肪Crude lipid 7.65 7.71 7.82 7.72 7.75 7.65 粗灰分Ash 10.54 10.76 10.76 10.59 10.42 10.01 赖氨酸Lysine 2.71 2.71 2.71 2.71 2.71 2.71 蛋氨酸Methionine 0.95 0.95 0.95 0.95 0.95 0.95 注: 1多维多矿预混料为无锡华诺威动物保健品有限公司提供的淡水虾多维多矿预混料Note: 1 Vitamin and mineral premix are provided by Wuxi Hanove Animal Health Products Co., Ltd. 1.3 饲养管理
PVC养殖桶(Φ1500 mm, 高1000 mm, 加水后含水体800 L)随机分为6组, 每组饲料投喂4个养殖桶。采用静水养殖, 桶内放置塑料假叶子作为遮蔽物和躲避场所, 持续增氧, 隔天换水。养殖期间每周测定水质指标2次, 溶解氧≥ 6 mg/L, 氨氮含量<0.2 mg/L、pH 7.0—8.5、水温 25—28℃。投喂量为虾体重量的3%, 每天投喂3次(7:00、12:00和18:00), 投喂结束后1h吸出残饵和粪便, 隔天对养殖桶进行换水。饲养试验持续8周。
1.4 样品采集
在养殖试验结束后, 禁食24h。对每个养殖桶称重, 对存活的试验虾进行计数, 并根据以下公式计算存活率(SR)、末均重(FBW)、增重率(WGR)、特定生长率(SGR)、饵料系数(FCR)、蛋白质效率(PER)等生长相关指标。
存活率(SR, %)=(n2/n1)×100
增重率(WGR, %)=(w2–w1)/w1×100
特定生长率(SGR, %/d)=(Ln w2–Ln w1)/d×100
饲料系数(FCR)= f /(w2–w1)
蛋白质效率(PER)=(w2–w1)/(f×p)×100
式中, n1为试验初虾尾数, n2为试验末虾尾数, w1为试验初虾均重, w2为试验末虾均重, d为养殖天数, f为摄食饲料量, p为饲料蛋白质含量。
每桶随机取6尾虾采血, 虾置于冰上, 0.5 mL注射器自围心腔以抗凝剂和血淋巴1﹕1的比例采血(抗凝剂: 柠檬酸三钠 13.2 g/L、柠檬酸 4.8 g/L、葡萄糖14.7 g/L), 4℃ 3000 r/min离心10min制备血清, 3尾虾混合成血淋巴混合样, –20℃保存, 以备血淋巴生化指标测定。随后采集该6尾虾的肝胰腺, 其中2尾虾的肝胰腺混合成1个样, 每桶共采集3个肝胰腺混合样, –20℃保存, 用于肝胰腺消化酶测定。另取2尾虾的肝胰腺置于TRIzol (TaKaRa, 大连, 中国)中, –80°℃保存, 用于蛋白质和脂代谢相关基因测定。此外, 每桶随机取6尾虾, 混合成一个全虾样品, –20℃保存, 以备全虾体成分测定。随机取12尾虾的肌肉混合, –20℃保存, 以备肌肉氨基酸含量测定。
1.5 营养成分测定及肌肉氨基酸测定
根据AOAC[17]方法测定饲料和全虾样品的水份、粗蛋白质、粗脂肪和灰分含量。饲料或全虾在105℃烘箱中干燥至恒重后测得水份含量。取0.5 g左右饲料或者全虾的干物质样品, 利用全自动凯氏定氮仪(海能, 中国)通过凯氏定氮法测定粗蛋白。索氏提取法利用石油醚浸提出脂肪, 测定粗脂肪; 马弗炉550℃灼烧6.5h, 测定粗灰分。
肌肉氨基酸含量根据《饲料中氨基酸的测定》(GB/T 18246-2019)进行测定。肌肉冷冻干燥后, 用6 mol/L盐酸水解24h后, 氨基酸自动分析仪(sykam S-433D, 赛卡姆, 德国)进行测定及分析。
1.6 血淋巴生化指标及肝胰腺消化酶活性测定
血淋巴总蛋白(Total protein, TP)、总胆固醇(Total cholesterol, TC)、甘油三酯(Triglyceride, TG)、尿素(Urea)、葡萄糖(Glucose, GLU)均采用全自动生化分析仪(BS-400型, 迈瑞, 深圳, 中国)利用相应测定试剂盒(深圳迈瑞医药国际有限公司)分析测定。
取0.1 g肝胰腺样品, 加入0.9 mL无菌生理盐水, 冰浴匀浆, 4℃ 4000 r/min离心10min, 取上清液。胰蛋白酶(TRY)、脂肪酶(LPS)和淀粉酶(AMY)均按试剂盒(南京建成生物工程研究所)提供的方法进行测定。
1.7 蛋白质代谢和脂代谢相关基因表达
取TRIzol保存的肝胰腺样品, 用RNAiso plus (TaKaRa, 大连, 中国)提取总RNA, 琼脂糖凝胶电泳和Nanodrop 2000测定RNA浓度和纯度, 调节RNA浓度至500 ng/μL。反转录试剂盒PrimeScriptTM RT Master Kit (TaKaRa, 大连, 中国)将RNA反转录成cDNA, 反应体系为20 μL(5 × gDNA 2 μL, gDNA Eraser 1 μL, RNase free H2O 5 μL, Total RNA 2 μL, 42℃孵育2min; 加入5 × Primer buffer 4 μL, PrimeScriptTM RT Enzyme Mix 1 μL, Rt Primer Mix 1 μL, RNase free H2O 4 μL)。反转录程序为: 37℃ 15min, 85℃ 5s。合成的cDNA模板, 采用TB GreenTM Premix Ex TaqTM Kit(TaKaRa, 大连, 中国)在定量PCR仪(Bio-Rad, USA)进行荧光定量PCR反应。反应体系20 μL(SYBR Premix Ex Taq 10 μL, Primer 各0.8 μL, dd H2O 6.4 μL, cDNA 2 μL), 反应程序为: 95℃ 预变性30s; 95℃ 5s, 60℃ 30s, 72℃ 30s (循环30次); 溶解曲线温度范围为50—95℃。本试验所用基因的引物序列见表 2[8—12], 所有引物委托上海捷瑞生物工程有限公司合成。以β-actin为内参基因, 根据2−ΔΔCt法[13]计算基因相对表达量。
表 2 基因引物序列Table 2. RT-PCR primer sequence目的基因
Target gene引物序列
Primer sequence (5′—3′)序列登录号
GenBank
accession No.参考文献
Referencetor AACAAGTCTCGTCCGTGTCC — Zhou 等[8] TTGAGCAGCTTCACGGCTTA atf4 GGCGGTGCAGTTAAACACTC — Zhou等[8] GTCAGTTTCACCCATGTCGC s6k GGTCTTTGAGGGCTTTACG ON693253 郑金仙等[9] GTCCAGCAGAGTTTGGTGTAT acc CAAGGTCCACTACATGGTCT KP690138 丁志丽等[10] ACTCTTCCCAAACTCTCTCC fas CGGTCAGACAAACTACGGCT MK307767.1 Wang等[11] CACTGAATAGCCACCCCAGG elovl6 TGGTGCACAGTATCATGTAC KU953779 Luo等[12] TCATAGGAAACGTGACACTC hsl GAAGGCCAGCGCTAATTTCG MK633965.1 Wang等[11] TCGAACCACCCATGAGAAGC sr-bⅠ TTATCCCTGGTGTGAATGTG KP658863 丁志丽等[11] GAACTCTTCCCATTCCAACT β-actin GTGCCCATCTACGAGGGTTA FL589653.1 Luo等[12] CGTCAGGGAGCTCGTAAGAC 注: tor, target of rapamycin雷帕霉素靶蛋白; atf4, activating transcription factor 4转录激活因子4; s6k, ribosomal protein S6 kinase核糖体S6激酶; acc, acetyl-CoA carboxylase乙酰辅酶A羧化酶; fas, fatty acid synthase脂肪合成酶; hsl, hormone-sensitive lipase激素敏感脂肪酶; sr-bⅠ, scavenger receptor class B type Ⅰ, B类Ⅰ型清道夫受体; elovl6, elongase of very-long-chain fatty acids长链脂肪酸延长酶; β-actin, β-肌动蛋白 1.8 数据统计与分析
结果数据用平均值±标准误(mean±SE)表示。利用SPSS 20.0软件对数据进行单因素方差分析(One-way ANOVA), 使用Turkey进行多重比较, 当P<0.05表示差异显著。使用GraphPad Prism8.0进行作图。
2. 结果
2.1 乙醇梭菌蛋白替代鱼粉对日本沼虾生长、饲料利用率的影响
在CAP替代鱼粉饲喂日本沼虾8周后, 其生长和饲料利用率如表 3所示。CAP替代不同水平鱼粉对日本沼虾存活率没有显著影响。与对照组相比, D2和D3组日本沼虾的FBW、WGR和SGR差异不显著(P>0.05), 而D4、D5和D6组日本沼虾的FBW、WGR和SGR则显著降低(P<0.05)。此外, D5 和D6组FCR显著高于对照组(P<0.05), 而其他各组与对照组差异不显著(P>0.05), 而其他3组FCR则显著高于D1组。PER恰好相反, D5和D6组PER显著低于对照组(P<0.05)。
表 3 乙醇梭菌蛋白替代鱼粉后对生长和饲料利用的影响Table 3. Effects of CAP replacing fishmeal on growth performance and feed utilization指标Index 鱼粉替代水平 Fishmeal replacement (%) D1 (0) D2 (10%) D3 (20%) D4 (30%) D5 (40%) D6 (50%) 存活率SR (%) 74.67±1.33 88.50±2.99 86.00±8.52 85.33±3.53 80.50±4.57 90.50±2.50 末均重FBW (g) 0.76±0.01c 0.56±0.01b 0.57±0.02bc 0.46±0.02a 0.37±0.02a 0.39±0.06a 增重率WGR (%) 461.01±14.90c 392.07±18.74bc 380.87±36.65bc 288.17±10.19ab 199.56±10.89a 253.54±58.93a 特定生长率SGR (% /d) 2.45±0.05c 2.27±0.06bc 2.22±0.12bc 1.92±0.06ab 1.54±0.06a 1.73±022a 饵料系数FCR 1.66±0.04a 1.91±0.08ab 2.01±0.23ab 2.29±0.15ab 3.63±0.18c 3.02±0.53bc 蛋白质效率PER 145.03±3.69c 126.27±5.81bc 122.92±11.75bc 106.57±7.54abc 66.71±3.25a 89.66±19.81ab 注: n=4, 同一行右上角含有相同英文上标字母或者无上标表示差异不显著(P ≥ 0.05); 下同Note: n=4. Means in each line sharing the same letter or absence of superscripts are not significantly different determined by Tukey’s test (P ≥ 0.05); The same applies below 2.2 乙醇梭菌蛋白替代鱼粉对日本沼虾体成分的影响
饲料中CAP替代不同水平鱼粉对日本沼虾的全虾体成分包括水分、粗蛋白、粗脂肪和灰分等指标均没有产生显著的影响(P>0.05)。
表 4 乙醇梭菌蛋白替代鱼粉后对体成分的影响Table 4. Effects of CAP replacing fishmeal on shrimp composition指标Index 鱼粉替代水平 Fishmeal replacement (%) D1 (0) D2 (10%) D3 (20%) D4 (30%) D5 (40%) D6 (50%) 水份Moisture (%) 76.97±0.07 77.11±0.39 76.89±0.38 76.91±0.73 76.967±0.31 76.76±0.49 粗蛋白Protein (%) 14.99±0.15 15.82±0.30 15.26±0.27 15.70±0.38 15.86±0.27 15.91±0.28 粗脂肪Lipid (%) 3.04±0.24 2.85±0.32 3.38±0.21 3.63±0.29 2.98±0.32 3.32±0.22 灰分Ash (%) 5.13±0.43 5.82±0.16 5.33±0.40 6.22±0.20 5.85±0.52 6.17±0.26 2.3 乙醇梭菌蛋白替代鱼粉对日本沼虾肌肉中氨基酸的影响
CAP替代不同水平鱼粉对日本沼虾肌肉中必需氨基酸影响不显著(P>0.05), 但显著影响日本沼虾肌肉非必需氨基酸和总氨基酸含量(P<0.05)。除甘氨酸、精氨酸和苯丙氨酸以外, D2组和D3组日本沼虾肌肉氨基酸含量与对照组差异不显著(P>0.05)。 D6组日本沼虾肌肉的精氨酸含量显著低于对照组(P<0.05), 而其组氨酸、异亮氨酸和赖氨酸等必需氨基酸、以及天冬氨酸、甘氨酸、谷氨酸等非必需氨基酸均显著高于对照组(P<0.05)。
表 5 乙醇梭菌蛋白替代鱼粉对日本沼虾肌肉氨基酸含量的影响Table 5. Effect of CAP replacing FM on the amino acid profile of M. nipponense’s muscle氨基酸含量
Amino acid (%)鱼粉替代水平 Fishmeal replacement (%) D1 (0) D2 (10%) D3 (20%) D4 (30%) D5 (40%) D6 (50%) 亮氨酸Leu 1.52±0.01ab 1.48±0.00a 1.54±0.01ab 1.58±0.01ab 1.58±0.05ab 1.62±0.01b 组氨酸His 0.51±0.01a 0.50±0.00a 0.53±0.00a 0.53±0.01a 0.50±0.01a 0.61±0.03b 异亮氨酸Ile 0.90±0.01a 0.88±0.01a 0.94±0.01ab 0.95±0.00ab 0.92±0.04ab 1.00±0.01b 精氨酸Arg 1.67±0.03c 1.15±0.02b 1.58±0.04c 1.51±0.06bc 1.40±0.12bc 1.27±0.01ab 赖氨酸Lys 1.57±0.02a 1.56±0.00a 1.59±0.01a 1.67±0.00b 1.61±0.02ab 1.73±0.01c 蛋氨酸Met 0.59±0.01 0.59±0.01 0.61±0.01 0.59±0.00 0.61±0.00 0.62±0.01 苯丙氨酸Phe 0.83±0.01b 0.76±0.00a 0.80±0.00ab 0.85±0.01b 0.76±0.00a 0.86±0.01b 苏氨酸Thr 0.72±0.01 0.70±0.00 0.71±0.01 0.74±0.00 0.71±0.00 0.75±0.00 缬氨酸Val 0.88±0.01 0.93±0.03 0.94±0.00 0.90±0.02 0.91±0.01 0.95±0.02 必需氨基酸EAA 9.16±0.11 8.52±0.01 9.23±0.08 9.30±0.01 8.97±0.25 9.39±0.04 天冬氨酸Asp 2.04±0.03a 1.96±0.02a 2.06±0.02a 2.02±0.02a 1.96±0.04a 2.15±0.00b 丝氨酸Ser 0.73±0.01 0.70±0.00 0.71±0.01 0.73±0.01 0.68±0.02 0.71±0.01 甘氨酸Gly 1.30±0.00a 1.43±0.01b 1.54±0.03c 1.50±0.00bc 1.63±0.02d 1.60±0.00cd 丙氨酸Ala 1.32±0.01 1.34±0.02 1.31±0.00 1.39±0.03 1.36±0.02 1.32±0.02 半胱氨酸Cys 0.27±0.00 0.30±0.29 0.32±0.01 0.27±0.01 0.30±0.02 0.29±0.01 酪氨酸Tyr 0.70±0.01ab 0.63±0.00a 0.65±0.01ab 0.71±0.02ab 0.68±0.00ab 0.73±0.00b 谷氨酸Glu 2.99±0.05ab 2.86±0.01a 2.97±0.01ab 3.14±0.01b 3.00±0.01ab 3.27±0.04c 脯氨酸Pro 0.91±0.04b 0.90±0.01b 0.88±0.00ab 0.91±0.02b 0.72±0.08a 1.01±0.03b 非必需氨基NEAA 10.23±0.14ab 10.09±0.02a 10.43±0.08bc 10.66±0.04c 10.45±0.07bc 11.06±0.01d 总氨基酸TAA 19.39±0.25ab 18.61±0.01a 19.65±0.16bc 19.95±0.05bc 19.43±0.31ab 20.45±0.03c 2.4 乙醇梭菌蛋白替代鱼粉对日本沼虾血淋巴生化的影响
由表 6可知, D2组和D3组日本沼虾血淋巴总蛋白含量与对照组差异不显著(P>0.05), 但是D4、D5和D6组日本沼虾血淋巴总蛋白含量显著低于对照组和D2组(P<0.05)。D6组日本沼虾血淋巴尿素氮含量最低, 且显著低于对照组和D2组(P<0.05)。CAP替代高于10%鱼粉时, 日本沼虾血淋巴总胆固醇、甘油三酯显著低于对照组(P<0.05), 葡萄糖显著高于对照组(P<0.05)。
表 6 乙醇梭菌蛋白替代鱼粉后对血淋巴生化的影响Table 6. Effects of CAP replacing FM on hemolymph biochemical indexes指标Index 鱼粉替代水平 Fishmeal replacement (%) D1 (0) D2 (10%) D3 (20%) D4 (30%) D5 (40%) D6 (50%) 总蛋白TP (g/L) 43.14±1.56bc 45.92±2.61c 33.69±3.89ab 33.00±2.00a 31.99±2.09a 26.67±1.28a 总胆固醇TC (mmol/L) 0.78±0.12b 0.87±0.07b 0.32±0.03a 0.37±0.03a 0.26±0.02a 0.29±0.02a 甘油三酯TG (mmol/L) 18.90±1.25b 16.98±1.21b 8.08±0.57a 9.57±0.42a 8.63±0.48a 9.41±0.47a 葡萄糖GLU (mmol/L) 4.12±0.97a 5.16±0.88ab 9.32±1.75bc 8.86±0.81bc 9.82±0.78c 11.18±0.97c 尿素氮Urea (mmol/L) 1.66±0.06b 1.65±0.13b 1.41±0.15ab 1.33±0.05ab 1.24±0.12ab 1.00±0.05a 2.5 乙醇梭菌蛋白替代鱼粉对日本沼虾肝胰腺消化酶活性的影响
CAP替代鱼粉显著影响日本沼虾肝胰腺消化酶活性。在CAP替代10%鱼粉时, 日本沼虾肝胰腺脂肪酶活性与对照组相比, 显著升高(P<0.05)。在CAP替代高于10%鱼粉时, 日本沼虾肝胰腺的消化酶活性与对照组差异不显著(P>0.05)。此外, D4和D5组胰蛋白酶、脂肪酶活性及D6组淀粉酶活性显著低于D2组(P<0.05)。
2.6 乙醇梭菌蛋白替代鱼粉对日本沼虾肝胰腺基因表达的影响
CAP替代不同水平鱼粉显著影响日本沼虾肝胰腺内蛋白质和脂肪代谢相关基因的表达。在CAP替代10%鱼粉时, 蛋白和脂肪代谢基因相对表达量降低, 但与对照组差异不显著(P>0.05)。在CAP替代鱼粉达到20%时, tor、s6k1和atf4基因相对表达量上升。D3组tor基因相对表达量显著高于对照组和D2组(P<0.05)。除D2组外, 其余各组s6k1基因相对表达量与对照组差异不显著(P>0.05), 但显著高于D2组(P<0.05)。D4和D5组atf4基因相对表达量显著高于D2组(P<0.05)。在脂质合成相关基因中, D3、D4和D5组acc基因相对表达量同样与对照组差异不显著(P>0.05), 但显著高于D2组(P<0.05)。D3、D5和D6组fas基因相对表达量显著高于D2组。D6组fas基因表达较对照组显著上调(P<0.05)。D3组和D5组elovl6基因相对表达量显著高于D2和D4组(P<0.05)。与对照组相比, 各试验组日本沼虾肝胰腺hsl和sr-bⅠ基因相对表达量差异不显著(P>0.05), 除D3组sr-bⅠ基因相对表达量显著高于对照组之外(P<0.05)。D2组hsl表达量显著低于D3、D5、D6组(P<0.05); D5组sr-bⅠ基因相对表达量显著低于D3和D6组(P<0.05)。
3. 讨论
3.1 乙醇梭菌蛋白替代鱼粉对日本沼虾生长的影响
乙醇梭菌(Clostridium autoethanogenum)是一种天然的非致病性菌株, 是一种革兰氏阳性、成短杆状、能形成孢子的严格厌氧菌。CAP是由乙醇梭菌以炼钢废气中的一氧化碳为碳源、发酵生产工业乙醇, 经细菌分离、喷雾干燥后得到的副产物[14]。本研究结果显示在日本沼虾饲料中使用CAP作为蛋白源, 对日本沼虾的存活率无显著影响, 且CAP替代50%的鱼粉时, 日本沼虾存活率最高。据报道CAP作为单细胞蛋白, 在黑鲷(Acanthopagrus schlegelii)[14]和大口黑鲈[2]饲料中添加18%而不影响其生长; 在建鲤饲料中添加量可达20%[1], 在大口黑鲈饲料中可以替代15%的鱼粉[3]。此外, CAP在吉富罗非鱼中可以替代豆粕, 使用量达到20%时能显著提高其生长[4]。在甲壳类动物中, CAP最高可替代凡纳滨对虾饲料中30%鱼粉而不会对虾的生长表现产生不利影响[5]。克氏原螯虾的研究结果表明, CAP替代25%的鱼粉生长效果最佳, 替代全部鱼粉时也不影响克氏原螯虾的生长[6]。本研究发现日本沼虾饲料中CAP替代20%鱼粉对其生长无影响。此外, 日本沼虾中研究发现泰森鸡肉粉、鸡蛋粉、肠黏膜蛋白粉及水解羽毛粉等动物性蛋白也可以替代饲料中20%的鱼粉而对日本沼虾的生长不产生显著影响[15]。这表明CAP作为新的单细胞蛋白, 可以在水产动物饲料中进行应用, 但是在不同水产动物中差异较大。
CAP粗蛋白含量高, 可达85%以上, 且总氨基酸占蛋白质含量的85%, 富含赖氨酸, 其氨基酸构成与鱼粉相似, 含有多种微量元素, 且不含抗营养因子[13]。在本试验中, CAP替代30%以上的鱼粉时, 其FCR显著升高而PER显著降低, 这说明虽然CAP粗蛋白含量高于鱼粉, 但其蛋白质利用率显著低于鱼粉。这一结果与凡纳滨对虾类似, 当CAP替代超过30%鱼粉时, FCR显著降低[5]; 但是与克氏原螯虾的结果略有不同, CAP替代鱼粉对FCR无显著影响[6]。在黑鲷[13]、建鲤[1]和吉富罗非鱼[4]等鱼类中, 随着CAP添加量的增加, PER显著增加; 而在大口黑鲈中, CAP替代25%鱼粉时, FCR显著升高[3]。这说明不同物种对于CAP的消化吸收利用率存在一定的差异, 总体来看, 鱼类对CAP的利用率优于甲壳类。
3.2 乙醇梭菌蛋白替代鱼粉对日本沼虾肌肉品质的影响
本研究结果表明CAP对日本沼虾水分、粗蛋白、粗脂肪和灰分无影响, 表明饲料中CAP替代鱼粉不会影响日本沼虾养成分。这与建鲤和吉富罗非鱼的研究结果相似, 饲料中添加CAP不影响建鲤和吉富罗非鱼的体组成[1, 4]。此外, 大西洋鲑(Salmo salar)和庸鲽(Hippoglossus hippoglossus)也有相似结果, 饲料中添加细菌蛋白不影响大西洋鲑和庸鲽体成分[16—19]。与之相反, 在南美白对虾中, 对虾肌肉的粗蛋白会随着CAP添加量的上升而下降, 而肌肉水份则呈相反的趋势[5]; CAP会导致大口黑鲈肌肉粗脂肪含量下降[2]。产生这样差异的原因还需进一步研究。
肌肉是鱼最大的可食部分, 因此肌肉氨基酸含量不仅反应所摄食的饲料营养氨基酸平衡, 也代表水产品的营养品质的重要指标。在本研究中, CAP的应用对日本沼虾肌肉必需氨基酸影响不显著, 但是对非必需氨基酸和总氨基酸含量产生一定的影响。这可能是由于CAP与鱼粉的氨基酸组成差异导致的。日粮中CAP过量会显著提高日本沼虾肌肉中非必需氨基酸和总氨基酸含量。但在南美白对虾中表现出了与日本沼虾相反的趋势, 当45%以上的鱼粉被CAP替代时, 肌肉中必需氨基酸的含量下降[5, 20]。在本研究中发现, CAP过量使用不影响虾体肌肉必需氨基酸含量, 这可能与配方时, 调节了赖氨酸和蛋氨酸等限制性必需氨基酸的水平, 在一定程度上对饲料氨基酸的平衡进行了调节。由此可见, CAP的氨基酸组成较鱼粉还有所差距, 当利用CAP替代鱼粉时可能需要对必需氨基酸进行补充调节。
3.3 乙醇梭菌蛋白替代鱼粉对日本沼虾代谢的影响
日本沼虾饲料中CAP替代10%鱼粉对血淋巴总蛋白、尿素氮、总甘油三酯、总胆固醇和葡萄糖等含量影响不显著, 这可能与CAP替代10%鱼粉时日本沼虾肝胰腺的蛋白酶、脂肪酶和淀粉酶等消化酶活性在一定程度上升高有关。而当日本沼虾饲料中CAP替代20%以上鱼粉时, 血淋巴总蛋白和尿素氮水平显著降低, 这一现象显示出CAP对日本沼虾的蛋白质代谢产生了一些负面影响。此外, 在CAP替代20%鱼粉时, 显著降低血淋巴中胆固醇、甘油三酯的含量, 且显著提高葡萄糖含量, 这说明CAP可能会降低葡萄糖的糖异生作用, 降低日本沼虾体内的脂质合成。血淋巴总甘油三酯和总胆固醇减少的原因也可能是由于CAP存在的某些生物活性化合物具有促进脂质代谢的功能[21]。CAP提高血淋巴葡萄糖水平, 也可能表明CAP的添加显著增强了日本沼虾的能量调节, 这与建鲤的研究结果一致[1]。因此, 在使用CAP作为蛋白源时, 可能在饲料中需要提供更多的脂质以调节动物体内的糖脂代谢过程。
甲壳类动物肝胰腺消化酶活性可以体现机体营养代谢水平[8]。本研究结果表明在CAP替代10%鱼粉时, 日本沼虾肝胰腺的蛋白酶、脂肪酶和淀粉酶均达到峰值; 而在CAP替代20%鱼粉时, 日本沼虾肝胰腺的蛋白酶、脂肪酶和淀粉酶均较峰值下降。这说明在CAP替代水平较低时, 动物机体可以通过消化酶调节来加强机体对脂质的消化和吸收, 进而加强对脂质代谢的调控。而本研究中血淋巴总胆固醇和总甘油三酯的结果能说明这一问题, 当在CAP替代20%及以上鱼粉时, 血淋巴总胆固醇和总甘油三酯水平显著下降。但是, 各处理组日本沼虾肝胰腺的消化酶与对照组差异基本不显著, 这在一定程度上说明CAP替代鱼粉不会对日本沼虾肝胰腺中消化酶活性产生负面影响。当其他动物蛋白如鸡蛋粉、肠溶蛋白、羽毛粉等替代鱼粉时, 日本沼虾肝胰腺的消化酶也没有显著的负面影响[15]。
3.4 乙醇梭菌蛋白替代鱼粉对日本沼虾肝胰腺基因表达的影响
雷帕霉素靶蛋白(Target of rapamycin, TOR)是调节蛋白质合成、细胞骨架重塑及细胞内蛋白质通过自噬降解的细胞信号通路的一个重要基因。活化的TOR可以磷酸化下游靶蛋白——核糖体蛋白S6激酶-1 (Ribosomal protein S6 Kinase-1, S6K1), S6K1磷酸化的增加导致核糖体蛋白S6的过度磷酸化, 从而促进mRNA的翻译, 促进蛋白质合成[22]。本研究结果显示, 在日本沼虾饲料中CAP替代20%鱼粉会提高肝胰腺中tor和s6k1的表达水平, 但替代水平高于20%时, tor基因相对表达量会降低, 这可能是CAP替代20%鱼粉对日本沼虾生长无显著负面影响的主要原因。而在吉富罗非鱼中, CAP的添加不影响tor基因的表达水平, 但在50和100 g/kg CAP组中提高了s6k1基因的表达水平[4]。饲料中蛋白质缺乏或必需氨基酸不平衡激活氨基酸反应信号转导通路, 导致激活转录因子4 (Activating transcription factor 4, ATF4)高表达[23]。本研究发现, CAP替代超过30%鱼粉时, 日本沼虾肝胰腺中atf4表达显著升高, 这表明CAP可能会导致氨基酸不平衡, 影响日本沼虾的生长。此外, 研究表明氨基酸的不平衡会改变氨基酸以外的代谢, 如脂代谢等。氨基酸不平衡激活氨基酸反应信号通路后, 在小鼠和大鼠上会抑制胆固醇合成、脂肪酸合成, 进而导致血清胆固醇降低[24, 25]。本研究也发现高CAP水平会导致日本沼虾血淋巴胆固醇和甘油三酯水平降低, 这可能与氨基酸反应信号通路被激活相关。
新的脂肪酸合成反应由细胞质中的乙酰辅酶A羧化酶(ACC)和脂肪酸合成酶(FAS)可以在细胞质内催化新脂肪酸合成。ACC以ATP依赖的方式催化乙酰辅酶A羧化成丙二酰辅酶A, 然后FAS以乙酰辅酶A和丙二酰辅酶A为底物催化的七个酶促反应生成棕榈酸酯[24]。脂肪酸合成速率受到动物机体营养和激素状况的严格调控以满足身体对脂质和能量储存的需求。本研究结果显示, CAP替代超过20%鱼粉会导致日本沼虾肝胰腺acc和fas相对表达水平升高, 这可能与血淋巴内总甘油三酯和总胆固醇降低有关, 过低的血淋巴脂质水平会自动反馈给机体需要提高脂质合成能力。这与吉富罗非鱼的研究结果相一致。当饲料中CAP水平超过100 g/kg时, fas基因表达水平会上调, 吉富罗非鱼的脂质合成能力得到了提高[4]。而在大口黑鲈中则相反, CAP的添加则减少了脂肪的合成, 使脂肪合成和代谢达到了平衡水平, 减少内源性脂肪酸的合成来预防脂肪的过度积累, 从而达到抑制炎症的效果[2]。elovl6基因是超长链脂肪酸延伸酶 (ELOVLs)家族成员之一, 具有催化饱和和单不饱和脂肪酸的延伸, 它的表达主要受转录因子和一些激素的调控, 是动物机体内脂肪酸代谢的关键表达调控基因之一, 也是一种重要的长链脂肪酸延伸和合成反应的限速酶[25]。在本研究中, elovl6的表达量在CAP替代20%和40%鱼粉时升高, 但与对照组差异不显著。激素敏感性脂肪酶(HSL)是一种中性脂肪酶, 是脂肪分解的限速酶之一[26]。清道夫受体B类I型(SR-BI), 是CD36超家族的一员, 包括参与哺乳动物和鱼类脂质稳态调节的跨膜蛋白。SR-BI可以与低密度脂蛋白、极低密度脂蛋白高密度脂蛋白结合, 选择性摄取胆固醇酯, 进而调节细胞胆固醇稳态、双向胆固醇流动等功能[27]。日本沼虾肝胰腺sr-bI基因的表达与饲料脂肪源相关[27]。在本试验中, CAP替代20%鱼粉时, 日本沼虾肝胰腺sr-bI和hsl基因表达显著升高, 说明CAP替代鱼粉后对日本沼虾肝胰腺的脂代谢也产生了一定的影响, 但具体的影响机制仍需要进一步研究。
4. 结论
综上所述, CAP作为新型的单细胞蛋白源, 在日本沼虾饲料中替代20%鱼粉时, 对日本沼虾生长无显著负面影响, 同时降低日本沼虾血淋巴总胆固醇和甘油三酯, 提高血淋巴葡萄糖水平。CAP替代20%鱼粉对日本沼虾生长无显著负面影响的可能原因在于其提高了肝胰腺tor基因的表达量。总之, 日本沼虾可以利用CAP作为蛋白源, 适量使用对日本生长、蛋白及脂肪代谢无影响。
-
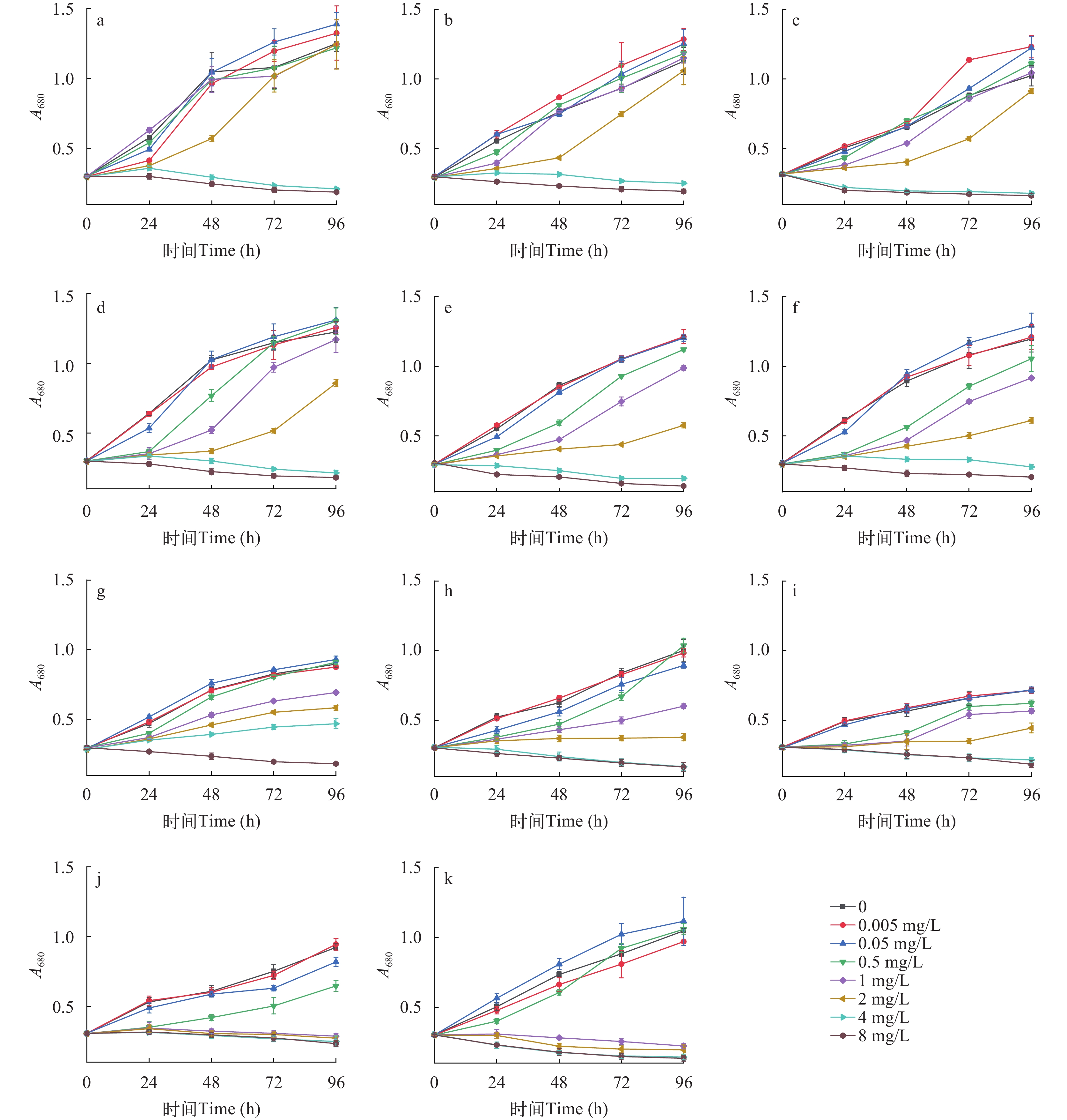
图 1 不同浓度Hg2+培养11种衣藻的生长曲线
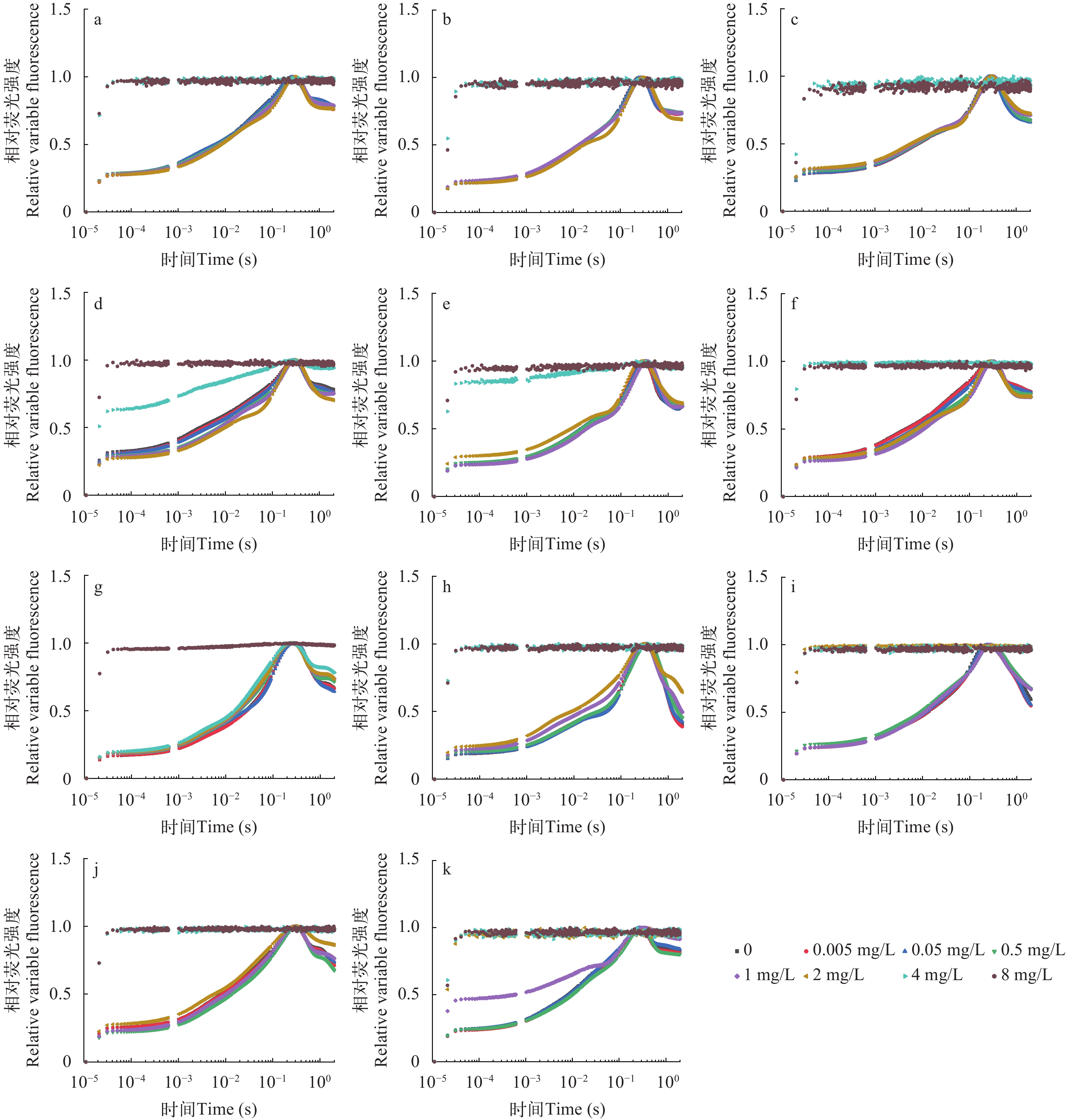
a—k分别代表FACHB-2217、FACHB-2218、FACHB-2219、FACHB-2222、FACHB-359、FACHB-333、FACHB-52、FACHB-1741、FACHB-2081、FACHB-264和FACHB-889; 对于所有图, 数据点代表每个独立培养物的3个重复实验的平均值; 下同
Figure 1. Growth curves of 11 species of Chlamydomonas are cultured at different Hg2+ concentrations
a—k stands for FACHB-2217, FACHB-2218, FACHB-2219, FACHB-2222, FACHB-359, FACHB-333, FACHB-52, FACHB-1741, FACHB-2081, FACHB-264, and FACHB-889 respectively; For all plots, the data points represent the average of the three replicates for each independent culture; the same applies below
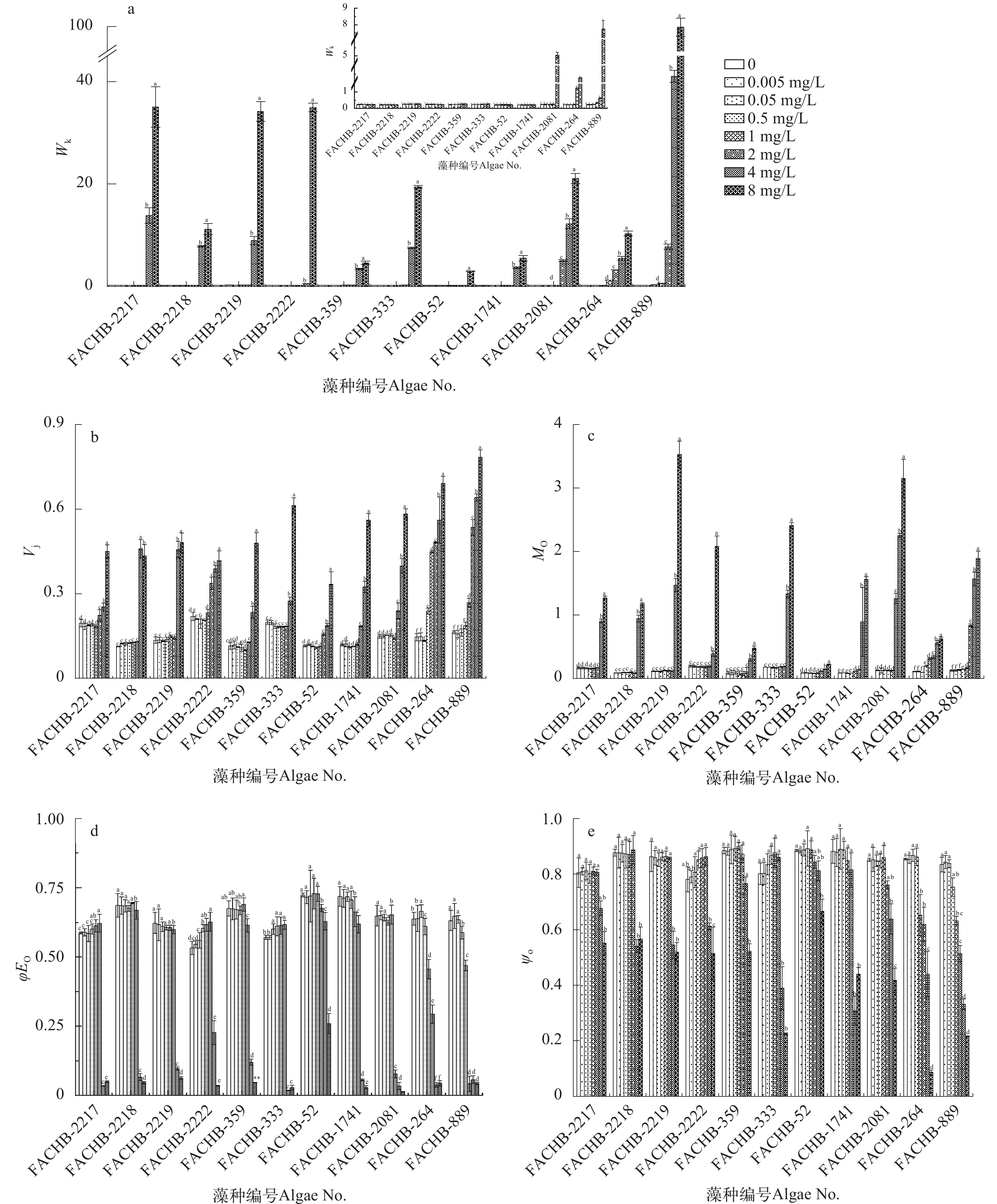
图 5 不同Hg2+浓度暴露后PSII供体侧和PSII受体侧光合参数的变化
a代表供体侧的光合活性; b—e均代表受体侧的光合活性; Wk表示PSⅡ中的OEC的状态, Vj表示${\rm{Q}}^-_{\rm{A}} $积累和再氧化的速率, Mo表示QA的还原速率, φEo表示吸收的能量用于电子传递的量子产额, ψo表示反应中心捕获的光能用于${\rm{Q}}^-_{\rm{A}} $下游电子传递的量子产额
Figure 5. Changes in photosynthetic parameters on the PSII donor side and PSII receptor side after exposure at different Hg2+ concentrations
a indicates the donor-side photosynthetic activity; b-e indicates the acceptor-side photosynthetic activity; Wk indicates the state of the OEC in PSII, Vj indicates the accumulation and reoxidation rate of ${\rm{Q}}^-_{\rm{A}} $, Mo indicates the rate of reduction of QA, φEo indicates the quantum yield of absorbed energy for electron transfer, ψo indicates the quantum yield of light energy captured by the reaction center for ${\rm{Q}}^-_{\rm{A}} $ downstream electron transfer
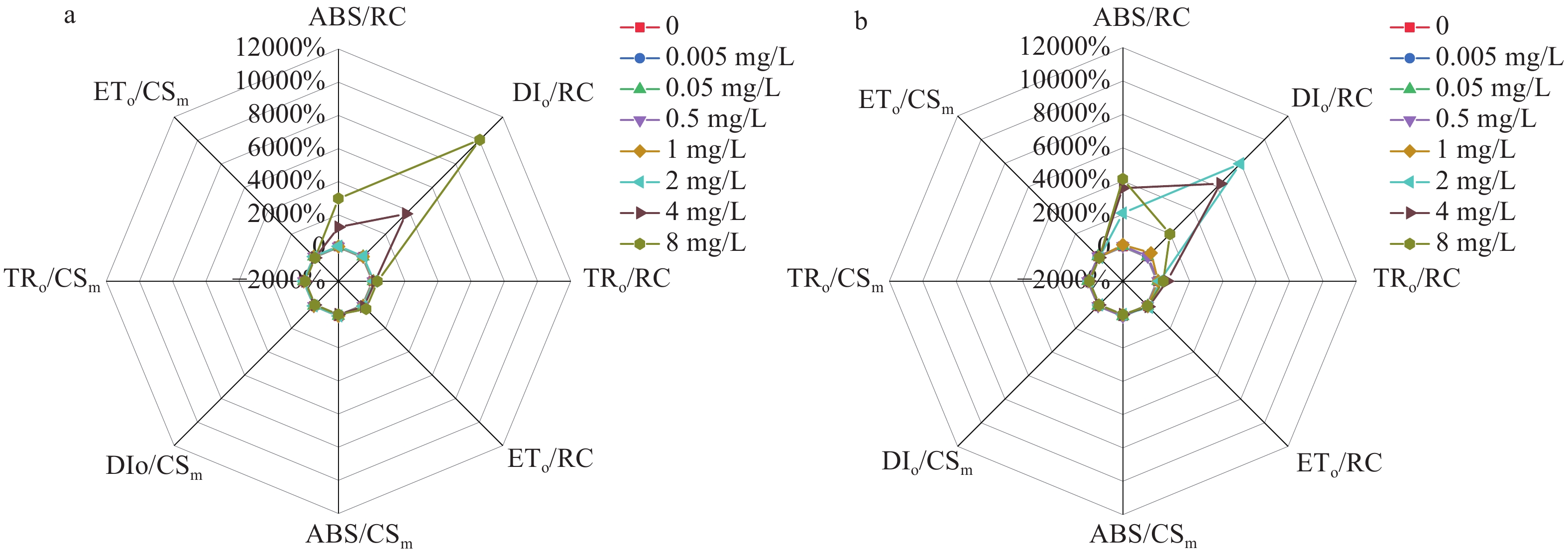
图 6 不同Hg2+浓度对衣藻比活性能量参数的影响
a和b分别代表FACHB-2217和FACHB-889; ABS/RC表示单位反应中心吸收的光能; DIo/RC 表示单位反应中心耗散的能量; TRo/RC 表示单位反应中心捕获的用于还原QA的能量; ETo/RC表示单位反应中心捕获的用于电子传递的能量; ABS/CSm表示单位受光截面吸收的能量; DIo/CSm表示单位受光截面耗散的能量; TRo/CSm表示单位受光截面捕获用于还原QA的能量; ETo/CSm表示单位受光截面捕获用于电子传递的能量
Figure 6. Effect of different Hg2+ concentrations on specific activity energy parameters of Chlamydomonas
a and b represent FACHB-2217 and FACHB-889, respectively; ABS/RC indicates the light energy absorbed per reaction center; DIo/RC indicates the energy dissipated per reaction center; TRo/RC indicates the energy captured per reaction center for the reduction of QA; ETo/RC indicates the energy captured per unit reaction center for electron transfer; ABS/CSm indicates the energy absorbed per unit of light receiving cross section; DIo/CSm indicates the energy dissipated per unit of light received cross section; TRo/CSm indicates the energy captured per unit light-receiving cross section for QA reduction; ETo/CSm indicates the energy captured for electron transfer per unit light-receiving cross section
表 1 不同Hg2+浓度暴露后反应中心密度的变化
Table 1 Changes in reaction center density after exposure at different Hg2+ concentrations (RC/CSo)
藻种编号
Algae number浓度 Concentration (mg/L) 0 0.005 0.05 0.5 1 2 4 8 FACHB
-221723021.119±
232.537a22133.969±
470.998a21924.927±
259.492a21835.076±
525.614a21421.918±
467.696a16466.723±
2326.579b14.183±
1.163c10.115±
2.84cFACHB
-88920117.67±
311.455a20041.95
2±229.019a20544.755±
199.27b20563.941±
143.53b2654.183±
203.988c24.788±
2.113d20.38±
0.189d15.295±
2.039d注: 表中数据为3个重复的平均值; 同一行相同右上角含有相同英文上标字母或无上标表示差异不显著 (P≥0.05); 下同Note: Data are means of triplicates. Means in each bar sharing the same superscript letter or absence of superscripts are not significantly different determined by Tukey’s test (P≥0.05), the same applies below -
[1] Farhan A, Zulfiqar M, Samiah R, et al. Removal of toxic metals from water bynanocomposites through advanced remediation processes and photocatalytic oxidation [J]. Current Pollution Reports, 2023(9): 338-358.
[2] Douglas T A, Loseto L L, Macdonald R W, et al. The fate of mercury in Arctic terrestrial and aquatic ecosystems, a review [J]. Environmental Chemistry, 2012, 9(4): 321-355. doi: 10.1071/EN11140
[3] Mergler D. Ecosystem approaches to mercury and human health: a way toward the future [J]. Ambio, 2021, 50(3): 527-531. doi: 10.1007/s13280-020-01455-0
[4] So S C A, Tsoi M F, Cheung A J, et al. Blood and urine inorganic and organic mercury levels in the united states from 1999 to 2016 [J]. American Journal of Medicine, 2021, 134(1): 20-30. doi: 10.1016/j.amjmed.2020.06.023
[5] Futsaeter G, Wilson S. 2013. The UNEP global mercury assessment: sources, emissions and transport [J]. E3S Web of Conferences, 2013(1): 36001. doi: 10.1051/e3sconf/20130136001
[6] Lin Y, Vogt R, Larssen T. Environmental mercury in China: a review [J]. Environmental Toxicology and Chemistry, 2012, 31(11): 2431-2444. doi: 10.1002/etc.1980
[7] Mao Y, Liu W, Yang X, et al. Syntrichia caninervis adapt to mercury stress by altering submicrostructure and physiological properties in the Gurbantünggüt Desert [J]. Scientific Reports, 2022(12): 11717. doi: 10.1038/s41598-022-15822-2
[8] Ibrahim M, Nawaz S, Iqbal K, et al. Plant-derived smoke solution alleviates cellular oxidative stress caused by arsenic and mercury by modulating the cellular antioxidative defense system in wheat [J]. Plants, 2022, 11(10): 1379. doi: 10.3390/plants11101379
[9] Asztalos E, Sipka G, Kis M, et al. The reaction center is the sensitive target of the mercury (Ⅱ) ion in intact cells of photosynthetic bacteria [J]. Photosynthesis Research, 2012, 112(2): 129-140. doi: 10.1007/s11120-012-9749-2
[10] De Filippis L F, Hampp R, Ziegler H. The effects of sublethal concentrations of zinc, cadmium and mercury on euglena. growth and pigments [J]. Zeitschrift für Pflanzenphysiologie, 1981, 101(1): 37-47.
[11] Murthy S D S, Mohanty P. Mercury ions inhibit photosynthetic electron transport at multiple sites in the cyanobacterium Synechococcus 6301 [J]. Journal of Biosciences, 1993, 18(3): 355-360. doi: 10.1007/BF02702993
[12] Clijsters H, Van Assche F. Inhibition of photosynthesis by heavy metals [J]. Photosynthesis Research, 1985, 7(1): 31-40. doi: 10.1007/BF00032920
[13] Deng C, Zhang D, Pan X, et al. Toxic effects of mercury on PSI and PSII activities, membrane potential and transthylakoid proton gradient in Microsorium pteropus [J]. Journal of Photochemistry and Photobiology B:Biology, 2013(127): 1-7. doi: 10.1016/j.jphotobiol.2013.07.012
[14] Singh R, Dubey G, Singh V P, et al. High light intensity augments mercury toxicity in cyanobacterium nostoc muscorum [J]. Biological Trace Element Research, 2012, 149(2): 262-272. doi: 10.1007/s12011-012-9421-x
[15] Patra M, Bhowmik N, Bandopadhyay B, Sharma, et al. Comparison of mercury, lead and arsenic with respect to genotoxic effects on plant systems and the development of genetic tolerance [J]. Environmental and Experimental Botany, 2004, 52(3): 199-223. doi: 10.1016/j.envexpbot.2004.02.009
[16] Hoober J K. The chlamydomonas sourcebook [J]. Science, 1989, 246(4936): 1503-1504. doi: 10.1126/science.246.4936.1503.b
[17] 谢传晓, 韩伟, 余增亮. 模式生物衣藻及其研究进展 [J]. 遗传, 2003, 25(3): 350-354. doi: 10.16288/j.yczz.2003.03.025 Xie C X, Han W, Yu Z L. Progress of Chlamydomonas as a model organism [J]. Hereditas, 2003, 25(3): 350-354. doi: 10.16288/j.yczz.2003.03.025
[18] Lichtenthaler H K, Wellburn A R. Determinations of total carotenoids and chlorophylls a and b of leaf extracts in different solvents [J]. Biochemical Society Transactions, 1983, 11(5): 591-592. doi: 10.1042/bst0110591
[19] Lu N, Wei D, Jiang X L, et al. Fatty acids profiling and biomarker identification in snow alga Chlamydomonas nivalis by NaCl stress using GC/MS and multivariate statistical analysis [J]. Analytical Letters, 2012, 45(10): 1172-1183. doi: 10.1080/00032719.2012.673094
[20] Strasser R, Srivastava A, Tsimilli-Michael M. The fluorescence transient as a tool to characterize and screen photosynthetic samples [J]. Probing Photosynthesis Mechanisms Regulation and Adaptation, 2000(25): 445-483.
[21] Strasser R J, Tsimilli-Michael M, Srivastava A. Analysis of the Chlorophyll a Fluorescence Transient [M]. Chlorophyll a Fluorescence. Dordrecht: Springer, 2004: 321-362.
[22] Chen K, Chen L, Fan J, et al. Alleviation of heat damage to photosystem II by nitric oxide in tall fescue [J]. Photosynthesis Research, 2013, 116(1): 21-31. doi: 10.1007/s11120-013-9883-5
[23] 刘璐, 闫浩, 夏文彤, 等. 镉对铜绿微囊藻和斜生栅藻的毒性效应 [J]. 中国环境科学, 2014, 34(2): 478-484. Liu L, Yan H, Xia W T, et al. Toxic effect of cadmium on Microcysis aeruginosa and Scenedesmus obliquus [J]. China Environmental Science, 2014, 34(2): 478-484.
[24] 陶虎春, 阳赛, 丁凌云, 等. 两种赤潮藻对汞富集和甲基化影响的研究 [J]. 北京大学学报(自然科学版), 2019, 55(4): 709-716. Tao H C, Yang S, Ding L Y, et al. Study on the effect of two red-tide algae on mercury biocondensation and methylation [J]. Acta Scientiarum Naturalium Universitatis Pekinensis, 2019, 55(4): 709-716.
[25] 王文欣, 饶本强. 实验室条件下Hg2+胁迫对集球藻生理生化特性的影响 [J]. 信阳农业高等专科学校学报, 2012, 22(3): 92-96. Wang W X, Rao B Q. Study on the physiological and biochemical properties of Palmellococcus sp. subjected to Hg2+ stress in laboratory condition [J]. Journal of Xinyang Agricultural College, 2012, 22(3): 92-96.
[26] Wu Y, Zeng Y, Qu J A Y, et al. Mercury effects on Thalassiosira weissflogii: applications of two-photon excitation chlorophyll fluorescence lifetime imaging and flow cytometry [J]. Aquatic Toxicology, 2012(110/111): 133-140. doi: 10.1016/j.aquatox.2012.01.003
[27] Nowicka B, Pluciński B, Kuczyńska P, et al. Physiological characterization of Chlamydomonas reinhardtii acclimated to chronic stress induced by Ag, Cd, Cr, Cu and Hg ions [J]. Ecotoxicology and Environmental Safety, 2016(130): 133-145. doi: 10.1016/j.ecoenv.2016.04.010
[28] Wu Y, Wang W X. Differential acclimation of a marine diatom to inorganic mercury and methylmercury exposure [J]. Aquatic Toxicology, 2013(138/139): 52-59. doi: 10.1016/j.aquatox.2013.04.012
[29] Jamla M, Khare T, Joshi S, et al. Omics approaches for understanding heavy metal responses and tolerance in plants [J]. Current Plant Biology, 2021(27): 100-213.
[30] Zushi K, Kajiwara S, Matsuzoe N. Chlorophyll a fluorescence OJIP transient as a tool to characterize and evaluate response to heat and chilling stress in tomato leaf and fruit [J]. Scientia Horticulturae, 2012(148): 39-46. doi: 10.1016/j.scienta.2012.09.022
[31] Strasser R J, Tsimilli-Michael M, Qiang S, et al. Simultaneous in vivo recording of prompt and delayed fluorescence and 820-nm reflection changes during drying and after rehydration of the resurrection plant Haberlea rhodopensis [J]. Biochimica et Biophysica Acta (BBA)- Bioenergetics, 2010, 1797(6/7): 1313-1326.
[32] Rai L C, Singh A K, Mallick N. Studies on photosynthesis, the associated electron transport system and some physiological variables of Chlorella vulgaris under heavy metal stress [J]. Journal of Plant Physiology, 1991, 137(4): 419-424. doi: 10.1016/S0176-1617(11)80310-X
[33] Zhang X, Ma F, Zhu X, et al. The acceptor side of photosystem Ⅱ is the initial target of nitrite stress in Synechocystis sp. strain PCC 6803 [J]. Applied and Environmental Microbiology, 2017, 83(3): 2916-2952.
[34] Che X, Ding R, Li Y, et al. Mechanism of long-term toxicity of CuO NPs to microalgae [J]. Nanotoxicology, 2018, 12(8): 923-939. doi: 10.1080/17435390.2018.1498928
[35] Hakala M, Tuominen I, Keränen M, et al. Evidence for the role of the oxygen-evolving manganese complex in photoinhibition of Photosystem II [J]. Biochimica et Biophysica Acta (BBA)- Bioenergetics, 2005, 1706(1/2): 68-80.
[36] Strasser B J. Donor side capacity of Photosystem Ⅱ probed by chlorophyll a fluorescence transients [J]. Photosynthesis Research, 1997, 52(2): 147-155. doi: 10.1023/A:1005896029778
[37] Xia J, Li Y, Zou D. Effects of salinity stress on PSⅡ in Ulva lactuca as probed by chlorophyll fluorescence measurements [J]. Aquatic Botany, 2004, 80(2): 129-137. doi: 10.1016/j.aquabot.2004.07.006
[38] Pan X, Deng C, Zhang D, et al. Toxic effects of amoxicillin on the photosystem Ⅱ of Synechocystis sp. characterized by a variety of in vivo chlorophyll fluorescence tests [J]. Aquatic Toxicology, 2008, 89(4): 207-213.
[39] 许萍萍, 涂晓杰, 成凤凤, 等. 庆大霉素对斜生栅藻生长与光合活性的影响 [J]. 环境科学与技术, 2021, 44(8): 146-153. Xu P P, Tu X J, Cheng F F, et al. Toxic effects of gentamicin on growth and activity of photosynthetic system Ⅱ of Scenedesmus obliquus [J]. Environmental Science & Technology, 2021, 44(8): 146-153.
[40] Ralph P J, Gademann R. Rapid light curves: a powerful tool to assess photosynthetic activity [J]. Aquatic Botany, 2005, 82(3): 222-237. doi: 10.1016/j.aquabot.2005.02.006
[41] Deblois C P, Dufresne K, Juneau P. Response to variable light intensity in photoacclimated algae and cyanobacteria exposed to atrazine [J]. Aquatic Toxicology, 2013(126): 77-84. doi: 10.1016/j.aquatox.2012.09.005
[42] Platt T, Gallegos C L, Harrison W G. Photoinhibition of photosynthesis in natural assemblages of marine-phytoplankton [J]. Journal of Marine Research, 1980, 38(4): 687-701.
[43] 夏建荣, 邹定辉. 利用OJIP叶绿素a荧光评估干出对石莼(Ulva lactuca)光系统Ⅱ的影响 [J]. 海洋通报, 2007, 149(4): 50-55. Xia J R, Zhou D H. Assessing the effect of drying out on Ulva lactuca photosystem Ⅱ using OJIP chlorophyll a fluorescence (Ulva lactuca) photosystem Ⅱ using OJIP chlorophyll a fluorescence assessment [J]. Marine Science Bulletin, 2007, 149(4): 50-55.
[44] 夏亦雪, 许萍萍, 阮港, 等. 汞对雪衣藻光合系统Ⅱ及能量分配的影响 [J]. 生态毒理学报, 2023, 18(3): 388-397. doi: 10.7524/AJE.1673-5897.20220919002 Xia Y X, Xu P P, Ruan G, et al. Toxic effects of mercury on photosynthetic system Ⅱ and energy allocation in Chlamydomonas nivalis [J]. Asian Journal of Ecotoxicology, 2023, 18(3): 388-397. doi: 10.7524/AJE.1673-5897.20220919002
[45] 梁英, 冯力霞, 田传远, 等. 盐胁迫对塔胞藻生长及叶绿素荧光动力学的影响 [J]. 中国海洋大学学报(自然科学版), 2006, 36(5): 726-732. doi: 10.16441/j.cnki.hdxb.2006.05.011 Liang Y, Feng L X, Tian C Y, et al. Effects of salt stress on the growth and chlorophyll fluorescence of Pyramidomonas sp [J]. Periodical of Ocean University of China, 2006, 36(5): 726-732. doi: 10.16441/j.cnki.hdxb.2006.05.011



 下载:
下载: