INDUCTION OF MEIOGYNOGENESIS IN MONOPTERUS ALBUS AND GENETIC HOMOZYGOSITY ANALYSIS OF THE GYNOGENIC OFFSPRING
-
摘要:
为了培育性状优良、遗传稳定的黄鳝(Monopterus albus)群体, 研究探索了人工诱导黄鳝减数分裂雌核发育方法。针对养殖性状优良的深黄大斑鳝进行种质纯合, 创制出3个深黄大斑鳝雌核发育群体。流式细胞术和染色体计数分析表明雌核发育黄鳝的细胞DNA含量、染色体数目均与野生型相同。性腺组织学切片观察表明雌核发育黄鳝卵巢发育正常。微卫星多样性分析表明雌核发育黄鳝群体的有效等位基因(Ne)、平均香农指数(I)、平均多态信息指数(PIC)、平均观测杂合度(Ho)及平均期望杂合度(He)等参数均极显著低于野生群体, 雌核发育群体的遗传纯合度显著提高。雌核发育群体之间的遗传距离增大, 遗传相似系数变小。深黄大斑鳝雌核发育群体为培育性状优良的黄鳝养殖品种提供了育种材料。
Abstract:Swamp eel (Monopterus albus) is an important freshwater culture fish in China and has the characteristic of hermaphroditism and natural sexual reversal. Currently, there is a lack of artificial varieties within swamp eel cultivation, and the fry of mainly rely on the wild catching. Gynogenesis, a method for rapidly obtaining fish population with stable heredity and excellent character, was explored in this study. Meiogynogenesis induction was established in swamp eel, resulting in the creation of three gynogenic populations characterized by deep-yellow coloration. Flow cytometry analysis showed that the cellular DNA contents of gynogenic eels were consistent with those of wild type fish, and chromosome counting confirmed the diploid nature with 48 chromosomes. Histological analysis demonstrated the development of ovaries in the gonads of gynogenic eels, indicating normal diploid functionality. Microsatellite diversity analysis showed that the effective number of alleles (Ne), Shannon’s information index (I), polymorphism information content (PIC), observed heterozygosity (Ho) and expected heterozygosity (He) in gynogenic eels were significantly lower than those in the wild population. The genetic homozygosity in gynogenetic eels exhibited a significant improvement. The genetic distance increased and the genetic similarity decreased between gynogenetic groups. In summary, the gynogenetic population of the deep-yellow swamp eels provides new materials for breeding excellent varieties.
-
Keywords:
- Meiogynogenesis /
- Microsatellite /
- Genetic homozygosity /
- Variety breeding /
- Monopterus albus
-
黄鳝(Monopterus albus)是我国重要的淡水名优养殖对象, 养殖年产量达31.4万吨(2022年中国渔业统计年鉴)。黄鳝生长速度快、肉味鲜美、营养价值高, 深受东亚地区居民喜爱[1, 2]。黄鳝具有雌雄同体天然性逆转的繁殖特性, 雌鱼怀卵量少, 雄鱼性成熟周期长。黄鳝全人工繁育困难, 迄今没有人工培育的养殖品种。黄鳝养殖的苗种还主要依赖捕捞野生幼鱼, 过度捕捞导致野生资源破坏严重[3]。黄鳝养殖业的可持续发展迫切需要建立种质创制技术, 为培育优良性状的养殖品种提供技术支撑。
由于生存环境及遗传因素的影响, 自然界有多种类群的黄鳝, 其最明显的外部特征是具备不同的体色和花斑。深黄大斑鳝、浅黄细斑鳝和青灰鳝是3种体色花斑差异较大黄鳝类群。深黄大斑鳝体色深黄, 背部有3列黑褐色带状斑点, 腹部无花纹; 浅黄细斑鳝体色浅黄, 背部分布黑褐色不规则的斑点, 腹部花纹较浅; 青灰鳝体色青灰, 全身分布有黑褐色不规则的小斑点[4, 5]。不同体色和花斑黄鳝的生长速度、繁殖力、营养价值存在差异。已有研究表明深黄大斑鳝生长速度、繁殖力显著高于浅黄细斑鳝和青灰鳝[4, 6, 7]。深黄大斑鳝肌肉中必需氨基酸和二十碳五烯酸等脂肪酸含量高于浅黄色细斑鳝和青灰鳝[8]。因而, 深黄大斑鳝是人工养殖的优质类群。自然界的深黄大斑鳝群体通常与其他类群杂交, 遗传背景较杂, 自交后代性状遗传不稳定。纯化野生深黄大斑鳝的优良性状, 筛选获得遗传稳定的群体, 可为培育优秀的黄鳝养殖品种奠定基础。
雌核发育是快速纯化鱼类种质的有效方法。人工诱导鱼类雌核发育通常是指采用紫外照射灭活的异源精子刺激卵子发育, 冷(或热)激处理诱导染色体加倍而成二倍体子代的单性繁殖方式。雌核发育具有操作简便、诱导效率高等特点, 成为快速提高鱼类遗传纯合度及固定母本性状的有效手段[9]。采用人工诱导雌核发育技术先后培育出了建鲤[10]、大黄鱼“闽优1号”[11]、长丰鲢[12]、牙鲆 “北鲆1号”和“北鲆2号”[13]、翘嘴鳜“武农1号” (2022水产新品种推广指南)等养殖鱼类新品种。微卫星分子标记具有高多态性、共显性和简单孟德尔遗传方式的特点, 是分析鱼类雌核发育群体遗传纯合度的高效方法。采用微卫星分子标记检测表明牙鲆、裸腹鲟和鳙等雌核发育群体遗传多态性显著下降, 纯合度提高[9, 13, 14]。
本团队在突破黄鳝人工催产繁殖技术获得高质量胚胎的基础上, 建立了高效特异的黄鳝基因编辑技术[15], 并探索了黄鳝有丝分裂雌核发育技术[16]。黄鳝有丝分裂雌核发育的难度非常大, 雌核发育胚胎的存活率较低。本研究建立了黄鳝高效的减数分裂雌核发育技术, 并获得了雌核发育的深黄大斑鳝群体。筛选出高多态性微卫星分子标记对雌核发育黄鳝群体进行遗传纯合度分析, 雌核发育深黄大斑鳝群体的遗传纯合度显著提高。
1. 材料与方法
1.1 实验材料
本研究采用的黄鳝亲鱼购买自武汉市白沙洲农贸市场。挑选腹部膨大、柔软有弹性、怀卵明显的雌性深黄大斑鳝。依照本团队报道的方法对雌鳝进行催产[15]。每千克体重雌鱼腹腔注射30 mg鲤脑垂体、100 µg LHRH-A2和5000 IU HCG。注射催产剂后雌鱼置于26℃水温, 效应时间预计40h。卵子成熟时腹部卵粒游离感明显, 生殖孔处剪开小口后挤出成熟卵子, 储存在干燥的玻璃皿。黄鳝雄鱼解剖性腺取出精巢, 剪碎研磨后于Hanks’精子保存液中4℃避光保存。
1.2 异源精子灭活
黄河鲤雄鱼来自中国科学院水生生物研究所水产良种基地, 鳜和泥鳅雄鱼购自武汉市白沙洲农贸市场。在每千克雄鱼胸鳍下或腹腔注射2.5 μg LHRH-A2和0.5 mg DOM催产剂。12h后挤压腹部从生殖孔处收集精液, 加入3倍体积的Hanks’精子保存液稀释, 4℃避光保存。在解剖镜下精子加水激活观察并记录精子游动时间, 确认精子的活力。异源精子采用紫外照射的方法进行灭活, 每隔5min取精子在解剖镜下观察精子活力, 紫外照射的精子加水激活游动时间降低50%时停止照射。灭活的异源精子4℃避光保存。
1.3 授精与热休克处理
将100 μL灭活的精液加入盛有30 mL曝气水的玻璃皿(直径9 cm)中, 轻轻摇匀后立即加入黄鳝卵子授精。受精卵于室温静置5min后置于40.5℃水浴中热激处理3.5min, 随后迅速转移到26℃曝气水清洗2次。受精胚置于28℃静水孵化, 此为雌核发育组。黄鳝精子与卵子授精为野生型对照组。异源精子与黄鳝卵子授精为杂交对照组。灭活异源精子与黄鳝卵子授精且不经热激处理为单倍体对照组。
1.4 受精率和孵化率统计
黄鳝卵受精后约2h完成第一次卵裂, 动物极可观察到分裂沟和大小均匀的两个细胞, 此时统计总的受精卵数目。受精后2d的胚胎发育到原肠中期, 可见胚胎50%外包, 此时统计正常发育的胚胎数目。受精后10d进入心脏搏动期, 观察统计正常发育胚胎和畸形胚胎数目。受精后2h正常分裂的胚胎数与总卵数的比例为受精率; 2d存活胚胎数与总受精卵数的比例为原肠胚率; 10d存活胚胎数与受精卵数的比例为总孵化率; 10d后发育正常的胚胎数与受精卵数的比例为正常孵化率。
1.5 倍性鉴定
参照本团队已建立的方法对雌核发育和对照组黄鳝胚胎细胞进行倍性检测[16]。受精后7—8d存活的雌核发育组正常胚胎、雌核发育组畸形胚胎、单倍体对照组胚胎、野生型对照组胚胎分别置于解剖镜下用镊子撕去卵膜、除去卵黄, 将胚胎组织转移至20 μL CyStain DNA 1Step溶液中(Sysmex Corporation), 避光环境下将胚胎充分剪碎, 移液器轻轻吹打使细胞分散。流式细胞仪(CytoFlex S)检测分析胚胎细胞DNA 相对含量。
采用滴片法对黄鳝胚胎进行染色体计数分析。受精后7—8d的胚胎在解剖镜下撕去卵膜, 转移到新鲜配制的8 mg/mL秋水仙素溶液中室温孵育3h, 使染色体停滞在有丝分裂中期。孵育后的胚胎在解剖镜下去除卵黄囊, 随后转移至1%柠檬酸钠溶液中室温低渗处理8—10min使细胞膨胀。更换1%柠檬酸钠溶液在冰上静置低渗处理20min。样品采用新鲜配制的Carnoy’s固定液(甲醇﹕冰醋酸 = 3﹕1) 4℃固定过夜。次日将胚胎沥干后转移至50 μL 50%乙酸溶液, 剪刀将胚胎剪碎后移液器充分吹打使细胞分离。随即将细胞悬液从 1.7 m 高处滴到–80℃预冷处理的载玻片上, 酒精灯上迅速烤干。附有样品的载玻片于37℃烘箱中烘烤过夜。载玻片在26℃环境下经吉姆萨染色液染色30—40min后流水充分冲洗。显微镜下观察染色体的形态并拍照。
1.6 基因组DNA提取
取母本和子代黄鳝的尾鳍组织, 采用Universal Genomic DNA Kit (Cwbio, China)试剂盒依照说明书提取基因组DNA。DNA浓度和质量使用分光光度计(Nanodrop One)进行检测。基因组DNA置于–20℃保存备用。
1.7 微卫星引物筛选
从 National Center for Biotechnology Information (NCBI)网站获取黄鳝基因组序列(NW_018127919.1)。利用SSRHunter1.3软件对黄鳝基因组进行微卫星序列筛选。采用NCBI网站上的Primer-BLAST工具对筛选获得的微卫星序列进行PCR引物设计。引物由生工生物工程(上海)股份有限公司合成。PCR扩增筛选母本黄鳝为杂合子(扩增产物凝胶电泳为两条带)的微卫星位点。微卫星引物5′端加FAM荧光染料标记用于雌核发育群体遗传多样性分析。引物筛选和遗传多样性检测的PCR反应体系为20 µL, 包括2×SYBR Green mix 10 μL, 上游引物 F (10 μmol/L) 0.5 μL, 下游引物 R (10 μmol/L)0.5 μL, DNA 模板(30—50 ng)1 μL, ddH2O补足至20 μL。反应程序如下: 95℃变性3min; 进行如下 35个循环: 95℃变性15s, 55℃退15s, 72℃延伸10s; 终延伸5min; 12℃, ∞。
1.8 雌核发育群体微卫星分析
选取体型较大、怀卵较多的深黄大斑鳝雌鱼10尾, 每尾鱼人工催产获得206—604枚成熟卵。黄鳝卵与灭活鲤精子授精5min后采用40.5℃热水浴处理3.5min诱导倍性恢复, 制备雌核发育的深黄大斑鳝群体。取雌核发育黄鳝尾组织, 抽提基因组DNA为模板, 采用筛选获得的微卫星引物PCR扩增微卫星片段。通过毛细管电泳和自动荧光扫描技术对微卫星位点重复序列片段进行多态性分型。扩增的DNA片段荧光峰谱为单峰或双峰分别表示该微卫星位点为纯合型或杂合型。采用GenAIEx6软件对各群体微卫星位点的基因分型数据分析, 计算群体的平均等位基因数(Na)、平均有效等位基因数(Ne)、平均观测杂合度(Ho)、平均期望杂合度(He)、平均香农指数(I)。采用Run cervus软件计算群体的多态信息指数(PIC)。采用popGENE软件对群体进行聚类分析。
1.9 性腺组织学切片分析
雌核发育黄鳝和野生对照组黄鳝幼鱼出膜后养殖在室内循环水系统, 以水蚯蚓开口, 随后水蚯蚓与血虫混合投喂。2、3和4月龄对雌核发育和野生对照黄鳝性腺进行组织学切片分析。黄鳝经 MS-222 (90 mg/L)浸泡麻醉后, 解剖取出性腺于波恩试液中固定10h, 固定的性腺组织经乙醇梯度脱水、二甲苯透化后浸蜡包埋。组织样本用切片机制成7 μm的切片贴附到载玻片, 采用苏木精和伊红染色, 中性树胶封片。全自动数字玻片扫描仪(Leica, Aperio Versa 8, Germany)采集分析性腺切片图像。
1.10 数据处理与分析
采用Statistica 6.0软件进行数据统计分析。有效等位基因(Ne)、平均香农指数(I)、平均多态信息指数(PIC)、平均观测杂合度(Ho)和平均期望杂合度(He)均用平均值±标准误(mean±SE)展示, 单因素方差分析(one-way ANOVA)及Bonferroni事后检验分析显著性差异, 当P<0.05时认为存在显著性差异, P<0.01认为存在极显著差异。采用GraphPad Prism 8完成作图。
2. 结果
2.1 异源精子筛选
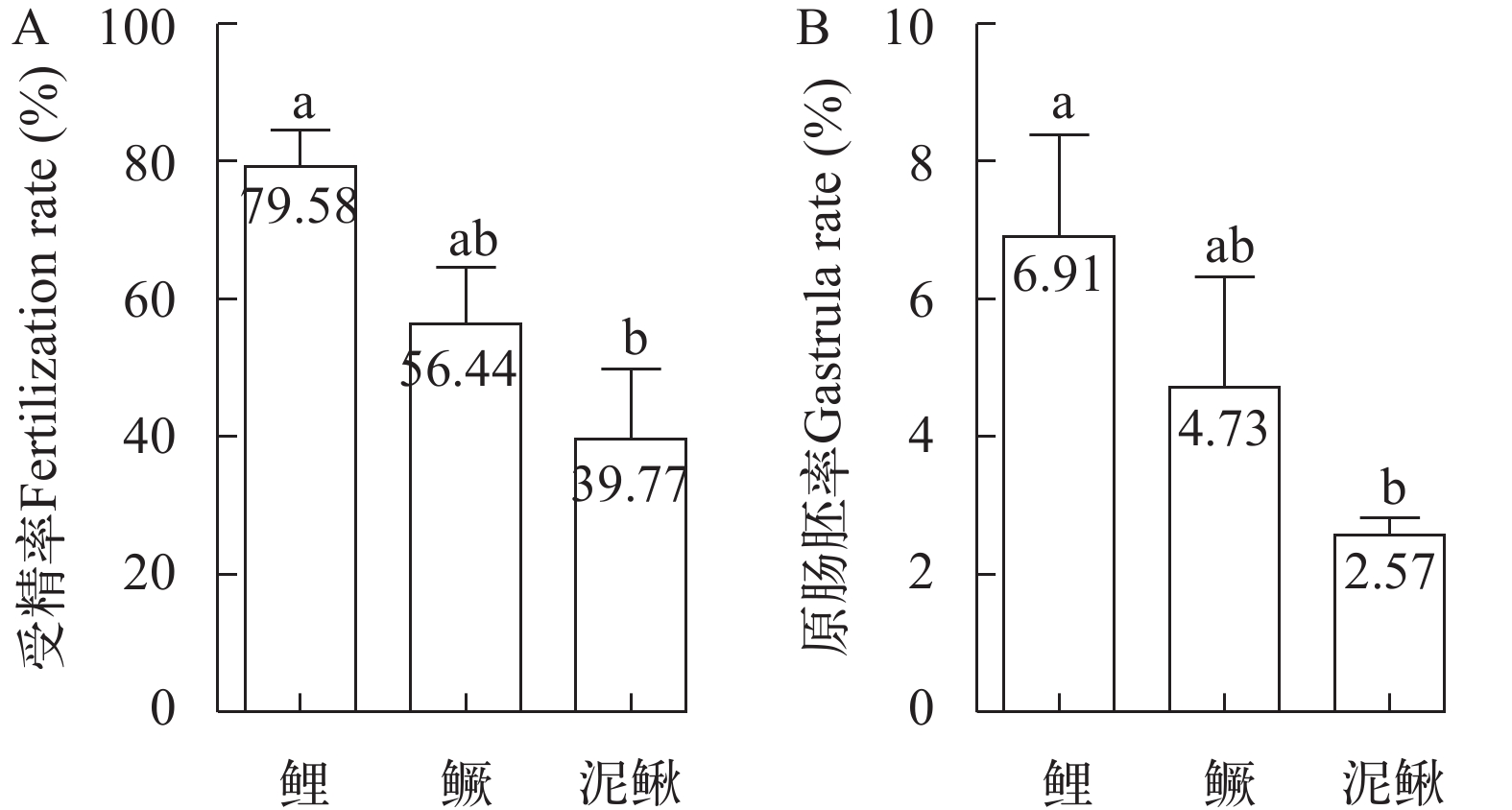
本研究比较了鲤、鳜和泥鳅灭活精子诱导黄鳝卵雌核发育的效率。灭活鲤精子、灭活鳜精子、灭活鳅精子刺激黄鳝卵子雌核发育的平均受精率分别为79.58%、56.44%和39.77%。灭活鲤精子的受精率显著高于灭活泥鳅精子, 但与灭活鳜精子差异不显著。灭活鲤精子、灭活鳜精子、灭活鳅精子诱导黄鳝卵子雌核发育到原肠胚的比例分别为6.91%、4.73%和2.57%。灭活鲤精子诱导雌核发育的效率显著高于灭活泥鳅精子, 但与灭活鳜精子差异不显著(图 1)。
2.2 灭活鲤精子刺激黄鳝卵雌核发育
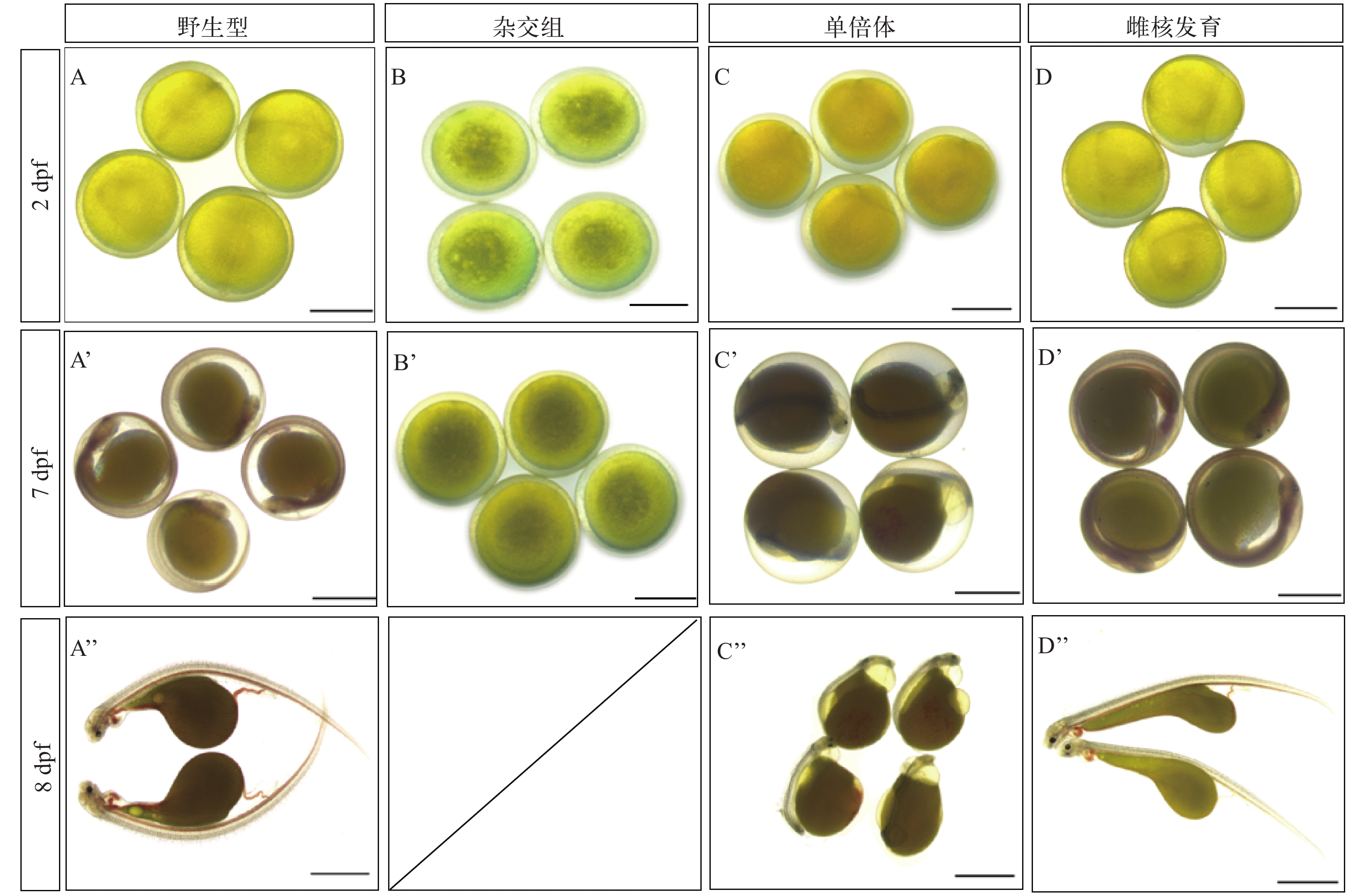
为了检测灭活鲤精子刺激黄鳝卵雌核发育胚胎发育情况, 本研究设置了黄鳝卵与黄鳝精子授精、黄鳝卵与鲤精子授精、黄鳝卵与灭活鲤精子授精、黄鳝卵与灭活鲤精子授精后热激诱导倍性恢复等对照组和雌核发育实验组。以黄鳝卵与黄鳝精子授精的野生型胚胎为参照, 受精后2d胚胎发育至体节期(Segmentation period), 受精后7d胚胎发育至孵化期(Hatching period), 第8天孵化出膜(图 2A、A’和A’’)。黄鳝卵与鲤精子无法正常受精, 胚胎不发育(图 2B和B’); 黄鳝卵与灭活的鲤精子受精, 胚胎可发育但是体节期时胚胎脊椎弯曲、血管发育异常、围心腔肿大、心脏发育畸形等特征, 胚胎无法正常出膜(图 2C、C’和C’’); 在黄鳝卵与灭活鲤精子受精后, 热激处理诱导倍性恢复的胚胎发育正常, 雌核发育黄鳝胚胎发育特征、出膜时间与野生型相同(图 2D、D’和D’’)。
2.3 雌核发育黄鳝的倍性检测
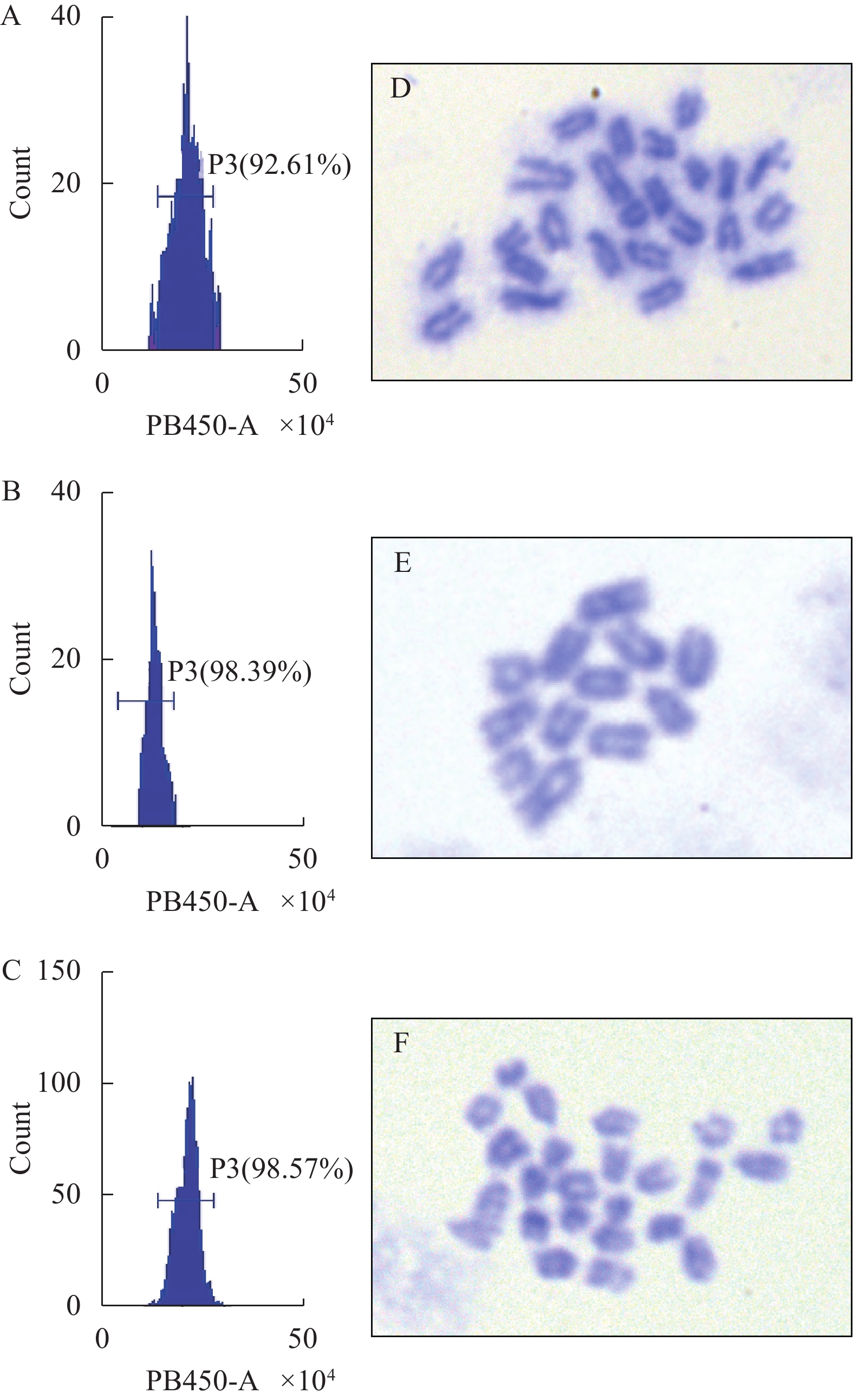
本研究采用流式细胞法和染色体计数法分析了对照组和雌核发育组黄鳝胚胎细胞的DNA含量和染色体数目。流式细胞法分析表明黄鳝卵与精子受精的野生型胚胎细胞DNA含量的PB450-A值约为20.94×104 (图 3A)。黄鳝卵与灭活鲤精子授精后不经热激处理的胚胎细胞DNA含量PB450-A值大约为12.91×104, 细胞DNA含量约为野生型的一半(图 3B)。在黄鳝卵与灭活鲤精子授精后, 再经热激处理诱导倍性恢复, 雌核发育组黄鳝胚胎中细胞DNA含量的PB450-A值为20.97×104, 雌核发育与野生对照组黄鳝胚胎细胞DNA含量相似(图 3C)。染色体计数法分析表明野生型黄鳝的染色体为24条(图 3D)。黄鳝卵与灭活鲤精子授精获得的胚胎染色体数目为12条, 证明其为单倍体(图 3E)。黄鳝卵与灭活鲤精子授精后热休克诱导倍性恢复的雌核发育黄鳝胚胎染色体数目为24条, 证明其为二倍体(图 3F)。
2.4 建立深黄大斑鳝雌核发育群体
每尾深黄大斑鳝催产获得成熟卵数存在差异, 本研究在206—604枚。卵子采用雌核发育繁殖子代。在授精后2d, 统计发育至50%外包的胚胎数为12—72枚, 受精率为2.09%—29.88%。在授精后10d, 统计发育至心搏期的胚胎数为8—52枚。发育至出膜期的幼鱼数为6—48尾, 胚胎总孵化率41.03%—76.47%。少量孵化出膜的幼鱼发育畸形, 正常幼鱼的比例为33.33%—70.59% (表 1)。本研究选取成活率最高的三个雌核发育群体Ga (16尾)、Gb (11尾)、Gc (21尾)及一个野生型对照群体WT (10尾)用于后续分析。
表 1 十尾雌性深黄大斑黄鳝雌核发育的胚胎数目、受精率和孵化率Table 1. Statistics of embryo number, fertilization rate, and hatching rate of the ten gynogenic rice-field eels组别
Group体重
Weight (g)体长
Length (cm)卵数量
No. of egg50%外包
胚胎数量
No. of 50%
epiboly embryo受精率
Fertilization
rate (%)心搏期
胚胎数量
No. of heart
pulsati embryo总孵化率
Hatching
rate (%)10d存活的
胚胎数
No. of 10
dpf embryo正常孵化率
Normal hatching
rate (%)1 96.1 42.55 420 21 5.00 13 61.90 7 33.33 2 79.9 42.5 317 32 10.09 18 56.25 13 40.63 3 95.4 45.8 319 26 8.15 12 46.15 9 34.62 4 78.4 42.0 604 39 6.46 16 41.03 15 38.46 5 63.0 40.5 241 72 29.88 30 41.67 25 34.72 6 66.3 39.0 383 48 12.53 20 41.67 17 35.42 7 147.4 48.8 573 12 2.09 8 66.67 6 50.00 8 113.7 46.4 575 68 11.83 52 76.47 48 70.59 9 104.2 42.8 206 14 6.80 9 64.29 7 50.00 10 75.6 40.0 280 54 19.29 33 61.11 28 51.85 2.5 雌核发育黄鳝性腺发育特征
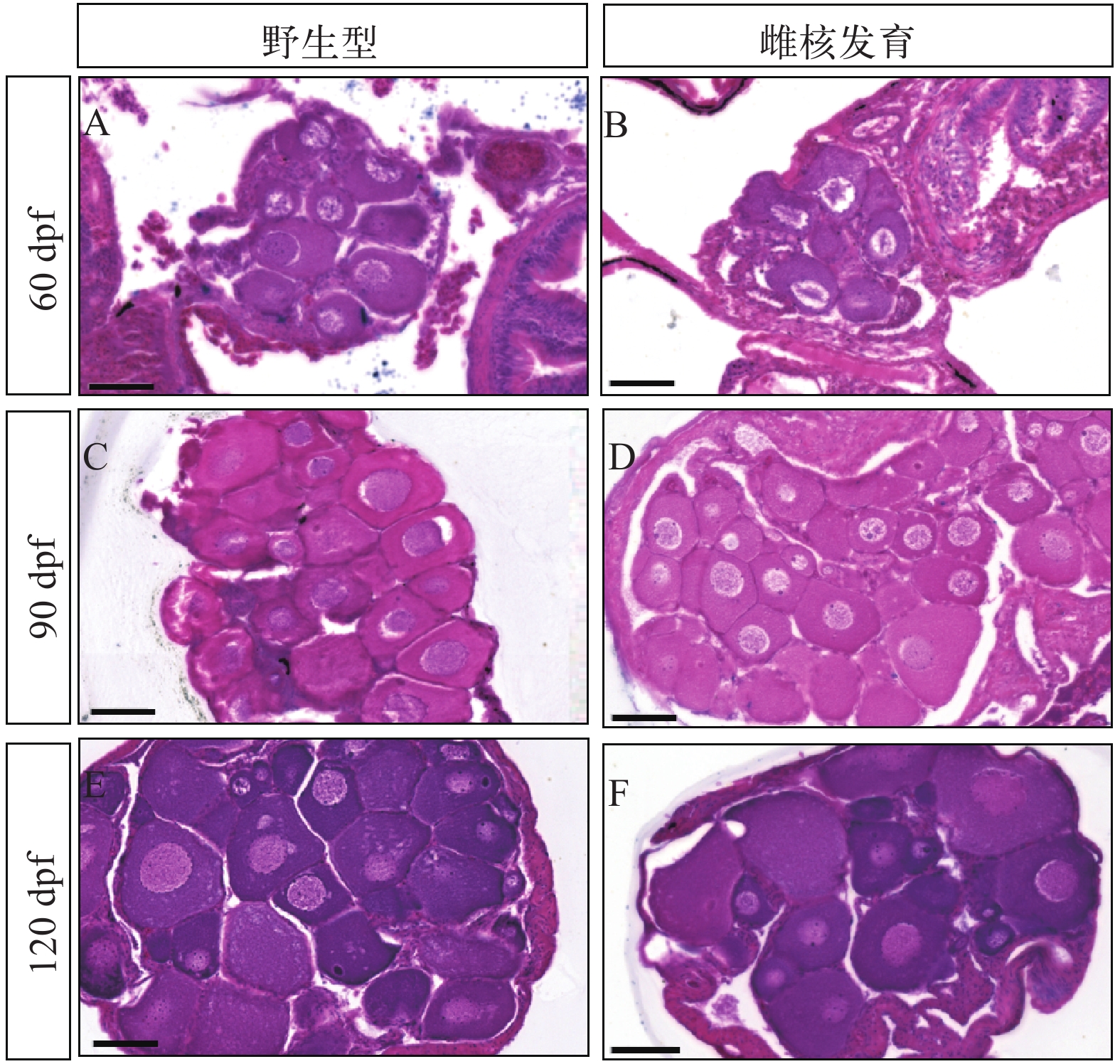
采用组织学切片对比分析了野生型和雌核发育黄鳝性腺发育特征。2月龄时野生型和雌核发育黄鳝性腺均分化为卵巢, 内部充满初级卵母细胞(图 4A和4B)。3月龄和4月龄时野生型和雌核发育黄鳝性腺内卵母细胞不断增多并充满整个卵巢(图 4C—F)。雌核发育黄鳝性腺分化发育与野生型相同, 均先发育为卵巢。
2.6 雌核发育黄鳝遗传纯合度
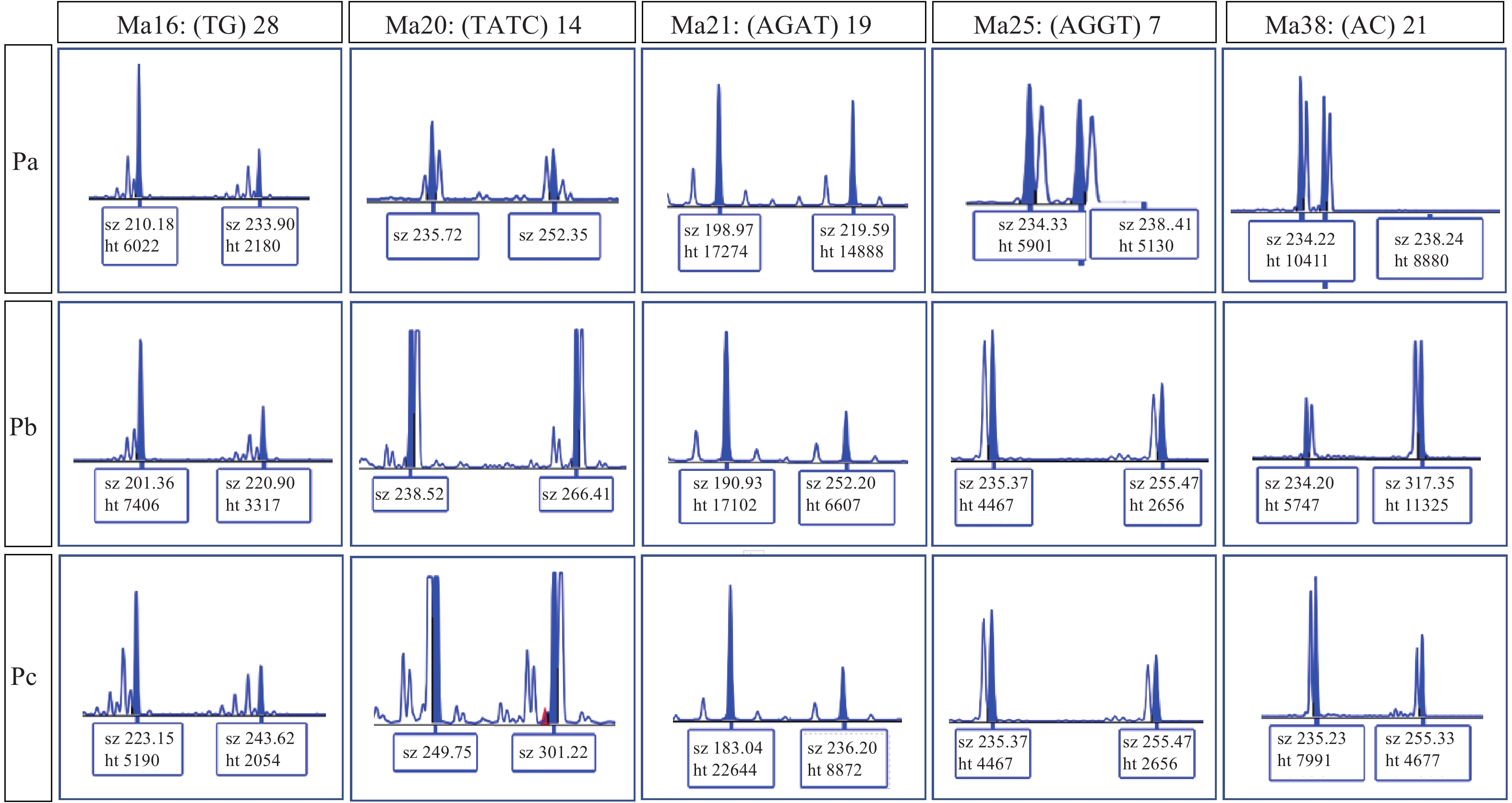
采用SSRHunter1.3软件对NCBI数据库中黄鳝基因组进行微卫星序列筛选。选取其中100个微卫星位点对雌核发育母本Pa、Pb和Pc的多态性进行分析, 筛选出 5个微卫星位点在3个母本中均具有多态性, 引物序列和微卫星重复序列如表 2。毛细管电泳和自动荧光扫描分析显示Ma16、Ma20、Ma21、Ma25和Ma38等5个微卫星位点在Pa、Pb和Pc三个亲本个体都是杂合子(图 5)。
表 2 黄鳝5个多态性微卫星标记的PCR扩增引物名称、序列及微卫星重复序列特征Table 2. The name, sequence of PCR amplification primers of 5 polymorphic STRs and repeat motif引物名称
Primer name引物序列
Primer sequence (5′—3′)核心重复
序列
Repeat motifMa16-FAM-F FAM-TTGGGGCTTTAGGGGACATA TG Ma16-FAM-R AGCAGTATTAATCTCAGCACC Ma20-FAM-F FAM-CAGGCTTCATTGCTGTTGCT TATC Ma20-FAM-R CACTTGGTATTTGCTGTCCTTGA Ma21-FAM-F FAM-CCGCTGCACCGTTTGAATTG AGAT Ma21-FAM-R ACTGCAGCTTGACTGAGCCT Ma25-FAM-F FAM-GTGGAACAGGTAGGTAGGTGA AGGT Ma25-FAM-R TGTTTGTTCTCTGTTGCTGCTT Ma38-FAM-F FAM-CTTGGATCCCCTGCATCAGA AC Ma38-FAM-R TTAGGTTCAGGCAAGTGGTGG 采用该5个微卫星位点对雌核发育群体进行遗传纯合度分析。Ga、Gb、Gc和WT四个群体的平均有效等位基因数(Ne)分别为1.969、1.879、1.701和3.121, 雌核发育群体的平均有效等位基因数目显著低于野生型群体。平均香农指数(I)分别为0.685、0.657、0.602和1.18, 雌核发育群体的平均香农指数显著低于野生型。平均多态信息指数(PIC)分别为0.371、0.356、0.327和0.604, 雌核发育群体多态信息指数显著低于野生型。平均观测杂合度(Ho)分别为0、0.350、0.010和0.880, 雌核发育群体也显著低于野生型(表 3)。微卫星位点多样性分析表明3个雌核发育群体的遗传多样性相较于野生型明显降低。
表 3 雌核发育群体(Ga、Gb和Gc)与野生群体(WT)5个微卫星位点遗传多样性参数Table 3. Genetic diversity parameters of the five SRT loci in gynogenetic (Ga, Gb and Gc) and wild type (WT) rice-field eels雌核发育群体Ga 雌核发育群体Gb 雌核发育群体Gc 野生群体WT N Na Ne I PIC Ho He N Na Ne I PIC Ho He N Na Ne I PIC Ho He N Na Ne I PIC Ho He Ma16 16 2 1.969 0.685 0.371 0 0.508 12 2 2 0.693 0.375 0.167 0.522 21 2 1.69 0.598 0.325 0 0.418 10 4 3.704 1.345 0.68 1 0.768 Ma20 16 2 1.969 0.685 0.371 0 0.508 12 2 2 0.693 0.375 0.167 0.522 21 2 1.69 0.598 0.325 0 0.418 10 4 3.704 1.345 0.68 1 0.768 Ma21 16 2 1.969 0.685 0.371 0 0.508 12 2 1.986 0.69 0.373 0.25 0.518 21 2 1.747 0.619 0.336 0.048 0.438 10 4 3.704 1.345 0.68 1 0.768 Ma25 16 2 1.969 0.685 0.371 0 0.508 12 2 1.704 0.604 0.328 0.583 0.431 21 2 1.69 0.598 0.325 0 0.418 10 3 2.247 0.938 0.491 0.7 0.584 Ma38 16 2 1.969 0.685 0.371 0 0.508 12 2 1.704 0.604 0.328 0.583 0.431 21 2 1.69 0.598 0.325 0 0.418 10 3 2.247 0.938 0.491 0.7 0.584 Mean 16 2 1.969 0.685 0.371 0 0.508 12 2 1.879 0.657 0.356 0.35 0.485 21 2 1.701 0.602 0.327 0.01 0.422 10 3.6 3.121 1.182 0.604 0.88 0.695 SE 0 0 0 0 0 0 0 0 0 0.071 0.022 0.025 0.096 0.022 0 0 0.011 0.004 0.005 0.01 0.004 0 0.245 0.357 0.1 0.104 0.073 0.045 注: He. 期望杂合度(Expected heterozygosity); Ho. 观测杂合度(Observed heterozygosity); I. 香农指数(Shannon’s information index); N. 样本数(Number of samples); Na. 等位基因数(Number of different alleles); Ne. 有效等位基因数(Number of effective alleles); PIC. 多态信息指数(Polymorphism information content)。Ma16、Ma20、Ma21、Ma25和Ma38表示5个微卫星位点; Mean. 平均值; SE. 标准误 2.7 雌核发育群体纯合性与遗传分化分析
本研究分析了雌核发育和野生型群体中5个微卫星位点纯合子数目及比例。Ga雌核发育群体中所有个体的5个微卫星位点均为纯合子, 比例为100%; Gb雌核发育群体中微卫星位点纯合子比例为63.84%; Gc雌核发育群体中微卫星位点纯合子比例为99.05%; 野生型群体中微卫星位点的纯合子比例为12% (表 4)。雌核发育群体的纯合子比例相较于野生型显著提高。本研究继续分析了3个雌核发育群体和野生型群体遗传距离和遗传相似指数(表 5)。雌核发育群体间遗传距离增加, 遗传相似指数降低。雌核发育Gc群体与WT群体来自相同的母本, 因而遗传距离最小, 遗传相似系数最大。这表明雌核发育黄鳝群体产生了明显的遗传分化。
表 4 雌核发育群体(Ga、Gb和Gc)及野生群体(WT)中微卫星位点纯合型个体数目和比例Table 4. The number and proportion of homozygotes in the five SRT loci of gynogenetic (Ga, Gb and Gc) and wild type (WT) rice-field eel微卫星位点
SRT locus雌核发育
群体Ga雌核发育
群体Gb雌核发育
群体Gc野生群体
WT数目 比例
(%)数目 比例
(%)数目 比例
(%)数目 比例
(%)Ma16 16/16 100 10/12 83.33 21/21 100 0/10 0 Ma20 16/16 100 10/12 83.33 21/21 100 0/10 0 Ma21 16/16 100 9/12 69.23 20/21 95.24 0/10 0 Ma25 16/16 100 5/12 41.66 21/21 100 3/10 30 Ma38 16/16 100 5/12 41.66 21/21 100 3/10 30 平均值Mean 100 63.84 99.05 12 表 5 雌核发育群体(Ga、Gb和Gc)与野生群体(WT)间遗传距离(对角线上)和遗传相似系数(对角线下)Table 5. Genetic distance (upper right) and genetic identity (lower left) among gynogenetic (Ga, Gb and Gc) and wild type (WT) rice-field eelsGa Gb Gc WT — 1.402 0.954 0.861 Ga 0.246 — 0.992 0.847 Gb 0.385 0.371 — 0.182 Gc 0.423 0.429 0.833 — WT 3. 讨论
本研究建立了黄鳝高效的减数分裂雌核发育技术, 获得了3个深黄大斑鳝雌核发育群体。筛选出遗传多样性高的微卫星位点对雌核发育黄鳝群体进行遗传纯合度分析, 雌核发育黄鳝种质纯合度显著提高。黄鳝雌核发育性腺发育与野生型相同, 可育的雌核发育黄鳝为遗传稳定的良种培育提供材料。
筛选高效刺激雌核发育的异源精子是建立黄鳝雌核发育技术的重要条件。采用异源精子刺激雌核发育时常常导致无法授精或产生杂交子代。因而, 雌核发育所需的异源精子既可以刺激卵子授精又不产生存活的杂交子代或杂交子代形态特征与雌核发育子代存在明显差异[17]。本团队前期在分析泥鳅受精卵第二极体排出细胞学观察的基础上, 筛选灭活鲤精子可高效诱导泥鳅雌核发育。建立泥鳅减数分裂雌核发育技术, 培育出全雌群体[18]。本研究比较了鲤、鳜、泥鳅等异源精子刺激黄鳝卵雌核发育的效果。尽管灭活鲤、鳜、泥鳅精子均可诱导黄鳝雌核发育, 但灭活鲤精子诱导黄鳝卵雌核发育的效率最高。正常鲤精子与黄鳝卵杂交无法产生存活的胚胎。灭活鲤精子与黄鳝卵子授精的杂交胚胎为单倍体, 无法正常发育出膜。因此, 灭活鲤精子是高效刺激黄鳝雌核发育的异源精子。本研究采用黄鳝卵授精后40.5℃水浴热休克处理3.5min以抑制第二极体排出以诱导染色体二倍化[19]。流式细胞法分析雌核发育黄鳝胚胎细胞DNA含量与野生二倍体相同。细胞染色体计数分析表明雌核发育黄鳝的染色体数目为24条。这表明雌核发育黄鳝为正常二倍体。
深黄大花斑黄鳝的生长速度和繁殖力均具有较明显的优势[4, 6], 是自然界中优质的黄鳝类群。纯化野生深黄大花斑黄鳝种质, 可为培育遗传稳定的优良黄鳝养殖品种奠定基础。雌核发育是快速获得高遗传纯合度鱼类群体的有效方法, 连续三代雌核发育即可建立近交系[20]。本研究采用减数分裂雌核发育技术获得了3个深黄大斑黄鳝第一代雌核发育群体, 筛选出亲本中都是杂合子的5个微卫星位点用于雌核发育群体遗传纯合度分析。微卫星多态性分析表明雌核发育黄鳝子代群体的遗传多样性相对于野生型群体明显降低, 雌核发育群体的遗传纯合度显著提高。但是, 雌核发育黄鳝子代群体中还是出现部分微卫星位点杂合子的现象。利用微卫星标记对兰州鲇减数分裂雌核发育后代的遗传纯合度进行分析, 也表明雌核发育组的纯合性(0.63)高于正常对照组(0.32)[21]。鳙减数分裂雌核发育群体利用微卫星标记分析表明一代雌核发育群体和二代雌核发育群体的杂合度分别比F0亲本降低了42%和60%[9]。微卫星分子标记分析表明雌核发育可以显著提升子代的遗传纯合度, 但一代雌核发育无法获得高纯合度的群体。减数分裂雌核发育群体中出现杂合现象的原因可能减数分裂过程中产生同源染色体的联会和交换, 杂合程度与染色体交换次数相关[22]。本研究第一雌核发育群体遗传纯合度显著提高, 但是获得遗传稳定的黄鳝种质需要进行二次甚至多次雌核发育。
性腺组织学分析表明雌核发育黄鳝性腺先发育为卵巢, 性腺发育特征与野生型相同。雌核发育黄鳝可具备生殖能力。黄鳝雌雄同体、先雌后雄的繁殖特性导致黄鳝雌雄亲本发育不同步, 本研究获得的雌核发育群体难以通过家系内自行繁殖子代。本团队前期建立了人工诱导黄鳝雄性定向发育技术, 可将1年龄的黄鳝培育为具生殖功能的雄鱼[23]。此外, 本团队建立了黄鳝高效基因编辑技术, P0代可获得基因功能缺少的个体[24]。因而, 遗传纯合度显著提高的黄鳝雌核发育技术、雄性定向发育技术和高效基因编辑技术相结合将为黄鳝优良种质创制及养殖新品种培育提供重要的技术支撑。
-
表 1 十尾雌性深黄大斑黄鳝雌核发育的胚胎数目、受精率和孵化率
Table 1 Statistics of embryo number, fertilization rate, and hatching rate of the ten gynogenic rice-field eels
组别
Group体重
Weight (g)体长
Length (cm)卵数量
No. of egg50%外包
胚胎数量
No. of 50%
epiboly embryo受精率
Fertilization
rate (%)心搏期
胚胎数量
No. of heart
pulsati embryo总孵化率
Hatching
rate (%)10d存活的
胚胎数
No. of 10
dpf embryo正常孵化率
Normal hatching
rate (%)1 96.1 42.55 420 21 5.00 13 61.90 7 33.33 2 79.9 42.5 317 32 10.09 18 56.25 13 40.63 3 95.4 45.8 319 26 8.15 12 46.15 9 34.62 4 78.4 42.0 604 39 6.46 16 41.03 15 38.46 5 63.0 40.5 241 72 29.88 30 41.67 25 34.72 6 66.3 39.0 383 48 12.53 20 41.67 17 35.42 7 147.4 48.8 573 12 2.09 8 66.67 6 50.00 8 113.7 46.4 575 68 11.83 52 76.47 48 70.59 9 104.2 42.8 206 14 6.80 9 64.29 7 50.00 10 75.6 40.0 280 54 19.29 33 61.11 28 51.85 表 2 黄鳝5个多态性微卫星标记的PCR扩增引物名称、序列及微卫星重复序列特征
Table 2 The name, sequence of PCR amplification primers of 5 polymorphic STRs and repeat motif
引物名称
Primer name引物序列
Primer sequence (5′—3′)核心重复
序列
Repeat motifMa16-FAM-F FAM-TTGGGGCTTTAGGGGACATA TG Ma16-FAM-R AGCAGTATTAATCTCAGCACC Ma20-FAM-F FAM-CAGGCTTCATTGCTGTTGCT TATC Ma20-FAM-R CACTTGGTATTTGCTGTCCTTGA Ma21-FAM-F FAM-CCGCTGCACCGTTTGAATTG AGAT Ma21-FAM-R ACTGCAGCTTGACTGAGCCT Ma25-FAM-F FAM-GTGGAACAGGTAGGTAGGTGA AGGT Ma25-FAM-R TGTTTGTTCTCTGTTGCTGCTT Ma38-FAM-F FAM-CTTGGATCCCCTGCATCAGA AC Ma38-FAM-R TTAGGTTCAGGCAAGTGGTGG 表 3 雌核发育群体(Ga、Gb和Gc)与野生群体(WT)5个微卫星位点遗传多样性参数
Table 3 Genetic diversity parameters of the five SRT loci in gynogenetic (Ga, Gb and Gc) and wild type (WT) rice-field eels
雌核发育群体Ga 雌核发育群体Gb 雌核发育群体Gc 野生群体WT N Na Ne I PIC Ho He N Na Ne I PIC Ho He N Na Ne I PIC Ho He N Na Ne I PIC Ho He Ma16 16 2 1.969 0.685 0.371 0 0.508 12 2 2 0.693 0.375 0.167 0.522 21 2 1.69 0.598 0.325 0 0.418 10 4 3.704 1.345 0.68 1 0.768 Ma20 16 2 1.969 0.685 0.371 0 0.508 12 2 2 0.693 0.375 0.167 0.522 21 2 1.69 0.598 0.325 0 0.418 10 4 3.704 1.345 0.68 1 0.768 Ma21 16 2 1.969 0.685 0.371 0 0.508 12 2 1.986 0.69 0.373 0.25 0.518 21 2 1.747 0.619 0.336 0.048 0.438 10 4 3.704 1.345 0.68 1 0.768 Ma25 16 2 1.969 0.685 0.371 0 0.508 12 2 1.704 0.604 0.328 0.583 0.431 21 2 1.69 0.598 0.325 0 0.418 10 3 2.247 0.938 0.491 0.7 0.584 Ma38 16 2 1.969 0.685 0.371 0 0.508 12 2 1.704 0.604 0.328 0.583 0.431 21 2 1.69 0.598 0.325 0 0.418 10 3 2.247 0.938 0.491 0.7 0.584 Mean 16 2 1.969 0.685 0.371 0 0.508 12 2 1.879 0.657 0.356 0.35 0.485 21 2 1.701 0.602 0.327 0.01 0.422 10 3.6 3.121 1.182 0.604 0.88 0.695 SE 0 0 0 0 0 0 0 0 0 0.071 0.022 0.025 0.096 0.022 0 0 0.011 0.004 0.005 0.01 0.004 0 0.245 0.357 0.1 0.104 0.073 0.045 注: He. 期望杂合度(Expected heterozygosity); Ho. 观测杂合度(Observed heterozygosity); I. 香农指数(Shannon’s information index); N. 样本数(Number of samples); Na. 等位基因数(Number of different alleles); Ne. 有效等位基因数(Number of effective alleles); PIC. 多态信息指数(Polymorphism information content)。Ma16、Ma20、Ma21、Ma25和Ma38表示5个微卫星位点; Mean. 平均值; SE. 标准误 表 4 雌核发育群体(Ga、Gb和Gc)及野生群体(WT)中微卫星位点纯合型个体数目和比例
Table 4 The number and proportion of homozygotes in the five SRT loci of gynogenetic (Ga, Gb and Gc) and wild type (WT) rice-field eel
微卫星位点
SRT locus雌核发育
群体Ga雌核发育
群体Gb雌核发育
群体Gc野生群体
WT数目 比例
(%)数目 比例
(%)数目 比例
(%)数目 比例
(%)Ma16 16/16 100 10/12 83.33 21/21 100 0/10 0 Ma20 16/16 100 10/12 83.33 21/21 100 0/10 0 Ma21 16/16 100 9/12 69.23 20/21 95.24 0/10 0 Ma25 16/16 100 5/12 41.66 21/21 100 3/10 30 Ma38 16/16 100 5/12 41.66 21/21 100 3/10 30 平均值Mean 100 63.84 99.05 12 表 5 雌核发育群体(Ga、Gb和Gc)与野生群体(WT)间遗传距离(对角线上)和遗传相似系数(对角线下)
Table 5 Genetic distance (upper right) and genetic identity (lower left) among gynogenetic (Ga, Gb and Gc) and wild type (WT) rice-field eels
Ga Gb Gc WT — 1.402 0.954 0.861 Ga 0.246 — 0.992 0.847 Gb 0.385 0.371 — 0.182 Gc 0.423 0.429 0.833 — WT -
[1] Zhang J, Che C, Cai M, et al. Taurine improves health of juvenile rice field eel (Monopterus albus) fed with oxidized fish oil: Involvement of lipid metabolism, antioxidant capacity, inflammatory response [J]. Aquaculture Reports, 2022(27): 101388. doi: 10.1016/j.aqrep.2022.101388
[2] Yang D, Chen F, Ruan G, Aquaculture of the Paddy Eel, Monopteros albus: Success Stories and Modern Trends [B]. Aquaculture in China. 2018: 283-296. https://doi.org/10.1002/9781119120759.ch3_9.
[3] Liang H, Guo S, Li Z, et al. Assessment of genetic diversity and population structure of swamp eel Monopterus albus in China [J]. Biochemical Systematica and Ecology, 2016(68): 81-87. doi: 10.1016/j.bse.2016.06.006
[4] 王彦, 张世萍, 占学伟. 不同体色黄鳝繁殖力比较研究 [J]. 湖北农业科学, 2008, 47(5): 571-572. Wang Y, Zhang S P, Zhan X W. Comparative study on fecundity of Monopterus albus with different body colors [J]. Hubei Agricultural Sciences, 2008, 47(5): 571-572.
[5] 吴秀林, 丁炜东, 曹哲明, 等. 不同体色黄鳝生物学特性的研究现状及前景 [J]. 淮海工学院学报(自然科学版), 2014, 23(3): 80-87. Wu X L, Ding W D, Cao Z M, et al. Research status and prospects on biological characteristics of Monopterus albus with different colors [J]. Journal of Huaihai Institute of Technology (Natural Science Edition), 2014, 23(3): 80-87.
[6] 陈芳, 杨代勤, 苏应兵. 3种不同体色黄鳝生长速度的比较 [J]. 长江大学学报(自然科学版), 2009, 6(3): 33-34. Chen F, Yang D Q, Su Y B. Comparative study on growth speed of Monopterus albus of different body colors [J]. Journal of Yangtze University (Natural Science Edition), 2009, 6(3): 33-34.
[7] 杨代勤, 陈芳, 阮国良, 等. 3种品系黄鳝的繁殖力比较研究 [J]. 水生态学杂志, 2009, 30(4): 133-135. Yang D Q, Chen F, Ruan G L, et al. Comparative study on fecundity of different strains of Monopterus albus [J]. Journal of Hydroecology, 2009, 30(4): 133-135.
[8] 吴秀林, 丁炜东, 曹哲明, 等. 三种体色野生黄鳝肌肉营养成分的分析 [J]. 食品工业科技, 2016, 37(1): 351-355. Wu X L, Ding W D, Cao Z M, et al. Analysis of nutritive composition in muscle of wild Monopterus albus with three kinds of colors [J]. Science and Technology of Food Industry, 2016, 37(1): 351-355.
[9] Pang M, Yu X, Zhou Y, et al. Two generations of meiotic gynogenesis significantly elevate homogeneity and confirm genetic mode of sex determination in bighead carp (Hypophthalmichthys nobilis) [J]. Aquaculture, 2022(547): 737461. doi: 10.1016/j.aquaculture.2021.737461
[10] Zhang J, Doyle R W, Sun X, et al. Rapid response of Jian carp (Cyprinus carpio var. Jian) to on-farm domestication selection in China [J]. Aquaculture, 1995, 137(1/2/3/4): 277. doi: 10.1016/0044-8486(96)83572-1
[11] 赵广泰, 刘贤德, 王志勇, 等. 大黄鱼连续4代选育群体遗传多样性与遗传结构的微卫星分析 [J]. 水产学报, 2010, 34(4): 500-507. doi: 10.3724/SP.J.1231.2010.06624 Zhao G T, Liu X D, Wang Z Y, et al. Genetic structure and genetic diversity analysis of four consecutive breeding generations of large yellow croaker (Pseudosciaena crocea) using microsatellite markers [J]. Journal of Fisheries of China, 2010, 34(4): 500-507. doi: 10.3724/SP.J.1231.2010.06624
[12] 梁宏伟, 李忠, 罗相忠, 等. 长丰鲢与长江鲢形态差异与判别分析 [J]. 水生生物学报, 2015, 39(5): 1059-1064. Liang H W, Li Z, Luo X Z, et al. Morphological differences and discriminant analysis between Changfeng and Yangtze River siler carp [J]. Acta Hydrobiologica Sinica, 2015, 39(5): 1059-1064.
[13] 王桂兴, 张晓彦, 孙朝徽, 等. 牙鲆连续四代减数分裂雌核发育家系的遗传特征分析 [J]. 渔业科学进展, 2019, 40(6): 48-55. Wang G X, Zhang X Y, Sun Z H, et al. Genetic analysis of four generations of a successive meiogynogenetic population in the Japanese flounder, Paralichthys olivaceus [J]. Progress in Fishery Sciences, 2019, 40(6): 48-55.
[14] Saber M H, Noveiri S B, Pourkazemi M, et al. Induction of meiotic gynogenesis in ship sturgeon Acipenser nudiventris using UV-irradiated heterologous sperm [J]. Journal of Applied Genetics, 2014, 55(2): 223-229. doi: 10.1007/s13353-013-0188-3
[15] Feng K, Luo H, Li Y, et al. High efficient gene targeting in rice field eel Monopterus albus by transcription activator-like effector nucleases [J]. Science Bulletin, 2017, 62(3): 162-164. doi: 10.1016/j.scib.2017.01.018
[16] Luo H, Feng K, Chen J, et al. Telophase of the first cleavage is the key stage for optimally inducing mitotic gynogenesis in rice field eel (Monopterus albus) [J]. Aquaculture, 2020(523): 735241. doi: 10.1016/j.aquaculture.2020.735241
[17] 刘海金, 候吉伦, 刘奕. 牙鲆雌核发育研究进展 [J]. 中国水产科学, 2017, 24(4): 902-912. Liu H J, Hou J L, Liu Y. Gynogenesis in Japanese flounder: a review [J]. Journal of Fishery Sciences of China, 2017, 24(4): 902-912.
[18] 钟汶蓉, 陶彬彬, 徐闻, 等. 人工诱导泥鳅雌核发育的细胞学研究和诱导参数优化 [J]. 水生生物学报, 2024, 48(2): 334-341. Zhong W R, Tao B B, Xu W, et al. Cytological study on artificially induced gynogenesis and optimization of induced parameters in loach, Misgurnus anguillicaudatus [J]. Acta Hydrobiologica Sinica, 2024, 48(2): 334-341.
[19] 常重杰, 杜启艳, 卢龙斗等. 热休克诱导三倍体黄鳝的研究 [J]. 河南师范大学学报(自然科学版), 1997, 25(2): 60-63. Chang Z J, Du Q Y, Lu L D, et al. Studies on the induction of triploidy ricefield fish (Monopterus albus) [J]. Journal of Henan Normal University, 1997, 25(2): 60-63.
[20] Zhang H, Liu S J, Zhang C, et al. Induced gynogenesis in grass carp (Ctenopharyngodon idellus) using irradiated sperm of allotetraploid hybrids [J]. Marine Biotechnology, 2011, 13(5): 1017-1026. doi: 10.1007/s10126-011-9365-8
[21] Li L, Lian Z, Xiao W, et al. Induction of meiotic gynogenesis in Lanzhou catfish (Silurus lanzhouensis) with heterologous sperm and evidence for female homogamety [J]. Aquaculture Research, 2022, 53(9): 3318-3330. doi: 10.1111/are.15839
[22] Xiao J, Zou T, Chen L, et al. Microsatellite analysis of different ploidy offspring of artificial gynogenesis in Cyprinus carpio [J]. Journal of Fish Biology, 2011, 78(1): 150-165. doi: 10.1111/j.1095-8649.2010.02848.x
[23] Jiang Y, Luo H, Hou M, et al. Aromatase inhibitor induces sex reversal in the protogynous hermaphroditic rice field eel (Monopterus albus) [J]. Aquaculture, 2022(551): 737960. doi: 10.1016/j.aquaculture.2022.737960
[24] Hou M, Feng K, Luo H, et al. Multi-locus gene editing effectively knocked out cyp19a1a and foxl2 in Monopterus albus, a hermaphroditic fish [J]. Aquaculture, 2023(565): 739130. doi: 10.1016/j.aquaculture.2022.739130
-
期刊类型引用(1)
1. 宋焱龙,罗红瑞,陶彬彬,陈戟,罗大极,陈贶新,周文宗,胡炜. 黄鳝自然性逆转的遗传基础与优良种质创制研究进展. 水生生物学报. 2025(01): 123-131 .  本站查看
本站查看
其他类型引用(1)



 下载:
下载: