ESTIMATION OF THE SEAMOUNT EFFECT ON PLANKTONIC BACTERIA DIVERSITY AND DISTRIBUTION USING ENVIRONMENTAL RNA
-
摘要:
研究采用环境RNA技术探究西太平洋M4海山区细菌多样性, 并与基于环境DNA技术的研究结果进行比较, 解析细菌代谢活性特征。结果表明基于环境RNA和DNA技术检获的物种构成相似, 但真光层中蓝细菌在RNA中的占比明显高于DNA, 显示其高代谢活性; 而α变形菌在RNA中的占比明显小于DNA, 代谢活性低; γ变形菌在RNA中占比更大且随水层加深而增加。物种间关系网络复杂度随着水深的增加呈先升高后下降的趋势。基于RNA数据构建的网络较DNA数据网络简单, 且随着水深增加变化趋势更加显著, 去除蓝细菌后网络变化剧烈, 而去除α变形菌对网络影响小。综上, 研究基于环境RNA技术提供了海山区浮游细菌多样性及分布更加完整的认知, α变形菌在海山区多样性占比和其在群落中作用可能被高估。
Abstract:Seamounts are widely distributed across the ocean floor, harboring diverse and unique biological communities due to their distinctive topography and hydrodynamic environment. Previous studies utilizing environmental DNA sequencing identified cyanobacteria, gammaproteobacteria, and alphaproteobacteria as dominant taxa, playing pivotal roles in the high biodiversity observed in seamount area. However, environmental DNA can not differentiate between living or dead cells, providing an incomplete picture of the distribution of active bacteria. Environmental RNA, prone to degradation outside the cell, offers insights into the biodiversity of active taxa. We investigated the diversity of active bacteria in the M4 seamounts of the western Pacific Ocean using environmental RNA sequencing in comparison with the results of studies based on environmental DNA sequencing, comparing the results with studies based on environmental DNA sequencing. While the species composition exhibited similarities between RNA and DNA datasets, the proportion of cyanobacteria in RNA was notably higher in DNA in the euphotic zone, indicating elevated metabolic activity. Conversely, the proportion of alphaproteobacteria was significantly lower in the RNA dataset, suggesting reduced metabolic activity. Gammaproteobacteria proportions increased in the RNA dataset at greater seawater depths. The co-occurrence network showed increasing complexity followed by a decrease with rising water depth. The RNA-based network was simpler than its DNA counterpart, yet variations along the water depth were more pronounced. Removing cyanobacteria caused a drastic change in the network, whereas the removal of alphaproteobacteria had minimal impact. In conclusion, this study enhances our understanding of active bacterioplankton diversity and distribution in seamounts through environmental RNA sequencing. The proportion of alphaproteobacteria in the total bacterial community and their role in the co-occurrence network in seamounts may have been overestimated.
-
Keywords:
- Deep sea /
- Environmental RNA /
- Bacteria /
- Microbial diversity /
- Seamount effect
-
位于热带和亚热带的寡营养海域, 对全球的物质循环及生物群落结构具有重要的影响。寡营养海域真光层中无机营养含量低, 各种成分不均衡, 制约着浮游植物的生长, 进而影响着该区域的生态系统[1]。
海山是海洋中位于海平面以下、高度1000 m及以上的隆起地形[2]。按照山顶到海平面的距离可以分为浅水海山(200 m以下)、中层海山(200—400 m)及深水海山(400 m以上)三种类型[3]。海山的特殊地形和水文环境可将深层的无机营养输送到真光层, 并通过泰勒柱的影响, 使其在海山顶部维持足够长的时间, 促进浮游植物的生长, 进而提升该区域的初级生产力, 这种现象被称为“海山效应”[4, 5]。通常, 海山区域浮游生物的多样性和生物量明显高于周围环境, 可为海山区大型底栖生物提供食物, 促进“海底花园”的形成, 成为海洋生物研究的热点[6]。
细菌作为主要初级生产者, 在海山区行使重要功能。近年来, 关于海山区细菌多样性及分布的研究日益增加。前人研究表明“海山效应”可以显著提升蓝细菌的生物量。前人通过测定C4海山上的叶绿素浓度和分布, 并基于光合色素对浮游植物群落进行分析, 发现蓝细菌是DCM层的优势类群[7]。平顶海山区浮游细菌、真菌及原生动物多样性的研究也表明蓝细菌在200 m以上的水层中相对丰度较高[5, 8, 9]。
海山区域异养细菌分布和多样性研究发现, 海山区域存在丰富多样和高生物量的异养细菌[8]。其中, Y3海山30 m以浅和150 m以深异养细菌生物量占绝对优势, 75—100 m水层自养型生物占绝对优势; M2 海山75 m以浅和 200 m以深异养细菌占绝对优势, 110—150 m自养型生物占绝对优势。变形菌是异养细菌中最为重要的类群, 其中α变形菌在海山各个水层均有分布。α变形菌在西太平洋的M5深水海山的1000 m以上的水层占优势, 且随着水深的增加逐渐减少, 其中在100 m以上的水层中α变形菌的相对丰度占50%左右[9]。在海山区1000 m以深的水层, α变形菌也普遍存在。Giljgan等[10]研究发现, 滞留在北大西洋海山周围, 由深层海水形成的闭合环流——鞘流中有丰富的α变形菌, 其中SAR11是鞘流中的优势类群, 相对丰度占比约40%。
前人研究多基于环境DNA技术, 直接从环境样品中获取的DNA片段, 进行扩增和测序, 进而研究生物群落构成[11]。但环境DNA不能区分有生命或死亡状态的细胞, 无法获知海山区有代谢活性细菌的分布。而RNA在细胞外易降解, 因此环境RNA可用于研究具有代谢活性的生物多样性。M4浅水海山位于西太平洋寡营养海域, 前人研究已发现该海山处存在明显的海山效应[7]。因此以该海山作为研究目标, 可深入探究寡营养海域海山对生态系统, 尤其是生物多样性的影响。本研究采用环境RNA技术探究西太平洋M4海山区细菌多样性, 并与基于环境DNA技术的研究结果进行比较, 解析海山区主要浮游细菌类群蓝细菌、γ变形菌和α变形菌的相对比例及其代谢活性特征。
1. 材料与方法
1.1 样品采集和环境参数测量
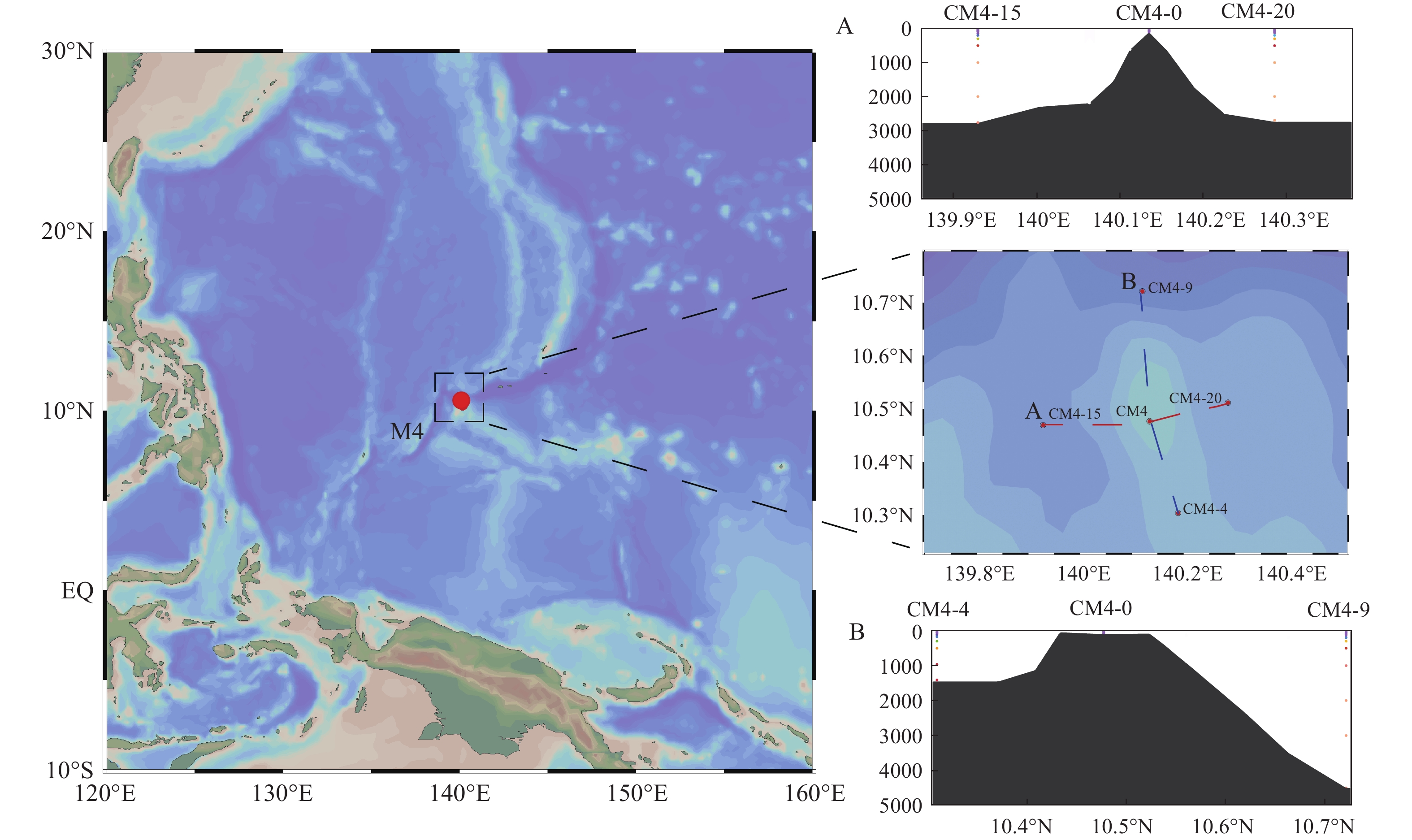
本研究样品采集于西太平洋寡营养海域的M4浅水海山(10.3°—10.7°N, 139.9°—140.3°E), 共选取5个采样点。在海山山顶, 设置采样点CM4, 并参考海流方向, 以山顶采样点为中心取十字型, 在海山周边设置4个采样点, 每个采样点根据实际水深设置垂向采样层次。其中CM4 (140.13°E—10.48°N)为山顶采样点, CM4-15 (139.93°E—10.47°N)和CM4-20 (140.29°E—10.51°N)分布于A断面, CM4-4 (140.19°E—10.30°N)和CM4-9 (140.12°E—10.72°N)分布于B断面。海山山顶与海平面的距离为57 m, CM4-9是最深的采样点, 距海平面4512 m (图 1)。
用Niskin瓶从各个站位的九个水层(3 m、叶绿素最大值层(DCM)、200、300、500、1000、2000、3000 m和底层)采集海水, 每层采集20 L。将水样先经孔径为200 μm的筛绢过滤, 再经0.22 μm的聚碳酸酯膜过滤, 将滤膜放到−80℃下冷冻保存。DCM层是根据配备荧光探针的电导率-温度-深度(CTD)剖面仪测量的荧光值确定。温度和盐度通过CTD剖面仪测量。溶氧值及无机营养(${\rm{NO}}^-_3 $-N、${\rm{NO}}^-_2 $-N、${\rm{NH}}^+_4 $-N、${\rm{PO}}^{3-}_4 $-P和${\rm{SiO}}^{3-}_3 $-Si)采用国际通用方法测量 [12, 13]。
1.2 DNA和RNA提取、PCR扩增和高通量测序
根据使用说明, 用凯杰DNA/RNA提取试剂盒(AllPrep DNA/RNA Mini Kit, Qiagen, Germany)从滤膜中提取DNA。用引物U341F和R685扩增原核微生物的16S rRNA基因 V4区。引物序列为U341F: 5′-CCTACGGGRSGCAGCAG-3′[14], R685: 5′-ATCTACGCATTTCACCGCCAC-3′[15]。PCR体系为50 μL, 包括2 μL模板DNA、1 μL正向引物、1 μL反向引物、25 μL 扩增混合液和21 μL ddH2O。PCR反应条件: 94℃预变性 5min; 94℃变性 50s, 53℃退火 50s, 72℃延伸 50s, 25 个循环; 72℃延伸 6min, 最后于4℃保存。
同时采用凯杰DNA/RNA提取试剂盒(AllPrep DNA/RNA Mini Kit, Qiagen, Germany) 从滤膜中提取RNA。提取的RNA进行纯化后, 用试剂盒将RNA逆转录成互补DNA(cDNA), 以合成的cDNA为模板, 进行上述PCR扩增。为了防止误差, 每份DNA和cDNA样本的PCR扩增重复3次, 混合, 用NEBNextUltra™ DNA试剂盒建立样品文库。测序采用 Illumina HiSeq 平台。
1.3 数据处理和统计分析
对测序后得到的原始数据(Raw Data), 进行过滤筛选, 通过vsearch和rdp去嵌合得到有效数据(Clean Data)。USEARCH分析获得扩增子变异序列ASV表[16], 经R包“vagen”进行抽平至10000, 用于后续统计分析。序列注释选用rdp_16s_v18数据库。
R包“vagen”进行α多样性分析及可视化, “ggplot2”包进行物种组成分析及可视化, “FEAST”包进行溯源分析及可视化, “linkET”包进行Mantel检验。
定量化不同生态过程影响的主要步骤如下: 运用FastTree (-gtr 模式)基于最大似然法构建ASV代表序列系统发育树, 参照ASV丰度信息, 以发育树为基础测量β-Nearest Taxon Index (βNTI), 计算样品间平均β多样性最近距离(Abundance weighted β-mean nearest taxon distance, βMNTD), 并利用零模型(999次随机取样)计算平均距离之间的偏差[17]。当βMNTD 值大于零模型估计值, 即βNTI>2, 表示微生物群落受异质化选择的影响; 当βMNTD 值小于零模型估计值, 即βNTI<−2, 则表示微生物群落受同质化选择的影响。统计分析采用Chase和Stegen的方法[18, 19], 计算样品间的 Bray-Curtis 距离(RCbray), 当RCbray值>0.95表示微生物群落受扩散限制, RCbray 值<−0.95表示微生物群落受同质性扩散影响, 当−0.95<RCbray<0.95表示微生物群落受漂变影响。整合βNTI 值和RCbray 分析结果, 评估群落组装过程中同质选择和异质选择, 以及扩散限制、同质化扩散和漂变的相对贡献。
1.4 共现网络的构建
共现网络分析用于研究微生物之间的关系。共现网络通过分子生态网络分析平台(MENAP)构建[20]。将样品按照聚类分为五组(表层、DCM层、200—300、500—1000及2000 m以下)分别构建网络。网络构建参数: (1)保留每组相对丰度高于0.05%, 且在半数以上样品中出现的ASV; (2)根据随机矩阵理论确定阈值为0.91。
2. 结果
2.1 西太平洋M4浅水海山细菌的α多样性分析
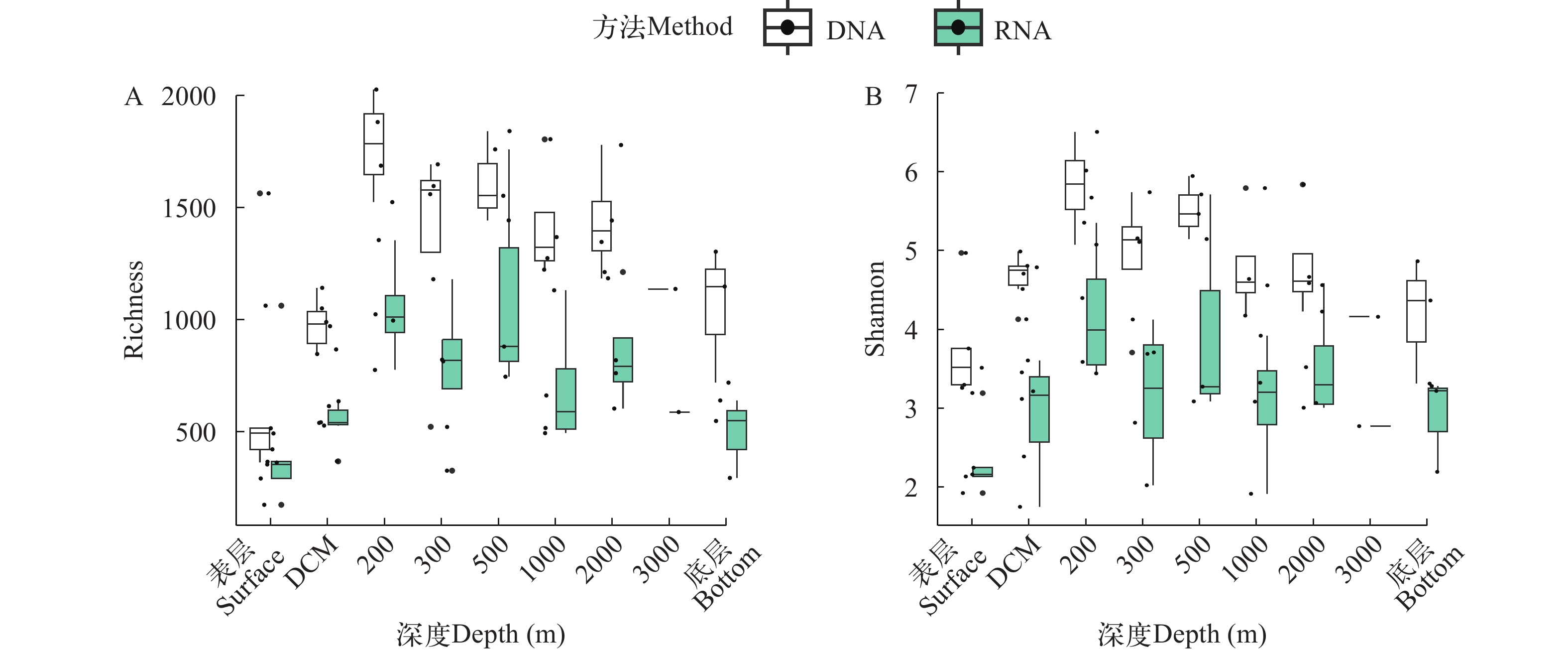
基于环境RNA技术检获的群落α多样性低于基于环境DNA技术检获的α多样性。基于环境RNA和DNA技术检获的多样性趋势相同, 随着水深的增加呈先升高后下降的趋势, 且α多样性最高值均出现在200 m层(图 2)。
2.2 西太平洋M4浅水海山区细菌物种组成与溯源分析
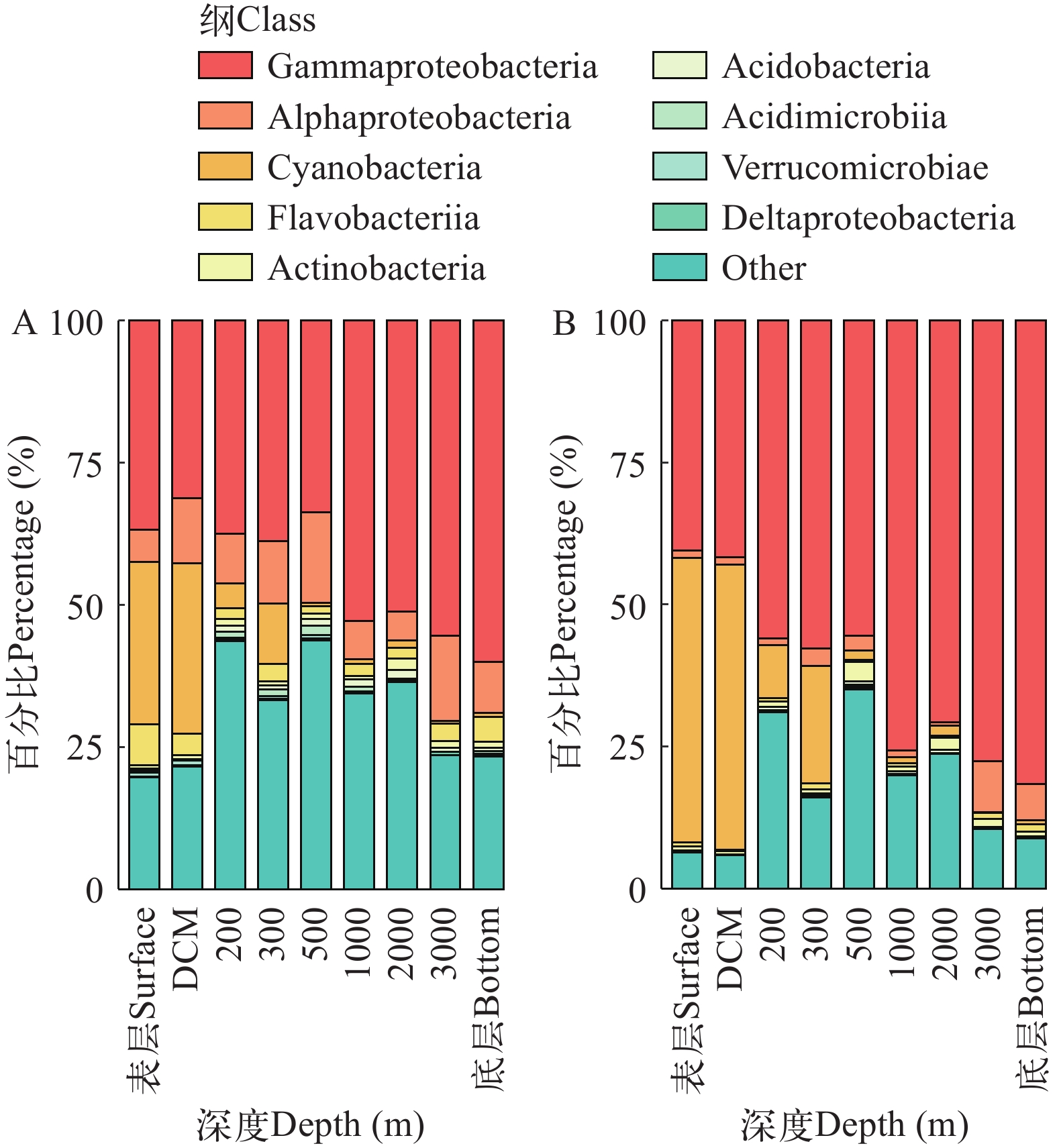
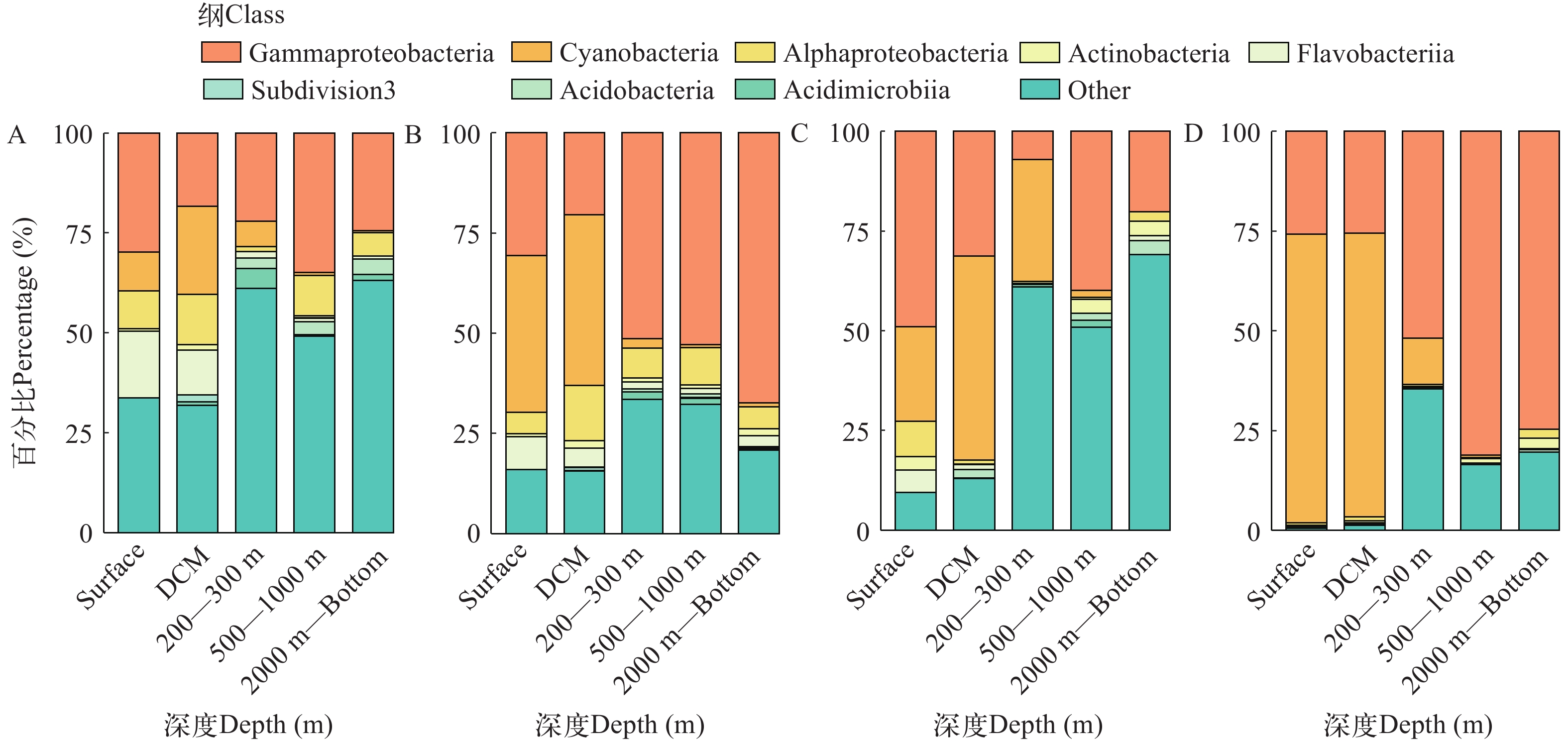
基于环境DNA与RNA技术检获的主要物种相同, 但相对丰度有所不同。两组数据中各个水层的最优势细菌类群为γ变形菌, 且其相对丰度在RNA中更高, 均呈现随着水层的加深而增加的趋势。α变形菌在RNA数据的各个水层中占比低于DNA数据。200 m以上的水层中蓝细菌在RNA数据中占比更高(图 3)。
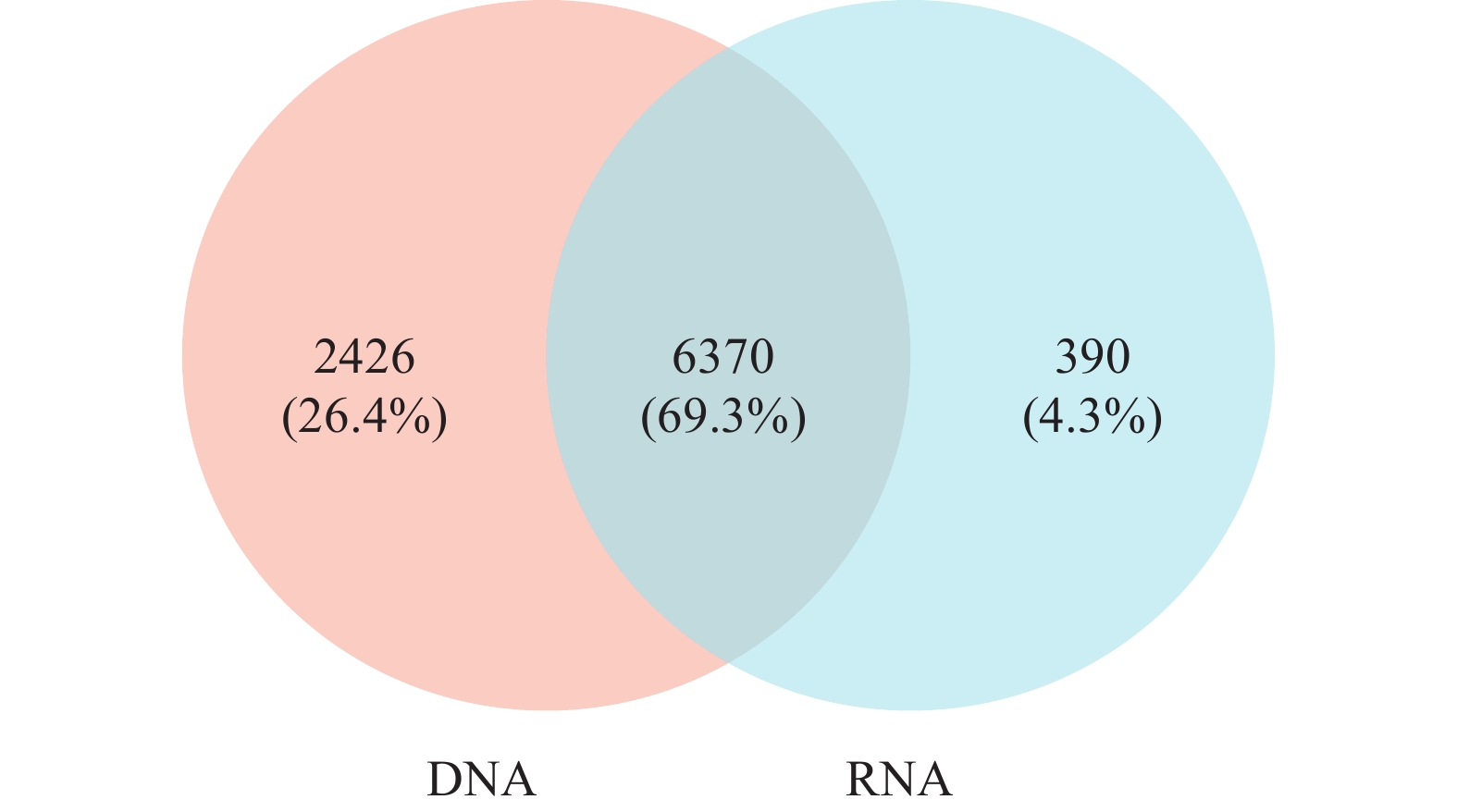
DNA和RNA重叠部分有6370个ASV (69.3%), DNA非重叠部分有2426个ASV (26.4%), RNA非重叠部分有390个ASV (4.3%)。DNA与RNA的非重叠部分都属于低丰度ASV。在重叠部分中, DNA中高丰度ASV占3.81%, RNA中高丰度ASV占1.96% (图 4)。对DNA和RNA的重叠部分与非重叠部分细菌类群的纲、目、科水平进行分析。在非重叠DNA数据中, 在纲水平, α变形菌纲相对丰度最高26.4%, 其次是γ变形菌纲13.5%和黄杆菌纲(Flavobacteriia) 5.01%; 在目水平, 黄杆菌目(Flavobacteriales)相对丰度最高为5.01%, 其次是疣微菌目(Verrucomicrobiales)占3.14%; 在科水平, SAR11科相对丰度最大占17.9%, 其次是黄杆菌科(Flavobacteriaceae)3.04%。在非重叠RNA数据中, 在纲水平, γ变形菌纲相对丰度最高19.1%, 其次是α变形菌纲7.27%; 在目水平, 涅瓦菌目(Nevskiales)相对丰度最大占2.13%, 其次是红杆菌目(Rhodobacterales)相对丰度为1.47%; 在科水平, Family_Ⅱ (2.44%)相对丰度最大, 其次是红杆菌科(Rhodobacteraceae)占1.47%。在重叠DNA数据中, 在纲水平, γ变形菌纲相对丰度最大41.5%, 其次是蓝细菌纲13.1%和α变形菌纲9.09%。在目水平, 交替单胞菌目(Alteromonadales)相对丰度最大占22.5%; 在科水平, 交替单胞菌科(Alteromonadaceae)相对丰度最高22.5%, 其次是Family_Ⅱ(13.0%)和SAR11 (6.35%)。在重叠RNA数据中, 在纲水平, γ变形菌纲相对丰度最高55.9%, 其次是蓝细菌纲22.9%和α变形菌纲2.18% ; 在目水平, 交替单胞菌目(Alteromonadales)相对丰对最大占37.6%; 在科水平, 交替单胞菌科(Alteromonadaceae)相对丰度最高37.6%, 其次是Family_Ⅱ (22.4%; 图 5)。
通过上述数据, 在非重叠部分中α变形菌纲在RNA (7.27%)的占比小于DNA(26.4%), 其次黄杆菌纲(Flavobacteriia)在DNA中的相对丰度(5.01%)大于RNA (0.36%); 在科水平, α变形菌纲下的SAR11科在DNA占比(17.9%)最大, 而在RNA中是红杆菌科(Rhodobacteraceae)占1.47%。重叠部分中γ变形菌纲和蓝细菌纲的相对丰度RNA要大于DNA, 而α变形菌纲的相对丰度是DNA大于RNA。
对DNA和RNA的重叠部分与非重叠部分细菌类群分析, 发现重叠部分包含29纲, 70目, 147科。在非重叠部分中, DNA数据包含的多样性高于RNA数据。其中DNA数据包含28纲, 58目, 96科; RNA数据包含14纲, 33目, 49科。
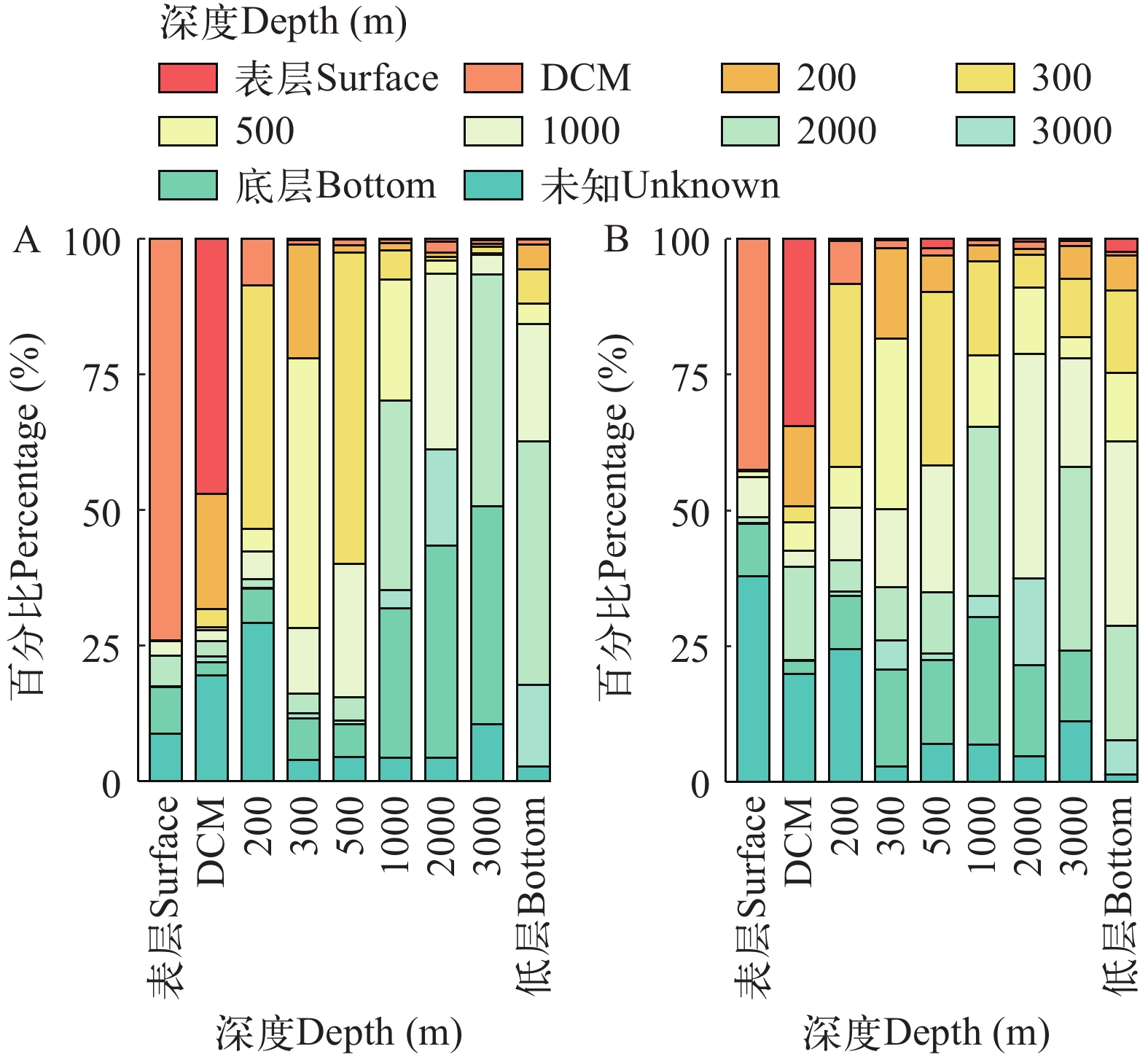
溯源分析结果显示, 无论是基于DNA还是RNA技术检获的群落都受到上升流影响, 二者结果有一定的差异但趋势相同。基于RNA数据, 300 m以浅的水层中来自相邻更深的水层占比和500 m以深的水层中来自相邻更浅的水层占比, 均低于基于DNA数据的占比(图 6)。
2.3 西太平洋M4浅水海山细菌的β多样性分析
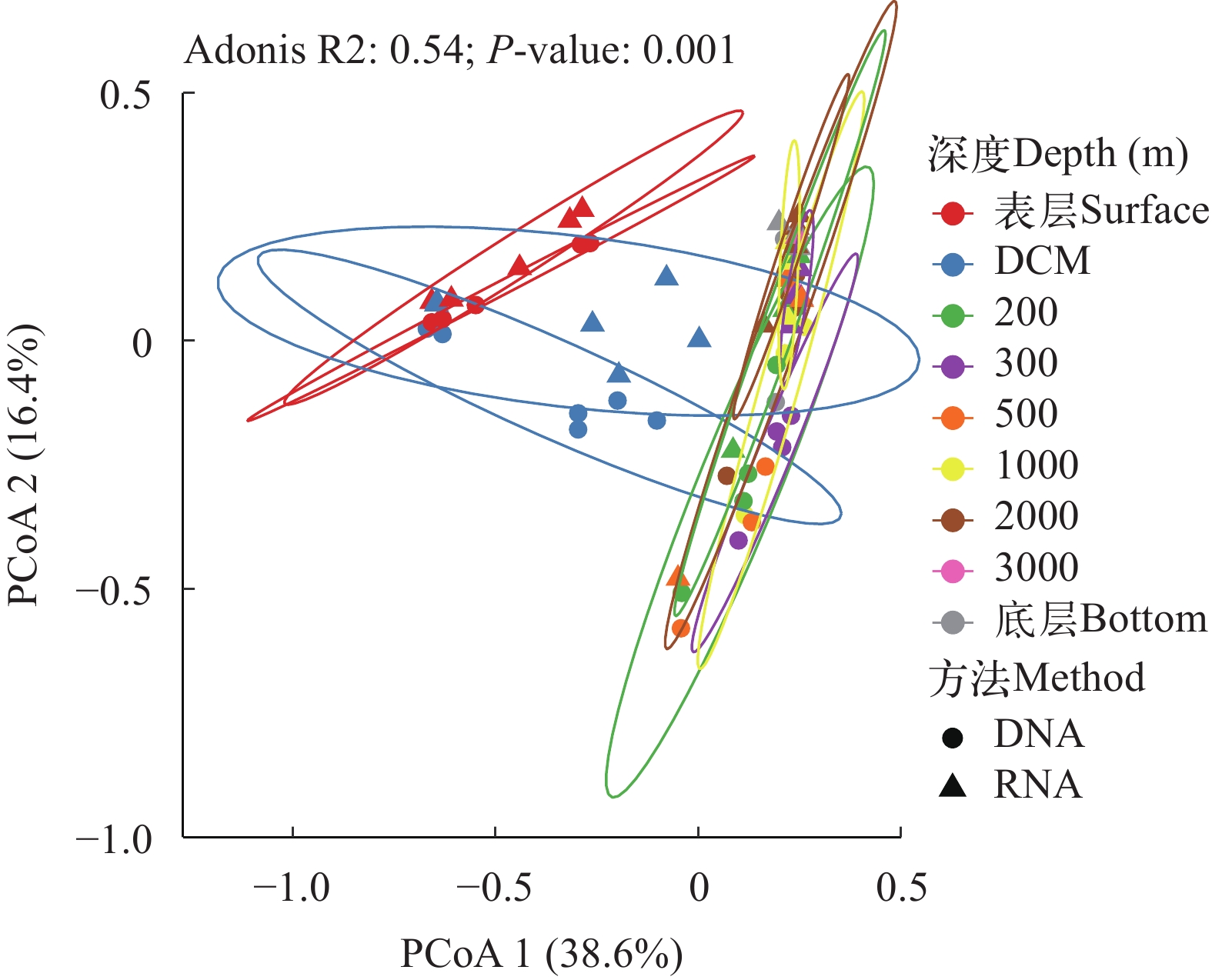
通过Bray-Curtis距离计算的M4海山的9个水层的DNA和RNA数据的主坐标分析。使用pairwiseAdonis检验分析, 结果显示, 每个水层的两组数据之间的差异不大, 但垂向上的差异更显著, 其中表层和DCM层相对于其他水层的群落差异大(R2为0.54, P<0.001); 而其他水层之间的群落差异较小(图 7)。
2.4 西太平洋M4浅水海山细菌的共现网络
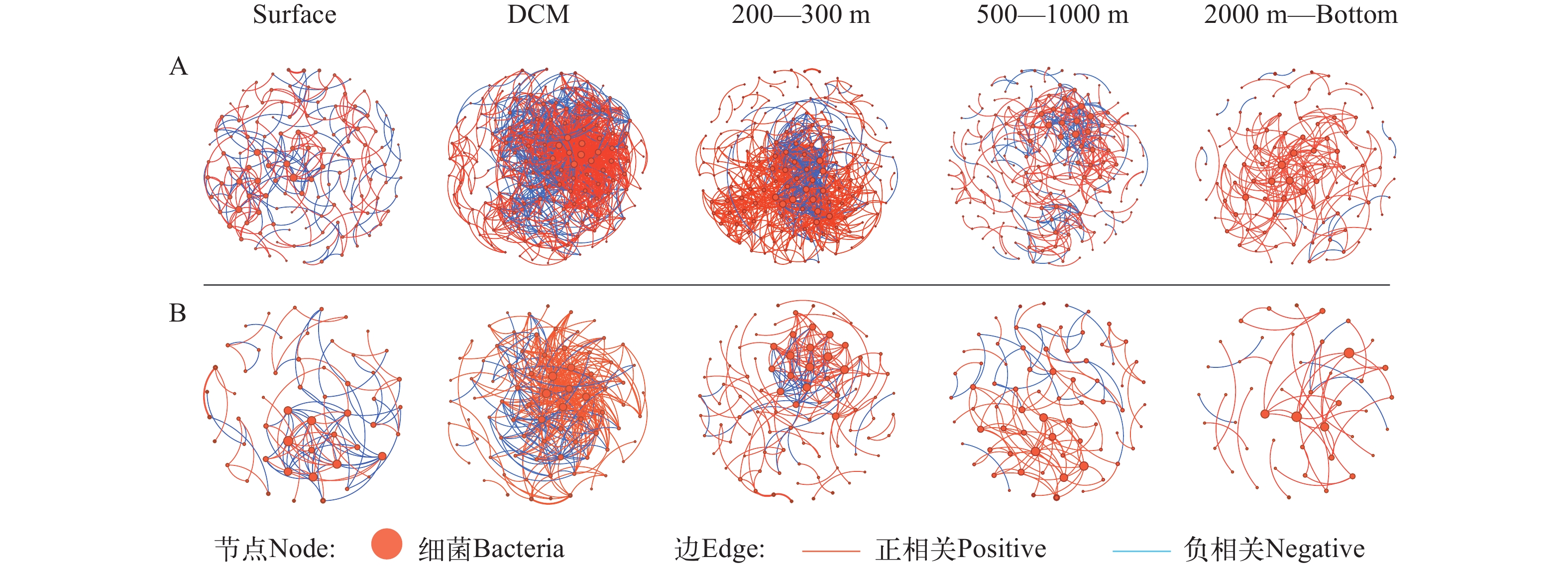
基于DNA和RNA数据构建的共现网络, 边数和节点数都随着深度的增加呈先升高后下降的趋势。但RNA网络比DNA网络简单且变化趋势更明显。两组数据各水层的共现网络都是正相关的边数占比随着水深的增加而升高, 负相关的边数占比随着水深的增加而减小(图 8)。平均节点度可以反应共现网络中的相互作用强度[21, 22], 两组数据中DCM层的平均节点度都是最高的, 且随着水深的增加呈先升高后下降的趋势, 这与总边数的趋势相同, 说明网络越复杂网络的相互作用越强(表 1)。
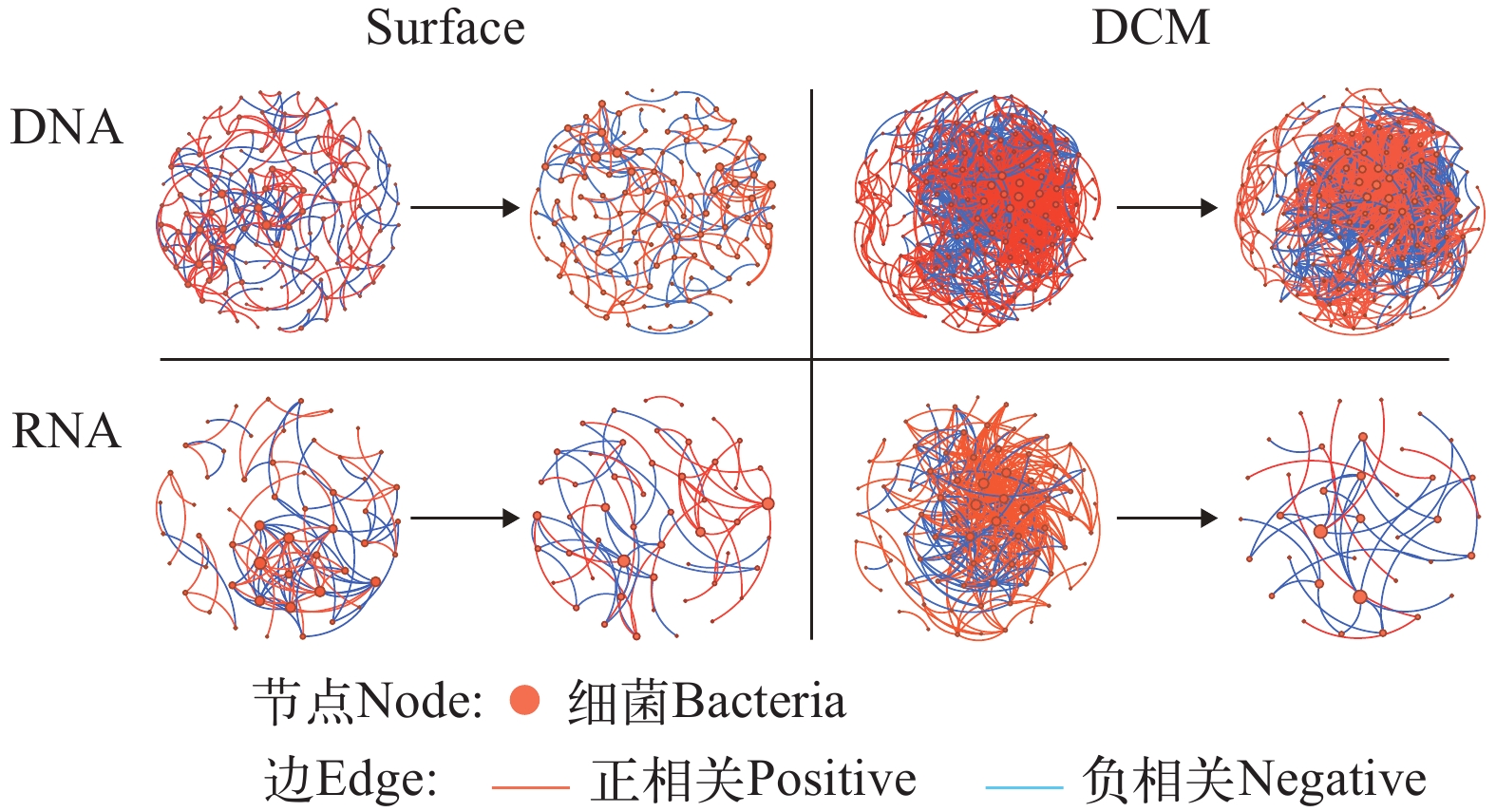
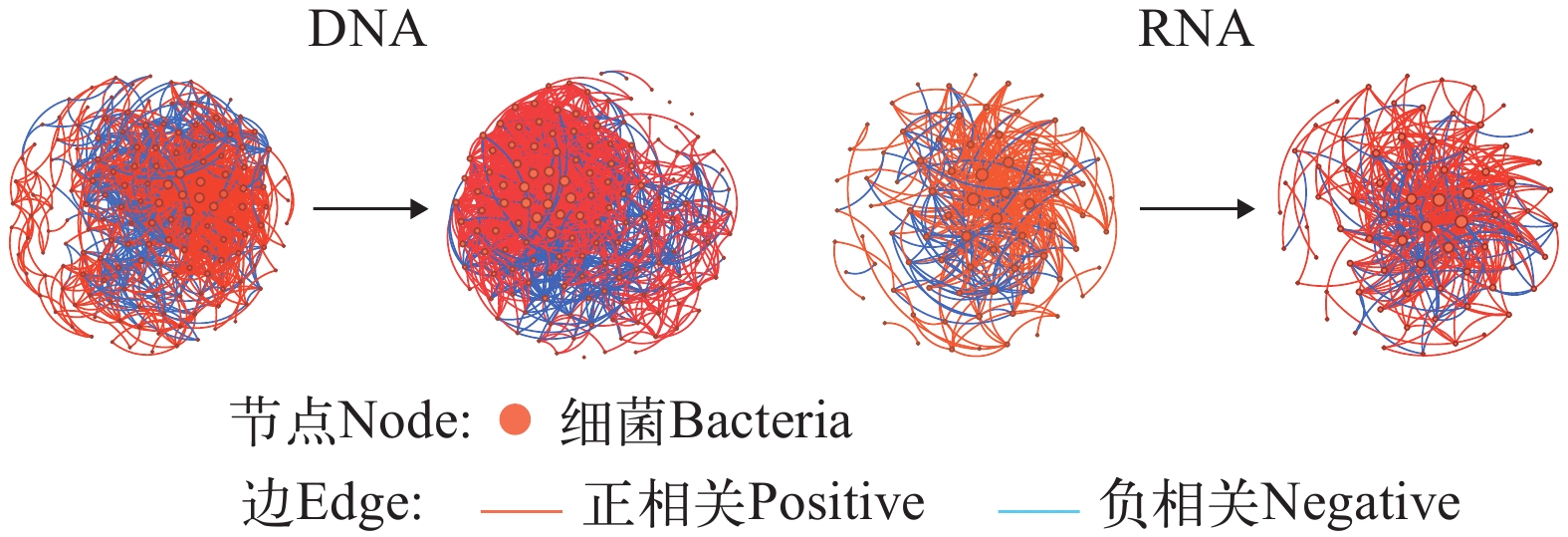
![]() 图 8 基于环境DNA (A)和RNA (B)检获的M4海山各个水层的细菌共现网络阈值为0.91, 网络中每个节点的度映射为大小, 橙边表示正相关, 蓝边表示负相关Figure 8. Bacterial co-occurrence network of communities in each water layer of M4 Seamount based on the eDNA (A) and eRNA (B)With a cutoff of 0.91, the degree of each node in the network is mapped to the size. The orange edges indicate the positive correlations and the blue ones indicate the negative correlation表 1 M4海山DNA和RNA的各个水层的共现网络基本参数Table 1. The basic parameter of co-occurrence network from each layer in the M4 Seamount
图 8 基于环境DNA (A)和RNA (B)检获的M4海山各个水层的细菌共现网络阈值为0.91, 网络中每个节点的度映射为大小, 橙边表示正相关, 蓝边表示负相关Figure 8. Bacterial co-occurrence network of communities in each water layer of M4 Seamount based on the eDNA (A) and eRNA (B)With a cutoff of 0.91, the degree of each node in the network is mapped to the size. The orange edges indicate the positive correlations and the blue ones indicate the negative correlation表 1 M4海山DNA和RNA的各个水层的共现网络基本参数Table 1. The basic parameter of co-occurrence network from each layer in the M4 Seamount参数Parameter DNA RNA 表层Surface DCM 200—300 m 500—1000 m ≥2000 m 表层Surface DCM 200—300 m 500—1000 m ≥2000 m 总节点数Node 127 186 173 174 108 54 80 90 73 46 总边数Edge 233 1854 777 392 198 106 374 182 114 42 正相关占比Positive (%) 57.9 76.6 74.1 69.4 92.9 48.1 78.6 79.1 79.8 88.1 负相关占比Negative (%) 42.1 23.4 25.9 30.6 7.1 51.9 21.4 20.9 20.2 11.9 平均节点度Average degree 3.67 19.9 8.98 4.51 3.67 3.93 9.35 4.04 3.12 1.83 蓝细菌在两组数据的表层和DCM层时的相对丰度和节点数占比最大, 随着水深不断增加占比逐渐减少。对比两组数据, RNA数据中蓝细菌的相对丰度和节点数的占比相对更大, 更能够体现蓝细菌的活性。α变形菌在两组数据中的主要类群是SAR11, SAR11在DNA数据各个水层的占比要远远大于其在RNA数据各个水层的占比, 其中SAR11在DNA数据中的DCM层占比最大为11.6%, 而SAR11在RNA数据的DCM层的占比为0.46%, 说明α变形菌的活性不高。两组数据中γ变形菌都普遍存在, 且随着水深的增加γ变形菌的相对丰度和节点数也不断增加(图 9)。
2.5 去蓝细菌的对比分析
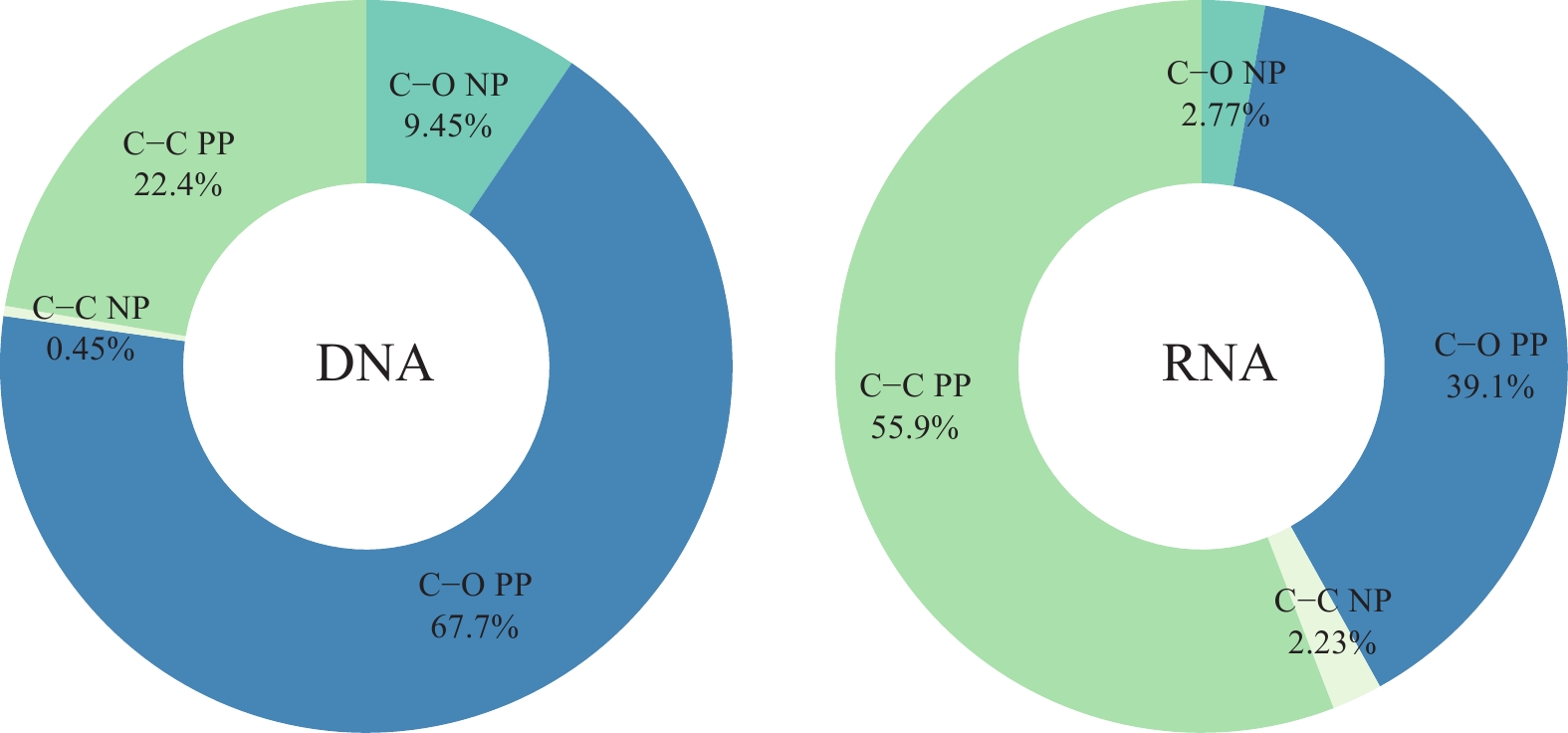
蓝细菌在DCM层的网络中边的占比大(图 10)。在两组数据中, 蓝细菌的正相关边数均占主导; 其中在DNA数据中蓝细菌与其他异养细菌的正相关边数占比为67.7%, 而在RNA数据中蓝细菌与蓝细菌的正相关边数占比55.9%, 大于蓝细菌与其他异养细菌占比39.1%。
![]() 图 10 基于环境DNA和RNA技术检获的DCM层共现网络中的与蓝细菌相关的边数占比C—C PP. 蓝细菌之间的正相关; C—C NP. 蓝细菌之间的负相关; C—O PP. 蓝细菌与其他细菌的正相关; C—O NP. 蓝细菌与其他细菌的负相关Figure 10. Percentage of Cyanobacteria-related edges in DCM layer co-occurrence networks based on the eDNA and eRNAC—C PP. Positive correlation between cyanobacteria; C—C NP. Negative correlation between cyanobacteria; C—O PP. Positive correlation of cyanobacteria with other bacteria; C—O NP. Negative correlation of cyanobacteria with other bacteria
图 10 基于环境DNA和RNA技术检获的DCM层共现网络中的与蓝细菌相关的边数占比C—C PP. 蓝细菌之间的正相关; C—C NP. 蓝细菌之间的负相关; C—O PP. 蓝细菌与其他细菌的正相关; C—O NP. 蓝细菌与其他细菌的负相关Figure 10. Percentage of Cyanobacteria-related edges in DCM layer co-occurrence networks based on the eDNA and eRNAC—C PP. Positive correlation between cyanobacteria; C—C NP. Negative correlation between cyanobacteria; C—O PP. Positive correlation of cyanobacteria with other bacteria; C—O NP. Negative correlation of cyanobacteria with other bacteria在两组数据中, 蓝细菌在表层和DCM层的相对丰度最大, 因此分别去除DNA和RNA数据中的蓝细菌, 并对比去除前后的共现网络变化。结果发现, 去除蓝细菌后的网络要比未去除的网络简单(图 11)。RNA数据的DCM层共现网络的边数下降了89.6%(边数从374减少到39), 而DNA数据的DCM层共现网络的边数下降38.7%(边数从1854减少到1137; 表 2)。
表 2 去除蓝细菌前后M4海山表层和DCM层的共现网络的参数Table 2. The basic parameter of the co-occurrence network in the surface and DCM layers of the M4 Seamount before and after the removal of cyanobacteria参数Parameter DNA RNA Surface (前) Surface (后) DCM (前) DCM (后) Surface (前) Surface (后) DCM (前) DCM (后) 总节点数Node 127 114 186 159 54 51 80 37 总边数Edge 233 191 1854 1137 106 66 374 39 正相关占比Positive (%) 57.9 55.5 76.6 70.5 48.1 54.5 78.6 23.1 负相关占比Negative (%) 42.1 44.5 23.4 29.5 51.9 45.5 21.4 76.9 平均节点度Average degree 3.67 3.35 19.9 14.3 3.93 2.59 9.35 2.11 2.6 去α变形菌的对比分析
DCM层的α变形菌去除后, DNA数据网络的边数下降20.9%, 而RNA数据网络的边数下降1.34%。对比DNA和RNA两组数据, RNA数据的网络变化没有DNA的网络变化明显(图 12和表 3)。
表 3 去除α变形菌前后M4海山DCM层的共现网络的参数Table 3. The basic parameter of the co-occurrence network in the DCM layer of the M4 Seamount before and after the removal of alphaproteobacteria参数Parameter DNA RNA DCM
(前)DCM
(后)DCM
(前)DCM
(后)总节点数Node 186 145 80 75 总边数Edge 1854 1466 374 369 正相关占比Positive (%) 76.6 80.1 78.6 78.6 负相关占比Negative (%) 23.4 19.9 21.4 21.4 平均节点度Average degree 19.9 20.2 9.35 9.84 2.7 西太平洋M4浅水海山的细菌的代谢活性分析
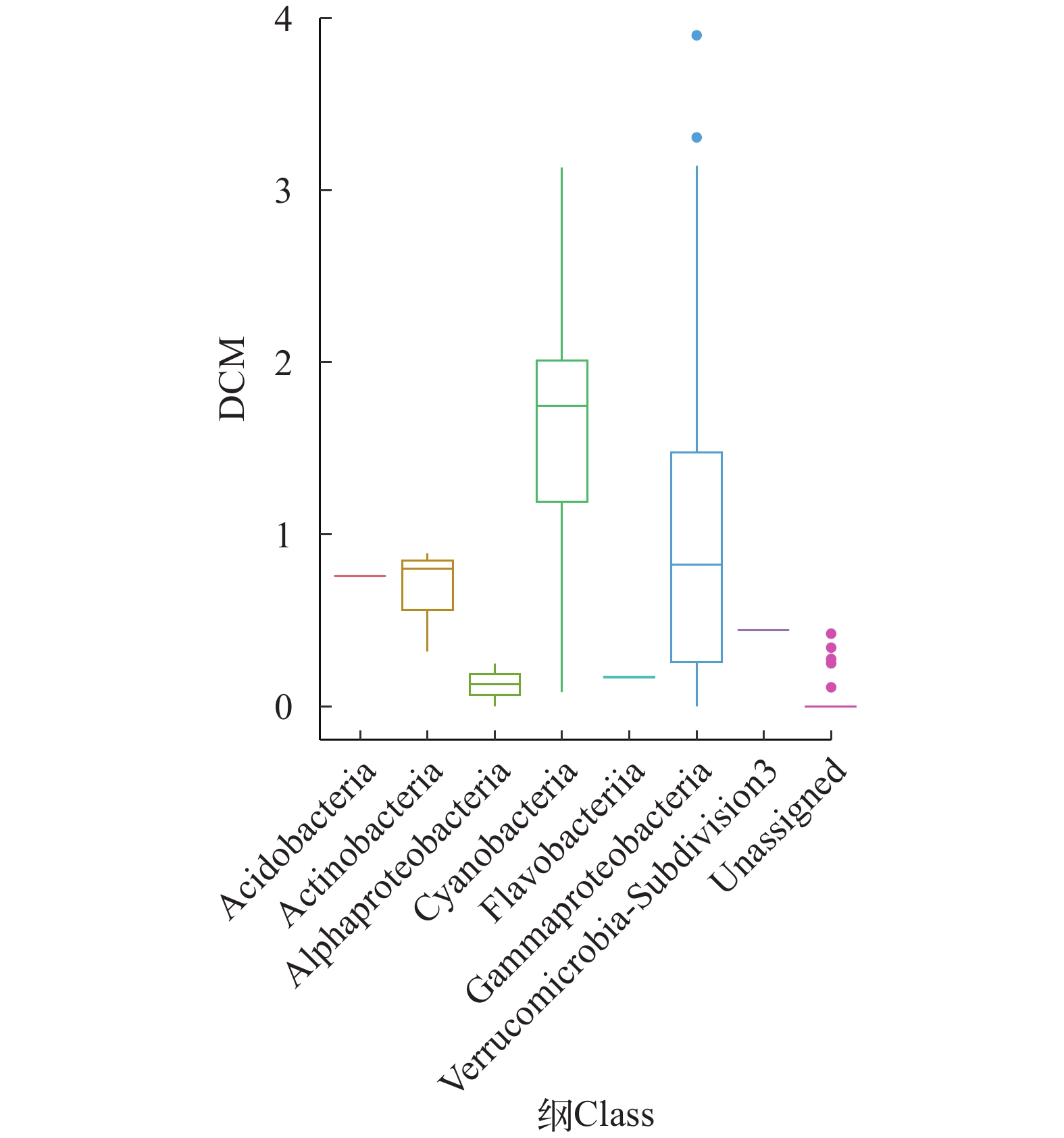
通过RNA/DNA的比率为来推断细菌主要类群的代谢活性, 值越大说明代谢活性越高。结果显示, 蓝细菌在DCM层的代谢活性最强, 其次是γ变形菌、放线菌(Actinobacteria)、酸杆菌(Acidobacteria), 而α变形菌代谢活性相对较弱(图 13)。
3. 讨论
前人研究多利用环境DNA, 由于DNA在环境中存留时间长, 无法确定检测的物种是否有代谢活性。相较于DNA, RNA为单链结构, 易降解, 在环境中存留时间短, 检获的生物更具代谢活性[23, 24]。本研究采用环境RNA技术, 分析了西太平洋M4海山区的细菌群落结构特征, 并与环境DNA技术进行比较, 解析了海山区细菌群落的代谢活性特征。
结果显示, DNA和RNA检获共有ASV占比69.3%, 显著高于DNA独有的26.4%, RNA检获的独有ASV仅占4.3%。仅通过DNA检获的ASVs主要来自死亡生物或者胞外DNA, 但也可能归因于RNA的逆转录过程会导致部分物种丢失。前人研究发现, 在浅水海山中, 蓝细菌是100 m以上水层的优势细菌类群[8], 在深水平顶海山中, 蓝细菌在200 m以上的水层中占优势[5]。这与本文的研究结果相似, 无论在DNA还是RNA的数据中在真光层的蓝细菌的相对丰度较高, 且RNA明显高于DNA, 显示蓝细菌的代谢活性高。
前人研究还发现太平洋深水海山1000 m以上的水层中, α变形菌占优势[9], 且在大西洋深水海山的鞘水中发现丰富的α变形菌[10]。上述深水海山的研究均基于环境DNA技术的数据。本研究则进一步发现浅水海山中α变形菌在RNA中的占比低于DNA, 显示代谢活性低。此外, 这一结果还得到网络分析的验证。共现网络分析的结果显示, 细菌网络随水深的增加呈现先升高后下降的趋势, RNA的网络较DNA的更简单且变化趋势更显著。而且, 在去除蓝细菌后的网络中, RNA网络变化明显大于DNA; 而在去除α变形菌的网络中, RNA网络变化不明显。由此可见, 前人的研究可能高估了α变形菌在海山区多样性占比及其在群落中的作用。环境RNA较环境DNA能检获到有代谢活性的物种分布, 可为海山浮游细菌的多样性及分布提供更完整的认知。
-
图 8 基于环境DNA (A)和RNA (B)检获的M4海山各个水层的细菌共现网络
阈值为0.91, 网络中每个节点的度映射为大小, 橙边表示正相关, 蓝边表示负相关
Figure 8. Bacterial co-occurrence network of communities in each water layer of M4 Seamount based on the eDNA (A) and eRNA (B)
With a cutoff of 0.91, the degree of each node in the network is mapped to the size. The orange edges indicate the positive correlations and the blue ones indicate the negative correlation
图 10 基于环境DNA和RNA技术检获的DCM层共现网络中的与蓝细菌相关的边数占比
C—C PP. 蓝细菌之间的正相关; C—C NP. 蓝细菌之间的负相关; C—O PP. 蓝细菌与其他细菌的正相关; C—O NP. 蓝细菌与其他细菌的负相关
Figure 10. Percentage of Cyanobacteria-related edges in DCM layer co-occurrence networks based on the eDNA and eRNA
C—C PP. Positive correlation between cyanobacteria; C—C NP. Negative correlation between cyanobacteria; C—O PP. Positive correlation of cyanobacteria with other bacteria; C—O NP. Negative correlation of cyanobacteria with other bacteria
表 1 M4海山DNA和RNA的各个水层的共现网络基本参数
Table 1 The basic parameter of co-occurrence network from each layer in the M4 Seamount
参数Parameter DNA RNA 表层Surface DCM 200—300 m 500—1000 m ≥2000 m 表层Surface DCM 200—300 m 500—1000 m ≥2000 m 总节点数Node 127 186 173 174 108 54 80 90 73 46 总边数Edge 233 1854 777 392 198 106 374 182 114 42 正相关占比Positive (%) 57.9 76.6 74.1 69.4 92.9 48.1 78.6 79.1 79.8 88.1 负相关占比Negative (%) 42.1 23.4 25.9 30.6 7.1 51.9 21.4 20.9 20.2 11.9 平均节点度Average degree 3.67 19.9 8.98 4.51 3.67 3.93 9.35 4.04 3.12 1.83 表 2 去除蓝细菌前后M4海山表层和DCM层的共现网络的参数
Table 2 The basic parameter of the co-occurrence network in the surface and DCM layers of the M4 Seamount before and after the removal of cyanobacteria
参数Parameter DNA RNA Surface (前) Surface (后) DCM (前) DCM (后) Surface (前) Surface (后) DCM (前) DCM (后) 总节点数Node 127 114 186 159 54 51 80 37 总边数Edge 233 191 1854 1137 106 66 374 39 正相关占比Positive (%) 57.9 55.5 76.6 70.5 48.1 54.5 78.6 23.1 负相关占比Negative (%) 42.1 44.5 23.4 29.5 51.9 45.5 21.4 76.9 平均节点度Average degree 3.67 3.35 19.9 14.3 3.93 2.59 9.35 2.11 表 3 去除α变形菌前后M4海山DCM层的共现网络的参数
Table 3 The basic parameter of the co-occurrence network in the DCM layer of the M4 Seamount before and after the removal of alphaproteobacteria
参数Parameter DNA RNA DCM
(前)DCM
(后)DCM
(前)DCM
(后)总节点数Node 186 145 80 75 总边数Edge 1854 1466 374 369 正相关占比Positive (%) 76.6 80.1 78.6 78.6 负相关占比Negative (%) 23.4 19.9 21.4 21.4 平均节点度Average degree 19.9 20.2 9.35 9.84 -
[1] Salihoglu B, Garçon V, Oschlies A, et al. Influence of nutrient utilization and remineralization stoichiometry on phytoplankton species and carbon export: a modeling study at BATS [J]. Deep Sea Research Part I:Oceanographic Research Papers, 2008, 55(1): 73-107. doi: 10.1016/j.dsr.2007.09.010
[2] Staudigel H, Koppers A, Lavelle J W, et al. Defining the word “seamount” [J]. Oceanography, 2010, 23(1): 20-21. doi: 10.5670/oceanog.2010.85
[3] Caron D A, Lim E L, Miceli G, et al. Grazing and utilization of chroococcoid cyanobacteria and heterotrophic bacteria by protozoa in laboratory cultures and a coastal plankton community [J]. Marine Ecology Progress Series, 1991, 76(3): 205-217.
[4] Rogers A D. The biology of seamounts: 25 years on [J]. Advances in Marine Biology, 2018(79): 137-224.
[5] Zhao R, Zhao F, Zheng S, et al. Bacteria, protists, and fungi may hold clues of seamount impact on diversity and connectivity of deep-sea pelagic communities [J]. Frontiers in Microbiology, 2022(13): 773487.
[6] Morato T, Hoyle S D, Allain V, et al. Seamounts are hotspots of pelagic biodiversity in the open ocean [J]. Proceedings of the National Academy of Sciences of the United States of America, 2010, 107(21): 9707-9711.
[7] Dai S, Zhao Y, Li X, et al. The seamount effect on phytoplankton in the tropical western Pacific [J]. Marine Environmental Research, 2020(162): 105094.
[8] 赵丽, 赵燕楚, 王超锋, 等. 热带西太平洋Y3和M2海山微食物网主要类群生态分布与比较 [J]. 海洋与湖沼, 2017, 48(6): 1446-1455. doi: 10.11693/hyhz20170600160 Zhao L, Zhao Y C, Wang C F, et al. Comparison in the distribution of microbial food web components in the Y3 and M2 seamounts in the tropical western Pacific [J]. Oceanologia et Limnologia Sinica, 2017, 48(6): 1446-1455. doi: 10.11693/hyhz20170600160
[9] Sun Q, Song J, Li X, et al. Bacterial vertical and horizontal variability around a deep seamount in the tropical Western Pacific Ocean [J]. Marine Pollution Bulletin, 2020(158): 111419.
[10] Giljan G, Kamennaya N A, Otto A, et al. Bacterioplankton reveal years-long retention of atlantic deep-ocean water by the tropic seamount [J]. Scientific Reports, 2020, 10(1): 4715. doi: 10.1038/s41598-020-61417-0
[11] Rees H C, Maddison B C, Middleditch D J, et al. REVIEW: The detection of aquatic animal species using environmental DNA – a review of eDNA as a survey tool in ecology [J]. Journal of Applied Ecology, 2015, 51(5): 1450-1459.
[12] SGordon L, Jennings J, Ross A, et al. A Suggested Protocol for Continuous Flow Automated Analysis of Seawater Nutrients (Phosphate, Nitrate, Nitrite and Silicic Acid) in the WOCE Hydrographic Program and the Joint Global Ocean Fluxes Study [M]//Orego: OCE Hydrographic Program Office, Methods Manual WHPO, 1993.
[13] Parsons T R, Maita Y, Lalli C M. Fluorometric Determination of Chlorophylls [M]. A Manual of Chemical & Biological Methods for Seawater Analysis. Amsterdam: Elsevier, 1984: 107-109.
[14] Hansen M C, Tolker-Nielsen T, Givskov M, et al. Biased 16S rDNA PCR amplification caused by interference from DNA flanking the template region [J]. FEMS Microbiology Ecology, 1998, 26(2): 141-149. doi: 10.1111/j.1574-6941.1998.tb00500.x
[15] Wang Y, Qian P Y. Conservative fragments in bacterial 16S rRNA genes and primer design for 16S ribosomal DNA amplicons in metagenomic studies [J]. PLoS One, 2009, 4(10): e7401. doi: 10.1371/journal.pone.0007401
[16] Liu Y X, Qin Y, Chen T, et al. A practical guide to amplicon and metagenomic analysis of microbiome data [J]. Protein & Cell, 2021, 12(5): 315-330.
[17] Stegen J C, Lin X, Fredrickson J K, et al. Quantifying community assembly processes and identifying features that impose them [J]. The ISME Journal, 2013, 7(11): 2069-2079. doi: 10.1038/ismej.2013.93
[18] Chase J M, Kraft N J B, Smith K G, et al. Using null models to disentangle variation in community dissimilarity from variation in α-diversity [J]. Ecosphere, 2011, 2(2): art24.
[19] Stegen J C, Lin X, Fredrickson J K, et al. Estimating and mapping ecological processes influencing microbial community assembly [J]. Frontiers in Microbiology, 2015(6): 370.
[20] Deng Y, Jiang Y H, Yang Y, et al. Molecular ecological network analyses [J]. BMC Bioinformatics, 2012(13): 113.
[21] Gan H, Li X, Wang Y, et al. Plants play stronger effects on soil fungal than bacterial communities and co-occurrence network structures in a subtropical tree diversity experiment [J]. Microbiology Spectrum, 2022, 10(3): e0013422. doi: 10.1128/spectrum.00134-22
[22] Ma B, Wang H, Dsouza M, et al. Geographic patterns of co-occurrence network topological features for soil microbiota at continental scale in Eastern China [J]. The ISME Journal, 2016, 10(8): 1891-1901. doi: 10.1038/ismej.2015.261
[23] Giroux M S, Reichman J R, Langknecht T, et al. Environmental RNA as a tool for marine community biodiversity assessments [J]. Scientific Reports, 2022, 12(1): 17782. doi: 10.1038/s41598-022-22198-w
[24] Xu D, Li R, Hu C, et al. Microbial eukaryote diversity and activity in the water column of the South China Sea based on DNA and RNA high throughput sequencing [J]. Frontiers in Microbiology, 2017(8): 1121.
-
期刊类型引用(1)
1. 尹婷婷,赵峰,刘巍岳,徐奎栋. 基于环境RNA研究西太平洋浅水海山区真核微生物多样性及其与细菌的关系. 海洋与湖沼. 2024(05): 1213-1222 .  百度学术
百度学术
其他类型引用(0)



 下载:
下载: