FUNCTIONAL GROUP CHARACTERISTICS AND INFLUENCING FACTORS OF PHYTOPLANKTON IN EMERGENCY WATER SUPPLY OF EAST TAIHU LAKE
-
摘要:
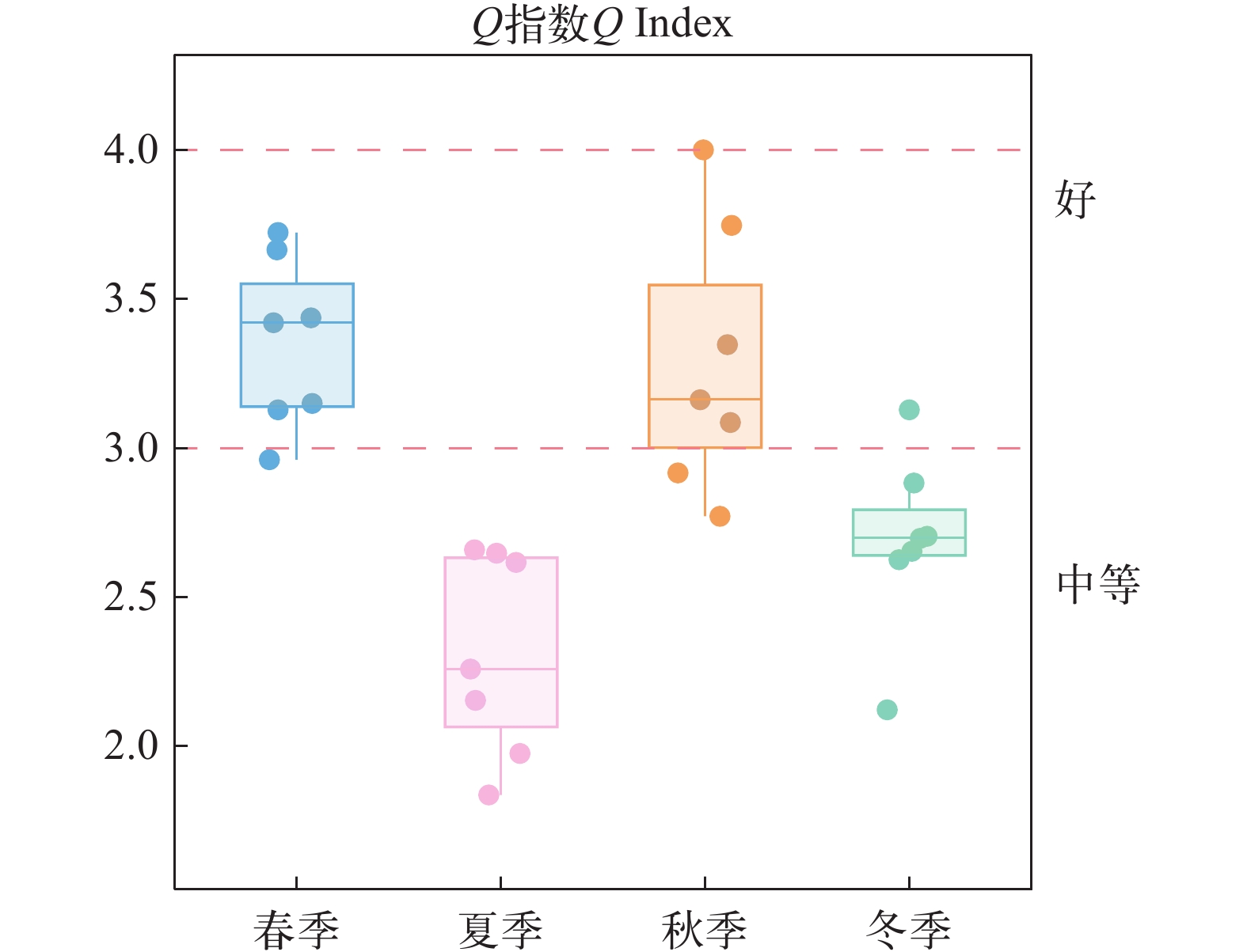
研究于2022年5月—2023年2月对东太湖应急水源地的浮游植物和环境因子进行了4个季度的调查分析, 旨在探明水源地浮游植物功能群特征动态及其与环境因子之间的关系。结果表明: (1)共鉴定出浮游植物7门128种, 共划分为21个功能群, 包括喜好高营养扰动的功能群MP、P、S1, 喜好高营养低扰动的H1、W1, 以及具广适性的LO等, 表现为夏秋季功能群种类数较多, 秋季功能群生物量明显高于其他季节, 指示水体生境特征为水浅、分层较少、透明度低、高营养状态; (2)优势功能群有7个(E、H1、LO、MP、P、S1、W1), 具明显的季节性, 表现为春LO/W1/P→夏H1/S1/MP→秋LO/P/MP→冬E/H1/LO的季节演替, 生物量占比最大的主要为以甲藻为主的功能群LO和以硅藻为主的功能群MP; (3)冗余分析(RDA)和方差分解分析(VPA)表明, 水温(WT)、氨氮(${\rm{NH}}^+_4 $-N)、总磷(TP)和电导率(Cond)是影响水源地浮游植物优势功能群生物量的主要环境因子, 其中功能群LO与WT、${\rm{NH}}^+_4 $-N、TP、Cond均呈负相关, 功能群W1、S1、MP均与WT、${\rm{NH}}^+_4 $-N、TP、Cond呈正相关; (4)功能群Q指数评价结果(2.91±0.11)表明水源地整体水质状态“中等”, 但在夏季时水质较差、营养水平和蓝藻丰度较高, 依然面临蓝藻水华问题。建议严格控制外源营养输入, 加强生态系统结构调控, 提升生态系统的稳定性和自净能力, 以控制蓝藻水华发生和保障供水安全。
Abstract:From May 2022 to February 2023, four quarterly surveys were conducted to investigate the dynamic characteristics of phytoplankton functional groups and their relationships with environmental factors in the emergency water supply for East Taihu Lake. The results showed that: (1) A total of 128 species belonging to 7 phyla of phytoplankton were identified and classified into 21 functional groups, including MP, P, and S1, which prefer high nutrient disturbance, as well as H1 and W1, which prefer high nutrient and low disturbance environments. The LO group exhibited wide adaptability. Functional group species was higher in summer and autumn, with autumn showing significantly higher biomass, suggesting the water habitat was shallow, weakly stratified, less transparent, and in a high trophic state. (2) Seven dominant functional groups (E, H1, LO, MP, P, S1, and W1) were identified, displaying clear seasonality and a succession pattern: spring (LO/W1/P)→summer (H1/S1/MP)→autumn (LO/P/MP)→winter (E/H1/LO). The dinoflagellates-dominated LO group and the diatom-dominated MP group constituted the largest proportion of the total. (3) RDA and VPA analysis showed that WT, ${\rm{NH}}^+_4 $-N, TP, and Cond were the main environmental factors affecting the biomass of dominant phytoplankton groups. Functional groups LO was negatively correlated with WT, ${\rm{NH}}^+_4 $-N, TP, and Cond, while groups W1, S1, and MP showed positive correlations with these variables. (4) The Q-index evaluation of functional groups (2.91±0.11) indicated that the overall water quality of the source was “medium”. However, during the summer, water quality deteriorated, with high nutrient levels and elevated cyanobacterial abundance, indicating an ongoing risk of cyanobacterial blooms. It is recommended to strictly control external nutrient input, strengthen ecosystem regulation, and enhance the stability and self-purification ability of the ecosystem to mitigate bloom occurrences and ensure water supply safety.
-
Keywords:
- Water supply lake /
- Phytoplankton /
- Functional group /
- Environmental factors /
- Q index /
- East Taihu Lake
-
中国作为世界淡水鱼养殖大国之一, 淡水渔业养殖发展迅速, 2020年我国全社会渔业经济总产值27543.47亿元, 其中淡水养殖产值为6387.15亿元[1]。黄颡鱼(Pelteobagrus fulvidraco), 俗称黄辣丁, 鲿科, 黄颡鱼属动物, 作为我国淡水养殖主要品种之一, 分布广、肉鲜味美及营养价值高, 广受消费者喜爱[2]; 但淡水鱼具土腥味, 实际生产中常将其放到清水池中暂养净化或以微流水处理, 以提升鱼肉品质[3-6], 且有研究表明暂养是改善水产品异味最可靠的方法[7], 还利于降低鱼类捕捞应激[3]。袁小琛等[3]研究发现适时的暂养处理可以显著提高鳙(Aristichthys nobilis)的肌肉品质和营养价值。Palmeri等[6]研究发现, 鳕鲈(Maccullochella peelii)经过短期暂养可以有效改善鱼肉风味。草鱼(Ctenopharyngodon idella)经过20d以上暂养和断食, 可提高其品质, 显著增加肌肉弹性、硬度及内聚力等结构参数[5], 且短期暂养可减少草鱼鱼肉中的鱼腥味和泥土味[8], 短期暂养也会影响鲫(Carassius auratus)的营养品质、食用品质和质构特性[9]。罗非鱼(Oreochromis mossambicus)暂养后鱼肉中辛醛和壬醛等物质含量降低, 苯甲醛和苯环芳烃类物质含量增加, 有利于脱除不良气味, 产生良好气味[10]。暂养净化后团头鲂(Megalobrama amblycephala)肌肉引起腥味、青草味等的一些醇、酸及烃类物质含量会降低, 呈现肉香、芳香味的醇、酸及烃类物质含量升高[11]。暂养环境因子也会影响动物肌肉品质, 陈亚楠等[12]发现, 温度12℃、氨氮质量浓度0、暂养密度1﹕4(m/v)的暂养环境有利于维持和提高斑点叉尾鮰(Ictalurus punctatus)的肌肉品质。微流水处理也可显著提高鳙和草鱼肌肉品质, 改善鱼肉滋味特征和气味特征, 适宜微流水处理后鱼肉腥味明显减弱, 鲜味明显增强[4, 13]。暂养对于不同鱼类影响不同, 最适暂养时间也不同, 而目前水产养殖中未有暂养处理对黄颡鱼肌肉品质和营养价值的影响研究。因此, 本试验开展不同暂养时间对黄颡鱼生长特性、血清生化指标、肌肉营养成分、肌肉氨基酸与脂肪酸组成、肌肉质构的影响研究, 旨在为提升黄颡鱼肌肉品质及营养价值提供改良途径, 为暂养处理在渔业生产中的应用提供理论基础。
1. 材料与方法
1.1 试验材料
试验在湖北省荆州市湖北太湖港水产产业技术研究院有限公司进行, 试验鱼购自湖北省某渔业养殖基地, 其初始体质量为(15.69±2.28) g, 体质健康的一龄黄颡鱼。试验池直径3 m, 深度2.5 m, 水深1.5 m。试验用水为上游太湖港水库优质水源, 经沙滤、沉淀和曝气后使用, 出水口流速200 L/h, 水温为20—23℃, pH为7.5—8.5。
1.2 试验设计与饲养管理
试验分为暂养0(对照组)、20d、30d和40d, 共4组。放养密度均为30 kg/m3, 每个暂养时间设置3个重复, 共12个养殖试验池。试验期间投喂黄颡鱼配合饲料(荆州市天佳饲料有限公司, 蛋白含量42%, 脂肪含量8%), 根据鱼体质量的变化使用对应规格的饲料。每天投喂3次, 投喂时间分别为08:00、14:00和19:00, 投喂量为鱼体质量的1.0%—1.5%, 观察其摄食情况。
1.3 样品采集和指标检测
水质指标监测 根据《水和废水检测分析方法》, 养殖过程中每隔10d测定试验池水体中总氮、总磷、氨态氮、亚硝态氮浓度和溶氧。各项指标均为各组所得平均值。
样品采集 暂养0组在试验开始后禁食24h取样, 暂养20d、30d和40d组分别在试验结束后禁食24h取样。对各试验池中的黄颡鱼称重, 统计存活尾数, 准确测量其体重和体长。计算生长指标: 增重率(WGR)、特定生长率(SGR)和成活率(SR); 每组随机抽取6尾黄颡鱼, 尾静脉采血, 750×g离心10min后取上清, 置于–20℃冰箱中保存, 用以测定血清生化指标; 于冰盘上解剖取其内脏、肝脏后称重, 计算肝体指数(HSI)和脏体指数(VSI), 同时根据体长和体重计算肥满度(CF); 每组随机抽取15尾黄颡鱼, 去皮剖离肌肉, 用于测定肌肉常规营养成分、氨基酸组成及含量和脂肪酸组成及含量; 每组随机取6尾黄颡鱼, 取黄颡鱼侧线以上靠近头部的肌肉, 剪成10 mm×10 mm×5 mm的方块, 进行肌肉质构测定。
指标测定 血清白蛋白(ALB)、总胆红素(TBIL)、总胆汁酸(TBA)、总胆固醇(TC)、肌酐(CRE)、尿酸(UA)、尿素(URE)、葡萄糖(GLU)含量和尿酐比(UCR)均采用全自动生化分析仪测定。总蛋白(TP)、γ-谷氨酰基转移酶(γ-GGT)、谷草转氨酶(AST)、谷丙转氨酶(ALT)和碱性磷酸酶(ALP)活性均采用南京建成生物工程研究所试剂盒测定。
肌肉常规营养成分的测定: 水分采用105℃恒温烘干法(GB/T6435-2006)测定; 粗蛋白质的测定采用凯氏定氮法(GB/T6432-1994)测定; 粗脂肪采用索氏乙醚抽提法(GB/T6433-2006)测定; 粗灰分采用马弗炉灼烧法(GB/T6438-1992)测定。黄颡鱼肌肉氨基酸组成及含量: 按食品安全国家标准(GB5009.124-2016)进行测定; 脂肪酸组成及含量按食品安全国家标准(GB/T 5009.168-2016)进行测定。
营养品质评价方法: 根据氨基酸评分标准模式[14]和中国预防医学科学院营养与食品卫生研究所提出的鸡蛋蛋白质模式进行营养评价。分别计算氨基酸评分(AAS)、化学评分(CS)和必需氨基酸指数(EAAI)。肌肉质构检测: 利用TA-XT Plus型物性测试仪对肌肉的硬度、弹性、凝聚性、胶黏性、咀嚼性、回复性及黏性进行检测。
计算公式 增重率WGR (%)=100×(Wt–W0)/W0;
特定生长率SGR (%/d)=100×(lnWt–lnW0)/t;
成活率SR (%)=100×St/S0;
肥满度SF (g/cm3)=100×W/L3;
肝体指数HSI=100×W肝脏/W;
脏体指数VSI=100×W内脏/W;
AAS=样品中某必需氨基酸含量(mg/g N)/[FAO/WHO标准模式中该氨基酸含量(mg/g N)];
CS=样品中某必需氨基酸含量(mg/g N)/全鸡蛋蛋白质中该氨基酸含量(mg/g N);
EAAI=[(100×A/AE)×(100×B/BE)×(100×C/CE)×···×(100×G/GE)]1/n。
式中, Wt表示养殖t时间时的体重; W0表示试验开始时体重; St表示养殖t时间时成活的尾数; S0表示试验开始时养殖尾数; W表示体重; W肝脏 表示肝脏重; W内脏 表示内脏重; L表示体长; n为比较的必需氨基酸个数; A、B、C、···, G为肌肉粗蛋白质中各必需氨基酸含量(%, 干物质基础); AE、BE、 CE、···, GE为全鸡蛋蛋白质中相对应的必需氨基酸含量(%, 干物质基础)。
1.4 数据统计与处理
数据经Excel 2019初步处理, 再使用SPSS 26.0软件进行统计学分析, 采用单因素方差分析(One-way ANOVA), 及并结合Duncan氏法多重比较, 以P<0.05表示差异显著, 数据均用“平均值±标准差”表示。
2. 结果
2.1 暂养期间试验池水质指标监测
如表 1所示, 暂养40d组水体总氮含量显著高于对照组和暂养20d组(P<0.05); 水体中氨态氮、亚硝态氮和溶氧含量, 各组间无显著性差异(P>0.05)。
表 1 暂养期间试验池水质指标监测Table 1. Monitoring water quality index of the test pond during purging time (mean±SE, mg/L)组别
Group氨态氮
Ammonia nitrogen亚硝态氮
Nitrite nitrogen总氮
Total nitrogen总磷
Total phosphorus溶氧
Dissolved oxygen0 0.04±0.03 0.01±0.03 1.56±0.19b 0.10±0.06 9.8±0.5 20d 0.03±0.02 0.01±0.02 1.41±1.29b 0.09±0.14 10.8±1.1 30d 0.04±0.06 0.01±0.01 2.01±0.13ab 0.12±0.23 9.7±0.8 40d 0.05±0.07 0.01±0.01 2.89±0.32a 0.13±0.07 9.5±0.4 注: 同列数据肩标不同小写字母表示差异显著(P<0.05), 相同或无字母表示差异不显著(P>0.05)。下同 Note: In the same column, values with different small letter superscripts show significantly difference (P<0.05), while with the same or no letter superscripts show no significantly difference (P>0.05). The same applies in below 2.2 暂养时间对黄颡鱼生长性能的影响
如表 2所示, 暂养40d组黄颡鱼末体重和增重率显著高于暂养20d和30d组(P<0.05)。暂养20d组黄颡鱼特定生长率显著高于暂养30d和40d组(P<0.05), 各组黄颡鱼成活率均高于90%。各组黄颡鱼肥满度和肝体比无显著性差异(P>0.05)。
表 2 暂养时间对黄颡鱼生长性能的影响Table 2. Effects of purging time on growth performance of Pelteobagrus fulvidraco组别Group 末体重
Wt (g)增重率
WGR (%)特定生长率
SGR (%/d)成活率
SR (%)肥满度
CF (g/cm3)肝体比
HSI脏体比
VSI0 100±0.00a 1.95±0.23 2.06±0.14 13.03±1.99 20d 39.84±1.06c 153.94±12.6c 4.66±0.18a 92.4±3.81b 1.92±0.20 2.02±0.19 12.97±2.49 30d 46.10±2.31b 193.82±16.8b 3.59±0.15b 92.7±1.35b 2.12±0.17 2.12±0.12 12.82±2.17 40d 55.52±1.44a 253.86±20.7a 3.16±0.20c 90.3±2.51b 2.32±0.12 2.23±0.11 12.54±2.45 2.3 暂养时间对黄颡鱼血清生化指标的影响
如表 3所示, 在肝功能指标中, 暂养30d和40d组黄颡鱼血清中的ALB和TP含量显著高于对照组和暂养20d组(P<0.05), γ-GGT和ALP活性, 以及TBA和TC含量显著低于对照组和暂养20d组(P<0.05); 暂养40d组黄颡鱼血清中的TBIL含量和AST活性显著低于其他组(P<0.05); 随着暂养时间延长, 各组间ALT活性呈降低趋势, 但无显著性差异(P>0.05)。在肾功能指标中, 暂养30d和40d组黄颡鱼血清中CRE含量和UCR显著低于对照组和暂养20d组(P<0.05)。各组黄颡鱼血清中UA、URE和GLU含量无显著性差异(P>0.05)。
表 3 暂养时间对黄颡鱼血清生化指标的影响Table 3. Effects of purging time on serum biochemical indexes of Pelteobagrus fulvidraco血清生化指标
Serum biochemical index组别Group 0 20d 30d 40d 白蛋白ALB (g/L) 10.1±1.4b 10.3±1.8b 13.5±2.1a 15.0±0.3a 总蛋白TP (g/L) 35.7±1.6b 36.3±0.9b 40.9±2.7a 44.8±3.9a 总胆红素TBIL (μmol/L) 9.8±1.9a 9.6±1.4a 7.8±1.0a 6.2±1.8b γ-谷氨酰基转移酶 γ-GGT (U/L) 6.1±0.7a 5.2±1.8a 2.8±0.2b 2.1±0.9b 谷草转氨酶AST (U/L) 322.7±5.2a 309.4±6.9a 289.6±5.8a 268.9±9.8b 谷丙转氨酶ALT (U/L) 242.0±8.2 241.5±8.7 238.6±11.5 222.8±6.7 碱性磷酸酶ALP (U/L) 95.9±9.8a 92.0±10.2a 67.1±4.1b 59.8±6.1b 总胆汁酸TBA (μmol/L) 16.8±3.1a 16.3±2.0a 14.9±6.1b 14.2±3.8b 总胆固醇TC (mmol/L) 10.1±2.7a 9.0±2.5a 6.1±0.6b 6.2±0.5b 肌酐CRE (μmol/L) 33.7±4.6a 29.1±6.2a 22.5±2.0b 19.6±2.4b 尿酸UA (μmol/L) 14.2±2.3 13.0±2.0 13.9±3.1 14.2±2.1 尿素URE (mmol/L) 2.2±0.3 2.3±0.6 2.1±0.2 2.1±0.3 葡萄糖GLU (mmol/L) 6.4±1.5 6.2±0.3 5.4±2.0 5.6±1.6 尿酐比UCR 9.6±1.5a 8.6±0.7a 6.7±2.1b 6.8±1.6b 注: 同行数据肩标不同小写字母表示差异显著(P<0.05), 相同或无字母表示差异不显著(P>0.05)。下同 Note: In the same row, values with different small letter superscripts show significantly difference (P<0.05), while with the same or no letter superscripts show no significantly difference (P>0.05). The same applies below 2.4 暂养时间对黄颡鱼肌肉常规营养成分的影响
如表 4所示, 暂养30d和40d组黄颡鱼肌肉中的粗蛋白质含量显著高于对照组和暂养20d组(P<0.05), 但粗脂肪含量显著低于对照组和暂养20d组(P<0.05); 各组黄颡鱼肌肉粗灰分和水分含量无显著性差异(P>0.05)。
表 4 暂养时间对黄颡鱼肌肉常规营养成分的影响(湿重, %)Table 4. Effects of purging time on muscle routine nutritional components of Pelteobagrus fulvidraco (wet weight, %)营养成分
Nutritional composition组别Group 0 20d 30d 40d 粗蛋白质CP 13.9±0.4b 15.7±0.2b 18.5±0.7a 18.9±0.8a 粗脂肪 EE 8.5±0.5a 7.8±0.3a 5.9±0.3b 5.8±0.2b 粗灰分Ash 1.2±0.1 1.2±0.1 1.2±0.2 1.2±0.1 水分Moisture 76.0±0.7 75.8±0.8 74.2±0.3 73.5±0.2 2.5 暂养时间对黄颡鱼肌肉氨基酸组成的影响
如表 5所示, 暂养30d和40d组黄颡鱼肌肉中亮氨酸(Leu)、异亮氨酸(Ile)、蛋氨酸(Met)、苏氨酸(Thr)、谷氨酸(Glu)和天冬氨酸(Asp)含量显著高于对照组和暂养20d组(P<0.05), 其余氨基酸含量各组间无显著差异(P>0.05)。暂养30d和40d组氨基酸总量(ΣAA)、必需氨基酸总量(ΣEAA)、非必需氨基酸总量(ΣNEAA)和鲜味氨基酸总量(ΣDAA)显著高于对照组和暂养20d组(P<0.05); 各组之间半必需氨基酸总量(ΣHEAA)无显著性差异(P>0.05)。
表 5 暂养时间对黄颡鱼肌肉氨基酸组成的影响(湿重, %)Table 5. Effects of purging time on muscle amino acid composition of Pelteobagrus fulvidraco (wet weight, %)氨基酸Amino acid 组别Group 0 20d 30d 40d 必需氨基酸 EAA 亮氨酸 Leu 1.21±0.02b 1.20±0.04b 1.39±0.02a 1.46±0.03a 异亮氨酸 Ile 0.58±0.03b 0.64±0.04b 0.66±0.02a 0.68±0.03a 苯丙氨酸 Phe 0.62±0.02 0.63±0.03 0.63±0.02 0.64±0.02 赖氨酸 Lys 1.41±0.04 1.43±0.03 1.48±0.03 1.47±0.04 蛋氨酸 Met 0.44±0.01b 0.49±0.02b 0.52±0.03a 0.54±0.03a 苏氨酸 Thr 0.75±0.02b 0.80±0.02b 0.83±0.05a 0.85±0.04a 缬氨酸 Val 0.68±0.02 0.69±0.03 0.72±0.04 0.71±0.03 半必需氨基酸 组氨酸 His 0.40±0.01 0.43±0.05 0.46±0.02 0.46±0.03 精氨酸 Arg 0.90±0.05 0.91±0.02 0.89±0.04 0.92±0.03 非必需氨基酸 谷氨酸 Glu* 1.77±0.11b 1.90±0.19b 2.20±0.16a 2.28±0.02a 天冬氨酸 Asp* 1.39±0.06b 1.59±0.24b 1.77±0.09a 1.81±0.03a 甘氨酸 Gly* 0.80±0.03 0.84±0.13 0.89±0.12 0.92±0.04 丙氨酸 Ala* 0.88±0.08 0.91±0.11 0.98±0.23 1.01±0.11 丝氨酸 Ser 0.70±0.02 0.72±0.22 0.75±0.10 0.78±0.10 脯氨酸 Pro 0.92±0.13 0.88±0.14 0.85±0.20 0.83±0.21 酪氨酸 Tyr 0.64±0.04 0.64±0.09 0.64±0.11 0.64±0.08 氨基酸总量 ΣAA 14.09±0.16b 14.70±0.28b 15.66±0.13a 16.00±0.11a 必需氨基酸总量 ΣEAA 5.69±0.03b 5.88±0.08b 6.23±0.09a 6.35±0.08a 半必需氨基酸总量 ΣHEAA 1.3±0.05 1.34±0.06 1.35±0.08 1.38±0.13 非必需氨基酸总量 ΣNEAA 7.1±0.10b 7.56±0.14b 8.08±0.10a 8.27±0.17a 鲜味氨基酸总量 ΣDAA 4.84±0.14b 5.24±0.20b 5.84±0.06a 6.02±0.07a 注: *代表鲜味氨基酸 Note: “*” represents delicious amino acids (DAA) 暂养时间对黄颡鱼肌肉的氨基酸评分(AAS)和化学评分(CS)值的影响见表 6。随暂养周期的延长, 必需氨基酸指数(EAAI)呈上升趋势, 暂养30d和40d组必需氨基酸指数显著高于对照组和暂养20d组(P<0.05), 暂养40d组黄颡鱼肌肉必需氨基酸指数最高。根据AAS和CS评分, 不同暂养周期下黄颡鱼肌肉中苯丙氨酸+酪氨酸评分最低, 其次为异亮氨酸, 说明各组第一限制性氨基酸均为苯丙氨酸+酪氨酸, 第二限制性氨基酸均为异亮氨酸。
表 6 暂养时间对黄颡鱼肌肉必需氨基酸评分、化学评分、必需氨基酸指数的影响Table 6. Effects of purging time on muscle essential AAS, CS and EAAI of Pelteobagrus fulvidraco (n=15)氨基酸Amino acid 0 20d 30d 40d 氨基酸评分
AAS化学评分
CS氨基酸评分
AAS化学评分
CS氨基酸评分
AAS化学评分
CS氨基酸评分
AAS化学评分
CS亮氨酸 Leu 0.46±0.07 0.40±0.07 0.46±0.05 0.40±0.02 0.53±0.13 0.46±0.07 0.56±0.09 0.47±0.14 异亮氨酸 Ile 0.36±0.05# 0.32±0.14# 0.40±0.02# 0.35±0.04# 0.50±0.04# 0.41±0.12# 0.54±0.02# 0.41±0.15# 赖氨酸 Lys 0.54±0.11 0.57±0.06 0.64±0.06 0.58±0.01 0.71±0.12 0.72±0.11 0.79±0.20 0.76±0.22 蛋氨酸+半胱氨酸 Met+Cys 0.41±0.10 0.33±0.11 0.48±0.05 0.36±0.06 0.51±0.04 0.42±0.16 0.58±0.18 0.44±0.08 苯丙氨酸+酪氨酸 Phe+Tyr 0.28±0.08* 0.32±0.06* 0.39±0.02* 0.33±0.02* 0.39±0.06* 0.36±0.05* 0.47±0.16* 0.39±0.11* 苏氨酸 Thr 0.53±0.09 0.38±0.09 0.57±0.10 0.40±0.05 0.60±0.04 0.52±0.10 0.66±0.18 0.55±0.07 缬氨酸 Val 0.61±0.08 0.59±0.05 0.62±0.08 0.60±0.04 0.69±0.05 0.64±0.11 0.76±0.18 0.69±0.17 必需氨基酸指数(EAAI) 52.68±1.80b 55.21±1.75b 60.17±1.97a 62.87±2.58a 注: *代表第一限制性氨基酸; #代表第二限制性氨基酸 Note: *represents the first limited amino acid; #represents the second limited amino acid 2.6 暂养时间对黄颡鱼肌肉脂肪酸组成的影响
如表 7所示, 暂养30d和40d组黄颡鱼肌肉中14-甲基十五烷酸甲酯、二十碳五烯酸甲酯(EPA-M)和n-6多不饱和脂肪酸(n-6 PUFA)含量显著高于对照组和暂养20d组(P<0.05); 暂养40d组黄颡鱼肌肉中二十二碳六烯酸甲酯(DHA-M)和二十碳五烯酸+二十二六烯酸(EPA+DHA)、单不饱和脂肪酸(MUFA)、多不饱和脂肪酸(PUFA)和单不饱和脂肪酸+多不饱和脂肪酸(MUFA+PUFA)含量显著高于其他组(P<0.05), 但二十碳五烯酸: 二十二碳六烯酸(EPA:DHA)比例显著低于其他组(P<0.05); 暂养30d组黄颡鱼肌肉中棕榈油酸甲酯、棕榈酸甲酯、反油酸甲酯、硬酯酸甲酯、二十碳三烯酸甲酯、花生烯酸含量显著低于其他组(P<0.05); 除上述脂肪酸外, 各组间其他脂肪酸含量无显著性差异(P>0.05)。
表 7 暂养时间对黄颡鱼肌肉脂肪酸组成的影响Table 7. Effects of purging time on muscle fatty acid composition of Pelteobagrus fulvidraco (mg/kg)脂肪酸Fatty acid 组别Group 0 20d 30d 40d 月桂酸甲酯 C12:0 0.86±0.03 0.94±0.04 0.91±0.06 1.01±0.03 肉豆蔻烯酸甲酯 C14:1 2.79±0.11 3.07±0.11 2.81±0.15 3.08±10 十四酸甲酯 C14:0 2.60±0.05 2.67±0.07 2.58±0.10 2.79±0.08 棕榈油酸甲酯 C16:1 20.11±0.25a 21.04±0.36a 16.73±0.45b 22.52±0.37a 棕榈酸甲酯 C16:0 57.88±0.23a 58.61±0.28a 48.72±0.35b 58.62±0.29a 14-甲基十五烷酸甲酯 0.63±0.18b 0.67±0.14b 0.82±0.05a 0.88±0.07a 14-甲基十六烷酸甲酯 1.23±0.04 1.24±0.03 1.21±0.03 1.26±0.05 亚油酸甲酯 96.01±6.75 97.17±5.21 103.30±8.46 108.06±4.70 反-9-十八碳烯酸甲酯 2405.39±359.12 2418.66±379.88 2533.57±436.17 2619.81±423.30 反油酸甲酯 C18:1T 302.11±27.13a 315.65±23.15a 284.38±29.77b 320.62±21.07a 11-反-十八烯酸 0.58±0.03 0.65±0.02 0.56±0.05 0.66±0.02 硬酯酸甲酯 54.29±0.10a 58.36±0.11a 49.22±0.29b 60.46±0.13a 花生四烯酸甲酯 C20:4 2.83±0.04 2.79±0.02 2.99±0.01 2.9±0.01 二十碳五烯酸甲酯(EPA-M) C20:5 3.06±0.04b 3.19±0.11b 3.54±0.05a 3.75±0.06a 二十碳三烯酸甲酯 C20:3 4.43±0.03a 4.61±0.08a 3.71±0.10b 4.66±0.08a 二十碳二烯酸甲酯 C20:2 4.01±0.04 4.25±0.09 4.07±0.12 4.26±0.08 花生烯酸 276.29±0.49a 290.29±0.33a 253.17±0.67b 289.14±0.30a 19-甲基十九烷酸甲酯 2.93±0.07 3.04±0.04 3.06±0.04 2.89±0.02 二十二碳六烯酸甲酯(DHA-M) C22:6 19.76±0.31b 20.37±0.27b 21.28±0.20b 26.47±0.25a 脂肪酸总量 3257.79±80.67 3307.27±79.33 3336.63±88.90 3533.84±83.34 单不饱和脂肪酸 MUFA 3007.27±60.11b 3049.36±56.77b 3091.22±67.97b 3255.83±64.35a 多不饱和脂肪酸PUFA 130.10±7.26b 132.38±5.56b 138.89±6.80b 150.10±3.41a 单不饱和脂肪酸+多不饱和脂肪酸 MUFA+PUFA 3137.37±34.07b 3181.74±35.66b 3230.11±49.05b 3405.93±36.00a n-3多不饱和脂肪酸 n-3 PUFA 3.06±0.17 3.19±0.07 3.54±0.12 3.75±0.16 n-6多不饱和脂肪酸 n-6 PUFA 107.28±1.01b 108.82±1.21b 114.07±1.59a 119.88±1.33a 二十碳五烯酸+二十二六烯酸 EPA+DHA 22.82±0.12b 23.56±0.14b 24.82±0.09b 30.22±0.15a 二十碳五烯酸:二十二碳六烯酸 EPA:DHA 0.154858±0.000024a 0.156603±0.000017a 0.166353±0.000021a 0.141670±0.000034b 饱和脂肪酸:不饱和脂肪酸 SFA:UFA 0.038382±0.000045 0.03945±0.000033 0.032972±0.000031 0.037555±0.000027 2.7 暂养时间对黄颡鱼肌肉质构的影响
如表 8所示, 暂养40d组黄颡鱼肌肉的硬度和胶黏性显著高于其他组(P<0.05); 暂养30d和40d组黄颡鱼肌肉的弹性、咀嚼性和回复性显著高于对照组和暂养20d组(P<0.05); 暂养30d组黄颡鱼肌肉的黏性显著高于其他组(P<0.05); 不同养殖周期黄颡鱼肌肉凝聚性无显著性差异(P>0.05)。
表 8 暂养时间对黄颡鱼肌肉质构特性的影响Table 8. Effects of purging time on muscle textural properties of Pelteobagrus fulvidraco质构特性
Textural properties组别Group 0 20d 30d 40d 硬度Hardness (g) 6009.1±637.0b 6042.8±698.8b 6725.6±539.6b 7999.3±577.4a 弹性Springiness (%) 0.64±0.16b 0.69±0.09b 0.84±0.02a 0.94±0.04a 凝聚性Cohesiveness 0.64±0.07 0.63±0.03 0.55±0.07 0.60±0.02 胶黏性Gumminess (g) 4007.8±352.8b 4120.8±318.6b 4220.0±339.0b 5070.7±409.2a 咀嚼性Chewiness (g) 4377.4±593.5b 4429.1±613.6b 5946.5±559.0a 5255.6±517.5a 回复性Resilience 42.2±3.9b 48.3±4.6b 57.7±2.3a 59.2±3.8a 黏性Viscosity (g.sec) –11.5±1.1a –10.7±0.7a –9.4±0.9b –12.3±0.9a 3. 讨论
3.1 暂养期间试验池水质对黄颡鱼的影响
良好的水质是水产养殖的首要条件, 而衡量水质好坏的指标主要有氨态氮、pH和DO等[15, 16]。黄颡鱼属于无鳞鱼, 对生长环境和养殖管理要求较高, 耐低氧能力差, 为了让其快速生长, 必须对水质进行严格把控, 并保持养殖池的溶氧在5 mg/L以上。并有研究显示, 水体中高氨态氮过高会胁迫大菱鲆[17] (Scophthalmus maximus)、大西洋比目鱼[18](Hippoglossus hippoglossus)等鱼类生长, 当氨氮含量>2 mg/L时, 对黄颡鱼的生长与饲料利用率有明显的抑制作用[19]。在本实验中, 流水来自上游优质水源水库, 能够保持在养殖池溶氧水平均超过9.0 mg/L, 氨态氮含量在0.03—0.05 mg/L, 亚硝态氮含量在0.01 mg/L, 因此, 开放流水养殖模式可为鱼类养殖提供安全的水质环境。
3.2 暂养时间对黄颡鱼生长性能的影响
暂养可减少鱼类应激反应、提高鱼肉品质及存活率, 还可帮助其适应新环境[3, 20]。黄颡鱼属小型鱼类, 生长速度较慢, 适当延长暂养周期, 可以提高养殖产量。本研究结果显示, 暂养时间的延长可以显著提高黄颡鱼的增重率, 其原因是由于试验鱼正处于快速生长期。暂养20d黄颡鱼特定生长率最高, 可能由于黄颡鱼前期生长发育较快, 后期发育减缓。形体指标是评价鱼体生长与健康的重要指标, 脏体比等指标增加时, 可能会引起鱼体内脏器官炎症或脂肪沉积, 影响内脏器官的生理功能[21]。本研究显示, 随着暂养周期的延长, 各试验组间脏体比虽无显著性差异, 但呈现逐渐降低的趋势, 因此适宜的暂养在一定程度上可以促进黄颡鱼肝脏健康。
3.3 暂养时间对黄颡鱼血清生化指标的影响
鱼类血液生化指标与其生理健康、物质代谢、营养及疾病状况有着密切关系[22, 23]。血清中的酶活力水平可以反映蛋白、肽类及氨基酸等物质的吸收代谢状况, ALB、TP及球蛋白等指标都可直观反映机体健康及免疫状况[24, 25]。TP可以反映机体蛋白质吸收和代谢状况, 其含量的增加可以促进机体蛋白质沉积, 促进鱼体生长[26]; 血清 ALB可以反映机体的营养能力[27]。本研究显示, 暂养30d和40d组血清中的ALB和TP显著高于对照组和暂养20d组, 说明适当延长黄颡鱼的暂养时间可提高其肝脏对蛋白质的吸收能力, 促进鱼体快速生长, 增强免疫力。血清ALT和AST作为肝脏细胞中重要的转氨酶, 可反映蛋白质代谢利用率, 间接指示氨基酸代谢强度[25], γ-GGT广泛存在于生物各组织及器官, 它们参与调节动物机体蛋白质合成与代谢, 可作为反映肝脏功能的重要指标[28], 在正常情况下血液中含量较低。研究结果表明, 随着暂养时间的延长, 黄颡鱼血清中的ALT、AST及γ-GGT含量呈下降趋势, 暂养40d组鱼类血清中AST和γ-GGT含量显著低于对照组, 试验结果证明暂养时间为40d时, 机体内氨基酸的代谢强度较低, 进而有利于鱼体蛋白的沉积, 这与肌肉中蛋白质含量结果一致。
TBIL、TBA和TC作为机体代谢废物, 其含量过高会对动物肝脏造成损伤。在本实验中, 暂养30d和40d组黄颡鱼血清中TBA和TC含量显著低于对照组和暂养20d组; 随着暂养周期的延长, 暂养40d组鱼类血清中TBIL含量显著低于其他各组, 研究表明适宜暂养时间可以降低黄颡鱼血清中TBIL、TBA和 TC等代谢废物的含量, 有利于机体的健康。血清中的CRE、UA、URE、GLU和UCR的含量过高会造成机体肾脏功能损伤[29], 暂养30d和40d组鱼类血清中CRE和UCR含量显著低于对照组和暂养20d组, URE和GLU含量随着暂养周期的延长呈下降趋势, 证明暂养40d组黄颡鱼肾功能状况最好, 适当延长开放流水养殖模式下的暂养时间能有效地改善鱼体的生理功能, 增强免疫力和代谢能力, 减轻人工养殖过程中造成的肝功能和肾功能损伤, 减少病害发生的优势。
3.4 暂养时间对黄颡鱼肌肉常规营养成分的影响
粗蛋白质、粗脂肪和粗灰分等物质是鱼类肌肉的重要常规成分, 其含量可以用来评价鱼类肌肉的营养品质, 且蛋白质作为六大营养要素之首, 其含量高低也是评价水产品品质和营养价值的重要指标[30, 31]。本研究显示, 暂养30d和40d组黄颡鱼肌肉中粗蛋白质含量显著高于对照组和暂养20d组, 粗脂肪含量显著低于对照组和暂养20d组, 表明暂养30d和40d组黄颡鱼肌肉品质更优, 具有高蛋白质低脂肪的特点。其原因可能是由于暂养30d和40d组黄颡鱼血清中ALB、TP等物质含量较高, 可以促进机体内蛋白质沉积; ALT和AST和γ-GGT等物质含量较低, 机体本身氨基酸代谢强度较低, 有利于蛋白质沉积; 这与短期暂养对鲫肉品质影响结果相似, 但鲫暂养后粗蛋白和粗脂肪都会降低, 其原因可能由于此试验过程不予喂食, 鱼体生命活动消耗脂肪和蛋白质[9]。n-3 PUFA能有效降低肝胰脏及腹腔脂肪组织中的脂质蓄积[32], 本研究显示, 延长暂养时间, 黄颡鱼肌肉n-3 PUFA含量呈上升趋势, 且暂养30d和40d组黄颡鱼肝肾功能状况较好, 能量消耗大, 从而降低脂质蓄积, 加快脂肪分解为机体供能, 降低鱼体脂肪储存含量; 因此, 在开放流水养殖模式下, 适宜的暂养时间有利于促进黄颡鱼肌肉高蛋白质低脂肪的形成。
3.5 暂养时间对黄颡鱼肌肉氨基酸组成的影响
必需氨基酸的种类、数量和组成比例是决定食物中蛋白质营养价值的重要指标[33]; 肌肉的美味程度与其鲜味氨基酸的组成和含量密切相关[34, 35]。本研究显示, 暂养40d组黄颡鱼肌肉中的必需氨基酸总量和鲜味氨基酸总量最高, 因此暂养40d黄颡鱼口感优于其他组。其原因可能由于暂养40d组黄颡鱼血清中ALT、AST和γ-GGT含量低, 氨基酸代谢强度低, 且其肝肾功能强, 能够有效吸收食物中机体所需氨基酸, 促进机体内必需氨基酸和鲜味氨基酸总量提高。因此可以减少淡水鱼特有的土腥味, 且其营养价值更高。这与周敏等[8]感官评定暂养过程中草鱼肉鱼腥味和泥土味降低的研究结果相似, 表明暂养会影响鱼体肌肉氨基酸组成, 从而促使鱼肉口感更佳。
蛋白质营养价值的评价取决于氨基酸组成[29]。本实验结果显示, 各组第一限制性氨基酸均为Phe+Tyr, 第二限制性氨基酸均为Ile; 这与刘梅等[29]研究发现野生与池塘内循环水养殖黄颡鱼的第一限制性氨基酸一致; 此外, 本实验中暂养40d组各种氨基酸的评分和必需氨基酸指数(EAAI)最高, 且与刘梅等[29]试验研究中野生组指数接近, 因此在开放流水养殖模式下, 适宜暂养时间可以促进鱼体氨基酸组成更合理, 鱼肉营养价值更高, 从而提升黄颡鱼肌肉品质。
3.6 暂养时间对黄颡鱼肌肉脂肪酸的含量影响
鱼体含有丰富的脂肪酸, SFA是机体重要的能量来源, 不饱和脂肪酸具有促进细胞正常生理、降低血液黏稠度和促进大脑发育等功能[36, 37]。PUFA作为人体和动物生长发育所需的必需脂肪酸, 还可显著提高肉质香味[36, 38]; EPA和DHA可作为衡量肌肉脂肪酸品质的指标[39], 其具有促进体内饱和脂肪酸代谢和提高免疫力的功能。本研究显示, 暂养40d组黄颡鱼肌肉中MUFA、PUFA及EPA+DHA含量最高, 黄颡鱼肌肉营养价值高于其他组。这与袁小琛等[3]适宜暂养可提高鳙肌肉必需脂肪酸和多不饱和脂肪酸的相对含量结果相似。因此, 在开放流水养殖模式下, 适宜暂养时间可以提高黄颡鱼肌肉脂肪酸含量和鱼体营养价值。
3.7 暂养时间对黄颡鱼肌肉质构的影响
质构作为肌肉组织的重要物理特性, 是目前用于评价水产品肉质最广泛的方法之一[33], 可以从硬度、弹性、咀嚼性和回复性等指标来客观评价肌肉的品质[40]。且鱼肉的硬度和弹性作为反映其品质的主要特质, 与鱼体的脂肪含量和肌纤维密切相关[41]。本研究显示, 暂养40d黄颡鱼肌肉硬度胶黏性、弹性、咀嚼性和回复性高, 鱼肉口感最好, 其原因可能由于暂养时间长, 鱼体脂肪含量低, 蛋白质含量高, 有利于肌原纤维蛋白、基质蛋白及肌纤维等肌肉微观结构生长有关。与上述结果类似, 适宜暂养可显著提高鳙肌肉弹性[3]; 草鱼经过50d的暂养, 其肌肉硬度、弹性和内聚性等指标显著高于对照组[5]。因此, 在开放流水养殖模式下适宜的暂养时间可促使黄颡鱼的肉质更加结实、富有弹性、有嚼劲及适口性更好。
4. 结论
在开放流水养殖模式下, 暂养40d对黄颡鱼肌肉品质和营养价值综合提升效果最好, 可增强鱼体肝肾功能、提高免疫与代谢能力、增加肌肉蛋白含量和降低脂肪含量, 同时增加肌肉中鲜味氨基酸含量, 减少池塘养殖鱼体中存在的土腥味, 增强鱼肉弹性, 适口性更佳。但还应探索延长暂养时间是否能进一步提升养殖品质; 且开放流水养殖模式成本较一般池塘养殖成本高, 所以暂养时间、养殖效益及养殖品质最佳效益平衡点需要进一步探索。
-
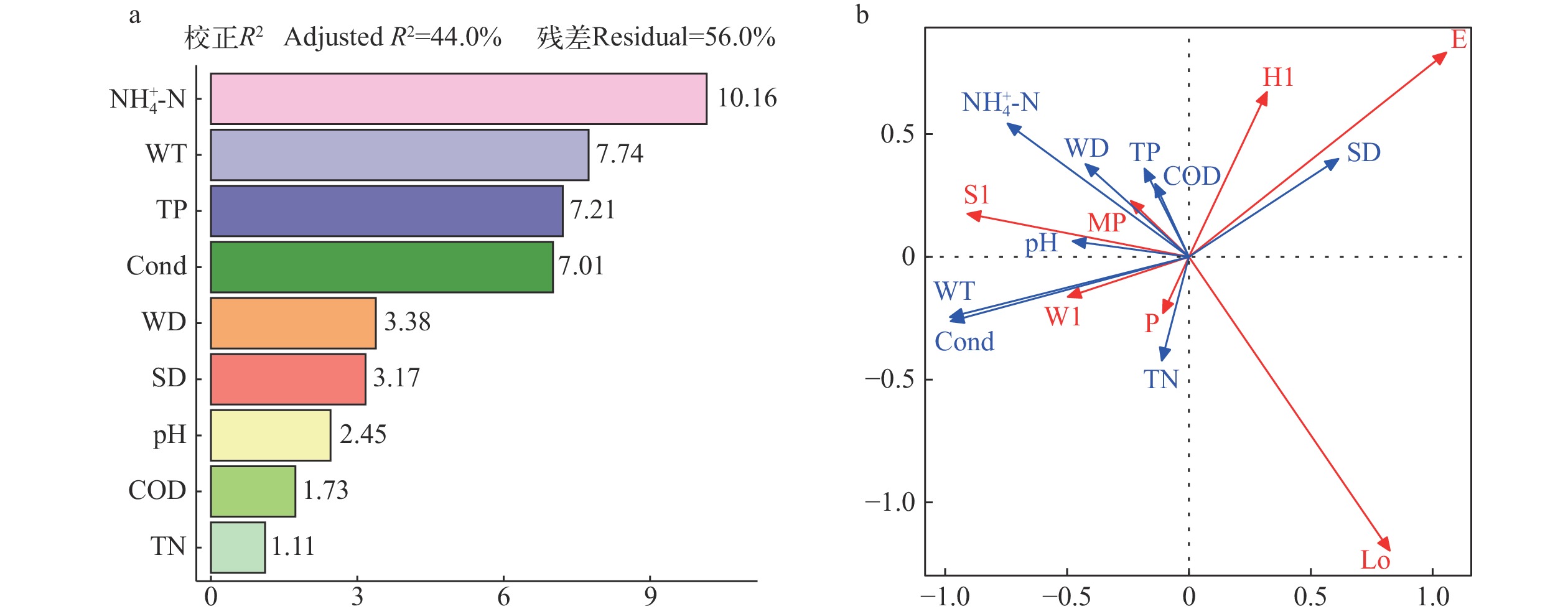
图 4 浮游植物优势功能群与环境因子的相关性分析
a. 所有环境因子单独解释率的重要性排序; b. 优势功能群与主要环境因子的RDA分析
Figure 4. Correlation analysis between phytoplankton dominant functional group and environmental factor
a. Importance ranking of individual explanatory rates of all environmental factors; b. RDA analysis of phytoplankton dominant functional group and major environmental factor
表 1 东太湖应急水源地水体理化指标季节变化(平均值±标准误)
Table 1 Seasonal changes of main physical and chemical indicators in the emergency water supply for East Taihu Lake (mean±SE)
环境因子
Parameter春季
Spring夏季
Summer秋季
Autumn冬季
WinterWD (m) 1.68±0.18 1.89±0.18 1.98±0.06 1.85±0.14 SD (m) 0.60±0.34ab 0.49±0.87b 0.50±0.02b 0.67±0.05a WT (℃) 22.26±0.07ab 31.27±0.05a 18.11±0.05bc 8.40±0.06c DO (mg/L) 8.55±0.15ab 5.15±0.07b 8.72±0.13a 9.55±0.08a pH 8.41±0.05ab 8.82±0.08a 8.28±0.17b 8.19±0.02b Cond
(µS/cm)360.47±1.46ab 439.17±0.44a 359.41±4.01ab 267.62±1.05b TN (mg/L) 0.73±0.04 0.63±0.02 0.73±0.09 0.58±0.05 TP (mg/L) 0.06±0.01b 0.05±0.00ab 0.04±0.00b 0.05±0.00a ${\rm{NH}}^+_4 $-N (mg/L) 0.04±0.00b 0.08±0.01a 0.06±0.01b 0.05±0.00b CODMn (mg/L) 3.64±0.06ab 3.82±0.04a 3.11±0.05b 3.61±0.05ab Chl.a
(µg/L)7.95±0.41b 10.97±0.87ab 12.36±0.60a 7.30±1.57b 注: 同一行数据上标注有不同字母代表有显著性差异 (P<0.05)Note: Different letters on the same line indicate significant differences (P<0.05) 表 2 东太湖应急水源地浮游植物功能群组成
Table 2 Phytoplankton functional group composition in the emergency water supply for East Taihu Lake
功能群
Functional group代表属/种
Representative species生境特征
Habitat characteristic出现频率
Frequency (%)F因子
F factorC 小环藻Cyclotella spp. 富营养、中小型水体 71.43 4 D 针杆藻Synedra spp.
菱形藻Nitzschia spp.富营养、浑浊、透明度低 96.43 4 E 锥囊藻Dinobryon sp.
鱼鳞藻Peridinium sp.贫营养或中营养、小型浅水水体 21.43 2 F 卵囊藻Oocystis sp.
月牙藻Selenastrum sp.
蹄形藻Kirchneriella spp.中或富营养型、洁净、深度混合 64.29 3 G 空球藻Eudorina elegans 富营养、停滞水体 21.43 0 H1 束丝藻Aphanizomenon spp.
长孢藻Dolichospermum spp.富营养、分层、含氮量低、浅水 71.43 1 J 四星藻Tetrastrum spp.
栅藻Scenedesmus spp.
多芒藻Golenkinia spp.
十字藻Crucigenia spp.富营养、混合、浅水 100.00 2 K 隐球藻Aphanocapsa sp. 富营养、浅水 10.71 5 LO 多甲藻Peridinium sp.
角甲藻Ceratium hirundinella
双眉藻Amphora spp.贫到富营养、中到大型水体、深水或浅水 64.29 3 MP 卵形藻Cocconeis spp.
曲壳藻Achnanthes sp.
舟形藻Navicula spp.
异极藻Gomphonema spp.经常性搅动、无机浑浊、浅水水体 100.00 5 N 鼓藻Cosmarium sp.
角星鼓藻Staurastrum sp.持续或半持续的混合水层 67.86 2 P 直链藻Melosira spp.
新月藻Closterium sp.持续或半持续的混合水层 89.29 5 S1 假鱼腥藻Pseudanabaena sp.
浮丝藻Planktothrix spp.浑浊、透明度低、混合水体 96.43 0 T 游丝藻Planctonema sp. 持续混合水层 17.86 5 TC 鞘丝藻Lyngbya sp. 富营养、静水或者流动缓慢、具挺水植物 64.29 2 W1 裸藻Euglena spp.
扁裸藻Phacus sp.小型有机、浅水水体 89.29 3 W2 囊裸藻Trachelomonas sp. 中营养、浅水 57.14 3 X1 纤维藻Ankistrodesmus spp.
单针藻Monoraphidium sp.超富营养、浅水 85.71 3 X2 蓝隐藻Chroomonas spp.
翼膜藻Pteromonas sp.中到富营养、浅水 89.29 4 X3 弓形藻Schroederia spp. 贫营养、混合、浅水 57.14 4 Y 隐藻Cryptomonas spp.
裸甲藻Gymnodinium aeruginosum静水 78.57 3 注: F因子根据文献生境及功能群特征赋值Note: F-factor are assigned values based on literature habitat and functional group characteristics -
[1] Yuan Y, Jiang M, Liu X, et al. Environmental variables influencing phytoplankton communities in hydrologically connected aquatic habitats in the Lake Xingkai basin [J]. Ecological Indicators, 2018(91): 1-12.
[2] Li X, Zhao Y, Chai F, et al. Phytoplankton community structure dynamics in relation to water environmental factors in Zhalong wetland [J]. International Journal of Environmental Research and Public Health, 2022, 19(22): 14996. doi: 10.3390/ijerph192214996
[3] Sun X, Wang W. The impact of environmental parameters on phytoplankton functional groups in northeastern China [J]. Ecological Engineering, 2021(164): 106209.
[4] Bai Y, Huang T, Miao W. Spatio-temporal dynamics of phytoplankton in a diversion reservoir and the major influencing factors: taxonomic versus functional groups classification [J]. Environmental Science and Pollution Research International, 2023, 30(51): 111344-111356. doi: 10.1007/s11356-023-30111-9
[5] Zhang M, Lv X, Dong J, et al. Multiple habitat templates for phytoplankton indicators within the functional group system [J]. Hydrobiologia, 2023, 850(1): 5-19. doi: 10.1007/s10750-022-05024-2
[6] Han L, Li Q, Chen W, et al. The key environmental factors driving the succession of phytoplankton functional groups in Hongfeng Reservoir, southwest China [J]. Journal of Oceanology and Limnology, 2022, 40(4): 1472-1484. doi: 10.1007/s00343-021-1120-z
[7] 胡韧, 蓝于倩, 肖利娟, 等. 淡水浮游植物功能群的概念、划分方法和应用 [J]. 湖泊科学, 2015, 27(1): 11-23.] doi: 10.18307/2015.0102 Hu R, Lan Y Q, Xiao L J, et al. The concepts, classification and application of freshwater phytoplankton functional groups [J]. Journal of Lake Sciences, 2015, 27(1): 11-23. [ doi: 10.18307/2015.0102
[8] Reynolds C S, Huszar V, Kruk C, et al. Towards a functional classification of the freshwater phytoplankton [J]. Journal of Plankton Research, 2002, 24(5): 417-428. doi: 10.1093/plankt/24.5.417
[9] Padisák J, Crossetti L O, Naselli-Flores L. Use and misuse in the application of the phytoplankton functional classification: a critical review with updates [J]. Hydrobiologia, 2009(621): 1-19.
[10] Salmaso N, Naselli-Flores L, Padisák J. Functional classifications and their application in phytoplankton ecology [J]. Freshwater Biology, 2015, 60(4): 603-619. doi: 10.1111/fwb.12520
[11] Padisák J, Borics G, Grigorszky I, et al. Use of phytoplankton assemblages for monitoring ecological status of lakes within the water framework directive: the assemblage index [J]. Hydrobiologia, 2006(553): 1-14.
[12] Wu Z, Wang F, Wang X, et al. Water quality assessment using phytoplankton functional groups in the middle-lower Changjiang River, China [J]. Limnologica, 2023(99): 126056.
[13] 张虎军, 宋挺, 朱冰川, 等. 太湖蓝藻水华暴发程度年度预测 [J]. 中国环境监测, 2022, 38(1): 157-164.] Zhang H J, Song T, Zhu B C, et al. Annual forecast of the extent of cyanobacteria bloom in Taihu Lake [J]. Environmental Monitoring in China, 2022, 38(1): 157-164. [
[14] 黄祥飞. 湖泊生态调查观测与分析 [M]. 北京: 中国标准出版社, 2000.] Huang X F. Survey, Observation and Analysis of Lake Ecology [M]. Beijing: Standards Press of China, 2000. [
[15] 胡鸿钧, 魏印心. 中国淡水藻类: 系统、分类及生态 [M]. 北京: 科学出版社, 2006.] Hu H J, Wei Y X. The Freshwater Algae of China [M]. Beijing: Science Press, 2006. [
[16] 铁程, 张榆霞, 金玉, 等. 显微镜计数法测定浮游植物的研究进展及修订建议 [J]. 中国环境监测, 2018, 34(6): 179-186.] Tie C, Zhang Y X, Jin Y, et al. Research progress and revised recommendations of microscope count method for the enumeration of phytoplankto [J]. Environmental Monitoring in China, 2018, 34(6): 179-186. [
[17] 国家环境保护总局《水和废水监测分析方法》编委会. 水和废水监测分析方法 (第四版) [M]. 北京: 中国环境科学出版社, 2002.] Editorial Board of State Environmental Protection Administration “Water and Wastewater Monitoring and Analysis Methods”. Water and Wastewater Monitoring and Analysis Methods (4th edition) [M]. Beijing: China Environmental Science Press, 2002. [
[18] Borics G, Várbíró G, Grigorszky I, et al. A new evaluation technique of potamo-plankton for the assessment of the ecological status of rivers [J]. River Systems, 2007, 17(3/4): 465-486.
[19] 武宇圣, 朱韻洁, 庞燕, 等. 基于功能群的浮游植物群落驱动因子及水质评价适用性分析: 以骆马湖为例 [J]. 环境科学研究, 2023, 36(10): 1915-1926.] Wu Y S, Zhu Y J, Pang Y, et al. Driving factors of phytoplankton functional groups and applicability of water quality evaluation: a case study of Lake Luoma [J]. Research of Environmental Sciences, 2023, 36(10): 1915-1926. [
[20] Li C, Feng W, Chen H, et al. Temporal variation in zooplankton and phytoplankton community species composition and the affecting factors in Lake Taihu-a large freshwater lake in China [J]. Environmental Pollution, 2019(245): 1050-1057.
[21] Xiao L J, Wang T, Hu R, et al. Succession of phytoplankton functional groups regulated by monsoonal hydrology in a large canyon-shaped reservoir [J]. Water Research, 2011, 45(16): 5099-5109. doi: 10.1016/j.watres.2011.07.012
[22] 赵璐, 欧阳添, 纪璐璐, 等. 三峡水库蓄水对支流浮游植物功能群的影响及与资源利用效率的关系 [J]. 环境科学, 2023, 44(2): 857-867.] Zhao L, Ouyang T, Ji L L, et al. Impounding impacts of the Three Gorges Reservoir on phytoplankton function groups and its relationship with resource use efficiency [J]. Environmental Science, 2023, 44(2): 857-867. [
[23] Varol M. Phytoplankton functional groups in a monomictic reservoir: seasonal succession, ecological preferences, and relationships with environmental variables [J]. Environmental Science and Pollution Research International, 2019, 26(20): 20439-20453. doi: 10.1007/s11356-019-05354-0
[24] 张俊芳, 陈威, 宋以兴, 等. 雅砻江下游浮游植物群落结构时空变化特征及环境驱动因子 [J]. 长江流域资源与环境, 2023, 32(5): 950-960.] Zhang J F, Chen W, Song Y X, et al. Spatio-temporal variation of phytoplankton community structure and environmental driving factors in lower reaches of Yalong River [J]. Resources and Environment in the Yangtze Basin, 2023, 32(5): 950-960. [
[25] 朱爱民, 李嗣新, 胡俊, 等. 三峡水库支流拟多甲藻水华的形成机制 [J]. 生态学报, 2014, 34(11): 3071-3080.] Zhu A M, Li S X, Hu J, et al. The mechanism for occurrence of Peridiniopsis blooms in the tributaries of Three Gorges Reservoir [J]. Acta Ecologica Sinica, 2014, 34(11): 3071-3080. [
[26] 罗敏纳, 孙蓓丽, 朱冰川, 等. 太湖流域浮游植物功能类群分布特征及其与环境因子的关系 [J]. 湖泊科学, 2022, 34(5): 1471-1483.] doi: 10.18307/2022.0506 Luo M N, Sun B L, Zhu B C, et al. Distribution characteristics of phytoplankton functional groups and their relationship with environmental factors in Taihu Basin [J]. Journal of Lake Sciences, 2022, 34(5): 1471-1483. [ doi: 10.18307/2022.0506
[27] 董静, 李艳晖, 李根保, 等. 东江水系浮游植物功能群季节动态特征及影响因子 [J]. 水生生物学报, 2013, 37(5): 836-843.] doi: 10.7541/2013.107 Dong J, Li Y H, Li G B, et al. Seasonal dynamics characteristics and affecting physical factors of phytoplankton functional groups in Dongjiang River [J]. Acta Hydrobiologica Sinica, 2013, 37(5): 836-843. [ doi: 10.7541/2013.107
[28] Cao H, Zhang K, Deng D, et al. Environmental heterogeneity affecting spatial distribution of phytoplankton community structure and functional groups in a large eutrophic lake, Lake Chaohu, China [J]. Environmental Science and Pollution Research International, 2023, 30(32): 79001-79014. doi: 10.1007/s11356-023-28043-5
[29] Li X, Yu H, Wang H, et al. Phytoplankton community structure in relation to environmental factors and ecological assessment of water quality in the upper reaches of the Genhe River in the Greater Hinggan Mountains [J]. Environmental Science and Pollution Research International, 2019, 26(17): 17512-17519. doi: 10.1007/s11356-019-05200-3
[30] Liu J, Chen Y, Li M, et al. Water-level fluctuations are key for phytoplankton taxonomic communities and functional groups in Poyang Lake [J]. Ecological Indicators, 2019(104): 470-478.
[31] 陶敏, 岳兴建, 罗家林, 等. 四川丘陵区水库浮游植物功能群季节演替特征及驱动因子 [J]. 水生生物学报, 2021, 45(4): 826-837.] doi: 10.7541/2021.2020.236 Tao M, Yue X J, Luo J L, et al. Seasonal succession of phytoplankton functional groups and its driving factors in reservoirs in hilly regions of Sichuan Province [J]. Acta Hydrobiologica Sinica, 2021, 45(4): 826-837. [ doi: 10.7541/2021.2020.236
[32] Anderson S I, Barton A D, Clayton S, et al. Marine phytoplankton functional types exhibit diverse responses to thermal change [J]. Nature Communications, 2021, 12(1): 6413. doi: 10.1038/s41467-021-26651-8
[33] 李娜, 周绪申, 孙博闻, 等. 白洋淀浮游植物群落的时空变化及其与环境因子的关系 [J]. 湖泊科学, 2020, 32(3): 772-783.] doi: 10.18307/2020.0317 Li N, Zhou X S, Sun B W, et al. Spatiotemporal variation of phytoplankton community and its relationship with environmental factors in the Lake Baiyangdian [J]. Journal of Lake Sciences, 2020, 32(3): 772-783. [ doi: 10.18307/2020.0317
[34] Borics G, Tóthmérész B, Lukács B A, et al. Functional groups of phytoplankton shaping diversity of shallow lake ecosystems [J]. Hydrobiologia, 2012(698): 251-262.
[35] McCarthy M J, James R T, Chen Y, et al. Nutrient ratios and phytoplankton community structure in the large, shallow, eutrophic, subtropical Lakes Okeechobee (Florida, USA) and Taihu (China) [J]. Limnology, 2009, 10: 215-227. doi: 10.1007/s10201-009-0277-5
[36] Chen Y, Qin B, Teubner K, et al. Long-term dynamics of phytoplankton assemblages: Microcystis-domination in Lake Taihu, a large shallow lake in China [J]. Journal of Plankton Research, 2003, 25(4): 445-453. doi: 10.1093/plankt/25.4.445
[37] 叶琳琳, 吴晓东, 刘波, 等. 太湖西北湖区浮游植物和无机、有机氮的时空分布特征 [J]. 湖泊科学, 2017, 29(4): 859-869.] doi: 10.18307/2017.0409 Ye L L, Wu X D, Liu B, et al. Temporal and spatial distributions of phytoplankton and inorganic and organic nitrogen in northwest region of Lake Taihu [J]. Journal of Lake Sciences, 2017, 29(4): 859-869. [ doi: 10.18307/2017.0409
[38] 杨潇, 马吉顺, 张欢, 等. 鄱阳湖不同水文期浮游生物群落结构特征和影响因素及水质评价 [J]. 水生生物学报, 2021, 45(5): 1093-1103.] Yang X, Ma J S, Zhang H, et al. Community structure and the water quality during different hydrological periods in Poyang Lake [J]. Acta Hydrobiologica Sinica, 2021, 45(5): 1093-1103. [
[39] 刘洋, 安瑞志, 杨号, 等. 西藏拉鲁湿地浮游植物群落时空分布特征及其驱动因子 [J]. 湖泊科学, 2024, 36(2): 403-415.] doi: 10.18307/2024.0216 Liu Y, An R Z, Yang H, et al. Spatial-temporal distribution characteristics and its driving factors of phytoplankton community in Lhalu Wetland, Xizang, China [J]. Journal of Lake Sciences, 2024, 36(2): 403-415. [ doi: 10.18307/2024.0216
[40] Shen J, Qin G, Yu R, et al. Urbanization has changed the distribution pattern of zooplankton species diversity and the structure of functional groups [J]. Ecological Indicators, 2021(120): 106944.
[41] 夏莹霏, 胡晓东, 徐季雄, 等. 太湖浮游植物功能群季节演替特征及水质评价 [J]. 湖泊科学, 2019, 31(1): 134-146.] doi: 10.18307/2019.0113 Xia Y F, Hu X D, Xu J X, et al. Seasonal succession of phytoplankton functional group and assessment of water quality in Lake Taihu [J]. Journal of Lake Sciences, 2019, 31(1): 134-146. [ doi: 10.18307/2019.0113
[42] Crossetti L O, de M Bicudo C E. Phytoplankton as a monitoring tool in a tropical urban shallow reservoir (Garças Pond): the assemblage index application [J]. Hydrobiologia, 2008, 610(1): 161-173. doi: 10.1007/s10750-008-9431-z
[43] 王飞虎, 杨越, 张洋, 等. 黄河流域河南段浮游藻类功能群分布特征及影响因子 [J]. 水生生物学报, 2024, 48(3): 513-523.] Wang F H, Yang Y, Zhang Y, et al. Distribution characteristics and influencing factors of phytoplankton functional groups of the Yellow River basin in Henan Province [J]. Acta Hydrobiologica Sinica, 2024, 48(3): 513-523. [
-
期刊类型引用(5)
1. 胥晴,原居林,倪蒙,邹松保,刘梅,顾志敏. 不同净养时间和养殖密度下大口黑鲈的表型特征、健康状况及肌肉营养品质. 水产学报. 2025(01): 176-192 .  百度学术
百度学术
2. 汪兰,夏雨婷,胡澳,陈朗,郭晓嘉,乔宇,吴文锦,石柳,黄云,彭条凤,熊光权,陈胜. 维生素C对禁食黄颡鱼抗氧化能力和肌肉品质的影响. 广东海洋大学学报. 2024(01): 28-34 .  百度学术
百度学术
3. 胥晴,原居林,倪蒙,邹松保,刘梅,顾志敏. 生态净养对淡水养殖鱼类肌肉品质影响的研究进展. 水产科学. 2024(01): 152-162 .  百度学术
百度学术
4. 孙丽慧,包成荣,李倩,姜建湖,陈建明,高令梅,郭建林. 工厂化循环水养殖模式对大口黑鲈肌肉营养成分和挥发性风味物质的影响. 动物营养学报. 2024(05): 3192-3208 .  百度学术
百度学术
5. 周秀珍,张毅,周钦,丁雪燕,李明,贾加,黄菊,王扬. 循环水净化养殖过程中大口黑鲈生长及肌肉品质变化. 食品科学. 2024(11): 75-83 .  百度学术
百度学术
其他类型引用(4)



 下载:
下载: