HYDROSTATIC INDUCTION OF TRIPLOID LEUCISCUS BRANDTI (DYBOWSKI)
-
摘要:
研究运用组织学和对比试验等方法筛选静水压诱导三倍体勃氏雅罗鱼的最适条件。研究表明: (1)受精后5min的组织切片, 可见第二极体明显突出于受精卵卵膜, 准备排出第二极体。(2)诱导起始时间5min的受精率与对照组无显著性差异(P>0.05), 但显著高于其他试验组(P<0.05); 起始时间4min和5min的孵化率无显著差异(P>0.05), 但均显著低于对照组(P<0.05), 显著高于其他试验组(P<0.05); 起始时间5min的三倍体率显著高于其他试验组(P<0.05)。(3)静水压压强60 MPa的受精率与对照组之间无显著性差异(P>0.05), 但显著高于其他试验组(P<0.05); 65 MPa的孵化率显著低于其他各组(P<0.05), 50、55和60 MPa之间的孵化率无显著性差异(P>0.05), 但均显著低于对照组(P<0.05); 60 MPa的三倍体率显著高于其他试验组(P<0.05)。(4)诱导持续时间4min与5min之间的受精率无显著性差异(P>0.05), 但显著高于其他各试验组(P<0.05), 显著低于对照组(P<0.05); 各试验组的孵化率均显著低于对照组(P<0.05), 持续时间4min的孵化率和三倍体率均显著高于其他试验组(P<0.05)。在试验条件下, 当水温(17±1)℃时, 三倍体勃氏雅罗鱼的最佳诱导条件为受精后5min, 静水压强60 MPa, 持续处理时间4min。
Abstract:In this study, the optimum conditions for hydrostatic induction of triploid Leuciscus brandti were selected by means of histological and comparative tests. The results showed that: (1) The tissue section examined 5min after fertilization showed that the second polar body was obviously protruding from the egg membrane of the fertilized egg, indicating its readiness for discharge. (2) The fertilization rate of 5min initiation time was not significantly different from the control group (P>0.05), but was significantly higher than that of other experimental groups (P<0.05). There was no significant difference in incubation rate between 4min and 5min (P>0.05), but it was significantly lower than that of the control group (P<0.05), and significantly higher than that of other experimental groups (P<0.05). The triploid rate of the initial time of 5min was significantly higher than that of other experimental groups (P<0.05). (3) There was no significant difference between the fertilization rate of hydrostatic pressure 60 MPa and control group (P>0.05), but it was significantly higher than that of other experimental groups (P<0.05). The hatching rate of 65 MPa was significantly lower than that of other groups (P<0.05), and the hatching rate of 50, 55 and 60 MPa had no significant difference (P>0.05), but was significantly lower than that of the control group (P<0.05). The triploid rate of 60 MPa was significantly higher than that of other experimental groups (P<0.05). (4) There was no significant difference in fertilization rate between 4 and 5min induction duration (P>0.05), but it was significantly higher than that of other experimental groups (P<0.05), and significantly lower than that of the control group (P<0.05). The hatching rate of experimental groups was significantly lower than that of the control group (P<0.05), and the hatching rate and triploid rate lasting 4min were significantly higher than those of other experimental groups (P<0.05). Under the conditions of this experiment, with a water temperature of (17±1)℃, the best induction conditions for triploid Leuciscus brandti were 5min after fertilization, the hydrostatic pressure of 60 MPa, and the continuous treatment duration of 4min.
-
Keywords:
- Hydrostatic pressure /
- Triploidy /
- Ploidy identification /
- Induction conditions /
- Leuciscus brandti
-
勃氏雅罗鱼Leuciscus brandti (Dybowski), 又叫滩头鱼、大红线、金滩头、三块鱼等, 是唯一溯河洄游型产卵的鲤科鱼类。其易驯化、抗盐碱性高、垂钓时上钩率高; 且自身身体两侧有红色纵带, 色彩鲜艳; 同时肉质细嫩、味道鲜美, 营养价值较高, 此鱼是集垂钓、观赏和美食于一体的优质养殖品种[1]。但因其生长缓慢[2], 作为商品鱼个体规格偏小, 还未受到广大养殖户和消费者的青睐, 故此鱼的养殖前景和消费市场空间极大。目前勃氏雅罗鱼生长缓慢已成为亟需解决的难题, 而解决鱼类生长速度缓慢的最佳手段是三倍体人工育种技术。
水产动物三倍体人工育种技术属于“染色体组工程”的研究内容[3]。人工诱导的水产动物三倍体细胞中拥有三套染色体组, 单数的染色体组会导致减数分裂时染色体不能正常配对, 无法形成具有生殖能力的正常配子, 所以三倍体在理论上是不育的[4]。由于三倍体的不育性, 使其生长速度和肉制品质等特性均优于二倍体[5, 6]。主要原因有两方面, 一是三倍体鱼体内用于性腺发育的能量转移至生长等方面[7]; 二是避免了如二倍体鱼体因产卵而导致的生长停滞及身体损伤等现象[5]。目前, 国内外研究学者已在多种水产动物中成功诱导三倍体鱼种, 例如: 鲤(Cyprinus carpio)[8]、虹鳟(Oncorhynchus mykiss)[9]、美洲牡蛎(Crassostrea virginica)[10]、马苏大麻哈鱼(Oncorhynchus masou)[11]等。本试验将勃氏雅罗鱼作为研究对象, 通过组织切片及对比试验筛选出静水压诱导三倍体勃氏雅罗鱼的适宜条件, 旨在为勃氏雅罗鱼及其他雅罗鱼类的规模化三倍体制种提供技术参考和理论依据, 为勃氏雅罗鱼养殖业的发展奠定基础。
1. 材料与方法
1.1 试验鱼
本试验所用亲鱼引进于吉林省延边州图们江的野生3龄勃氏雅罗鱼, 雌鱼体重约为500—650 g, 雄鱼体重约为400—550 g, 选取性腺发育良好、体表无外伤的健康亲鱼暂养于延边马苏大麻哈水产良种场。
1.2 人工催产及授精
按照杨荣国等[12]的方法进行人工催产。利用LRH-A2+DOM两种药物作为催产药物, 采用背鳍基部注射法进行人工注射。水温(17±1)℃, 第一次注射LRH-A2 (25 mg/kg), 12h后第二次注射LRH-A2 (25 mg/kg)和DOM (6 mg/kg)的混合药剂, 12h后采用腹部挤压法进行干法授精, 授精后用鞣酸进行脱黏处理。
1.3 受精卵组织切片的制作
取0—6min内的受精卵进行石蜡切片的制作[13], 取样时间间隔为10s, 每次取样约30粒。观察受精卵的受精过程, 以了解勃氏雅罗鱼精子入卵及第二极体排出的时间, 为静水压诱导起始时间的筛选确定研究范围。
1.4 三倍体诱导
在(17±1)℃条件下, 用孔径300 μm的筛网将勃氏雅罗鱼的受精卵滤出, 然后装入到静水压力机(POWER TEAM)的压力舱中, 用水填满压力舱后设置压强开始静水压诱导试验。
筛选诱导的起始时间 在(17±1)℃条件下, 将试验分为5组, 每组取受精卵1000粒, 1组不处理直接孵化作为对照组, 4个试验组分别采用不同诱导起始时间(即受精3min、4min、5min和6min后的受精卵), 设置静水压强55 MPa, 持续时间为4min。处理完毕后移入孵化器中开始孵化。
筛选诱导的静水压强 静水压诱导的起始时间确定后, 进行静水压强的筛选。将试验分为5组, 每组取受精卵1000粒, 1组不处理直接孵化作为对照组, 4个试验组的静水压强分别为50、55、60和65 MPa, 持续时间为4min。处理完毕后移入孵化器中开始孵化。
筛选诱导的持续时间 静水压诱导起始时间及压强确定后, 进行持续处理时间的筛选。将试验分为5组, 每组取受精卵1000粒, 1组不处理直接孵化作为对照组, 4个试验组的持续处理时间分别为3min、4min、5min和6min。处理完毕后移入孵化器中开始孵化。
1.5 受精率和孵化率
受精卵孵化24h内, 每8h对孵化器上层漂浮的未成功受精的死亡卵粒进行收集, 以统计每个试验组的受精率; 受精卵孵化7d后计数每个试验组仔鱼出膜的数量, 统计孵化率。具体计算公式:
受精卵粒数=总卵粒数-未受精死亡卵粒数
受精率(%)=受精卵粒数/总卵粒数×100
孵化率(%)=出膜仔鱼数/受精卵粒数×100
1.6 倍性鉴定
以二倍体勃氏雅罗鱼仔鱼细胞中DNA为对照, 每组随机抽取破膜5d左右的仔鱼各40尾进行三倍体鉴定(CyFlow®倍性分析仪), 然后统计三倍体率。
三倍体率(%) =三倍体仔鱼数/检测仔鱼总数×100
1.7 数据分析
试验数据利用Excel 2018和SPSS 25.0软件进行单因素方差分析及多重比较, 显著水平设定为P<0.05, 数据采用“平均值±标准差”表示。
2. 结果
2.1 观察受精卵和第二极体
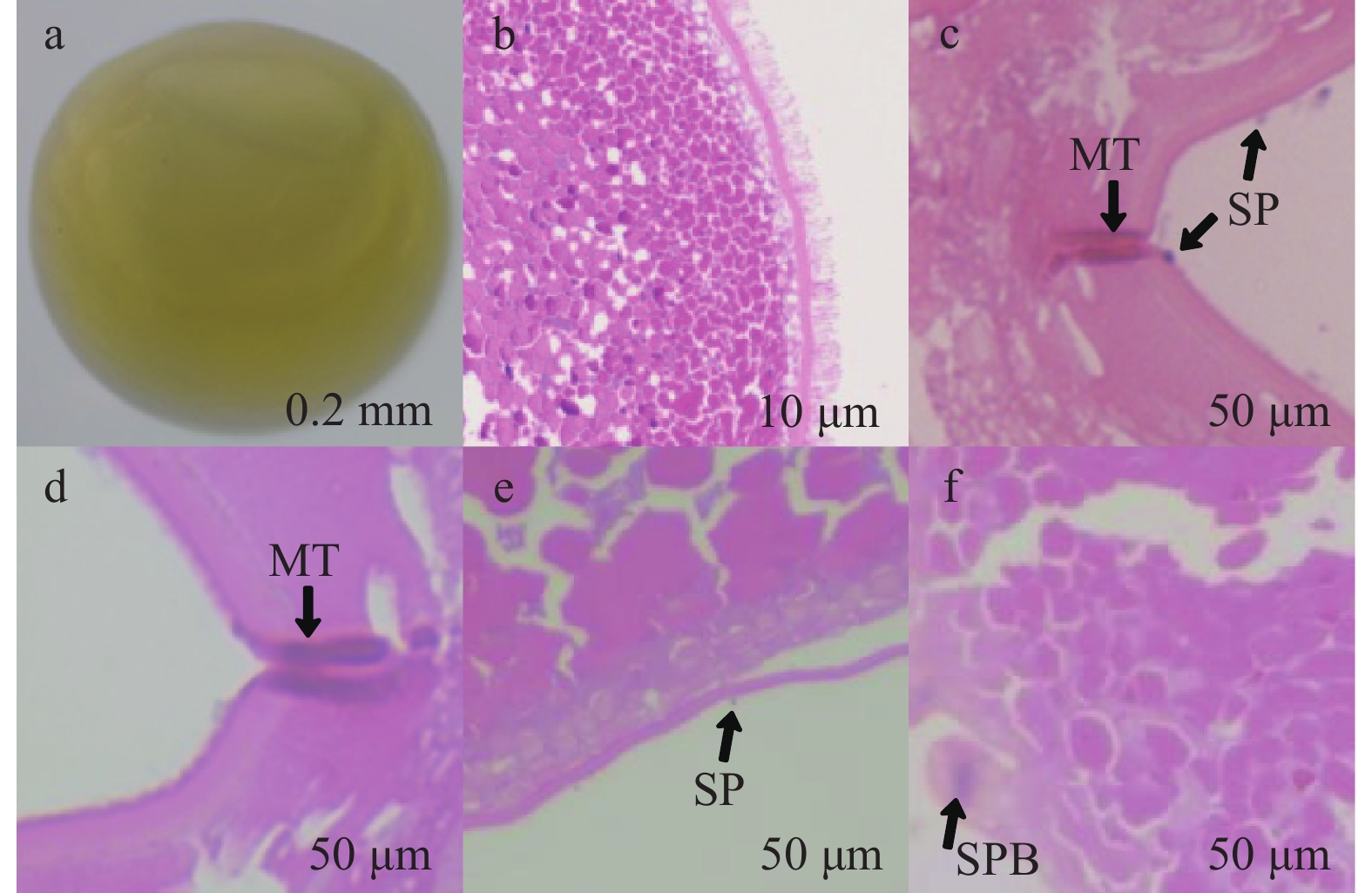
勃氏雅罗鱼卵子受精过程及第二极体的发生组织切片如图 1所示。
图 1a所示为勃氏雅罗鱼的成熟卵, 其颜色为明黄色, 圆球体, 平均直径约2 mm, 表面富有弹性, 内含有大量卵黄物质, 成熟卵遇水后表面有黏性, 吸水后会轻微膨胀。
图 1b所示, 卵膜与质膜相连, HE染色后颜色较深, 卵膜外有绒毛状结构。
图 1c所示, 在成熟卵动物极处, 卵膜表面深陷, 形成精孔器。精孔器呈漏斗状, 分为前庭和精孔管两个部分, 为精子进入卵细胞的通道。受精后10s, 可见少量精子聚集于精孔器的前庭, 个别精子进入到前庭1/3处, 此时精孔管为打开状态, 未见有堵塞物。卵细胞正处于第二次减数分裂中期, 开始准备受精。
图 1d所示, 在受精后2.5min, 通过精孔器的精子开始进入到卵子的细胞质内, 刺激卵子继续发育, 从而完成第二次减数分裂, 形成成熟卵核。此时, 精孔管上方开始闭合, 有絮状物堵塞。
图 1e所示, 在受精后3.5min, 卵子表面仍可见精子附着, 但此时, 精子已无法进入卵细胞内, 并且在观察过程中未发现有多精子入卵的现象, 初步判断, 勃氏雅罗鱼为单精入卵, 单精受精。
图 1f所示, 受精后4min, 第二次减数分裂进入末期, 组织切片显示第二极体已经形成。在受精后5min的受精卵切片中, 可见第二极体明显突出于受精卵卵膜, 卵子准备排出第二极体。
在对受精卵切片观察过程中发现, 同一批受精卵由于个体的差异性或受外界环境的影响, 导致个体间发育速度不完全一致。
2.2 筛选诱导的起始时间
试验比较了不同诱导起始时间对勃氏雅罗鱼受精率、孵化率和三倍体率的影响。结果如表 1所示, 诱导起始时间5min的试验组的受精率与对照组之间无显著差异(P>0.05), 但显著高于其他试验组的受精率(P<0.05)。
表 1 诱导起始时间对勃氏雅罗鱼受精率、孵化率和三倍体率的影响Table 1. Effect of initiation time of induction on fertilization rate, hatching rate, and triploid rate of Leuciscus brandti项目Item 诱导起始时间
Initiation time of induction (min)0/对照组 3 4 5 6 受精率
Fertilization rate (%)76.82±
1.60a61.93±
0.43d72.04±
1.65b75.36±
0.80a67.34±
1.66c孵化率
Hatchability (%)79.82±
0.61a61.56±
1.46c73.30±
1.79b78.80±
0.57b62.37±
1.21c三倍体率
Triploid rate (%)— 37.55±
2.44c48.51±
3.09b56.39±
1.75a51.64±
2.54b注: 表中数据为3个重复的平均值; 同一行数据右上角含有相同英文上标字母或无上标表示无显著差异(P≥0.05); 下同Note: Data are means of triplicates. Means in each bar sharing the same superscript letter or absence of superscripts indicate no significant difference determined by Tukey’s test (P≥0.05), the same applies below 各试验组的孵化率均显著低于对照组(P<0.05), 起始时间4min和5min的试验组的孵化率差异不显著(P>0.05), 但均显著高于其他试验组(P<0.05)。
起始时间5min的试验组三倍体率显著高于其他试验组(P<0.05)。
2.3 筛选诱导的静水压强
试验比较了不同静水压强对勃氏雅罗鱼受精率、孵化率和三倍体率的影响, 如表 2所示, 静水压强为60 MPa的试验组受精率与对照组差异不显著(P>0.05), 但显著高于其他试验组(P<0.05)。
表 2 静水压强对勃氏雅罗鱼受精率、孵化率和三倍体率的影响Table 2. Effects of hydrostatic pressure on fertilization rate, hatching rate, and triploid rate of Leuciscus brandti项目Item 静水压强
Hydrostatic pressure (MPa)大气压/
对照组50 55 60 65 受精率
Fertilization rate (%)76.82±
1.60a63.63±
1.65c72.30±
1.34b75.81±
0.62a50.48±
1.82d孵化率
Hatchability (%)79.82±
0.61a71.73±
2.00b70.27±
1.00b71.40±
2.08b57.65±
1.39c三倍体率
Triploid rate (%)— 43.22±
1.18d57.55±
3.09c70.53±
3.04a64.08±
3.68b各试验组的孵化率均显著低于对照组(P<0.05), 静水压强为50、55和60 MPa的试验组之间的孵化率差异不显著(P>0.05), 但均显著高于65 MPa试验组的孵化率(P<0.05)。
在4个试验组中, 三倍体率最高的为静水压强60 MPa的试验组, 其三倍体率显著高于其他试验组(P<0.05)。
2.4 筛选诱导的持续时间
试验比较了不同持续处理时间对勃氏雅罗鱼受精率、孵化率和三倍体率的影响(表 3), 各试验组的受精率均显著低于对照组(P<0.05), 持续处理时间为4min与5min的试验组的受精率差异不显著(P>0.05), 但均显著高于其他试验组(P<0.05)。
表 3 持续处理时间对勃氏雅罗鱼受精率、孵化率和三倍体率的影响Table 3. Effects of continuous treatment time on fertilization rate, hatching rate, and triploid rate of Leuciscus brandti项目Item 持续处理时间
Continuous treatment time (min)0/对照组 3 4 5 6 受精率
Fertilization rate (%)76.82±
1.60a67.82±
2.33c72.58±
2.31b69.01±
1.67bc59.52±
2.43d孵化率
Hatchability (%)79.82±
0.61a67.45±
0.97c70.59±
1.16b66.32±
2.72c60.59±
1.03d三倍体率
Triploid rate (%)— 81.72±
3.64c97.44±
0.62a89.60±
2.82b69.09±
6.64d各试验组的孵化率均显著低于对照组(P<0.05), 持续处理时间为4min的试验组的孵化率显著高于其他试验组(P<0.05)。
持续处理时间为4min的试验组的三倍体率显著高于其他试验组(P<0.05)。
2.5 倍性鉴定
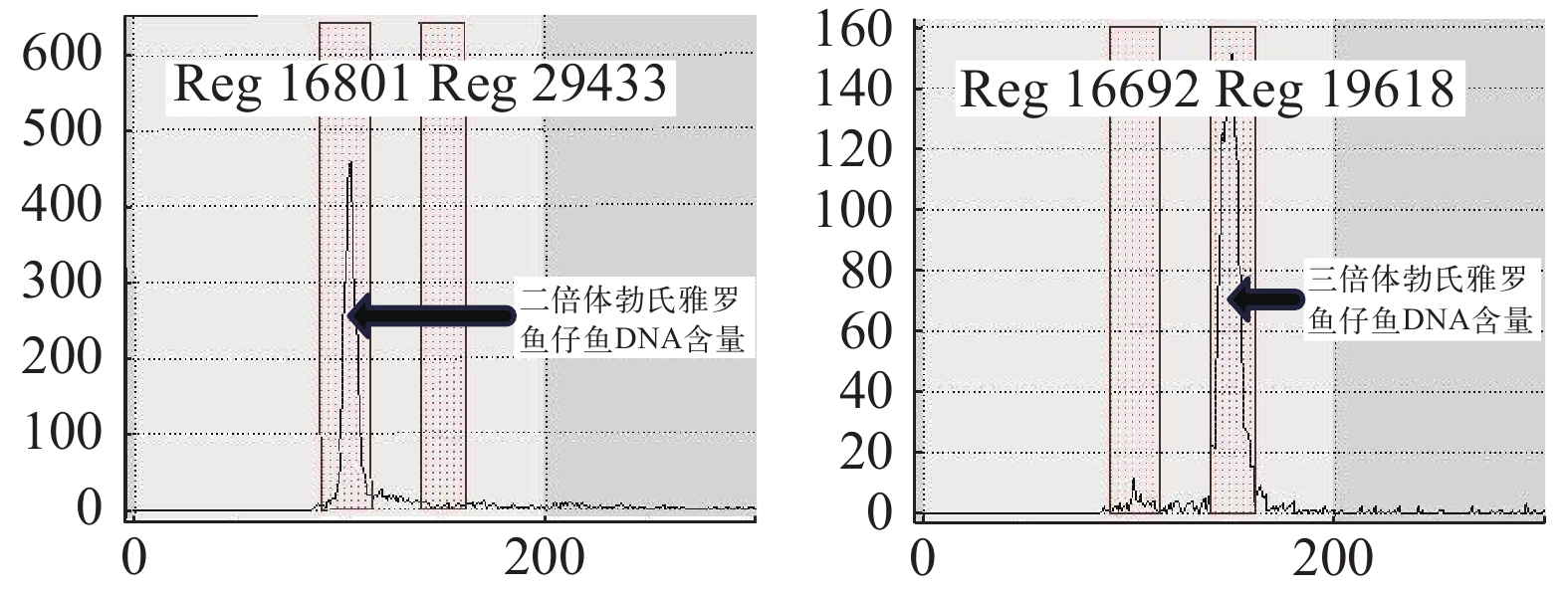
如图 2所示, 峰值所对应的横坐标为检测样本细胞的DNA相对含量, 在固定的参数条件下, 所检测的二倍体勃氏雅罗鱼仔鱼细胞中DNA相对含量聚集在100数值处附近, 各试验组所诱导获得的三倍体勃氏雅罗鱼仔鱼细胞中DNA相对含量聚集在150数值处附近, 三倍体仔鱼细胞DNA相对含量约为二倍体的1.5倍。
3. 讨论
3.1 三倍体勃氏雅罗鱼诱导条件的筛选
水产动物三倍体在理论上具有不育性, 所以减少了性腺发育时的能量消耗, 而在促进机体生长、延长水产动物生命周期和提高水产动物品质等多方面存在潜在价值[14]。人工诱导水产动物三倍体多是通过物理方法阻止受精卵排出第二极体, 来实现染色体的加倍, 从而发育成三倍体个体[15]。物理方法又分为温度休克和静水压两种, 在进行大规模生产时, 为降低经济成本, 获得更多的三倍体个体, 一次生产需处理较多的受精卵, 而温度休克在处理较多的受精卵时, 对受精卵处理的一致性较差, 往往难以获得理想的诱导效果; 而静水压处理程序比较简单, 处理的方式易于标准化, 通过在密闭空间里施加压力, 对压力缸内所有受精卵都能够实现同期处理, 处理时间较短, 对受精卵的损伤较小, 因此往往可获得较高的成活率和三倍体诱导率[16]。刘志鹏等[17]在半滑舌鳎(Cynoglossus semilaevis)受精后5min, 冷休克温度为4℃海水中对受精卵持续诱导20min, 获得了最高的三倍体率为35%, 而在此诱导条件下受精卵的孵化率只有5.5%, 后期通过观察发现在经过冷休克处理后, 胚胎在很大程度上受到了损伤后期无法发育, 导致了较低孵化率。陈松林等[18]在半滑舌鳎受精后5min, 采用36 MPa的静水压诱导受精卵4min, 得到了100%的三倍体率, 该诱导效果显著优于上述通过冷休克法获得的三倍体率。Peruzzi等[19]分别采用静水压法和冷休克法对狼鲈(Dicentrarchus labrax L.)进行了三倍体的诱导, 结果表明静水压试验组比冷休克组有更好的三倍体诱导效果。因此, 本试验采用静水压对勃氏雅罗鱼进行了三倍体的诱导, 获得的三倍体率最高约为97%, 受精率和孵化率分别达到了对照组的95%和88%, 获得了良好的诱导效果。
静水压诱导效果会受到压强大小、持续处理时间及诱导起始时间(即受精时间) 3个因素共同影响, 将这些影响因素把握好就能得到较好的诱导效果。在3个影响因素中, 首先需要掌握的是诱导起始时间, 因为三倍体诱导的原理就是通过一定的方式保留受精卵的第二极体, 从而实现染色体的加倍, 形成三倍体, 所以要在第二极体已经形成但还未排出的这段时间进行静水压的处理, 压力过早会抑制第二极体的形成, 压力过晚则无法达到保留第二极体的目的; 对于压强而言也是如此, 过高的压强会损伤受精卵, 导致畸形后代的产生, 甚至造成很高的死亡率, 而较低的压强无法抑制第二极体的排出, 形成高比例的二倍体; 当处理时间过长时也会导致染色体的受损, 影响胚胎的发育。
静水压诱导起始时间主要与水产动物的生存环境和生理特性即胚胎发育的速度有关, 大多数冷水性鱼类胚胎发育时间较长, 其处理开始的时间较晚, 如虹鳟等鲑科鱼类在受精后40min进行静水压处理效果较好[20, 21], 温水性鱼类胚胎发育较快, 一般在受精后4—5min进行处理, 如草鱼(Ctenopharyngodon idella)[22]、翘嘴鳜(Siniperca chuatsi)[23]。本试验所筛选出的静水压诱导勃氏雅罗鱼适宜起始时间同样为受精后5min。桂建芳等[24]对水晶彩鲫(Carassius auratus transparent colored variety)受精卵切片观察发现, 受精后4—5min受精卵进入第二次减数分裂末期, 受精后6min第二极体已排出。对勃氏雅罗鱼受精卵进行切片制备和观察, 发现受精后4min左右, 受精卵进入第二次减数分裂末期, 少量细胞切片显示第二极体已经形成, 但仍处于卵细胞内, 受精后5min受精卵切片中, 可见第二极体明显突出于受精卵卵膜, 准备排出第二极体, 观察结果与上述对水晶彩鲫受精卵研究结果相似。在以往通过静水压诱导水产动物三倍体的报道中, 所使用的最佳压力大多在50—65 MPa [24]。本试验所筛选出的勃氏雅罗鱼静水压最适压力为60 MPa, 与上述研究结果相符。持续处理时间与卵的特性有关, 鲤科鱼类静水压适宜持续处理时间为2—3min, 如草鱼[22]、团头鲂(Megalobrama amblycephala)[25]。桂建芳等[24]对静水压诱导水晶彩鲫三倍体适宜持续时间进行筛选时发现, 黏性卵比浮性卵所需要的持续时间相对要长, 原因可能是黏性卵的卵膜较厚, 卵的硬度相对强, 更能够承受压力作用, 所以需要的压力效应时间长。在本试验中, 研究对象勃氏雅罗鱼为黏性卵, 筛选出其静水压诱导三倍体所需持续处理时间为4min, 比同属于鲤科鱼类产浮性卵的草鱼所需要的持续处理时间长。
经过静水压压强、持续处理时间及诱导起始时间3个因素的对比试验最终确定三倍体勃氏雅罗鱼的最佳诱导条件为受精后5min, 60 MPa静水压强持续处理4min, 其三倍体率达到97%, 受精率和孵化率均在70%以上。尤颖哲[26]在利用静水压法诱导双斑东方鲀(Takifugu bimaculatus)三倍体的研究中发现其三倍体率在96%以上, 孵化率在77%以上, 分析结果发现, 静水压压强的大小和持续处理时间的长短均能对受精卵造成一定程度的损伤, 导致孵化率的下降。刘金相等[16]利用静水压法诱导牙鲆(Paralichthys olivaceus♀)×圆斑星鲽(Verasper variegatus♂)杂交三倍体的研究中发现其孵化率和三倍体率均在30%以下, 分析其原因可能是鱼卵的成熟程度不均一造成的。而造成本试验的受精率和孵化率均在70%以上的结果可能与上述报道有相似之处, 故还需进一步优化试验的方法和实验条件。
3.2 倍性鉴定
通过流式细胞仪测定细胞中DNA相对含量从而对群体进行倍性的区分, 是一种比较高效的倍性鉴定方式, 检测过程简洁, 结果精准, 已在动植物的倍性鉴定中得到广泛应用。在植物倍性鉴定方面, 已分别对番石榴(Psidium guajava Linn.)[27]、柑橘(Citrus)[28]、猕猴桃(Actinidia)[29]等进行了倍性分析, 准确性较高。郑春静等[30]通过对大黄鱼(Larimichthys crocea)进行二倍体和三倍体鉴定, 建立了流式细胞仪鉴定细胞三倍体的方法, 以二倍体为参照, 如诱导试验组中某个样品细胞DNA相对含量的峰值所对应的数值是对照组二倍体组对应数值的(1.5±0.1)倍, 则判定该检测样品为三倍体。在对黄姑鱼(Nibea albiflora)二倍体和三倍体倍性分析中, 二倍体试验组DNA相对含量的峰值在1024附近, 三倍体处理组的峰值聚集在1536, 三倍体处理组的DNA含量为二倍体的1.5倍[31]。张新辉等[32]采用流式细胞仪对团头鲂进行倍性鉴定, 二倍体DNA相对含量为2.90±0.08, 三倍体DNA相对含量为4.33±0.13, 三倍体是二倍体的1.49倍, 该倍性鉴定结果与染色体计数的结果相一致, 再次证明了利用流式细胞仪鉴定水产动物倍性的准确性。
本试验通过流式细胞仪对静水压诱导的勃氏雅罗鱼仔鱼进行了倍性鉴定, 以勃氏雅罗鱼二倍体细胞中DNA的相对含量为参照, 进行三倍体的筛选, 结果显示: 勃氏雅罗鱼二倍体细胞中DNA相对含量的峰值聚集在100数值附近, 三倍体细胞中DNA相对含量的峰值聚集在150数值附近, 三倍体为二倍体的1.5倍。该试验结果与上述通过流式细胞仪对其他水产动物进行倍性鉴定的结果相同, 说明试验对三倍体勃氏雅罗鱼的诱导是有效的, 可以通过静水压诱导获得三倍体勃氏雅罗鱼苗种。
4. 结论
通过静水压对勃氏雅罗鱼进行三倍体的诱导, 采用流式细胞仪进行倍性的鉴定, 综合受精率、孵化率和三倍体率结果, 筛选出本试验条件下静水压诱导三倍体勃氏雅罗鱼的适宜条件: 在(17±1)℃时, 受精后5min, 60 MPa静水压强持续处理4min, 可达到受精率72.58%、孵化率70.59%、三倍体率97.44%。本文首次建立了三倍体勃氏雅罗鱼苗种的静水压诱导法, 填补了我国通过静水压法诱导三倍体勃氏雅罗鱼的空白, 为其他雅罗鱼类的规模化三倍体制种提供技术参考和理论依据, 为勃氏雅罗鱼养殖业的发展奠定基础, 这有助于扩大勃氏雅罗鱼养殖和消费市场规模。
-
表 1 诱导起始时间对勃氏雅罗鱼受精率、孵化率和三倍体率的影响
Table 1 Effect of initiation time of induction on fertilization rate, hatching rate, and triploid rate of Leuciscus brandti
项目Item 诱导起始时间
Initiation time of induction (min)0/对照组 3 4 5 6 受精率
Fertilization rate (%)76.82±
1.60a61.93±
0.43d72.04±
1.65b75.36±
0.80a67.34±
1.66c孵化率
Hatchability (%)79.82±
0.61a61.56±
1.46c73.30±
1.79b78.80±
0.57b62.37±
1.21c三倍体率
Triploid rate (%)— 37.55±
2.44c48.51±
3.09b56.39±
1.75a51.64±
2.54b注: 表中数据为3个重复的平均值; 同一行数据右上角含有相同英文上标字母或无上标表示无显著差异(P≥0.05); 下同Note: Data are means of triplicates. Means in each bar sharing the same superscript letter or absence of superscripts indicate no significant difference determined by Tukey’s test (P≥0.05), the same applies below 表 2 静水压强对勃氏雅罗鱼受精率、孵化率和三倍体率的影响
Table 2 Effects of hydrostatic pressure on fertilization rate, hatching rate, and triploid rate of Leuciscus brandti
项目Item 静水压强
Hydrostatic pressure (MPa)大气压/
对照组50 55 60 65 受精率
Fertilization rate (%)76.82±
1.60a63.63±
1.65c72.30±
1.34b75.81±
0.62a50.48±
1.82d孵化率
Hatchability (%)79.82±
0.61a71.73±
2.00b70.27±
1.00b71.40±
2.08b57.65±
1.39c三倍体率
Triploid rate (%)— 43.22±
1.18d57.55±
3.09c70.53±
3.04a64.08±
3.68b表 3 持续处理时间对勃氏雅罗鱼受精率、孵化率和三倍体率的影响
Table 3 Effects of continuous treatment time on fertilization rate, hatching rate, and triploid rate of Leuciscus brandti
项目Item 持续处理时间
Continuous treatment time (min)0/对照组 3 4 5 6 受精率
Fertilization rate (%)76.82±
1.60a67.82±
2.33c72.58±
2.31b69.01±
1.67bc59.52±
2.43d孵化率
Hatchability (%)79.82±
0.61a67.45±
0.97c70.59±
1.16b66.32±
2.72c60.59±
1.03d三倍体率
Triploid rate (%)— 81.72±
3.64c97.44±
0.62a89.60±
2.82b69.09±
6.64d -
[1] 葛立新, 郑伟. 滩头鱼池塘养殖技术 [J]. 黑龙江水产, 2011, 30(6): 10-11.] Ge L X, Zheng W. Pond culture technology of Leuciscus brandti [J]. Northern Chinese Fisheries, 2011, 30(6): 10-11. [
[2] 郭贵良, 赵大威, 赵宁, 等. 滩头鱼商品鱼池塘养殖技术要点 [J]. 中国水产, 2020(9): 78-80.] Guo G L, Zhao D W, Zhao N, et al. Key points of pond culture technology of Leuciscus brandti commercial fish [J]. China Fisheries, 2020(9): 78-80. [
[3] 汪勇翔, 王永杰. 水产动物遗传育种研究进展 [J]. 现代农业科技, 2010(17): 324-325.] Wang Y X, Wang Y J. Research progress on genetics and breeding of aquatic animals [J]. Modern Agricultural Sciences and Technology, 2010(17): 324-325. [
[4] Zhang C, Li Q, Zhu L, et al. Abnormal meiosis in fertile and sterile triploid cyprinid fish [J]. Science China Life Sciences, 2021, 64(11): 1917-1928. doi: 10.1007/s11427-020-1900-7
[5] 陆莉莉, 高云云, 徐成勋, 等. 三种方法诱导福建牡蛎三倍体的比较研究 [J]. 中国海洋大学学报(自然科学版), 2024, 54(11): 157-164.] Lu L L, Gao Y Y, Xu C X, et al. A comparison of three triploid induction methods in Crassostrea angulate [J]. Periodical of Ocean University of China, 2024, 54(11): 157-164. [
[6] 卓琳莹, 管玲玲, 鲍守民, 等. 二、三倍体虹鳟肌肉感官品质差异的对比分析 [J]. 食品科学, 2022, 43(18): 209-215.] Zhuo L Y, Guan L L, Bao S M, et al. Comparison of sensory quality between diploid and triploid rainbow trout (Oncorhynchus mykiss) muscles [J]. Food Science, 2022, 43(18): 209-215. [
[7] 邓远, 苏金枝, 李振通, 等. 金虎杂交斑三倍体、二倍体生长、发育比较及形态性状差异分析 [J]. 海洋与湖沼, 2024, 55(5): 1302-1311.] Deng Y, Su J Z, Li Z T, et al. Comparison analysis of growth, development, and morphological characteristics triploid and diploid hybrid groupers [J]. Oceanologia et Limnologia Sinica, 2024, 55(5): 1302-1311. [
[8] Gervai J, Páter S, Nagy A, et al. Induced triploidy in carp, Cyprinus carpio L [J]. Journal of Fish Biology, 1980, 17(6): 667-671. doi: 10.1111/j.1095-8649.1980.tb02800.x
[9] Güner Y, Kayim M, Kızak V, et al. Production and performance of triploid rainbow trout in Turkey [J]. Indian Veterinary Journal, 2005(82): 1077-1079.
[10] Stanley J G, Allen S K, Hidu H. Polyploidy induced in the American oyster, Crassostrea virginica, with cytochalasin B [J]. Aquaculture, 1981, 23(1/2/3/4): 1-10.
[11] 魏凯, 郑伟, 时晓, 等. 热休克诱导马苏大麻哈鱼三倍体的初步研究 [J]. 淡水渔业, 2020, 50(2): 67-71.] Wei K, Zheng W, Shi X, et al. Preliminary study on heat shock-induced triploid of Oncorhynchus masou [J]. Freshwater Fisheries, 2020, 50(2): 67-71. [
[12] 杨荣国, 杨志江, 田洋, 等. 勃氏雅罗鱼苗种繁育及成鱼养殖技术 [J]. 河北渔业, 2012(1): 33-35.] Yang R G, Yang Z J, Tian Y, et al. Breeding of Leuciscus brandti and adult fish culture technology [J]. Hebei Fisheries, 2012(1): 33-35. [
[13] Ozawa A, Sakaue M. New decolorization method produces more information from tissue sections stained with hematoxylin and eosin stain and Masson-trichrome stain [J]. Annals of Anatomy-Anatomischer Anzeiger, 2020(227): 151431. doi: 10.1016/j.aanat.2019.151431
[14] 朱雪梅, 赵明军, 王宇光, 等. 水产品可食率与蛋白质贡献比较研究 [J]. 中国渔业质量与标准, 2021, 11(3): 32-39.] Zhu X M, Zhao M J, Wang Y G, et al. Comparative study on edible rate and protein contribution of aquatic products [J]. Chinese Fishery Quality and Standards, 2021, 11(3): 32-39. [
[15] Piferrer F, Beaumont A, Falguière J C, et al. Polyploid fish and shellfish: Production, biology and applications to aquaculture for performance improvement and genetic containment [J]. Aquaculture, 2009, 293(3/4): 125-156.
[16] 刘金相, 王旭波, 刘聪辉, 等. 静水压法人工诱导牙鲆(♀)×圆斑星鲽(♂)杂交三倍体的探索 [J]. 中国海洋大学学报(自然科学版), 2014, 44(2): 41-47.] Liu J X, Wang X B, Liu C H, et al. Induction of triploid hybrid of Japanese flounder (Paralichthys olivaceus, ♀) × spotted halibut (Verasper variegatus, ♂) by hydrostatic pressure shocks [J]. Periodical of Ocean University of China, 2014, 44(2): 41-47. [
[17] 刘志鹏, 王旭波, 翟介明, 等. 半滑舌鳎三倍体诱导研究 [J]. 中国海洋大学学报(自然科学版), 2012, 42(6): 77-80.] Liu Z P, Wang X B, Zhai J M, et al. Study on triploid induction in the half-smooth tongue sole (Cynoglossus semilaevis) [J]. Periodical of Ocean University of China, 2012, 42(6): 77-80. [
[18] 陈松林, 李文龙, 季相山, 等. 半滑舌鳎三倍体鱼苗的人工诱导与鉴定 [J]. 水产学报, 2011, 35(6): 925-931.] Chen S L, Li W L, Ji X S, et al. Induction and identification of artificial triploid fry in Cynoglossus semilaevis [J]. Journal of Fisheries of China, 2011, 35(6): 925-931. [
[19] Peruzzi S, Chatain B. Pressure and cold shock induction of meiotic gynogenesis and triploidy in the European Sea bass, Dicentrarchus labrax L.: relative efficiency of methods and parental variability [J]. Aquaculture, 2000, 189(1/2): 23-37.
[20] Lou Y D, Purdom C E. Diploid gynogenesis induced by hydrostatic pressure in rainbow trout, Salmo gairdneri Richardson [J]. Journal of Fish Biology, 1984, 24(6): 665-670. doi: 10.1111/j.1095-8649.1984.tb04837.x
[21] Chourrout D. Pressure-induced retention of second polar body and suppression of first cleavage in rainbow trout: production of all-triploids, all-tetraploids, and heterozygous and homozygous diploid gynogenetics [J]. Aquaculture, 1984, 36(1/2): 111-126.
[22] Cassani J R, Caton W E. Efficient production of triploid grass carp (Ctenopharyngodon idella) utilizing hydrostatic pressure [J]. Aquaculture, 1986, 55(1): 43-50. doi: 10.1016/0044-8486(86)90054-2
[23] 李勇明, 桂彬, 黎阳雨, 等. 静水压诱导翘嘴鳜雌核发育的研究 [J]. 水生生物学报, 2022, 46(5): 735-740.] Li Y M, Gui B, Li Y Y, et al. Preliminary study on gynogenesis of Siniperca chuatsi induced by hydrostatic pressure [J]. Acta Hydrobiologica Sinica, 2022, 46(5): 735-740. [
[24] 桂建芳, 梁绍昌, 孙建民, 等. 鱼类染色体组操作的研究 Ⅰ. 静水压休克诱导三倍体水晶彩鲫 [J]. 水生生物学报, 1990, 14(4): 336-344.] doi: 10.3724/issn1000-3207-1990-4-336-k Gui J F, Liang S C, Sun J M, et al. Studies on genome manipulation in fish i. induction of triploid transparent colored crucian carp (Carassius auratus transparent colored variety) by hydrostatic pressure [J]. Acta Hydrobiologica Sinica, 1990, 14(4): 336-344. [ doi: 10.3724/issn1000-3207-1990-4-336-k
[25] 李宝玉, 郑国栋, 崔文涛, 等. 团头鲂三倍体的微卫星遗传特征及生长性能分析 [J]. 水产科学, 2022, 41(2): 173-182.] Li B Y, Zheng G D, Cui W T, et al. Analysis of microsatellite markers and growth performance in artificial triploid of blunt snout bream Megalobrama amblycephala [J]. Fisheries Science, 2022, 41(2): 173-182. [
[26] 尤颖哲. 静水压法诱导双斑东方鲀三倍体的研究 [J]. 上海海洋大学学报, 2017, 26(3): 348-352.] doi: 10.12024/jsou.20160901869 You Y Z. Triploidy induction by hydrostatic pressure treatment in Takifugu bimaculatus [J]. Journal of Shanghai Ocean University, 2017, 26(3): 348-352. [ doi: 10.12024/jsou.20160901869
[27] 邵雪花, 李桂兰, 肖维强, 等. 基于流式细胞仪鉴定番石榴倍性方法的建立及应用 [J]. 生物技术通报, 2024, 40(2): 48-54.] Shao X H, Li G L, Xiao W Q, et al. Establishment and application of ploidy method for the identification of Psidium guajava by flow cytometry [J]. Biotechnology Bulletin, 2024, 40(2): 48-54. [
[28] 陈昊, 谢善鹏, 解凯东, 等. 柑橘13个多胚品种同源四倍体高效发掘与分子鉴定 [J]. 果树学报, 2023, 40(11): 2297-2306.] Chen H, Xie S P, Xie K D, et al. Efficient exploration and SSR identification of autotetraploids from the seedlings of thirteen apomictic Citrus genotypes [J]. Journal of Fruit Science, 2023, 40(11): 2297-2306. [
[29] 罗庆, 高建有, 李洁维, 等. 利用流式细胞仪对猕猴桃种质染色体倍性的鉴定 [J]. 生物学杂志, 2022, 39(6): 66-72.] Luo Q, Gao J Y, Li J W, et al. Identification of chromosome ploidy in kiwifruit germplasm by flow cytometer [J]. Journal of Biology, 2022, 39(6): 66-72. [
[30] 郑春静, 吴雄飞, 刘东海, 等. 用流式细胞仪检测大黄鱼三倍体 [J]. 细胞生物学杂志, 2006, 28(2): 253-256.] Zheng C J, Wu X F, Liu D H, et al. Triplont analysis of psendociaena crocea by flow cytometry [J]. Chinese Journal of Cell Biology, 2006, 28(2): 253-256. [
[31] 卢磊, 陈睿毅, 杨阳, 等. 黄姑鱼三倍体的诱导、鉴定及其性腺发育特征 [J]. 水生生物学报, 2023, 47(2): 290-297.] Lu L, Chen R Y, Yang Y, et al. The induction and identification of the triploid yellow drum (Nibea albiflora, sciaenidea) and characterization of their gonadal development [J]. Acta Hydrobiologica Sinica, 2023, 47(2): 290-297. [
[32] 张新辉, 罗伟, 高泽霞, 等. 团头鲂三倍体的诱导及其鉴定 [J]. 水产科学, 2013, 32(9): 503-508.] doi: 10.3969/j.issn.1003-1111.2013.09.002 Zhang X H, Luo W, Gao Z X, et al. Induction and identification of triploid in bluntnose black bream Megalobrama amblycephala [J]. Fisheries Science, 2013, 32(9): 503-508. [ doi: 10.3969/j.issn.1003-1111.2013.09.002



 下载:
下载: